盐酸羟考酮缓释片的制备及防滥用性能评估*
王佳瑜,高梓真,许向阳,刘新颖,毛文星,曾令高△
(1. 江苏恩华药业股份有限公司药物研究院·江苏省中枢神经药物研究重点实验室,江苏徐州 221000; 2. 重庆市食品药品检验检测研究院·国家药品监督管理局麻醉精神药品质量监测重点实验室,重庆 401121)
阿片类镇痛药能有效缓解中度至重度疼痛,被世界卫生组织(WHO)认定为三阶梯癌痛治疗的常规用药,是治疗急性疼痛的一线药物,但具有成瘾性,其滥用已在全球范围内成为日益严重的公共卫生问题[1]。为在满足疼痛管理临床需求的同时防止阿片类镇痛药的滥用,药品生产企业提出防滥用型制剂(ADFs)概念[2]。盐酸羟考酮是由阿片生物碱蒂巴因植物衍生物制成的半合成阿片类药物,是阿片受体完全激动剂,可与大脑及脊髓的阿片κ,µ受体结合,具有强大的镇痛作用[3]。盐酸羟考酮缓释片(商品名OxyContin®)由Purdue Pharma,L.P.(普渡制药)公司研发,通过美国食品和药物管理局(FDA)505(b)新药申请监管途径,于2010年4月成为FDA 首个赋予防滥用标签的药品,同期原普通缓释制剂撤市。处方使用相对分子质量高的聚氧乙烯(PEO)材料,并在工艺中增加熟化步骤作为防滥用核心技术,已申请中国专利(CN101583360B),授权有效期至2027 年8月24日[4-5]。PEO 是一种非离子的具有热塑性的亲水性聚合物,其外观为可自由流动白色粉末,相对分子质量为100 000~7 000 000(熔点为63~72 ℃)。该类聚合物热处理后会形成具有高机械强度的致密体,可赋予片剂很高的硬度,防止被咀嚼、切割、粉碎或研磨;使用水或醇等溶剂萃取时,会溶胀形成黏稠的凝胶,难以提取注射,是防滥用配方中最常用的基质材料。但该类聚合物受到高温、氧、机械作用的影响时易发生链裂解,生成相对分子质量较低的聚合物,进而影响其防滥用性能[6-12]。本研究中选择适当型号的PEO,采用热熔挤出(HME)技术制备盐酸羟考酮缓释片,并以黏度为指标,筛选处方中抗氧剂的种类及加入量对聚合物稳定性的影响;同时,按最优处方制备样品,与参比制剂进行溶出度、凝胶强度、可注射性、硬度、粉碎后颗粒粒度分布等各项防滥用特性及可提取性对比评估。现报道如下。
1 仪器与试药
1.1 仪器
TA.XTC-20型质构仪(上海保圣实业发展有限公司);MCR 302e 型流变仪(奥地利Anton Paar 公司);Pharma11 型热熔挤出机(美国Thermo Fisher 公司);PTB - 311E - 800 型硬度仪(德国Pharma Test 公司);Mettler SevenExcellence 型多参数测定仪(瑞士Mettler Toledo 公司);FADT-1202 自动取样溶出仪(上海富克斯公司);LC - 20AD 型液相色谱仪(日本Shimadzu 公司);SG-350C 型多功能食品加工机(北京瑞百利商贸有限公司);CZ300型振动筛分过滤机(新乡市诚鑫振动机械有限公司)。
1.2 试药
OxyContin®(Purdue Pharma L. P.,批号为WF1T4,规格为每片40 mg);盐酸羟考酮(甘肃普瑞制药有限公司,批号为CP0012103004,纯度为100.3%);Polyethylene oxide PolyoxTMWSR N750(批号为D682L77RJ3,相对分子质量为300 000),Polyethylene oxidePolyoxTMWSR 205(批号为D682H97PA3,相对分子质量为600 000),Polyethylene oxide PolyoxTMWSR 1105(批号为D682K8LPD1,相对分子质量为900 000),Polyethylene oxide PolyoxTMWSR 301(批号为D682K69PB3,相对分子质量为4 000 000),PolyethyleneoxidePolyoxTMCoagulant(批号为D682K1TRC3,相对分子质量为5000000),Polyethylene oxide PolyoxTMWSR 303(批号为D682KC7PR3,相对分子质量为7 000 000),均购于Specialty Products US,LLC;维生素E(巴斯夫<中国>有限公司,批号为55276377LO,纯度为99%);维生素C(上海源叶生物科技有限公司,批号为Y11S14Y13936,纯度为99%);二丁基羟基甲苯(BHT,江西阿尔法高科药业有限公司,批号为20220601,纯度为99.4%);庚烷磺酸钠(Fisher Chemical);磷酸、氯化钠(上海凌峰试剂有限公司);盐酸(国药集团化学试剂有限公司);异丙醇(Fisher 公司);乙醇、乙腈(美国Mreda公司)。
2 方法与结果
2.1 处方筛选
2.1.1 黏度测定
不同相对分子质量PEO 黏度测定:PolyoxTMWSR树脂是由环氧乙烷在多相催化剂作用下,碳氧键断裂实现开环,逐步聚合生成的非离子型聚合物[13],在制药工业中常用于渗透泵技术,亲水性基质系统、热熔挤出配方及防滥用技术。不同相对分子质量的聚合物可独立或搭配使用以达到相应效果,聚合物在这些应用中的性能主要取决于其相对分子质量(即黏度)。称取适量PEO,加异丙醇分散,加入纯化水制成浓度为1%的溶液,在磁力搅拌下使完全溶胀,将溶液滴于PP25/S型平板磨砂转子下,测试温度为25 ℃,剪切速率为0.1/s,采用流变仪测定不同相对分子质量的PEO。结果显示,在相同浓度下,凝胶黏度随相对分子质量加大而升高。详见图1。
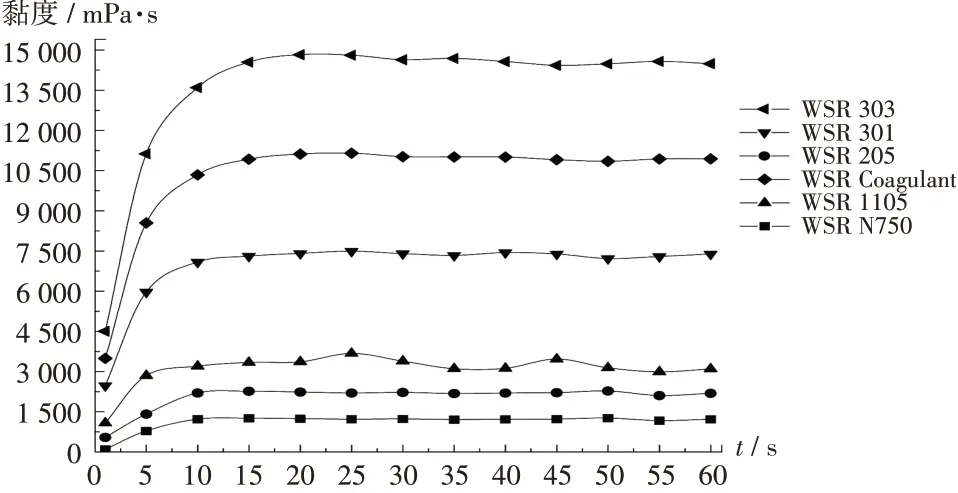
图1 不同相对分子质量聚氧乙烯的黏度曲线Fig.1 Viscosity profiles of PEO with different molecular weights
不同相对分子质量PEO 按比例混合后的黏度测定:PEO 受温度、氧、机械作用等的影响,会引发链裂解,使相对分子质量降低,高黏度是能应用于药物制剂防滥用体系至关重要的属性之一。研究表明,处方中加入相对分子质量低的PEO 作为工艺助剂,可降低相对分子质量高的PEO 分子之间的熔融黏度、摩擦力和链缠结,使HME过程更顺畅,增加相对分子质量高的PEO的稳定性[9]。将不同比例WSR N750(相对分子质量为300 000)和WSR 303(相对分子质量为7 000 000)混合,制成浓度为1%的溶液,采用流变仪测定黏度,并与专利CN101583360B中使用的PEO WSR 301的1%溶液比较。结果显示,处方中相对分子质量高的PEO 占比越大,溶液的黏度越高;当处方中WSR N750 - WSR 303为1∶6(m/m)时,溶液黏度与WSR 301 溶液黏度相近,表明该处方可用于替代原研专利处方中的辅料开展后续HME试验。详见图2。

图2 不同比例聚氧乙烯混合物的黏度曲线Fig.2 Viscosity profiles of PEO mixtures with different ratios
2.1.2 抗氧剂
HME 试验:采用HME 技术制备盐酸羟考酮缓释片时,PEO 在HME 过程中既受机械作用,又受热作用,两者皆使其发生裂解。机械作用引起的链断裂可通过加入低相对分子质量PEO、降低螺杆转速来改善,高温导致的自氧化降解可通过降低工艺温度、加入抗氧剂来减缓。抗氧剂可有效抑制自氧化过程中自由基的生成,降低自氧化速率,从而降低相对分子质量损失的速率,避免样品挤出后黏度大幅降低。维生素E、维生素C、BHT 为常用抗氧剂,其抗氧化机制为作为供氢体,释放活泼氢,捕捉自由基,中断PEO 自氧化过程的链式反应[14-15]。处方中盐酸羟考酮占比为27%,PEO WSR N750 与PEO WSR 303 比例为1∶6(m/m),处方1 不含抗氧剂,处方2加入0.05%维生素C,处方3加入0.10%维生素C,处方4 加入0.05%维生素E,处方5 加入0.10%维生素E,处方6 加入0.05%BHT,处方7 加入0.10%BHT。将PEO WSR N750、PEO WSR 303、抗氧剂、盐酸羟考酮混合物加入双螺杆热熔挤出机进行挤出。设置7 个加热区间及1 个口模温度分别为70,100,100,115,115,130,130,140 ℃,螺杆转速为80 r/ min,加热温度稳定后开始加料,剪切冷却后的挤出物。
黏度测试:挤出物粉碎后,配制成浓度为1%的溶液,采用流变仪测定由处方1-7 所制备的挤出物的黏度。结果显示,与物理混合物相比,不加抗氧剂的挤出物黏度明显下降;加入维生素C对挤出物黏度的下降无明显改善;加入维生素E 或BHT 后挤出物的黏度明显高于不加抗氧剂挤出物的黏度,且抗氧剂用量越大,PEO稳定性越好。加入0.10%维生素E或0.10%BHT的挤出物黏度与物理混合物的黏度均较接近,其中0.10%维生素E 效果更佳,即使用处方5 制备自研制剂。详见图3。

图3 物理混合物、无抗氧剂及含不同抗氧剂挤出物的黏度曲线Fig.3 Viscosity profiles of physical mixtures extrusions without antioxidant and extrusions with different antioxidants
2.2 防滥用性能评估[16-19]
体外释放:取自研制剂和参比制剂,在模拟胃液(无酶)中进行溶出试验,介质体积为900 mL,温度为37 ℃,采用篮法,转速为100 r/min。采用高效液相色谱(HPLC)法测定溶出度,色谱柱为Shimadzu Shim-pack VP-ODS柱(150 mm×4.6 mm,5µm),流动相为乙腈-庚烷磺酸钠缓冲液(1∶3,V/V),流速为1.0 mL/min,检测波长为230 nm,柱温为60 ℃,进样量为20µL。结果在模拟胃液(无酶)中,自研制剂与参比制剂的相似因子(f2)为80.02,表明两者体外释放行为相似。详见图4。

图4 自研制剂与参比制剂在模拟胃液(无酶)中的溶出曲线(n=6)Fig.4 Dissolution profiles of self-developed formulation and reference preparation in simulated gastric juice without enzyme(n=6)
凝胶强度:采用质构仪测定自研制剂和参比制剂的凝胶强度。将样品置培养皿中,加入pH 1.2盐酸氯化钠介质,静态溶胀8 h。采用5 kg 感应元,TA/ 0.5 凝胶探头,下压形变90%。结果显示,凝胶探头下压至相同形变比例时,对自研制剂施加的力远大于对参比制剂施加的力,表明自研制剂的凝胶强度大于参比制剂的凝胶强度。详见图5。
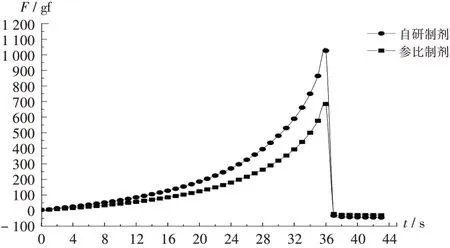
图5 自研制剂与参比制剂静态溶胀8 h的凝胶强度Fig.5 Gel strength of self-developed formulation and reference preparation which had statically swelled for 8 h
可注射性:通针性是决定可注射性的关键指标,是指药液可以通过注射针筒、注射针头顺利取出,不黏筒壁,不堵针头,主要以注射时所需压力和压强及顺滑程度来衡量。采用质构仪对自研制剂和参比制剂进行可注射性测试,测量参数包括注射活塞开始移动时所需的力和持续注射时活塞受到的阻力。将片剂粉碎,加水,搅拌至完全溶胀,采用20 kg 感应元,10 mL 注射器(含胶塞),下压模式,位移5 mm,测试速率为0.04 mm/s。结果显示,推动自研制剂凝胶通过针头所需的力更大,表明自研制剂可注射性更差。详见图6。
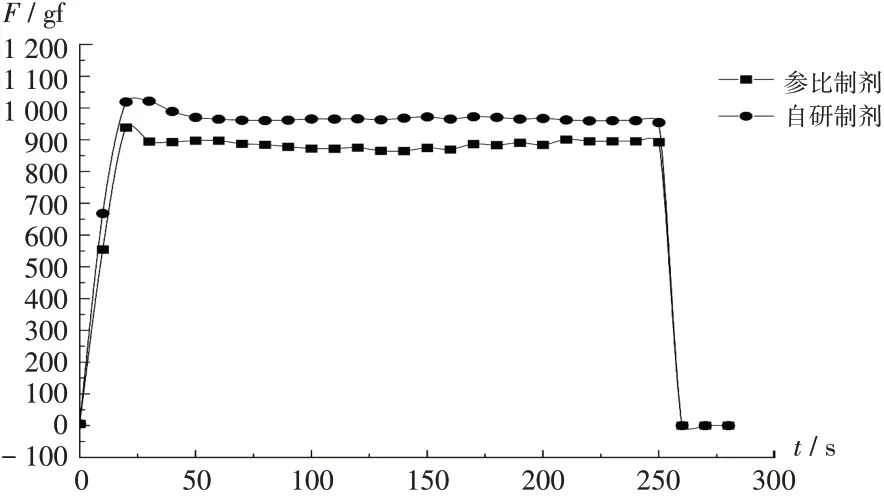
图6 自研制剂与参比制剂凝胶的可注射性Fig.6 Injectability of self-developed formulation and reference preparation gels
硬度:将硬度仪设置为胶囊模式检测片剂硬度,结果参比制剂和自研制剂的硬度均大于500 N;参比制剂与自研制剂被挤扁后均未碎裂,可有效防止被咀嚼、切割或研磨。详见表1。

表1 自研制剂与参比制剂的硬度(N)Tab.1 Hardness of self-developed formulation and reference preparation(N)
粉碎后粒度分布:鼻吸途径滥用通常是指对经物理处理的阿片类口服固体药物进行鼻吸。结合鼻吸途径给药特点及常见制药技术,鼻吸滥用途径的药学评估指标应包括可用于鼻吸颗粒的粒径和质量。通常<500µm的细颗粒占比可在一定程度上反映鼻吸滥用生物利用度。分别取自研制剂和参比制剂,在室温下使用多功能食品加工机粉碎处理30 s,采用振荡筛分离,标准筛网18 目、35 目、60 目、150 目,孔径分别为1 000,500,250,100µm,记录不同粒径的颗粒占比。其中,参比制剂<500 µm 的颗粒占比为12.41%,自研制剂<500 µm 的颗粒占比为8.06%,表明自研制剂粉碎后细颗粒更少,更能抵抗物理处理,防鼻吸滥用性能更佳。详见图7。

图7 自研制剂与参比制剂粉碎后的颗粒粒径(X±s,n=3)Fig.7 Particle size of self-developed formulation and reference preparation after crushing(X±s,n=3)
2.3 可提取性
PEO 易吸收水分而形成黏稠的凝胶或溶液,在片剂形式中,该材料允许药物通过扩散或侵蚀。当制成粉末并通过注射器进行静脉注射时,该制剂形成难以吸收(抽出)和分配的黏性溶液,进而导致注射针头堵塞以阻止静脉注射滥用[2]。通过可提取性对比仿制药与参比制剂抵抗外力破坏的能力,以评估两者防滥用特性的可比性。考察参比制剂和自研制剂的完整片剂在水、40%乙醇溶液、无水乙醇、异丙醇4 种提取介质中的药物提取率。将片剂置240 mL 溶剂中,于温度为20~25 ℃、搅拌转速为100 r/min条件下进行提取,搅拌90 min时取样1 mL,使用0.45µm聚四氟乙烯(PTFE)疏水性滤膜滤过,按“2.2 体外释放”项下方法测定盐酸羟考酮含量。
对于完整片剂,90 min内参比制剂和自研制剂在水中的提取率分别为24.97%和24.27%,在40%乙醇溶液中的提取率分别为20.08%和19.28%,在无水乙醇中的提取率分别为4.22%和3.85%,在异丙醇中的提取率分别为2.82%和2.85%,表明自研制剂与参比制剂的可提取性相当,只有一部分药物可通过传统方法被提取,可适度抵抗通过静脉途径的药物滥用。详见图8。

图8 自研制剂与参比制剂在不同溶剂中的提取率(X±s,n=3)Fig.8 Extraction rate of self-developed formulation and reference preparation in different solvents(X±s,n=3)
3 讨论
相对分子质量低的PEO 与相对分子质量高的PEO配比可实现不同的黏度性能,广泛应用于制药行业。本研究中采用物理/化学屏障防滥用技术制备盐酸羟考酮缓释片,建立了采用流变仪辅助处方筛选的方法,将相对分子质量低的PEO 与相对分子质量高的PEO 按比例混合后,通过流变仪测定各比例混合物的黏度,与参比制剂使用的PEO WSR 301 溶液的黏度进行对比,筛选得最优比例为WSR N750 - WSR 303(1∶6,m/m)。PEO WSR 303 提供了不可或缺的高黏度属性,而WSR N750的加入使螺杆扭矩降低,挤出工艺更流畅。以流变仪检测黏度为指标,对处方中加入的抗氧剂进行筛选,在HME试验中,维生素E和BHT均能作为稳定剂,可有效抑制HME 过程中PEO 的氧化降解,减少相对分子质量的损失,仍保持较高的黏度特性。以优选处方制备的自研制剂,与参比制剂进行初步的防滥用性能评估。结果显示,与参比制剂相比,自研制剂被挤压后外观更完整,粉碎后细颗粒更少,更难被物理破坏;自研制剂凝胶强度更高,可注射性更差;此外,自研制剂与参比制剂在水、40%乙醇溶液、无水乙醇、异丙醇中90 min 内可提取性相当。自研处方制备的样品防滥用特性不低于参比制剂,可为后续仿制药的研究提供参考。

