使用药代动力学管理工具myPKFiT预测中国血友病A患者凝血因子Ⅷ活性
华宝来 肖娟 赵永强
摘要:目的 在中国血友病A患者中评估用于指导使用无血浆/血清方法制备的基因重组人凝血因子Ⅷ剂量的管理工具myPKFiT对维持凝血因子Ⅷ活性水平至目标阈值和药代动力学参数的预测效果。方法 以中国既往接受过治疗的血友病A患者的疗效和安全性的研究(登记号:CTR20140434)中的9例重型血友病A患者为研究对象,应用myPKFiT对维持一定目标凝血因子Ⅷ活性阈值下的重组人凝血因子Ⅷ剂量进行预测,并评估myPKFiT对个体药代动力学参数的预测性能。结果 对于基于6种稀疏采样和2种给药方案的共12个方案组合,57%~88%的受试者可在至少80%的给药间隔内保持在目标凝血因子Ⅷ活性阈值1 U/dl(1%)之上。使用myPKFiT从稀疏采样获得的清除率及至凝血因子Ⅷ活性 1%时间的估计值与从密集采样中获得的数据相当。结论 myPKFiT能够提供足够的剂量预测值以使中国重型血友病A患者的凝血因子Ⅷ活性水平维持在稳态下的目标阈值以上,且对清除率和至凝血因子Ⅷ活性 1%的时间等关键药代动力学参数具有良好的预测性能。
关键词:血友病A;药代动力学;myPKFiT;凝血因子Ⅷ
中图分类号: R554+.1;R969.1文献标志码: A文章编号:1000-503X(2023)02-0200-06
DOI:10.3881/j.issn.1000-503X.15264
Prediction of Coagulation Factor Ⅷ Level in Chinese Hemophilia A Patients by the Pharmacokinetic Management Tool myPKFiT
HUA Baolai XIAO Juan ZHAO Yongqiang3
ABSTRACT:Objective To evaluate the performance of myPKFiT,a tool guiding the dosing of antihemophilic factor (recombinant) plasma/albumin-free method (rAHF-PFM),in maintaining the coagulation factor Ⅷ (FⅧ) level above a target threshold at the steady state and estimating the pharmacokinetics (PK) parameters in hemophilia A patients in China.Methods The data of 9 patients with severe hemophilia A in a trial (CTR20140434) assessing the safety and efficacy of rAHF-PFM in the Chinese patients with hemophilia A were analyzed.The myPKFiT was used to predict the adequate dose to maintain a patients FⅧ level above target threshold at the steady state.Furthermore,the performance of myPKFiT in estimating the pharmacokinetics parameters of individuals was evaluated.Results Twelve combinations of two dosing intervals and six sparse sampling schedules were investigated,and 57%-88% of the patients remained the FⅧ level above the target threshold of 1 U/dl (1%) for at least 80% of the dosing interval.The clearance and time to FⅧ level of 1% obtained from sparse sampling by myPKFiT were similar to those obtained from extensive sampling.Conclusions The myPKFiT can provide adequate dose estimates to maintain the FⅧ level above the target threshold at the steady state in Chinese patients with severe hemophilia A.Moreover,it demonstrates good performance for estimating key pharmacokinetics parameters,including clearance and time to FⅧ level of 1%.
Key words:hemophilia A;pharmacokinetics;myPKFiT;coagulation factor Ⅷ
Acta Acad Med Sin,2023,45(2):200-205
血友病A是凝血因子Ⅷ(factor Ⅷ,FⅧ)基因突變所致的遗传性出血性疾病[1],以关节、肌肉出血为最常见的临床表现。反复关节出血可导致关节畸形甚至致残,严重影响患者生活质量[2]。按需或预防性输注FⅧ制剂是现阶段血友病A治疗的主要措施,其中预防治疗因能显著降低出血频率而为世界血友病联盟血友病管理指南首推[3-4]。影响预防治疗效果的因素很多,如患者的出血表型、靶关节的状态、生活方式、预防治疗的方案和依从性、FⅧ制剂的半衰期和个体的药代动力学(pharmacokinetics,PK)等[5],目前尚无法用一个方案来维持和预测所有患者所需求的FⅧ水平[6]。由于不同患者间PK参数差别很大,近年PK指导下的个体化预防治疗越来越受到推崇。通过分析特定FⅧ制剂在患者体内的半衰期、体内回收率及峰谷值,可个性化制定预防治疗剂量和给药间隔,从而最大程度降低出血和关节损伤风险[6-7]。传统的PK分析方法存在采血次数多(10~11个时间点)、操作烦琐、患者依从性差等不足,迫切需要开发更为简捷、准确的监测PK的方法。
myPKFiT是专门为未添加任何血浆蛋白成分的注射用人重组FⅧ研发的PK指导管理工具,仅需2~3个时间点的血液样本(稀疏采样)即能快速简便地评估患者的PK特征,指导剂量调整,为制定个体化预防方案提供依据。myPKFiT的临床价值已在国外人群中得到验证[8-9],但在中国人群中尚无数据。本研究旨在回顾性分析中国血友病A患者基于myPKFiT的剂量方案对维持FⅧ活性水平至目标阈值的能力以及对PK参数的预测效能,以便为其在中国血友病A患者中的应用提供依据。
对象和方法
对象 评估注射用人重组FⅧ(百因止,Baxalta制药公司)治疗既往接受过治疗的血友病A患者的疗效和安全性的研究[safety and efficacy study of antihemophilic factor (recombinant) in Previously Treated Chinese Patients with severe/moderately severe hemophilia A,PTP研究](登记号:CTR20140434)是一项2014年6月至2016年5月在中国11家中心开展的前瞻性、多中心、开放标签、序贯性干预研究,目的是评估注射用人重组FⅧ治疗既往接受过治疗的血友病A患者的疗效、安全性和药代动力学[10-11]。本研究纳入PTP研究中PK资料完整的9例重型血友病A患者。所有受试者均无FⅧ抑制物史,入组筛选时抑制物为阴性(<0.6 BU/ml),未合并其他出血性疾病[10-11]。血液样本的FⅧ活性均在中心实验室应用一期凝血法进行检测。研究方案已获主要研究单位伦理委员会批准,所有受试者(或其监护人)均签署知情同意书。
PK血液标本的采集 PTP药物试验的PK研究采用密集采样方案:在给药前即刻 (0 min),给药后10 min及0.5、1、3、6、9、24、28、32、48 h采集标本,每例患者至少有10个时间点样本,共有9例患者获取完整的PK评估数据。为验证myPKFiT在中国血友病A患者中的预测效能,根据注射用人重组FⅧ的群体药代动力学模型研究中2~3个时间点稀疏采样方案[12],本研究利用部分密集采样的时间点的不同组合作为输入myPKFiT软件计算的采样点,即第1采集时间点(必须):输注后[(3~4)±0.5]h及第2或第2和3采集时间点:输注后(24±1)、(28±1)、(32±1)h中的任1或2个点。
PK参数的预测效能分析软件:来自稀疏采样的预测剂量和估算的PK参数直接从myPKFiT v3.0.SAS软件包第9.3版的注射用人重组FⅧ功能中获得,并用于其余分析。
输入核查 即适用性检查,是一种内置于myPKFiT软件中的观察异常值的诊断流程,评估某些FⅧ活性是否超出预期残差分布,目的是检查受试者是否适用于myPKFiT。通过输入核查的病例视为可评估的受试者。
myPKFiT的符合目的分析 使用上述myPKFiT软件,利用稀疏采样方案时间点对应的FⅧ活性水平和PTP研究中的实际给药剂量、输注时间,结合患者的体重、基础FⅧ活性水平,创建个体化PK曲线。然后根据FⅧ活性谷浓度水平目标值(如1 U/dl)和给药间隔(如每48 h或72 h)對注射用人重组FⅧ的预防剂量进行计算,得出预测剂量。
根据myPKFiT预测剂量及推荐剂量范围,得出myPKFiT给药指导规则:(1)每48 h给药时,预测剂量>40 U/kg的受试者被排除在符合目的分析之外;(2)每72 h给药时,预测剂量>80 U/kg的受试者再以48 h间隔进行评估;(3)将预测剂量<20 U/kg的受试者进行20 U/kg的符合目的分析。
若预测剂量在myPKFiT软件的推荐剂量范围内(每48 h 20~40 U/kg或 每72 h 20~80 U/kg),结合密集采样数据,用来自注射用人重组FⅧ的myPKFiT的预测剂量计算稳态下超出目标FⅧ活性阈值(>1 U/dl)的时间,继而计算在给药间隔内至少80%或90%的时间高于目标阈值的受试者百分比。
myPKFiT的预测效能分析 应用PTP临床研究密集采样标本检测出的高于定量下限[定义为FⅧ活性 1 U/dl(即1%)]的所有输注后FⅧ活性值得到完整的个体PK参数,包括清除率、稳态分布容积、终末半衰期(t1/2)和达到1%的时间。然后应用这些数据,对稀疏采样的myPKFiT的预测效能进行评估。
结果
一般资料 共有9例受试者纳入本研究,全部为男性;年龄15~37岁,中位年龄19岁;基线体重44.0~92.0 kg,中位基线体重72.0 kg;输注注射用人重组FⅧ剂量41.3~50.0 U/kg,中位剂量为45.5 U/kg。
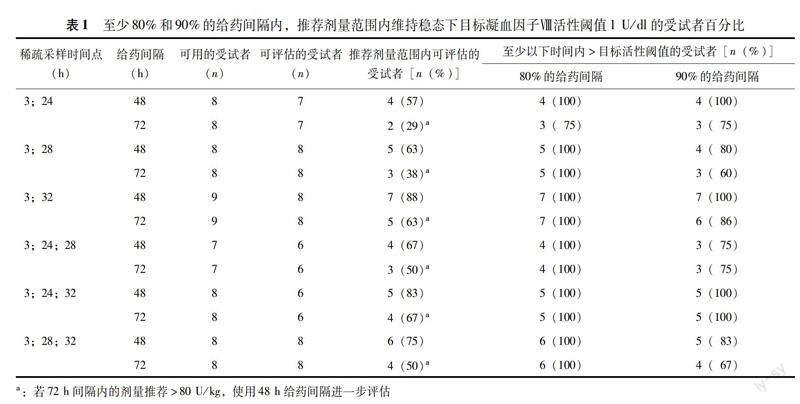
myPKFiT的符合目的分析结果 如果在指定时间点的所有FⅧ活性检测均高于1 U/dl的定量下限,则可评估给定受试者的稀疏采样方案,该受试者视为可用的受试者。根据每48 h或72 h给药以及6种稀疏采样方案,至少80%或90%的给药间隔时间(48或72 h)内FⅧ活性大于目标阈值(1 U/dl)的受试者百分比(推荐剂量范围内)。在各给药和稀疏采样方案的组合中,分别有7~9例可用的受试者,有6~8例通过输入核查(即可评估的受试者)。其中,myPKFiT给出的预测剂量在推荐剂量范围内且可评估的受试者占可评估人数的57%~88%,而且除1个方案组合外,其余均实现了在至少80%的给药间隔时间内大于目标阈值(表1)。因此,这些受试者可按此预测剂量进行方案调整。
无论给药间隔为48 h还是72 h,采样时间点在3 h和32 h时,预测剂量在推荐剂量范围内的比例均高达88%,且他们在给药间隔内维持在目标阈值以上的时间均超过80%。其中在每72 h给药时,8例受试者通过输入核查,其中2例的预测剂量在推荐剂量范围内,可维持稳态下FⅧ 活性目标阈值,因此可按此方案进行剂量调整;其余6例的预测剂量大于推荐剂量范围,根据给药指导规则,进一步按48 h间隔评估,其中5例的预测剂量在剂量推荐范围内。因此,共有7例可评估受试者的预测剂量在推荐剂量范围内,可在至少80%的给药间隔(72 h或48 h)内维持目标阈值。仅1例的预测剂量大于48 h间隔的推荐剂量范围,可考虑常规按体重给药(表1)。其他方案组合,可据此原则进行分析。
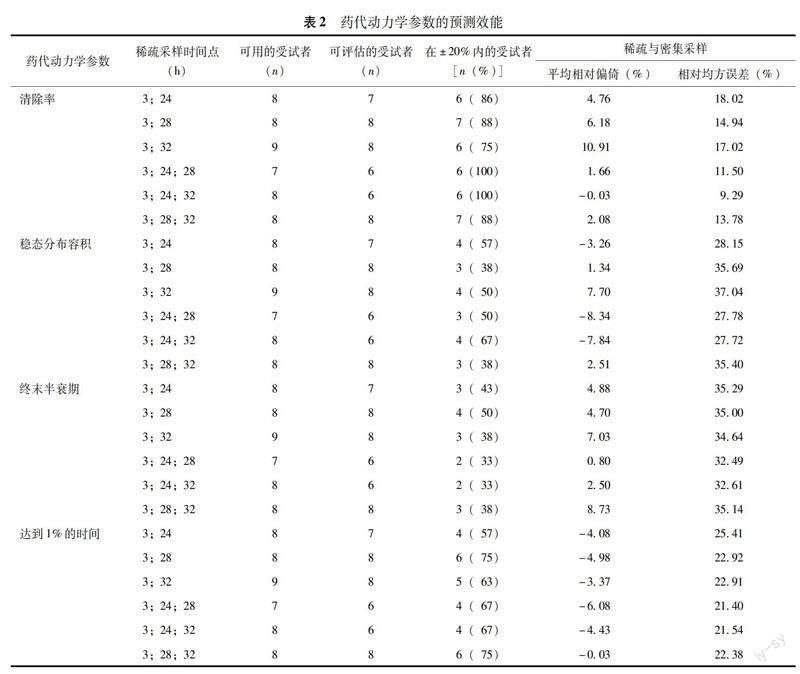
myPKFiT对PK参数的预测效能 对于不同稀疏采样方案,myPKFiT所得的PK估值与密集采样的估值差异≤20%的受试者百分比结果及相应的相对平均偏倚和相对均方误差结果显示,与密集采样比较,所有稀疏采样方案得到的清除率估值的差异≤20%的受试者比例均达75%~100%,达到1%的时间估值的差异≤20%的受试者比例达57%~75%。即使用myPKFiT和通过密集采样所得的上述两种PK参数估值相当(表2)。
讨论
血友病A预防治疗的目标是通过争取“零出血”降低致残率,改善生活质量。由于受年龄、体重、血型、血管性血友病因子等因素的影响,不同患者对FⅧ的代谢差异较大[6]。基于患者的PK特征制定的剂量方案可提供更为精准的个体化预防治疗,传统的密集采样方案采样次数多且需要洗脱期,临床应用受限。研究显示基于贝叶斯(Bayesian)算法研发的注射用人重组FⅧ PK相关辅助工具myPKFiT仅需2~3次采样即可实时可视化展现FⅧ活性变化曲线,警示出血风险,帮助患者确定适合自身的输注间隔和因子用量,为优化个体化治疗提供支撑[8-9,13]。
MyPKFiT的前期数据来自于注射用人重组FⅧ的3项Ⅰ/Ⅱ期PK研究[12,14-15],纳入青少年及成人重型患者100例、儿童重型患者52例,基于对他们超过2000次的FⅧ活性数据及236次注射用人重组FⅧ注射的评估,myPKFiT建立了个体化PK模型,研究显示输入3 h和24 h两次采样时间及FⅧ水平,myPKFiT即可预估每例患者的PK数据,输入目标谷值后即可模拟计算周剂量曲线图,同时可检验其数值是否在平均衰减曲线的95%置信区间内。由此,myPKFiT可为注射用人重组FⅧ生成预估的PK曲线,从而有助于医生为患者制定个体化预防治疗方案。随后多项研究证实基于myPKFiT进行剂量调整后带来的获益,如Mingot-Castellano等[9]的研究纳入36例接受注射用人重组FⅧ预防治疗的重度血友病A患者,调整为myPKFiT建议的方案后,在年总剂量没有增加的情况下,>15岁的患者年出血率和年关节出血率较前分别显著降低约2次。
本研究首次在中国重型青少年及成人血友病A患者中评估myPKFiT对维持FⅧ活性至目标阈值所需剂量的预测和指导价值,分别观察在注射用人重组FⅧ给药间隔为48 h或72 h时,在仅有2~3次FⅧ活性检测时达到目标阈值1 U/dl的比例,结果显示myPKFiT对57%~88%的可评估患者给出的预测剂量在推荐剂量范围内,其中绝大多数在80%以上给药间隔时间维持在目标阈值范围内,表明myPKFiT给出的预测剂量可使本研究多数患者的FⅧ活性水平维持在目标阈值以上。本研究2例患者的预测剂量在48 h或72 h给药间隔时均超过推荐剂量范围,个体PK特征分析显示,他们的清除率较高、半衰期较短以及达到1%的时间较短,这样的患者需要较短的给药间隔或较高的剂量,以维持目标FⅧ活性水平。
本研究显示无论给药间隔为48 h还是72 h,当采样时间点在3 h和32 h时,预测剂量在推荐范围的比例较高(88%),且所有患者在给药间隔内在目标阈值以上的时间超过80%,提示3 h和32 h的稀疏采样方案对于中国血友病A患者可能具有较高的预测指导价值。当给药间隔为48 h时,根据myPKFiT的给药指导规则,88%的可评估者可按预测剂量进行调整,仅1例应继续基于体重给药。当给药间隔为72 h时,8例可评估患者中2例可按myPKFiT的预测剂量每72 h给药,5例可按预测剂量每48 h给药,而剩余1例需继续基于体重给药。
在对PK参数的预测方面,myPKFiT从稀疏采样获得的PK参数估计值清除率和达到1%的时间与从密集采样获得的值相似,提示myPKFiT对这两个参数具有良好的预测性能。而终末半衰期和稳态分布容积这两个指标显示出潜在差异,这可能是由于一些观察到的FⅧ活性与时间曲线的显著变异性所致,多种参数组合可以产生基本相同的PK曲线。另外,有研究显示,FⅧ活性谷浓度及低FⅧ活性水平的维持时间较其他PK指标能更好地预测自发性出血风险[16]。中度血友病A患者 (FⅧ活性 1~5 U/dl)出血频率及关节病变的发生率均显著低于重型患者(FⅧ活性<1 U/dl)[17],而且随着FⅧ活性<1 U/dl的持续时间增加,自发性关节出血的发生风险增加[18]。因此,本研究将FⅧ活性水平维持在>1 U/dl的时间作为判断myPKFiT临床指导价值的主要评判指标。
本研究尚存在不足之处。首先,纳入的受试者人数为9例,属于小样本数据分析,后续尚需在真实世界中观察更多病例来明确myPKFiT的临床应用价值。其次,受试者有1例年龄<16岁(为15岁),体重<45 kg(为44 kg),尚不符合目前中国myPKFiT的适应证范围。国外已有研究显示myPKFiT在7~15岁患者中可获得与>16岁人群相似的临床获益[8],因此,其对于<16岁患者的指导价值也值得进一步观察和验证,以惠及更多患者。最后,本研究只分析了常用的48 h及72 h给药间隔的情况,对于需要缩短或延长给药间隔的方案仍需进一步结合群代模型指導治疗。
综上,本研究首次在中国血友病A患者中评估并证实myPKFiT对维持受试者FⅧ活性水平至目标阈值以上所需注射用人重组FⅧ剂量的预测作用,以及其对患者PK参数的预测效果。未来可以在更大样本量中观察并验证myPKFiT较基于体重的预防治疗方案在预防关节出血和病变方面以及FⅧ用量方面的获益。
(志谢:衷心感谢以下参与PTP研究的血友病中心及研究者:华中科技大学同济医学院附属协和医院胡豫、浙江大学附属第一医院金洁、中南大学湘雅医院赵谢兰、上海交通大学附属瑞金医院王学锋、首都医科大学附属北京儿童医院吴润晖、苏州大学第一附属医院吴德沛、中国医学科学院血液病医院杨仁池、福建医科大学附属协和医院杨凤娥、华中科技大学同济医学院附属同济医院胡群、沧州市中心医院王娟)
參 考 文 献
[1]中华医学会血液学分会血栓与止血学组,中国血友病协作组.血友病治疗中国指南(2020年版)[J].中华血液学杂志,2020,41(4):265-271.DOI:10.3760/cma.j.issn.0253-2727.2020.04.001.
[2]Funk MB,Schmidt H,Becker S,et al.Modified magnetic resonance imaging score compared with orthopaedic and radiological scores for the evaluation of haemophilic arthropathy[J].Haemophilia,2002,8(2):98-103.DOI:10.1046/j.1365-2516.2002.00585.x.
[3]Manco-Johnson MJ,Abshire TC,Shapiro AD,et al.Prophylaxis versus episodic treatment to prevent joint disease in boys with severe hemophilia[J].N Engl J Med,2007,357(6):535-544.DOI:10.1056/NEJMoa067659.
[4]Srivastava A,Santagostino E,Dougall A,et al.WFH guidelines for the management of hemophilia,3rd edition[J].Haemophilia,2020,26(Suppl 6):1-158.DOI:10.1111/hae.14046.
[5]Hazendonk HCAM,van Moort I,Matht RAA,et al.Setting the stage for individualized therapy in hemophilia:what role can pharmacokinetics play[J].Blood Rev,2018,32(4):265-271.DOI:10.1016/j.blre.2018.01.001.
[6]陈振萍,刘葳,蔡力生.药物代谢动力学指导血友病A治疗的中国专家共识[J].中国临床研究,2021,34(5):577-581.DOI:10.13429/j.cnki.cjcr.2021.05.001.
[7]Collins PW,Fischer K,Morfini M,et al.Implications of coagulation factor Ⅷ and Ⅸ pharmacokinetics in the prophylactic treatment of haemophilia[J].Haemophilia,2011,17(1):2-10.DOI:10.1111/j.1365-2516.2010.02370.x.
[8]lvarez-Román MT,Fernandez-Bello I,de la Corte-Rodríguez H,et al.Experience of tailoring prophylaxis using factor Ⅷ pharmacokinetic parameters estimated with myPKFiT in patients with severe haemophilia A without inhibitors[J].Haemophilia,2017,23(1):e50-e54.DOI:10.1111/hae.13141.
[9]Mingot-Castellano ME,Parra R,Núez R,et al.Improvement in clinical outcomes and replacement factor Ⅷ use in patients with haemophilia A after factor Ⅷ pharmacokinetic-guided prophylaxis based on Bayesian models with myPKFiT[J].Haemophilia,2018,24(5):e338-e343.DOI:10.1111/hae.13540.
[10]药物临床试验登记与信息公示平台.CTR20140434[EB/OL].(2014-07-07)[2022-11-09].http://www.chinadrugtrials.org.cn/clinicaltrials.searchlistdetail.dhtml.
[11]Zhao YQ,Hu Y,Jin J,et al.Phase 4 safety and efficacy study of antihemophilic factor (recombinant) in previously treated Chinese patients with severe/moderately severe hemophilia A[J].Clin Appl Thromb Hemost,2021,27:1076029621989811.DOI:10.1177/1076029621989811.
[12]Bjrkman S,Oh M,Spotts G,et al.Population pharmacokinetics of recombinant factor Ⅷ:the relationships of pharmacokinetics to age and body weight[J].Blood,2012,119(2):612-618.DOI:10.1182/blood-2011-07-360594.
[13]Pasca S,Zanon E.Savings without changing:how to use the myPKFiT device to improve treatment strategies in a cohort of patients with haemophilia A[J].Thromb Res,2019,183:1-3.DOI:10.1016/j.thromres.2019.08.022.
[14]Blanchette VS,Shapiro AD,Liesner RJ,et al.Plasma and albumin-free recombinant factor Ⅷ:pharmacokinetics,efficacy and safety in previously treated pediatric patients[J].J Thromb Haemost,2008,6(8):1319-1326.DOI:10.1111/j.1538-7836.2008.03032.x.
[15]Tarantino MD,Collins PW,Hay CRM,et al.Clinical evaluation of an advanced category antihaemophilic factor prepared using a plasma/albumin-free method:pharmacokinetics,efficacy,and safety in previously treated patients with haemophilia A[J].Haemophilia,2004,10(5):428-437.DOI:10.1111/j.1365-2516.2004.00932.x.
[16]Astermark J,Hart D,Lobet S,et al.Partnering to change the world for people with haemophilia:6(th) Haemophilia Global Summit,Prague,Czech Republic,24-26(th) September 2015[J].Eur J Haematol,2016,97(Suppl 84):3-23.DOI:10.1111/ejh.12761.
[17]Collins PW,Bjrkman S,Fischer K,et al.Factor Ⅷ requirement to maintain a target plasma level in the prophylactic treatment of severe hemophilia A:influences of variance in pharmacokinetics and treatment regimens[J].J Thromb Haemost,2010,8(2):269-275.DOI:10.1111/j.1538-7836.2009.03703.x.
[18]Collins PW,Blanchette VS,Fischer K,et al.Break-through bleeding in relation to predicted factor Ⅷ levels in patients receiving prophylactic treatment for severe hemophilia A[J].J Thromb Haemost,2009,7(3):413-420.DOI:10.1111/j.1538-7836.2008.03270.x.
(收稿日期:2022-09-02)
基金項目:国家自然科学基金(82070139)

