“微移动”在预防仰卧位手术患者术中骶尾部获得性压力性损伤中的效果研究
金亚仙,刘 静,申屠燕琴,宣飞飞,李玉红
树兰(杭州)医院, 浙江杭州 310006
压力性损伤(pressure injury,PI)是由持续的压力、剪切力或摩擦力引起的皮肤或皮下软组织的局部损伤,或两者兼而有之[1]。术中获得性压力性损伤(intraoperative acquired pressure injury,IAPI)指患者在手术过程中发生的PI,常发生于术后1~3 d[2],发生率高达4.7%~66.0%[3]。IAPI增加了患者生理和心理负担,随着PI的发生进展,患者术后并发症发生率上升,住院时间延长,由此增加护理难度及医疗资源的消耗,30 d内再次入院率和患者病死率也升高[2,4]。因此,预防IAPI发生受到高度重视,众多学者聚焦IAPI预防措施的研发与改进[5-6]。持续性压力直接作用于皮肤是发生PI的最主要原因之一[5]。翻身可以降低局部皮肤承受的压力,减少受压时间,既往研究强调预防PI最优策略为至少每隔2 h翻身1次,间隔时间至少15 min,30°侧卧位时,皮肤承受压力最小[7]。鉴于手术过程的特殊性,本研究团队提出“微移动”的概念,即每小时轮流向左或向右变换手术床角度15°,持续时间5 min,结合术中预防性使用硅胶泡沫软敷料,在降低仰卧位手术患者IAPI发生率方面取得较好效果。现报告如下。
1 对象与方法
1.1 对象
本研究方案已通过树兰(杭州)医院医学伦理委员会审核(批件号:2020074B)。采用G*Power 3.0.10软件进行样本量估算,以IAPI的发生率为样本量估算指标,以检验水准α=0.05、1-β=0.85,效应值0.22,两组例数相等进行估算,计算得样本总量186例。选择树兰(杭州)医院2020年1月21日至12月31日期间接受择期手术的患者200例。患者纳入标准:美国麻醉医师协会(American Society of Anesthesiologists,ASA)分级Ⅰ~Ⅱ级;年龄18~70岁;仰卧位,全身麻醉下实施择期腹部手术,预计手术时间≥2.5 h;术后拟返回外科病房。排除标准:术前已经存在PI的患者;患有影响PI观察的皮肤疾病,如湿疹、牛皮癣、白癜风或者身体着力部位皮肤合并感染的患者;机器人辅助腹腔镜手术的患者。剔除标准:术中出血量超过500 mL,出现休克、心博骤停需要大剂量血管活性药物的患者。所有患者了解研究过程,签署手术知情同意书后参加本研究。本研究为干预性前瞻性临床研究,采用随机分组、盲法设计。随机方法:采用Excel软件产生1~200之间不重复的随机整数,随机数字1~100为对照组,101~200为观察组。盲法:试验记录者和评估者、受试者以及数据统计者对处置方案不知情。
1.2 方法
两组除预防PI的干预措施不一致外,其余护理措施均保持一致。
1.2.1对照组
采用硅胶泡沫软敷料预防PI。患者进入手术室,经皮肤检查后,在患者骶尾部覆盖大小为12.5 cm×12.5 cm的硅胶泡沫软敷料。
1.2.2观察组
在对照组的基础上实施“微移动”方案。以麻醉诱导结束即刻为0时开始计时,同时按动手术床level键,建立“微移动”登记表,1 h后向右侧倾斜手术床15°,维持5 min,2 h后向左侧倾斜手术床15°,维持5 min,以此类推直至手术结束。
1.3 观察指标
1.3.1IAPI发生率
术后由对实施方案不知情的手术室护士及麻醉后复苏室(post-anesthesia care unit,PACU)护士两人共同评估患者骶尾部皮肤情况,两人意见不一致时,再请1名护士参加,以2对1的原则得出最后评估结果。评估标准:美国国家压力性损伤咨询委员会2019年PI分期标准[8],见表1。
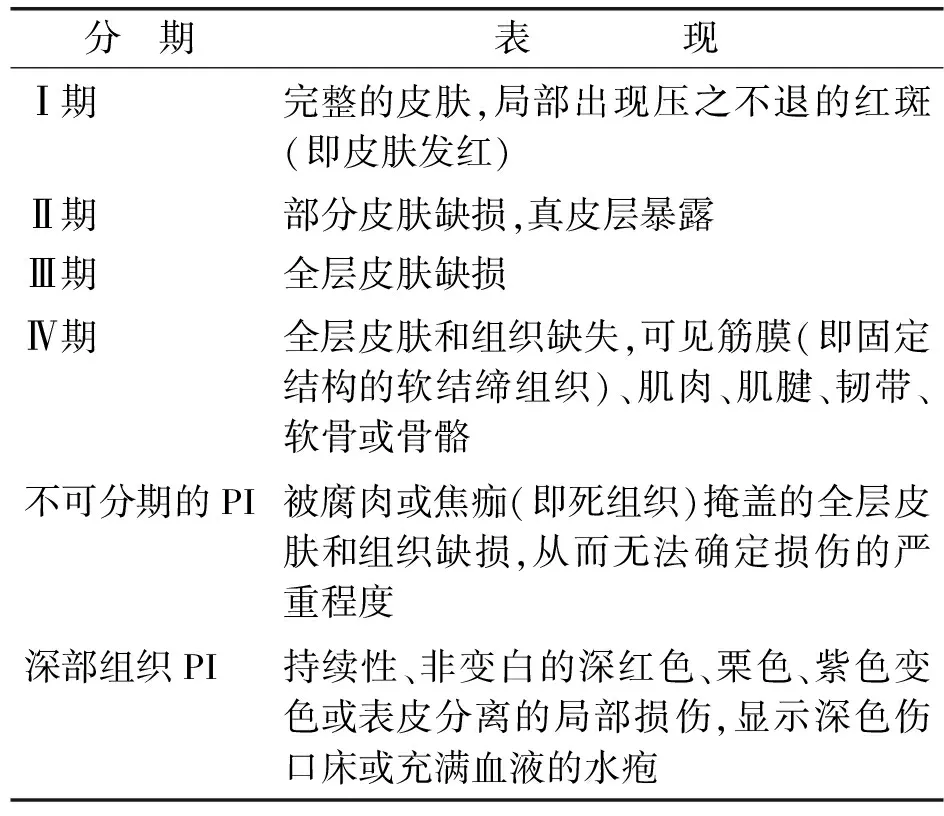
表1 2019年美国国家压力性损伤咨询委员会PI的分期及表现
1.3.2骶尾部皮肤相对温差
为减少室温、人为操作、身体不同部位温度不同等干扰因素的影响,用骶尾部皮肤相对温差描述骶尾部皮肤温度的变化。骶尾部皮肤相对温差(ΔT)是指试验区温度(骶尾部正中直径5 cm圆形区域内的平均温度,T1)与周围区域温度(身体中轴距尾骨10 cm以上直径5 cm圆形区域内的平均温度,T2)的温度差值(ΔT=T1-T2)[9]。测温于PACU内进行,测温时室温调节至24℃,患者入PACU后5 min内,PACU护士采用非接触式红外线体温计,距离测定区域3~5 cm,每个部位测量2次,取平均值。
1.4 统计学方法

2 结果
2.1 两组患者基本资料比较
两组患者性别、年龄、体重指数、术前血浆白蛋白浓度、术前合并疾病(糖尿病、高血压)、手术方式、手术种类、术中出血量、手术时间等基本资料比较差异无统计学意义(P>0.05),见表2。在研究期间,所有患者均未发生影响手术进程或坠床的不良事件。
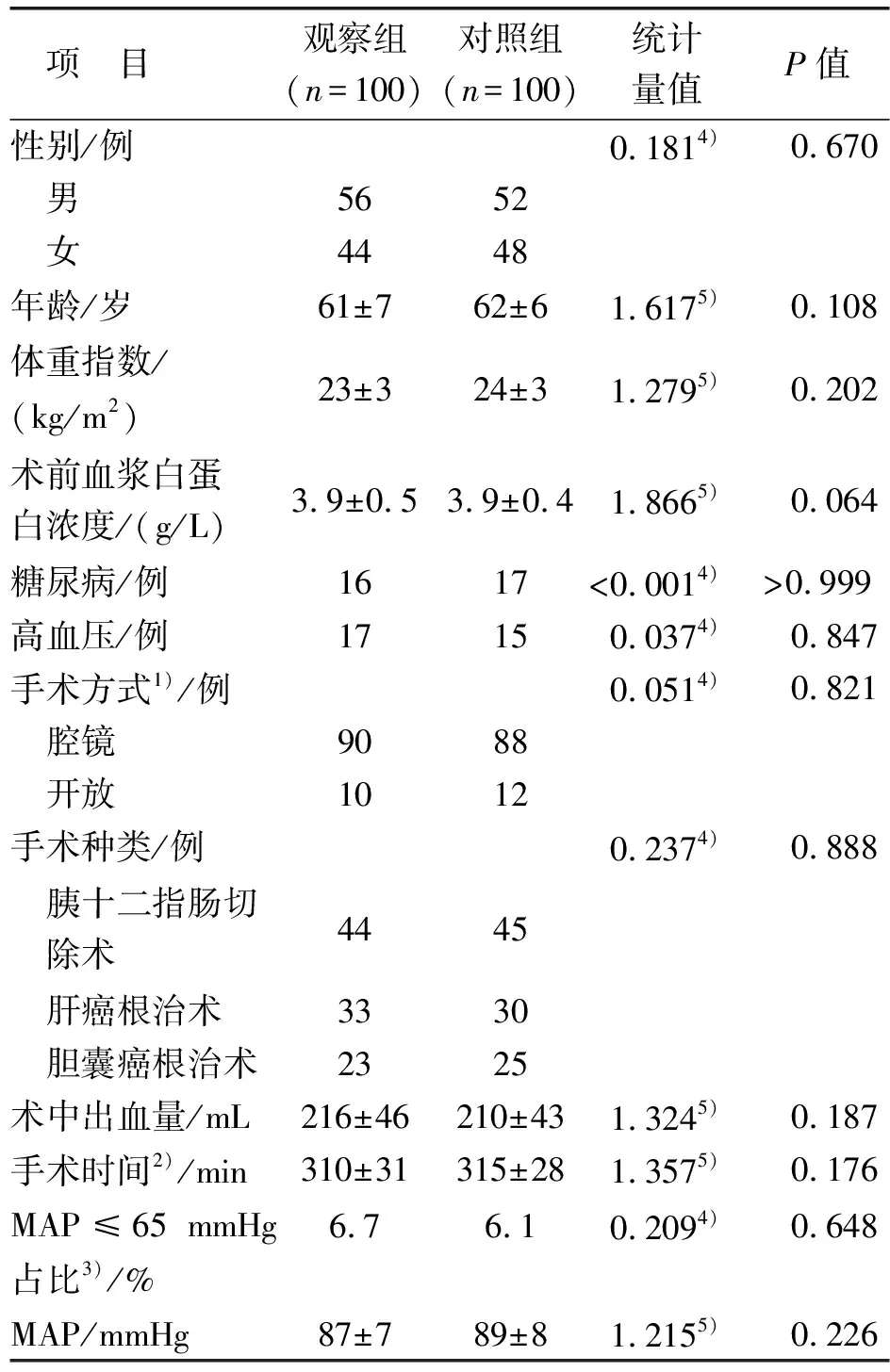
表2 两组患者基本资料比较
2.2 两组IAPI发生率及骶尾部皮肤相对温差比较
观察组100例中有2例发生IAPI(均为Ⅰ期),对照组100例中有10例发生IAPI(其中Ⅰ期8例、Ⅱ期2例),比较差异有统计学意义(2=4.344,P=0.037)。两组骶尾部皮肤相对温差比较差异有统计学意义(Z=-3.661,P<0.001)。两组患者IAPI发生率和骶尾部皮肤相对温差比较见表3。
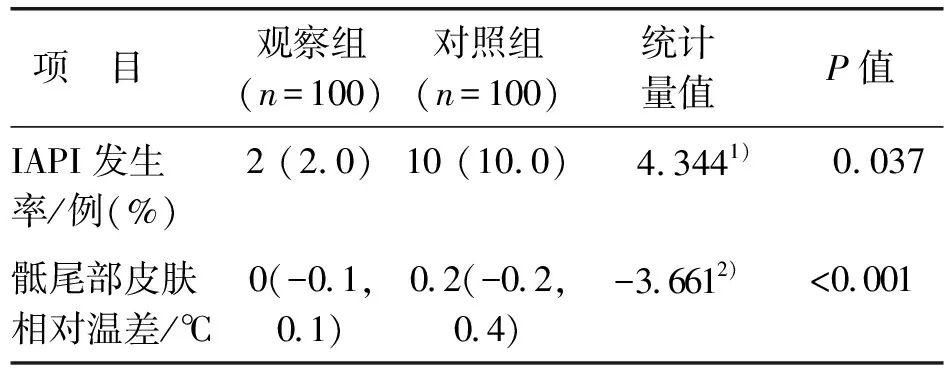
表3 两组患者IAPI发生率和骶尾部皮肤相对温差比较
3 讨论
3.1 IAPI的发病机制
IAPI的形成是一个复杂的过程,与麻醉分级、体重指数、术前肢体活动、受压部位皮肤状态、支撑面、术中血压、体温、出血量及手术时间等诸多因素相关[10]。其中垂直压力是PI发生的直接原因,一方面,局部组织细胞长时间持续受压,导致细胞形态和结构改变,另一方面当局部组织长时间承受超过正常毛细血管压力16~32 mmHg的垂直压力,可能使局部血流受阻,导致受压组织或器官微循环障碍、发生缺血缺氧性损伤,进一步发展为PI[6]。当受压组织缺血一段时间后血流重新恢复时,中性粒细胞和巨噬细胞聚集,炎性因子和氧自由基大量释放及钙超载等引起一连串逐级放大的损伤反应,最终造成细胞不可逆的损伤,即发生再灌注损伤,缺血-再灌注损伤已经被证实是PI发生的重要机制[11]。临床试验发现手术时间>6 h是发生PI的独立危险因素,手术时间>4 h,每增加0.4 h,PI的风险增加33%[12]。仰卧位的手术患者身体着力部位是枕部、肩胛部、骶尾部、足跟部,其中骶尾部IAPI发生率占比85%以上[13]。
3.2 “微移动”可以降低仰卧位手术患者骶尾部IAPI发生率
预防IAPI是手术中护理工作重点。相对于病房定时翻身减压有效预防PI,手术患者需要固定体位,从而导致局部持续压力时间过长,是预防IAPI的最大难点。随着手术时间延长,皮肤和相应组织的受压时间亦会延长,局部组织血流量减少,增加无氧代谢,加重组织缺氧程度,进而增加IAPI的风险[13]。因此临床实践指南强调PI的预防原则:使所有骨隆突处的压力最小化,使压力得到最大限度的重新分配。然而传统的凝胶垫、棉垫、泡沫辅料等支撑面只是通过增加受力面积来缓解压力,无法做到压力重新分配。变化体位,即翻身,是指患者身体的移动,能重新分配压力和剪切力,有效预防着力部位长时间持续受压[7]。身体横向倾斜,头部保持正常仰卧位的位置是预防骶尾部和枕部PI的有益干预措施,对于术中或者ICU气管插管的患者,这种体位摆放还可防止气管导管移位[14]。本研究团队致力于探讨仰卧位手术中通过手术床的“微移动”实现手术患者骶尾部的压力重新分配,降低IAPI发生率。国际手术室护士协会推荐,在不影响手术的情况下,每2 h变换体位 1次[15],由于手术过程中术野暴露和无菌的要求,定时变换体位的实施有一定难度。本研究利用手术床的固有功能,对患者术中每间隔1 h实施1次“微移动”,避免因“微移动”影响术者操作,“微移动”角度设定在15°,减压时间设定为5 min,每次操作前与术者充分沟通后实施。本研究结果显示,观察组发生2例IAPI,对照组发生10例,比较差异有统计学意义(2=4.344,P=0.037),提示“微移动”能降低仰卧位手术患者IAPI发生率。“微移动”可能通过着力部位压力的再分配,实现了降低骶尾部的垂直持续压力,防止因局部长时间受压导致血液循环受阻,因此切断了IAPI的形成机制,从而降低IAPI的发生率。
3.3 “微移动”可以降低仰卧位手术患者骶尾部皮肤相对温差
皮肤表面温度是导致PI发生的一个内在因素。PI发生前24~96 h,皮肤表面温度可升高1.28℃,皮肤温度不仅是PI发生的预警指标[16],还可以预测PI的治疗效果[17]。正常组织皮肤表面相对温差集中分布于0℃左右[5]。皮肤的各种损伤可能会显著影响皮肤血流,进而影响皮肤温度,炎症会导致体温升高,而灌注不良是导致体温过低的原因[17]。仰卧1 h会导致皮肤温度升高约3℃[18],皮肤温度每升高1℃,对反应性充血(缺血的一个指标)的影响就相当于皮肤界面压力增加8~15 mmHg[19],从而导致PI发生率上升。本研究结果显示,观察组患者骶尾部皮肤相对温差为0(-0.1,0.1)℃,对照组为0.2(-0.2,0.4)℃,比较差异有统计学意义(Z=-3.661,P<0.001),提示“微移动”可能可降低仰卧位手术患者骶尾部皮肤相对温差从而降低IAPI发生率。
3.4 本研究的局限性
本研究中的“微移动”方案仅用于仰卧位手术,在侧卧位或俯卧位等手术的应用效果还不明确。本研究样本量较小,且来自单中心,仍需大样本的临床研究进一步证实本研究结论。

