肠道支架置入联合腹腔镜手术治疗梗阻性左半结肠癌的临床疗效观察
杨智岗,车鸣桦,黄海,何承祥
上海市普陀区利群医院普外科 上海 200333
结直肠癌是常见的消化道恶性肿瘤[1]。8%~29%的结直肠癌患者伴有急性肠梗阻症状[2]。而左半结肠因管腔狭小、肠腔水分少,是梗阻好发的位置[3]。据文献报道,75%的结肠梗阻发生于乙状结肠、降结肠和直肠[4]。对于梗阻性左半结肠癌,传统的治疗方法是行急诊开腹手术解除梗阻,一期行肿瘤切除并行肠造口,二期行肠造口闭合术[5]。然而,急诊手术风险大、死亡率高,且二次手术容易增加患者的生理、心理和经济负担。20世纪90年代以来,金属支架广泛应用于结直肠狭窄性病变的治疗,为肠梗阻急诊手术向限期手术的转变创造了条件[6]。本研究回顾性分析我院普外科2016 年1 月至2022 年6 月收治的28 例梗阻性左半结肠癌患者,评价肠道支架置入联合腹腔镜手术治疗梗阻性左半结肠癌的临床疗效,现报道如下。
1 资料与方法
1.1 一般资料
选取我院普外科2016年1月至2022年6月收治的28例梗阻性左半结肠癌患者为研究对象,所有患者均行肠道支架置入联合腹腔镜手术。其中男性16例,女性12例;年龄59~85岁,平均年龄(73.4±10.6)岁。结肠脾曲3 例,降结肠8 例,乙状结肠9 例,直肠8例。本研究经医院伦理委员会审批通过,所有患者对手术知情同意并签署知情同意书。
1.2 纳入与排除标准
纳入标准:(1)符合梗阻性左半结肠癌的诊断标准[7]。症状表现为恶心、呕吐、腹部胀痛、肛门停止排气和排粪。腹部CT提示左半结肠肠壁增厚,近端肠腔扩张伴有气液平;(2)年龄18~85岁,性别不限;(3)一般情况尚可,可耐受手术。排除标准:(1)术前考虑肠穿孔;(2)接受过放化疗;(3)合并糖尿病、严重心脑血管疾病、呼吸系统疾病、凝血功能障碍,经内科治疗后病情无改善者。
1.3 治疗方法
(1)肠道支架置入术。患者入院后完善肠镜前准备,用生理盐水行清洁灌肠,保证远端肠腔视野清楚。肠镜下寻腔进镜至结肠肿瘤狭窄处,冲洗肠腔,去除肿瘤表面污秽,显露肠腔间隙。沿着肠腔间隙插入斑马导丝,使其通过肿瘤狭窄段(图1)。沿导丝置入造影管,通过造影明确导丝已通过狭窄段,并判断肿瘤长度,选择合适长度的金属支架,沿导丝插入支架(图2),保证支架两端均超过肿瘤2 cm左右后释放肠道支架(图3),观察支架释放过程是否有粪液流出,待支架放置牢固后退出肠镜(图4)。

图1 斑马导丝穿过肿瘤狭窄段
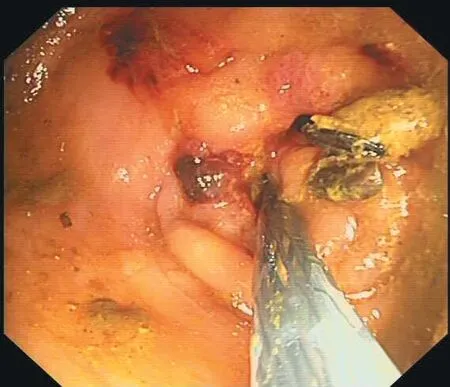
图2 沿导丝插入肠道支架
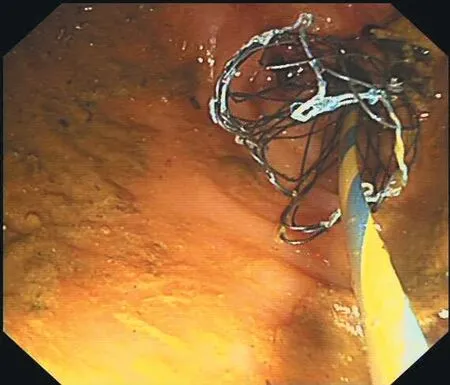
图3 释放肠道支架
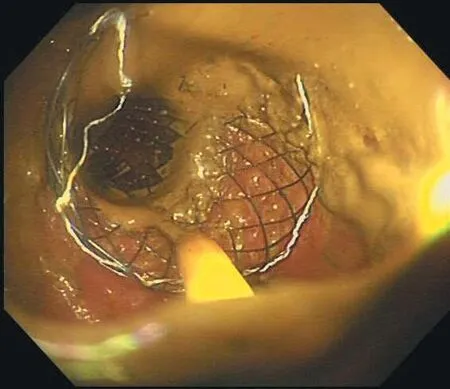
图4 肠道支架成功置入后改变
支架放置成功后,当天禁食禁水,常规予以抗感染补液治疗,并密切观察患者腹部体征及排粪、排气情况。第2天予以流质或半流质饮食,可根据化验结果来纠正电解质紊乱、进行肠内营养或肠外静脉营养等治疗。期间复查腹部平片或腹部CT,待肠梗阻症状缓解,且无支架移位脱落、肠穿孔等并发症发生后方可进行后续腹腔镜手术。一般在肠道支架置入术后2周实施腹腔镜手术,根据肿瘤的位置不同,采取相应的腹腔镜左半结肠癌根治术、腹腔镜乙状结肠癌根治术或腹腔镜直肠癌根治术。分别按照常规手术步骤进行全结肠系膜切除术和全直肠系膜切除术,不常规行预防性造口术。
(2)腹腔镜手术。①腹腔镜左半结肠癌根治术:患者取平卧位,常规5孔法操作。分离左半结肠系膜(图5),清扫肠系膜下动脉根部淋巴结(第253组)、结肠中动脉左支淋巴结、结肠左动脉淋巴结、乙状结肠动脉淋巴结及直肠上动脉淋巴结。沿Toldt间隙游离左半结肠,根据切除肠管的范围,保留足够的血供。延长脐上切口约5 cm,拖出游离的左半结肠,于肿瘤上下各10 cm处切断横结肠左侧及乙状结肠,行结肠端侧吻合。②腹腔镜乙状结肠癌根治术、腹腔镜直肠癌根治术:患者取半截石位,常规5孔法操作。切开乙状结肠系膜,清扫肠系膜下动脉根部淋巴结,在系膜根部切断肠系膜下动脉和静脉(图6)。分离直肠前、后间隙,切断乙状结肠系膜及直肠系膜,于肿瘤下端3~5 cm 处切断肠管。延长脐下切口约5 cm,拖出游离的肠管,切断肿瘤近端肠管,置入吻合器蘑菇头后重新建立气腹,经肛行结直肠端端吻合。
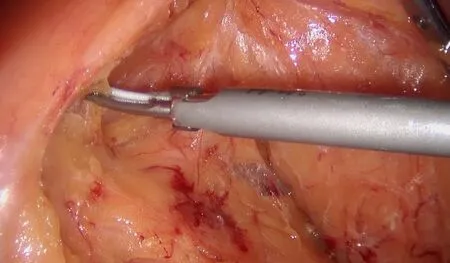
图5 分离左半结肠系膜

图6 离断肠系膜下动脉和静脉
1.4 观察指标
(1)肠道支架置入情况。观察记录肠道支架置入情况,肠道支架置入成功是指肠道支架能成功通过肿瘤狭窄段,支架两端开口超过肿瘤2 cm 以上,并可见粪液流出。
(2)相关临床指标。比较患者入院时和腹腔镜手术前的相关临床指标:白细胞计数、血红蛋白、白蛋白、血钾。
(3)腹腔镜手术情况。观察记录腹腔出血、切口感染、肠造口、吻合口漏、围手术期死亡等情况。
1.5 统计学分析
采用SPSS 25.0 统计学软件进行数据处理。计量资料以(±s)表示,比较采用t检验;计数资料以(n)表示。P<0.05为差异有统计学意义。
2 结果
2.1 肠道支架置入情况
所有患者均成功置入肠道支架,无肠道支架移位、脱落或肠穿孔。所有患者2周后均行腹腔镜手术。
2.2 患者入院时和腹腔镜手术前的相关临床指标比较
腹腔镜手术前患者的白细胞计数、血红蛋白水平、白蛋白水平、血钾浓度均优于入院时,差异有统计学意义(均P<0.05)。见表1。
表1 患者入院时与腹腔镜手术前的相关临床指标比较 ±s
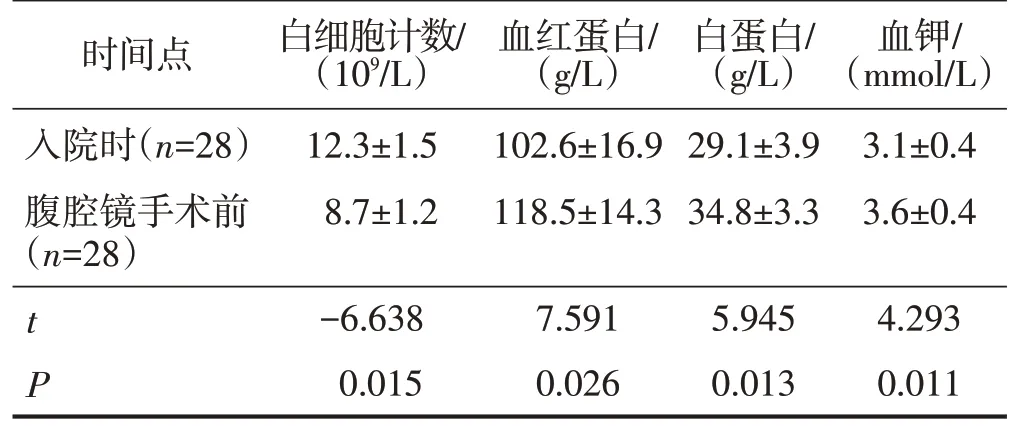
表1 患者入院时与腹腔镜手术前的相关临床指标比较 ±s
时间点入院时(n=28)腹腔镜手术前(n=28)t P白细胞计数/(109/L)12.3±1.5 8.7±1.2-6.638 0.015血红蛋白/(g/L)102.6±16.9 118.5±14.3 7.591 0.026白蛋白/(g/L)29.1±3.9 34.8±3.3 5.945 0.013血钾/(mmol/L)3.1±0.4 3.6±0.4 4.293 0.011
2.3 腹腔镜手术情况
腹腔镜手术后无腹腔出血患者,2例出现切口感染,3例行预防性末端回肠造口术,并于造口术后3个月后行造口还纳术,其中1例出现吻合口漏。上述患者经保守治疗后均痊愈出院,无围手术期死亡病例。
3 讨论
梗阻性左半结肠癌是结直肠外科较为棘手的问题[8]。梗阻性左半结肠癌患者由于回盲瓣的特殊结构,肿瘤生长容易造成闭襻性梗阻,肠内容物大量淤积,导致肠管扩张明显,肠壁组织水肿加剧,破坏了肠黏膜正常屏障功能,钾离子大量聚集在肠道内,容易引起低钾血症,进而导致四肢乏力、心律失常、呼吸困难等全身症状。此外,肠梗阻也可使肠道内细菌大量繁殖,并产生大量毒素,吸收入血后引起严重的感染,不及时干预会出现感染性休克而危及生命。梗阻性左半结肠癌传统治疗主张分期手术,手术方式包括:(1)一期肿瘤切除+近端结肠造口术,二期消化道重建术,即Hartmann 术式;(2)一期肿瘤切除+结肠吻合+吻合口近端结肠或末端回肠保护性造口术,二期造口关闭术;(3)一期结肠次全切除+肠吻合术等[9]。但是分期手术的住院时间往往较长,且一期急诊手术切除肿瘤,患者多处于急性炎症期,肠管等组织水肿严重,解剖结构不清晰,分离组织时易出血,淋巴结清扫往往不够彻底,术中进行肠减压等操作,不仅增加手术时间,还会增加切口感染的机会,手术风险较大[5,10]。据国外文献报道,急诊手术的死亡率为15%~20%[11],术后并发症发生率高达39%[12],40%的患者因身体原因无法耐受二期造口闭合术[13]。随着内镜下肠道支架置入技术的成熟,通过放置肠道支架缓解肠梗阻症状,待肠道功能恢复正常后进行有效的术前肠道准备,再实施腹腔镜手术,可避免急诊手术,减少肠造口[14-15]。
然而,关于肠道支架置入多久后实施腹腔镜手术目前尚无定论。陶玉荣等[16]研究表明,肠道支架置入后3 d 进行手术治疗是可行的。但也有研究表明,肠道支架后越早实施手术,肠道水肿越严重,手术并发症发生率和造口率也越高[15,17-18]。另有研究报道,肠道支架置入后10~14 d进行腹腔镜手术,可有效减少并发症的发生[19-20]。因此,肠道支架置入术后多久进行腹腔镜手术需要结合患者的肠道恢复情况及全身各项临床指标来确定。根据文献报道并结合临床经验,笔者团队决定于成功置入肠道支架2周后进行腹腔镜手术。
梗阻性左半结肠癌多见于高龄患者[21]。本研究纳入的28 例患者,平均年龄为73.4 岁,入院时表现出不同程度的低蛋白血症、低钾血症、感染及贫血。所有患者均在肠镜下成功置入肠道支架,无肠道支架移位、脱落或肠穿孔等现象,且所有患者2周后均行腹腔镜手术。研究结果显示,腹腔镜手术前患者的白细胞计数、血红蛋白水平、白蛋白水平、血钾浓度均优于入院时(均P<0.05),提示放置肠道支架有助于纠正低蛋白血症、电解质紊乱、贫血等问题,一定程度上缓解了肠梗阻的症状。术前2周进行抗感染治疗,也显示出了一定的有效性。腹腔镜手术后,28 例患者无腹腔出血患者,2 例出现切口感染,3 例行预防性末端回肠造口术,并于造口术后3个月后行造口还纳术,其中1例出现吻合口漏,经保守治疗后均痊愈出院,无围手术期死亡病例。总的来说,该腹腔镜手术较为成功,虽然出现切口感染和吻合口漏病例,但所有患者经治疗后均痊愈出院,无死亡病例,提示肠道支架置入联合腹腔镜手术可以实现术前有效的肠道准备,使临床医师能够进行术前肠镜检查,排除近端结肠病变,可减少术前的漏诊,有助于腹腔镜手术的顺利实施,对减少术后并发症有积极意义[22]。此外,多项研究表明,肠道支架置入联合腹腔镜手术是梗阻性结直肠癌的有效手术方式,与本研究结果一致[10,23-24]。
综上所述,肠道支架置入联合腹腔镜手术治疗梗阻性左半结肠癌安全可靠,术前先行肠道支架置入可有效地缓解肠梗阻症状,为进一步的腹腔镜手术提供了良好的机会。但本研究的样本量偏小,且缺乏对照组,所得结论存在一定的局限性,未来仍需进行更大样本量的临床随机对照试验加以证实。
利益冲突声明全体作者均声明不存在与本文相关的利益冲突。