卡瑞利珠单抗联合仑伐替尼治疗肝癌的效果及对肿瘤标志物的影响
陈灿敏,王育衡
(福建医科大学附属龙岩第一医院,福建 龙岩 364000)
作为临床常见的恶性肿瘤之一,肝癌发病率为257/1000万,死亡率为2037/1000万,居恶性肿瘤死亡第二位。对于患者而言,肝癌可导致患者出现腹痛、腹胀、恶心、呕吐、黄疸以及腹水等一系列症状[1]。患病后,若不能及时进行合理干预,则癌细胞可出现扩散与转移,继而对患者生命安全构成了极大危害[2]。在此期间,有研究显示,免疫治疗可以促进患者病情的控制与缓解。临床研究显示,通过免疫治疗后,患者PFS由5.5个月增至10.7个月,由此可见,这一疗法可以有效促进患者病情的合理控制,对于患者健康的保障具有一定的价值。同时,在采用免疫联合治疗后,患者预后1年的OS率可达到67.2%[3]。本文分析了卡瑞利珠单抗联合仑伐替尼治疗肝癌的效果,现整理报道如下。
1 资料与方法
1.1 一般资料
在2021年1月~2023年1月选取82例肝癌患者作为研究对象,采用随机数字列表法将其分为两组,对照组:男25例,女16例;年龄35~72岁,平均(54.22±2.47)岁;肝功能Child-Pugh分级A级6例,B级20例,C级15例;体质量52~91kg,平均(70.25±3.56)kg;疾病分期:II期19例,III期22例;研究组:男27例,女14例;年龄38~71岁,平均(54.31±2.66)岁;肝功能Child-Pugh分级A级8例,B级21例,C级12例;体质量56~90kg,平均(70.64±3.17)kg;疾病分期:II期20例,III期21例;相关内容已经上报伦理委员会并获得审批。两组患者一般资料差异无统计意义(P>0.05)。
1.2 纳入及排除标准
1.2.1纳入标准
(1)所有患者及其家属均对本次研究内容表示知情同意。(2)患者符合临床领域对于肝癌的诊断标准。(3)患者精神状态良好,可以配合医疗人员进行药物治疗。
1.2.2排除标准
(1)患者年龄>80周岁。(2)患者合并其他恶性肿瘤问题。(3)患者合并其他重要脏器功能障碍。(4)患者对于本次研究涉及的药物过敏。(5)患者在近1周内接受过其他药物治疗[4]。
1.3 方法
1.3.1对照组
采用仑伐替尼(国药准字HJ20200044)治疗,药物用法用量如下:口服,药用使用剂量依据患者个性情况进行调整。其中,体重<60kg的患者,8mg/次,1次/d,体重≥60kg的患者,12mg/次,1次/d,3周为1个疗程,连续治疗2个疗程。
1.3.2研究组
采用卡瑞利珠单抗(江苏恒瑞医药股份有限公司,国药准字S20190027)联合仑伐替尼治疗,其中,仑伐替尼用法用量同上。卡瑞利珠单抗用法用量如下:在每个疗程治疗的第1d对患者进行静脉滴注,将200mg药物与 0.9%的氯化钠注射液100mL混合摇匀后给药,持续滴注30min。滴注结束后指导患者进行仑伐替尼的口服。连续治疗2个疗程。
1.4 观察标准
1.4.1患者治疗客观缓解率
所有患者均在接受治疗2个月后结合影像学检查对于病灶情况进行评估。采用RECIST1.1进行评效。完全缓解(CR):所有靶病灶消失,全部病理淋巴结(包括靶结节和非靶结节)短直径必须减少至<10mm。部分缓解(PR):靶病灶直径之和比基线水平减少至少30%。疾病进展(PD):以整个研究过程中所有测量的靶病灶直径之和的最小值为参照,直径和相对增加至少20%(如果基线测量值最小就以基线值为参照);除此之外,必须满足直径和的绝对值增加至少5mm(出现一个或多个新病灶也视为疾病进展)。疾病稳定(SD):靶病灶减小的程度没达到PR,增加的程度也没达到PD水平,介于两者之间,研究时可以直径之和的最小值作为参考。客观缓解率(Objective response rate,ORR)= CR+PR。
1.4.2患者肿瘤标志物
包括癌胚抗原(CEA)正常参考范围是0~5ng/mL、血清甲胎蛋白(AFP)正常参考范围是0~25μg/L以及糖类抗原199(CA199)正常参考范围是0~37 U/mL。
1.4.3患者不良反应发生率
包括神经毒性、胃肠道不适、肝脏毒性、血压异常以及心脏功能异常。
1.5 统计学方法
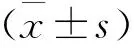
2 结果
2.1 患者治疗有效性对比
研究组客观缓解率是65.85%,对照组的是34.15%,研究组更高(P<0.05)。见表1。

表1 患者治疗有效情况
2.2 肿瘤标志物对比
研究组治疗前CEA、AFP以及CA199的指标分别是(34.66±2.31)ng/mL、(332.46±12.78)ng/mL、(254.70±10.45)U/mL;对照组治疗前CEA、AFP以及CA199的指标分别是(34.65±2.28)ng/mL、(333.27±13.69)ng/mL、(254.47±11.65)U/mL;统计计算结果显示,两组患者这三个指标的无统计学差异。经过治疗后,两组患者这三个指标均降低。研究组治疗后CEA、AFP以及CA199的指标分别是(18.12±1.22)ng/mL、(108.45±6.85)ng/mL、(178.45±5.24)U/mL;对照组治疗前CEA、AFP以及CA199的指标分别是(22.69±2.02)ng/mL、(135.65±7.67)ng/mL、(223.66±7.31)U/mL,对比数据可以发现,研究组患者的降低幅度更大(P<0.05)。见表2。
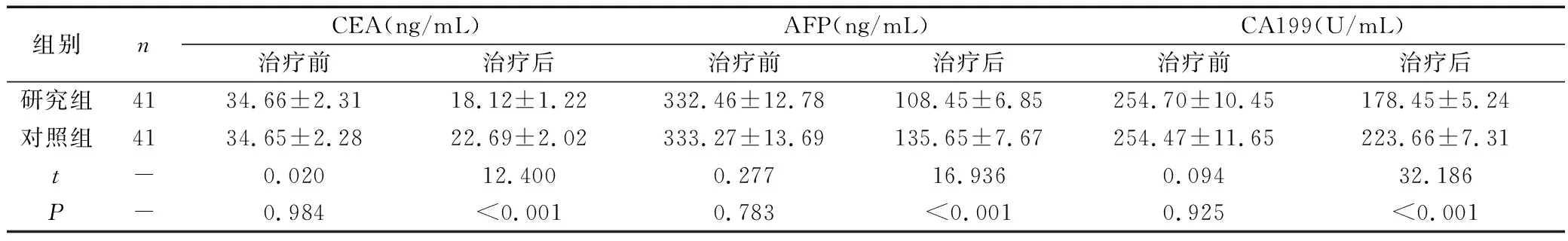
表2 肿瘤标志物水平
2.3 不良反应发生情况
研究组不良反应发生率是12.20%,对照组不良反应发生率是17.07%,两组不良反应发生率无统计学差异(P>0.05)。见表3。
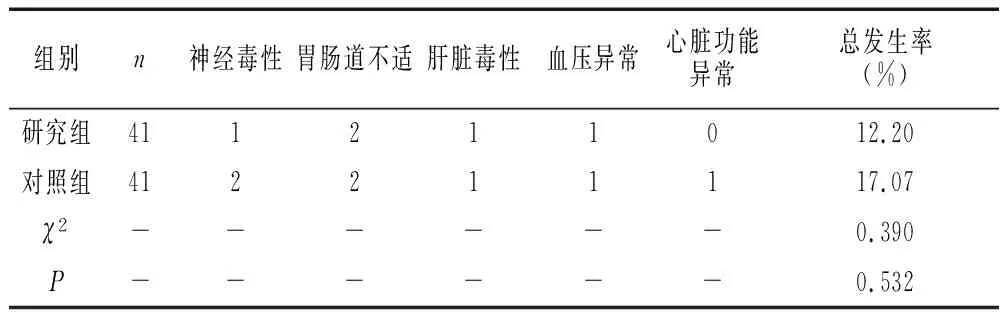
表3 患者不良反应发生情况
3 讨论
肝癌对于患者身心健康的危害极大。在日常生活中,病毒性肝炎、饮食不节、遗传因素以及长期饮酒等均有可能导致肝癌。在临床过程中患者常用药物治疗[5]。临床实践表明,抗肿瘤药物可以帮助患者激活自身免疫系统,对于患者免疫内环境的稳定具有积极作用。其中,作为肝癌一线治疗药物,仑伐替尼属于酪氨酸激酶受体抑制剂,其可以对血管内皮生长因子受体VEGFR1、VEGFR2以及VEGFR3的活性进行抑制[6]。有研究表明,该药物还可以抑制肿瘤病理性血管的生成,有利于控制瘤体生长[7]。实践表明,该药物还可以进一步促进患者免疫功能的持续优化与改善,其对于患者异常血管再正常化具有一定的促进意义。卡瑞利珠单抗属于抗PD-1人源化单克隆抗体,是我国自主研发的一类免疫检查点抑制剂药物[8]。该药物可以选择性的与患者体内的PD-1受体相结合,从而抑制其和PD-L1之间的相互作用,有助于阻断PD-1通路介导的免疫抑制反应。,实现对于T细胞免疫功能的恢复,有效规避了肿瘤细胞免疫逃逸问题的出现[9]。在临床研究过程中,医疗人员在肝癌患者治疗过程中往往将其肿瘤标志物水平作为评估患者治疗是否有效的依据。较为常用的标志物包括CEA、AFP以及CA199。CEA与CA199是较为常见的肿瘤标志物,其在肿瘤患者血清中具有高水平表达,可以帮助医疗人员评估患者肿瘤的成长情况。相比之下,AFP的表达水平可以帮助医疗人员对于患者肝癌严重程度进行评估与分析[10]。在临床过程中,部分研究资料指出,通过及时采用卡瑞利珠单抗与仑伐替尼进行联合治疗,上述指标均可以得到显著的控制,这一点与本文研究结果具有较强的一致性。
本次研究结果指出,通过采用卡瑞利珠单抗联合仑伐替尼治疗,患者的临床疗效可有所提升,且肿瘤标志物指标均得到了进一步的改善。由此可见,卡瑞利珠单抗联合仑伐替尼治疗对患者病情的控制具有良好的促进作用。与此同时,与单一使用仑伐替尼治疗相比,联合治疗组患者的不良反应发生率无统计学差异,证实了联合用药治疗方案在患者治疗期间具有较高的安全性。

