一期OLIF与TLIF治疗单节段腰椎结核的对比研究
木热提·卡哈尔,地力木拉提·艾克热木,徐阔,乌其坤·阿里玛斯,王浩
(新疆维吾尔自治区人民医院骨科中心脊柱二病区,新疆 乌鲁木齐 830000)
根据世界卫生组织的数据,2018年全球约有1 000万人感染了结核病,约有124万患者死于结核病[1]。在我国此病主要集中在经济较不发达的中西部偏远地区及西北乡村。作为一种全身性疾病,结核病可波及全身各个系统,尤其大的关节,比如脊柱、髋关节、膝关节、踝关节等,其中脊椎结核较为多见,其发生率为50%,主要发生于免疫力低下和老年患者[2]。脊柱结核早期不表现出典型症状,主要为腰背部疼痛,早期发现可通过正规抗结核治疗达到治愈。当相应椎体出现骨质破坏、周围形成脓肿、脊柱后凸畸形,出现相应的神经系统表现或出现截瘫等时考虑进行外科手术[3]。
1911年,阿尔比(Albee)和希布斯(Hibbs)描述了一种后路腰椎间融合治疗腰椎结核的方法。自此,使用后路腰椎间融合固定成为一种主流。后期技术的提升又出现采用后路正中切口病灶清除联合植骨融合内固定(posterior lumbar interbody fusion,PLIF)治疗腰椎结核,该技术主要用于治疗轻度病例,但后路手术存在增加手术创伤、手术时间和对原本无感染的中后柱可能带来继发性感染而且有时无法直视下对病灶清除等不足[4]。经椎间孔腰椎椎体间融合(transforaminal lumbar interbody fusion,TLIF)是Cloward在20世纪50年代描述的PLIF技术的一种改良术式,是目前广泛应用的脊柱融合技术之一。与PLIF相比,TLIF保留了韧带复合体、椎板和小关节,从而保持了脊柱的稳定性[5],但其对脊神经存在激惹、植骨融合不充分、术后出现慢性腰背部疼痛的可能。随着技术的不断改进,近几十年来发展了几种融合方法,其中前路腰椎间融合(anterior lumbar interbody fusion,ALIF)手术治疗腰椎结核已得到广泛应用,并取得了良好的临床效果。前路清创固定一直是腰椎结核的经典手术治疗方法,但前路手术存在手术创伤大、解剖结构复杂、多节段性病变难以处理等不足,目前不作为脊柱结核的首选方法[10-11]。近几年来,作为一种微创且安全的手术技术,斜外侧椎体间融合(oblique lumbar interbody fusion,OLIF)已被广泛用治疗进展性腰椎疾病[6-7]。该技术于1997年由Mayer等[8]首次提出,2012年由Silvestre等[9]正式命名为“OLIF”。应用这项技术可以减少失血,大面积去除死骨及椎旁脓肿,植骨接触面大,对多节段破坏进行有效处理,加快恢复、降低神经损伤的可能。
本研究回顾性分析2018年1月至2021年5月新疆维吾尔自治区人民医院收治的腰椎结核患者资料,将OLIF及TLIF两项术式治疗结果进行对比评价分析,目的在于:(1)探讨两种术式对腰椎结核的有效性;(2)总结两种术式治疗腰椎结核的适应证;(3)对比两种术式对腰椎结核的临床效果;(4)对手术方案选择提供参考。现就结果报告如下。
1 资料与方法
1.1 纳入及排除标准 纳入标准:(1)已诊断脊柱结核;(2)接受斜外侧入路病灶清除植骨融合内固定手术;(3)同期接受经椎间孔入路病灶清除植骨融合内固定手术治疗作为对照;(4)有完整随访记录的病例;(5)无其他手术禁忌证的患者。排除标准:(1)诊断为腰椎结核但可行抗结核保守治疗的病例;(2)诊断不明确或在外院行植骨融合内固定术的病例;(3)肿瘤导致骨质破坏或合并并发症出现的病例;(4)多节段腰椎结核的病例;(5)未按照随访时间随访或未按随访要求复查的病例。
1.2 一般资料 回顾性分析126例患者资料,最终通过筛查纳入48例。按照不同手术方式分为两组。OLIF手术组患者26例,男12例,女14例;年龄30~72岁,平均(49.62±16.70)岁,手术节段L1~25例,L2~38例,L3~45例,L4~56例,L5S12例。TLIF手术组患者22例,男12例,女10例;年龄30~75岁,平均(51.41±15.30)岁,手术节段L1~26例,L2~34例,L3~44例,L4~57例,L5S11例。两组患者性别、年龄、病程持续时间、身体质量指数(body mass index,BMI)比较差异无统计学意义(P>0.05,见表1)。本研究经新疆维吾尔自治区人民医院伦理委员会审批,所有纳入对象均已签署手术知情同意书。
1.3 临床表现 所有患者术前均主诉腰痛或下肢疼痛,均有腰部压痛及叩击痛,保守治疗超过6个月无效,存在腰椎椎管狭窄症状或间歇性跛行。术前检查:包括详细的实验室检查和影像学检查。实验室检查:所有患者入院后均完善结核T细胞学检查并且完善布氏杆菌病滴度检查作为排除标准。所有患者通过T细胞学检验均提示阳性,白细胞正常或轻度升高(除老年患者合并肺部感染等情况),血沉(erythrocyte sedimentation rate,ESR)超出正常范围(ESR>20 mm/h),C反应蛋白(C-reactive protein,CRP)明显升高。影像学检查:所有患者均完善腰椎X线片、腰椎CT及腰椎MRI,了解骨质破坏程度、椎旁脓肿的范围、椎管内硬膜外是否存在死骨或脓肿等。所有患者均有不同程度的骨质破坏且椎旁脓肿形成,部分患者椎管内存在死骨及脓肿压迫硬脊膜。
1.4 术前准备 所有患者入院后在术前均接受抗结核标准治疗(1~2周),口服四联结核药物,服用方法:异烟肼片(350 mg/d)、乙氨丁醇(300 mg/d)、吡嗪酰胺(250 mg/d)、利福平胶囊(450 mg/d)。待患者ESR有所下降后进行手术治疗。
1.5 手术指征及方法
1.5.1 OLIF手术指征 体型适中,BMI<25 kg/m2,病灶位于椎体前柱未波及椎体后缘,骨质破坏较为严重且出现后凸畸形,椎旁脓肿较大,椎管内无明显死骨及脓肿,必须通过较大植骨块支撑纠正塌陷椎体并恢复高度的病例。
1.5.2 OLIF手术方法 全麻生效后患者取右侧卧位,调整手术床使患者腰椎略凸向左侧,术者位于患者背侧。定位节段后,在体表做好切口标记,按照术前在X线片或CT测量骨缺损大小,暴露左侧髂嵴上缘,以骨刀取出相应大小的三面皮质髂骨块,缝合切口并无菌贴贴敷保护切口。沿体表标记切开皮肤、皮下,单节段切口长3~6 cm,外层分离腹外斜肌,按照肌纤维方向分离腹内斜肌、腹横肌及腹横筋膜。再钝性穿透腹横筋膜后,沿腹膜后间隙分离周围组织进入腰大肌前方。将腰大肌向椎体后方轻度剥离,充分暴露责任节段椎间隙,插入针头且C型臂透视确定为责任间隙。安装软组织撑开器,在责任椎间隙侧方切开纤维环,用髓核钳去除破碎髓核、椎体内及椎间隙后缘、对侧边缘的炎性肉芽组织及死骨脓肿,用刮除器处理剩余终板部分。将三面皮质髂骨块混合利福平植入处理间隙,C型臂确定植骨块大小及位置满意后,留置负压引流管,逐层缝合肌层、皮下及皮肤。根据患者具体经济情况选择后路椎弓根钉固定或皮质骨轨迹螺钉(cortical bone trajectory,CBT)固定。术中取出组织送病理学检查(见病理图)。
1.5.3 TLIF手术指征 体型及BMI不受影响,骨质破坏轻,未出现严重骨质破坏及椎旁脓肿,椎体前凸未明显丢失,椎管内出现脓肿及死骨造成压迫硬膜无法通过斜外侧处理椎管内病灶的病例。
1.5.4 TLIF手术方法 气管插管麻醉生效后患者调整为俯卧位状态,调整手术床使患者腰椎略后凸,在C型臂透视下确定病变节段,髂骨块切取方式同OLIF,在体表标记手术范围,一般为5~6 cm。沿术前体表标记取正中切口,切开皮肤及皮下组织达背阔肌筋膜,在棘突一侧或双侧切开筋膜层,沿棘突及胸最长肌及多裂肌间隙进入显露椎板及关节突关节,根据术前椎弓根情况确定使用椎弓根螺钉固定,固定完毕后,用咬骨钳咬除下关节突及部分上关节突。根据需要可咬除部分棘突与下椎板交界部分及部分下椎板,充分显露神经根及椎间盘,切开纤维环,用髓核钳去除破碎髓核、椎体内及椎管内死骨、脓肿及炎性肉芽组织,用终板刮勺处理上下终板,将三面皮质髂骨块混合利福平由一侧或双侧植入相应椎间隙,C型臂确定植骨块大小及位置满意后,留置负压引流管,逐层缝合肌层、皮下及皮肤。
1.6 术中病变组织改变 OLIF组中可见较大的骨质破坏及缺损且较大的腰大肌脓肿形成,周围肌肉组织因长期浸泡于脓液中导致组织变性且失去原有肌肉正常光泽度,肌肉组织水肿且发亮,部分血管在脓液的浸泡下与周围无法辨别或与周围组织出现黏连,弹性下降,轻微牵拉导致破裂出血,椎间隙内骨质破坏严重,主要集中在椎体前1/3,椎间隙消失,但中柱较为完整,部分纤维环内干酪样组织存在(见图1)。

图1 病理报告示干酪样坏死及结核性肉芽组织(抗酸染色,×40)
TLIF组中可见骨质破坏轻,未见大量骨质缺损,但椎间盘组织周围静脉丛充血且侧支循环增多,纤维环背侧完整,部分可见后纵韧带下方少量脓液,纤维环内压力增大,切开纤维环后脓液流出,可刮出破碎的终板组织,髓核组织变性,死骨量较少,干酪样组织不明显(见图2)。
1.7 术后处理 所有患者术后均给予抗炎、补液等对症处理2~3 d,术后引流量<50 mL给予拔除引流管。术后根据切口愈合情况3~7 d给予携带腰围固定带或胸腰椎固定支具早期负重进行功能锻炼。术后1周完成X线片检查,了解病灶节段植骨块及内固定物是否与术中透视结果一致。术后3个月、6个月及末次随访腰椎正侧位X线片。术后继续按标准服用四联抗结核药物12~18个月。负重功能锻炼时佩戴腰围固定带最少3个月。
1.8 评价指标 疼痛视觉模拟评分(visual analogue scale,VAS)[11]。0分:无任何疼痛感觉;1~3分:轻度疼痛,不影响正常工作及生活;4~6分:中度疼痛,影响工作,不影响生活;7~10分:重度疼痛,影响工作及生活。日常生活活动能力评分(activities of daily living,ADL)[12],满分100分为生活自理,无需依赖;61~99分表示有轻度依赖;41~60分表示有中度依赖;≤40分表示有重度依赖。功能障碍指数(Oswestry disability index,ODI)[13]评分表共10项,每项分值为0~5分,考虑到大部分患者为少数民族患者且部分患者未婚,未统计“性功能”的指标,故最少为45分。最终统计得分公式:9项得分之和/45×100%,0为正常,得分越高功能障碍越明显。

2 结 果
2.1 两组术中出血量、手术时间、住院时间比较 OLIF组平均手术出血量(331.60±166.20) mL,TLIF组为(256.80±133.00) mL,两组比较差异无统计学意义(P>0.05);OLIF组平均手术时间(131.10±30.90) min,TLIF组为(146.30±31.30) min,两组比较差异无统计学意义(P>0.05);OLIF组平均住院时间(19.30±6.50) d,TLIF组为(17.30±6.40) d,两组比较差异无统计学意义(P>0.05,见表2)。

表2 两组手术出血量、手术时间、住院时间比较
2.2 两组ESR、CRP比较 两组术前ESR、CRP比较差异无统计学意义(P>0.05),术后3个月复查两项指标基本恢复正常水平,术后6个月两组间指标比较差异无统计学意义(P>0.05)。组内术前及术后3、6个月ESR及CRP比较,差异有统计学意义(P<0.05,见表3~4)。
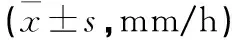
表3 两组手术前后ESR比较

表4 两组手术前后CRP比较
2.3 两组VSA评分及ADL评分、ODI指数比较 两组术前VAS评分及ADL评分、ODI指数差异无统计学意义(P>0.05),VSA评分术后3个月及6个月时较术前明显降低(P<0.01),ADL评分术后3个月及术后6个月较术前明显升高(P<0.01),ODI指数术后3个月及6个月较术前明显改善(P<0.01)。两组术后各项评分比较,差异无统计学意义(P>0.05,见表5~7)。
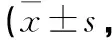
表5 两组手术前后VAS评分比较分)
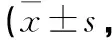
表6 两组手术前后ADL评分比较分)

表7 两组手术前后ODI指数比较
2.4 典型病例 (1)22岁男性患者,以“腰部疼痛伴活动受限1年加重3个月”为主诉入院,入院诊断为:L3~4椎体结核并骨质破坏,行OLIF病灶清除植骨融合联合后路固定术,术后功能改善。手术前后影像学资料见图3~6。(2)52岁女性患者,以“腰腿疼痛伴下肢无力1年”为主诉入院,入院诊断:L2~3椎体结核并骨质缺损,行前路病灶清除植骨融合联合TLIF后路单侧探查减压固定术,术后效果良好。手术前后影像学资料见图7~12。

图5 术前MRI示L4椎体整体破坏且椎旁两侧大量脓肿形成 图6 术后X线片示局部腰椎前凸正常,植骨块大小及位置良好

图7 术前X线片示L2~3骨质破坏并椎体向左侧弯 图8 术前CT示L3左侧椎弓根消失、坏死波及上终板 图9 术前CT示L3椎体死骨凸向椎管内且L2同时存在骨质破坏

图10 术前CT示L3椎管内继发性狭窄 图11 术前矢状位MRI示L2、L3骨质破坏并导致脊髓受压 图12 术后X线片示局部前凸部分恢复且植骨块大小及位置良好
3 讨 论
由于西部地区不同地域特殊的生态、气象、地理、社会经济文化、生活饮食习惯和医疗水平等的差异造成结核病发病率较高,腰椎结核是脊柱结核中最为常见的疾病之一,以腰骶痛伴功能障碍为主要表现,导致椎体、椎间盘的破坏、椎旁脓肿形成、造成脊髓神经根损伤等[14]。腰椎结核手术治疗主要以病灶清除、减压及稳定脊柱为主,通过牢固的内固定重建脊柱稳定性,控制甚至治愈病变从而改善患者生活质量[15]。对于早期发现无骨质破坏及神经症状的患者主要以长期足量使用抗结核药物联合胸腰支具制动的保守治疗为主;保守治疗效果欠佳、病灶导致脊柱不稳、压迫神经等情况时考虑行手术治疗[16]。
前路病灶清除联合后路固定是常见的手术方法[17],可提供彻底的清创和可靠的固定[18]。但传统的前路病灶清除联合前路固定手术存在创伤大、出血多、潜在损伤神经根的风险。随着脊柱微创手术技术的发展和手术器械的改进,更多传统开放手术被更为微创的手术方式取代。近几年斜外侧病灶清除植骨融合固定手术在脊柱外科不断兴起,该术式采用腰大肌和腹部大血管之间的间隙进入病灶部位[19],此手术入路有很多亮点,较后路手术避免了腰椎后部肌肉的损伤,可直视下清楚处理椎间隙及终板,较极外侧腰椎椎体间融合(extreme lumbar interbody fusion,XLIF)可避免潜在的腰丛、腰大肌的损伤风险,现广泛应用于腰椎椎体退变的治疗中。目前对于OLIF入路下治疗腰椎感染性疾病或退行性疾病在国内开展的研究较多,但主要集中于该术式的先进性及微创性,对于普及开展该术式的报道较少。
OLIF入路目前主要适用于单纯间隙骨质破坏的病例,对于椎管内脓肿或死骨的病例不适用,对于较大椎管内脓肿或死骨、神经压迫的病例,以后路减压融合固定为主。OLIF术式也存在它的局限性,要考虑患者BMI、年龄及身体一般情况,目前主要适用于L2~5,因为L1~2间隙位置较高,存在肋骨遮挡,术中处理需要切除部分肋骨,对于L5S1间隙,双侧髂骨为主要遮挡部位,操作不当可能导致髂血管损伤,风险较大,一般情况下,除有经验的术中操作外,对于年轻医师及基层单位,不建议使用该手术[20]。Fujibayashi等[21]通过对1 000多例行OLIF的患者进行问卷调查后发现并发症包括运动神经损伤(1%)、感觉神经损伤(3.5%)、腰大肌及髂腰肌无力(3%)、血管损伤(0.7%)、输尿管损伤(0.1%)、腹膜及胸膜损伤等。因为存在上述并发症,因此,对于术者在术前详细了解患者身体一般情况,通过高清影像学检查了解并评估腹部大血管情况及分支是否存在变异等来评判是否适合该术式。
目前二级以上的医院都在开展脊柱相关手术且往往较多的患者来自地方医院,存在病源优势,但因各县市级医院硬件及技术条件的影响,无法在当地开展OLIF手术,而且该术式对于术者的要求较高,必须要求了解腹膜后入路的解剖,要有特殊的操作工具,能在有限的手术空间中寻找腰大肌及血管间隙,辨别腹膜后脂肪及腹部动静脉、输尿管及交感神经。若术中出现腹膜、血管、输尿管等意外情况,要有立即处理的能力。对于腰椎结核性病变,基层单位可开展的手术方式主要以PLIF、TLIF等后路手术为主,因为此手术方式对于硬件设施的要求相对较低,医师学习曲线较短且该术式相对较为安全,虽然对于腰椎后方肌肉组织有一定的损伤,但长期随访中也可以看到患者的满意度及恢复度较高。对此,OLIF手术对于腰椎退行性变及腰椎感染性疾病的先进性不可否认,但对于经典手术方法TLIF术式来说,通过短期研究对比发现两者在同一性质的疾病的预后有着相似的结果,并且对于很多基层医院有着得天独厚的优势,但学习OLIF技术对于基层医院的脊柱专业能力提升更有意义,可提高社会效应及经济效应,可以做到地方病地方看,减少医疗资源的浪费,减轻上级医院的工作压力。
该项研究主要对两种术式治疗腰椎结核进行比较,虽然两组的适应证及同质性不同,但对于骨质破坏严重且缺损较大的病例,TLIF术式下无法使用较大的骨块进行间隙的支撑。本研究为回顾性对照研究,原始资料数量较少,而且是对既往病例资料进行数据分析,原始资料的数据可能存在一定的偏倚,因此对于明确的治愈率、并发症的恢复情况缺乏中长期的随访调查且需要大量的前瞻性研究来进一步分析。
综上所述,OLIF及TLIF术式在治疗单节段腰椎结核可以得到相似的治疗结果,OLIF主要尽可能保护腰椎后方结构,改善腰椎矢状位及冠状位失衡,而TLIF可通过后路解除神经根及脊髓的压迫,发挥直接作用,两种手术各有各的特点,因此建议临床医生根据患者的病情选择适当的手术方式。

