碱式碳酸铜层状复合材料制备及类芬顿催化性能研究
张璐瑶,王卫伟
(山东理工大学 材料科学与工程学院,山东 淄博 255049)
芬顿氧化法(Fenton)具有氧化能力高、降解速率快,可彻底降解有机污染物等优点,广泛应用于废水处理过程中。传统芬顿技术是以溶液中的亚铁离子作为催化剂活化过氧化氢,产生具有极高氧化能力的活性物质,降解有机污染物,是一种均相反应。然而反应所需溶液pH值范畴窄(~3),反应结束后需要调节溶液pH值为中性,参加芬顿反应的铁离子会以氢氧化铁等形式沉淀,催化剂不易回收再利用,若形成的含铁污泥进入环境会产生二次污染。这些问题极大地限制了芬顿技术的应用[1-4]。研究报道,非均相类芬顿氧化法是解决上述问题的一种有效途径。这是在传统芬顿技术基础上形成的一种新型氧化方法,采用变价过渡金属离子如Cu2+、Co2+、Ni2+、Mn3+等形成的固相催化剂代替Fenton反应中的Fe2+,在保证良好催化活性的同时实现了催化剂的重复利用[2-4]。固相催化剂材料是类芬顿性能提升的关键,因此开发一种稳定性好、催化性能优异、成本低、制备工艺简单的材料用于类芬顿技术是目前废水处理的研究热点。
与其他过渡金属离子相比,铜基催化剂具有适用范围广、催化活性高和成本低等特点,引起了研究人员的广泛关注[5-6]。研究发现将具有类芬顿性能的铜基催化剂固载于载体上获得复合催化剂,可以增加反应活性位点,提高反应速率和催化活性。载体的结构影响其催化活性。若使用多孔、二维结构等具有大比表面积的材料作为载体,可以将铜基催化剂很好的分散在载体表面,同时为固液反应提供大量的活性位点,提高催化性能[7-8]。层状双金属氢氧化物(LDHs)由于化学稳定性好、比表面积大和具有良好的吸附能力等特点,作为催化剂和载体广泛用于有机污染物的催化降解、催化制氢、催化还原二氧化碳等领域[9]。与其他载体相比,LDHs具有较强的金属协同作用,表面具有丰富的羟基活性基团,可以为催化反应提供大量的反应活性位点。同时LDHs特殊的层状结构可以为催化活性物质负载提供多种落位点,包括LDHs表面、LDHs层板上和LDHs层间[10-11]。因此LDHs是一种优异的催化剂载体,有利于催化剂活性调控。
本文选用镍铝LDHs(NiAl-LDHs)为载体,采用工艺简单、有效的绿色制备方法机械混合法,将铜基类芬顿层状催化剂(碱式碳酸铜,Cu2(OH)2CO3)负载于NiAl-LDHs表面,构成层状Cu2(OH)2CO3/NiAl-LDHs复合材料。研究机械混合过程对LDHs和Cu2(OH)2CO3形貌、结构和界面结合方式等影响。同时研究制备方法、界面结合方式等对其催化降解亚甲基蓝的反应动力学规律和降解机理。
1 实验部分
1.1 样品制备
实验药品有三水硝酸铜、六水硝酸镍、九水硝酸铝、氟化铵、尿素、双氧水(质量分数30%)、亚甲基蓝(MB),均为分析纯。
水热法制备NiAl-LDHs:将六水硝酸镍、九水硝酸铝、氟化铵和尿素,加入到50 mL水中,搅拌至溶解,浓度比为3∶1∶4∶10。将所得溶液转移到反应釜中,120 ℃下反应24 h。反应结束后,冷却至室温,将所得产物离心,去离子水和无水乙醇分别洗涤3次,50 ℃干燥。
水热法制备Cu2(OH)2CO3:将三水硝酸铜、氟化铵和尿素加入到50 mL去离子水中, 搅拌至溶解,各物质浓度比为1∶1.25∶5;于80 ℃下搅拌30 min,然后转移到反应釜中,90 ℃保温24 h;反应结束后,冷却至室温;离心,去离子水和无水乙醇分别洗涤3次;50 ℃干燥。
机械混合法制备Cu2(OH)2CO3/NiAl-LDHs复合材料:将0.2 g NiAl-LDHs与0.2 g Cu2(OH)2CO3放入研钵中研磨10 min,加入40 mL去离子水,超声处理至均匀,放置通风橱室温内,搅拌至干燥。
1.2 类芬顿性能测试
将25 mg样品加入到50 mL MB水溶液中(浓度20 mg/L),超声处理20 min,得到均匀分散的悬浮液。然后放置暗处,搅拌30 min,取样。再加入1 mL双氧水(质量分数30%)进行类芬顿反应,每隔5 min取样。每次取的样品立即过滤,并利用紫外可见分光光度计检测MB在664 nm的吸光度,根据朗伯比尔定律计算MB的浓度,利用公式(1)计算MB降解率。
(1)
式中C0和Ct分别为类芬顿反应开始(加入双氧水前)和加入双氧水后反应时间t/min时溶液中MB的浓度,mg/L。
1.3 分析表征
使用 D8 AD VANCE 多晶X射线衍射仪进行X射线衍射分析(XRD),以 Cu Kα 为衍射源(λ =0.154 06 nm)。利用FEI-Sirion 200 F型场发射扫描电镜(SEM)观察样品的形貌。利用透射电镜(TEM)和高分辨透射电镜(HRTEM)观察样品形貌和结构,仪器型号WJGS-032型场发射高分辨透射电镜。利用TU-1901型紫外可见分光光度计检测MB的吸收曲线。
2 结果与讨论
2.1 结构分析
利用XRD分析样品的结构和物相(如图1)。与标准卡片对比(JCPDS file No. 75-1163),样品Cu(OH)2CO3出现了多个尖锐的衍射峰,分别对应着单斜结构Cu2(OH)2CO3的(020)、(120)、(200)、(220)、(20-1)、(240)、(321)晶面,没有观察到其他杂质,如铜的氧化物或氢氧化物的特征峰[12]。NiAl-LDHs样品为典型的LDHs层状结构(JCPDS file No.48-0594)。根据(003)、(006)和(009)晶面间距(公式(2)),计算样品NiAl-LDHs的层间距约为0.761 nm,与层间阴离子为CO32-的LDHs相吻合[13]。
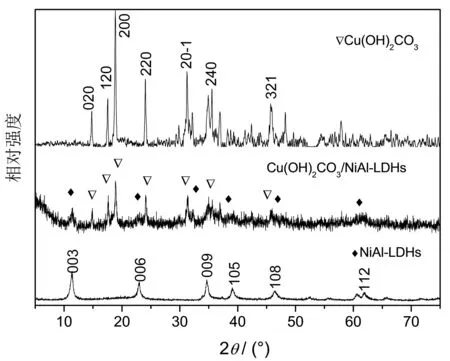
图1 样品的XRD谱图
d层间距=[d(003)+2d(006)+3d(009)]/3 ,
(2)
式中d(003)、d(006)、d(009)分别代表(003)、(006)和(009)晶面面间距。
利用机械混合法制备的层状复合材料的XRD图谱中同时出现了NiAl-LDHs的(003)、(006)、(009)、(105)、(112)晶面和Cu2(OH)2CO3的(020)、(120)、(200)、(220)、(20-1)、(240)等晶面的衍射峰。与单一样品的衍射峰相比,复合后Cu(OH)2CO3和NiAl-LDHs材料中衍射峰峰强降低,峰变宽,这是由于采用机械混合法制备复合材料的过程中,样品在研磨和不断搅拌的作用下受到剪切力,片状结构被打碎,尺寸减小导致的[14]。
2.2 形貌分析
图2(a)是Cu2(OH)2CO3/NiAl-LDHs复合材料的SEM照片。从图2(a)中可以看到复合材料为片状形貌,小碎片的尺寸约50 nm左右,大片约400 nm,同时利用TEM研究了复合材料的生长情况。由图2(b)可知,复合材料为大的薄片结构,表面附着细小薄片,图2(c)和2(d)分别对应着两种形貌和尺寸薄片的HRTEM照片。从图中可以看到,大的薄片的晶格间距为0.254 nm,对应NiAl-LDHs的(009)晶面;细小薄片结构的晶格间距为0.282 nm,对应于Cu(OH)2CO3的(20-1)晶面,进一步说明机械混合法成功将Cu2(OH)2CO3和NiAl-LDHs复合在一起,且在研磨和机械搅拌作用下,Cu2(OH)2CO3和NiAl-LDHs两种片状结构混合均匀。在随后持续搅拌作用下,片层结构会发生剥离,破碎,更加有利于两者的分散和结构,最终Cu2(OH)2CO3细小薄片附着在NiAl-LDHs片层表面,形成片/片界面结合方式[15]。

(a)SEM照片;(b)TEM照片;(c)和(d)HRTEM照片。图2 Cu2(OH)2CO3/NiAl-LDHs复合材料
2.3 类芬顿性能研究
以MB为降解物,研究复合前后样品类芬顿反应活性。图3分别是以NiAl-LDHs、Cu2(OH)2CO3和Cu2(OH)2CO3/NiAl-LDHs复合材料为催化剂,活化H2O2降解MB的降解曲线。从图中可以看到,在暗处搅拌30 min,没有添加H2O2的情况下,三种催化剂对MB均没有降解作用,且对MB的吸附效果差,吸附率均小于5%。当加入H2O2后,开始进行类芬顿反应。Cu2(OH)2CO3/NiAl-LDHs表现出最佳类芬顿催化降解效果,添加H2O2反应2 min后,MB完全脱色。对照实验单独使用Cu2(OH)2CO3为催化剂,需要反应30 min后MB才能完全脱色。单独使用NiAl-LDHs为催化剂时,未观察到NiAl-LDHs对MB有明显催化降解作用,反应30 min后MB降解率不到1%。根据上述分析可知,将Cu2(OH)2CO3和NiAl-LDHs复合有利于提高其对MB的催化反应活性。
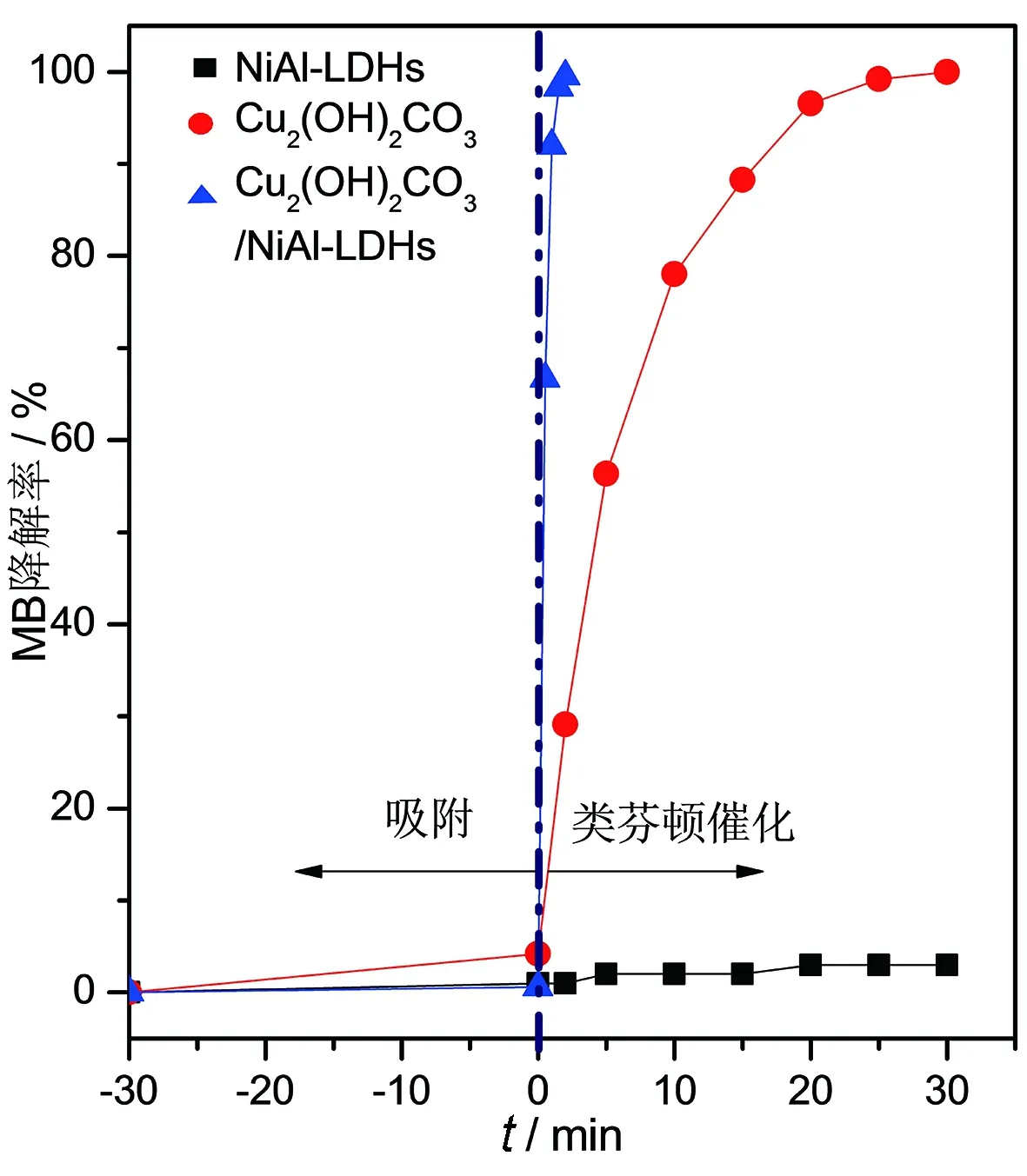
图3 NiAl-LDHs、Cu2(OH)2CO3和Cu2(OH)2CO3/NiAl-LDHs复合材料催化活化H2O2降解MB的降解曲线
研究了分别以Cu2(OH)2CO3和Cu2(OH)2CO3/NiAl-LDHs复合材料为催化剂时MB降解反应动力学规律。从拟合曲线和拟合数据(图4,公式(3))可以看到以Cu2(OH)2CO3和Cu2(OH)2CO3/NiAl-LDHs复合材料为催化剂时,MB的降解过程均符合拟一级动力学模型。以样品Cu2(OH)2CO3为催化剂时反应速率常数k为0.214 min-1,Cu2(OH)2CO3/NiAl-LDHs复合材料为催化剂时反应速率常数增加,达到1.367 min-1。进一步说明复合后有利于MB的催化降解反应。

图4 Cu2(OH)2CO3和Cu2(OH)2CO3/NiAl-LDHs复合材料催化活化H2O2降解MB拟一级反应动力学拟合曲线
-ln(Ct/C0)=kt,
(3)
式中:C0和Ct分别为加入双氧水前和加入双氧水后反应时间t/min时溶液中MB的浓度,mg/L;k为反应速率常数,min-1。
2.4 类芬顿反应机理研究
通过以上分析可知,通过简单的机械混合法,经过超声处理后仅需在去离子水中机械搅拌处理就可以将Cu2(OH)2CO3和NiAl-LDHs复合,成功实现了将具有类芬顿活性的层状Cu2(OH)2CO3固载于NiAl-LDHs的表面,提升其在H2O2体系下类芬顿降解MB的性能。Cu2(OH)2CO3和NiAl-LDHs均为片状结构,搅拌过程在剪切力作用下,NiAl-LDHs片层结构会被破坏,大片被打碎,尺寸变小,Cu(OH)2CO3也由板条状变成较小的碎片,如图2(a)所示。碎片化的NiAl-LDHs片与Cu2(OH)2CO3片层充分接触,形成了层片堆叠的形貌,有利于电子的传输。有文献报道[9,16],机械混合法制备过程中,复合材料中各部分除了存在表面缺陷外,还会产生一些特殊的微物理性能,这些因素都会提高材料的催化性能。
在H2O2类芬顿体系中,负载于NiAl-LDHs上的Cu2(OH)2CO3中的Cu2+与H2O2反应生成Cu+,如公式(4)和图5中的(I)。Cu+与H2O2发生类芬顿反应生成具有强氧化性的·OH;同时Cu+被氧化成Cu2+构成Cu+/Cu2+循环,如公式(5)和图5中的(II)O产出的·OH轰击MB大分子,将其降解为CO2和水,如公式(6)和图5中的(III)。
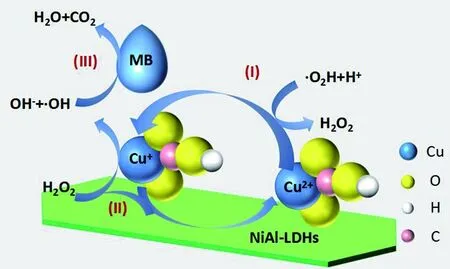
图5 Cu2(OH)2CO3/NiAl-LDHs复合材料类芬顿降解MB的机理图
将Cu2(OH)2CO3负载于NiAl-LDHs片状结构表面,生成具有层状结构的复合材料,这种层状结构有利于活性位点暴露,有效促进了反应体系中电子转移的效率,促进Cu+/Cu2+循环反应和·OH的生成,以及反应产物的输运,更大程度上提高催化剂类芬顿降解MB的反应速率[11]。
Cu2++H2O2→Cu++·O2H+H+,
(4)
Cu++H2O2→Cu2++OH-+·OH ,
(5)
·OH+MB→CO2+H2O。
(6)
3 结束语
本文利用机械混合法制备了层状Cu2(OH)2CO3/ NiAl-LDHs复合材料,在机械混合过程剪切力等的作用下,Cu2(OH)2CO3和NiAl-LDHs以片层结构相结合,表现出层状堆叠形貌。以亚甲基蓝为降解目标物,发现Cu2(OH)2CO3与NiAl-LDHs复合后有利于提高电子传输效率,反应速率增加,反应速率常数达到1.367 min-1,表现出最佳的反应活性。

