衰弱对椎体成型术治疗老年骨质疏松椎体压缩性骨折的疗效与预后影响
陈 辉 白建中 周 功 刘 涛 朱勋兵 蒋维利 牛国旗
随着人口老龄化的加剧,我国骨质疏松症的老年人群也将激增。据报道,至2050 年, 我国患骨质疏松症的人数将从6 000 万增至1.2 亿[1]。骨质疏松性椎体压缩骨折(osteoporotic vertebral compression fractures, OVCFs)是老年骨质疏松症患者最常出现的病理性骨折。椎体成型术(percutaneous vertebroplasty,PVP)或椎体后凸成型术(percutaneous kyphoplasty,PKP)是治疗OVCFs 最有效的外科术式,手术创伤小且恢复快,已成为OVCFs 外科治疗的“金标准”[2-3]。但是老年人群另一常见合并症——衰弱,同样不容忽视。衰弱主要是由于身体状况差、心理不健康、社交能力降低及生理储备能力下降等多种因素共同导致的一种身体亚健康状态。其可增加跌倒、骨质疏松性骨折、精神错乱、残疾甚至死亡等风险[4-6]。衰弱是否会对OVCFs患者行PVP 或PKP 术治疗后的疗效及预后产生影响,目前鲜有报道。本研究通过分析围手术期指标、术后18 个月随访时的功能疗效评分、再骨折率及病死率等,探讨衰弱对OVCFs 患者行PVP 或PKP 治疗的预后影响,现报道如下。
1 资料与方法
1.1 一般资料 前瞻性纳入2019 年1 月至2020 年6月蚌埠医学院第二附属医院收住的OVCFs 行PVP/PKP 手术的患者。纳入标准:①诊断明确为胸腰椎单个椎体新发的骨质疏松性压缩骨折者;②年龄>60 岁;③不合并其他部位的骨折者;④无明显手术禁忌证,且接受PVP 或PKP 手术者;⑤PVP 手术方式采用双边穿刺者;⑥一般资料及随访数据完整者;⑦所有纳入患者均知情手术风险并签署手术同意书。对于身体状况差,不能耐受手术的患者,予以排除。手术均由2 名经验丰富的副主任医师完成。本研究通过蚌埠医学院第二附属医院临床医学研究伦理委员会审批(审批号:2018-14)。
1.2 方法
1.2.1 研究方法 本研究为前瞻性队列研究。197 例患者符合纳入标准,将纳入的患者采用临床衰弱量表[7]进行评分,1 分为非常健康,随着分值的增加,患者衰弱程度逐渐加重,9 分代表重度衰弱。1~4 分为无衰弱组,5~7 分为衰弱组,≥8 分通常不能耐受手术,直接排除。对两组患者采用同样的治疗策略,术后完整随访18 个月。详细记录两组患者的疗效和预后情况。
1.2.2 手术方法 两组患者均采用俯卧位,局部麻醉,经皮双侧椎弓根入路穿刺注射骨水泥。
1.3 观察指标 比较衰弱组与非衰弱组术后的住院时间、总住院费用、术后疼痛不缓解发生率、术后功能改善情况[采用Oswestry 功能障碍指数问卷表(Oswestry disability index, ODI)][8]、椎体再骨折发生率及病死率。
1.4 统计学方法 采用SPSS 24.0 进行统计分析。计量资料进行正态性检验,正态分布的用±s表示,采用t检验、单因素方差分析进行组间比较,非正态分布采用Kruskal-WallisH检验进行组间比较。计数资料用频数和/或率表示,组间比较用χ2检验,若有一个单元格的期望频数<5,则使用Fisher 确切概率法。以P<0.05 为差异具有统计学意义。
2 结果
2.1 一般资料 衰弱组和非衰弱组患者年龄、ASA 分级≥3、非外伤腰背部疼痛情况比较,差异有统计学意义(P<0.05)。衰弱的发生率随年龄增长呈增加趋势,60~70 岁的发生率为13.2%,70~80 岁为17.5%,≥80岁为42.2%。两组患者性别、身体质量指数(body mass index,BMI)、手术时间、手术方式、骨水泥注射量差异均无统计学意义(P>0.05)。见表1。
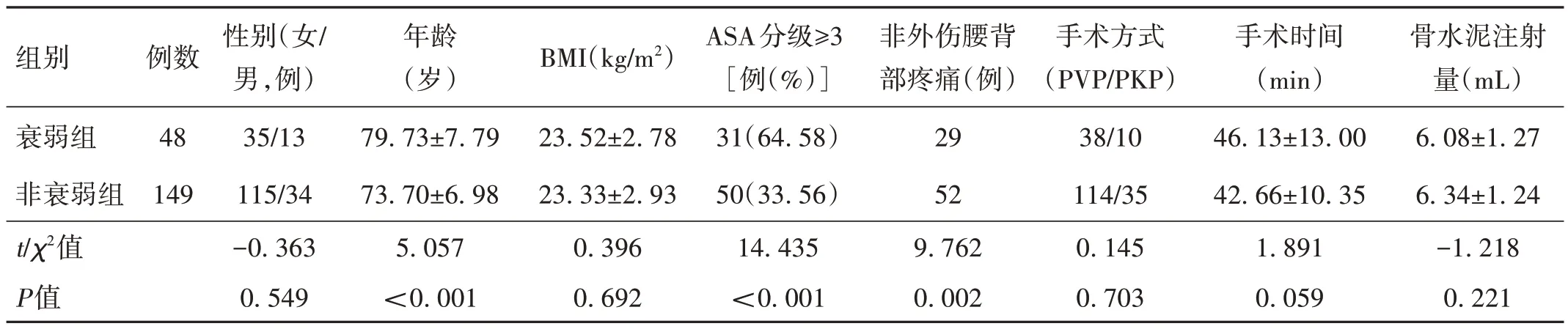
表1 两组患者一般临床资料比较
2.2 术后结局比较 衰弱组住院时间及手术费用多于非衰弱组,术后功能改善情况优于衰弱组,再次骨折的发生率高于非衰弱组,病死率高于非衰弱组,差异均有统计学意义(P<0.05)。见表2。
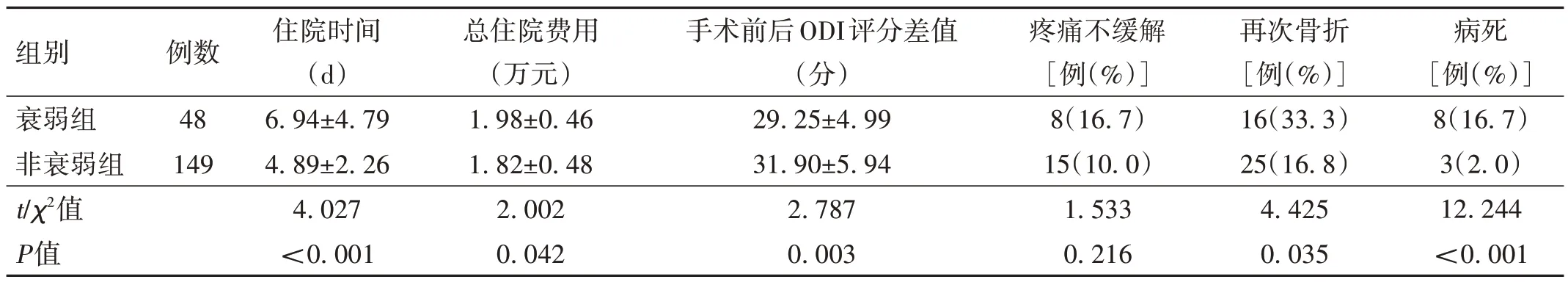
表2 两组患者围手术期指标及预后情况比较
2.3 OVCFs 术后发生并发症相关影响因素logistic 回归分析 以年龄(>75 岁、≤75 岁)、衰弱(有、无)、ASA分级≥3(是、否)、非外伤的腰背部疼痛(是、否)为自变量,以术后并发症(术后再骨折、术后疼痛不缓解)为因变量(无并发症发生赋值为0,有并发症发生赋值为1),进行logistic 回归分析,发现衰弱、高龄(>75 岁)、ASA 分级≥3 是OVCFs 术后出现并发症的独立危险因素。见表3。
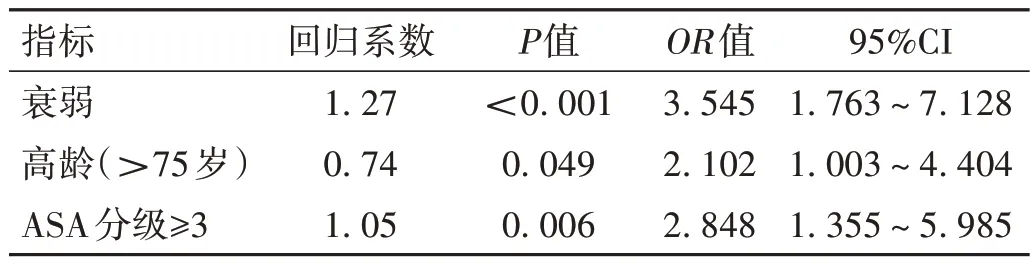
表3 OVCFs术后发生并发症相关影响因素logistic回归分析
3 讨论
本研究研究患者术前衰弱对OVCFs 术后影响,发现衰弱在该人群(>60 岁)中的发病率达24.4%。在既往的研究中,采用不同指标评估衰弱,结果不尽相同。Cooper 等[9]采用衰弱指数评估骨科患者的衰弱发生率约为35%,但采用衰弱表型其发生率约为41%。此外,纳入患者来源不同,衰弱的发生率也不相同。付傲等[10]对脊柱、创伤、关节等骨科多种疾病的患者进行研究,发现术前衰弱发生率约为31%。Wu 等[11]对我国>60 岁的老年人进行研究,共纳入5 301 人,衰弱发生率为7%。
既往研究显示,衰弱的主要危险因素包括高龄、合并较多基础疾病、营养不良、日常生活能力差等[12-13]。其中高龄患者,日常活动少,导致骨量丢失、四肢肌力减弱,是发生衰弱的一个显著危险因素[14];同时,本研究结果也表明,随着年龄增加,衰弱的发生率也逐渐增加。长期口服药物也是发生衰弱的一个危险因素,主要是药物的毒副作用加重肝肾功能的损害,导致患者生理机能变差。此外,朱杉杉等[15]研究发现,长期营养不良,导致心、脑等脏器功能减退,且增加了患者发生衰弱的风险。
本研究结果表明,衰弱组患者再骨折的风险高于非衰弱组。主要是由于衰弱老年人群,发生摔倒的风险增高[16],且骨折术后的预后差[17]。另,Bartosch 等[6]研究显示,衰弱可增加老年患者骨质疏松的风险,这也间接验证衰弱患者术后再骨折风险发生率较高。手术促进了OVCFs 患者功能的恢复,但衰弱患者功能恢复情况劣于非衰弱组,可能是由于衰弱患者本身生理储备能力降低导致其术后恢复较差,并且衰弱的老年患者,常常合并基础疾病,术前常需要其他科室进行辅助治疗,这也导致了衰弱患者的住院时间及手术费用均高于非衰弱组。此外,衰弱组术后18 个月内的病死率高于非衰弱组,衰弱组年龄大于非衰弱组,且身体状况较差等因素,导致衰弱组术后病死率较高。
在日常诊疗中应鼓励老年患者加强营养、合理膳食、锻炼身体、预防摔倒,从而延缓各器官、系统功能的衰退,降低发生衰弱风险[18],尤其对于高龄衰弱老年患者,应充分与患者及家属沟通,关注伴随基础疾病的治疗,提高衰弱患者术后的疗效及预后[19]。
衰弱对OVCFs 患者术后恢复不利,应给予关注。由于本研究样本量较少,研究结论还有待更大样本和多中心研究进一步验证。

