听力障碍与阿尔茨海默病相关性的Meta分析
王敏 郭文军 汤忠泉 赵晓敏 欧婷 李云涛
听力障碍(hearing impairment,HI)是指听觉系统中的传音、感音以及对声音的综合分析的各级中枢发生器质性或功能性异常,导致听力出现不同程度的减退。它是老年人常见的感觉障碍之一,常用纯音测听对听力水平进行判断,当4种频率(500 Hz、1000 Hz、2000 Hz、4000 Hz)的平均阈值超过25分贝时,即可定义为HI[1]。在HI的类型中,最常见的是年龄相关性听力障碍(age-related hearing impairment,ARHI),也被称作老年性耳聋。随着人口老龄化的发生,HI发病率呈现上升趋势[2],不仅影响老年人身心健康,更会降低其生活质量。AD是一种常见的神经系统退行性疾病,是导致痴呆的最主要原因[3]。相比于欧美发达国家,发展中国家的老龄人口比例相对较低,但AD患病率高于部分发达国家[4]。由于其发病率、患病率、死亡率均较高,目前已成为严重危害全人类生命健康的重大疾病之一[5]。
由于HI、AD均为年龄相关性疾病,近年来,人们对HI与认知功能障碍、痴呆之间的研究越来越多,一项Meta分析指出ARHI与认知障碍显著相关[6],而AD作为痴呆中的一种类型,目前有学者认为HI是AD潜在的最大可改变风险因素[7]。本研究通过Meta分析来探讨HI与AD的相关性,严格遵守MOOSE[8]报告规范的要求分析并书写。
1 资料与方法
1.1 文献检索策略 使用计算机检索PubMed、Web of Science、EmBase、Cochrane Library、中国知网(CNKI)、万方数据库、维普网(VIP)和中国生物医学文献服务系统(SinoMed)中关于HI与AD相关性的原始研究,检索时间为建库至2022-03-28。英文检索词包括Alzheimer disease、Alzheimer dementias、Alzheimer’s disease、senile dementia、Alzheimer type dementia、MCI、mild cognitive impairment、AD、hearing loss、hearing impairment、hearing dysfunction、hearing disorder等。中文检索词包括痴呆、失智、阿尔茨海默病、阿尔兹海默病、老年痴呆症、老年性痴呆、老年痴呆、听力障碍等。
1.2 纳入和排除标准
1.2.1 纳入标准:(1)研究类型为前瞻性队列研究;(2)暴露组与非暴露组(对照组)分别为听力障碍组及听力正常组;(3)结局指标为AD的发病率。
1.2.2 排除标准:(1)非中文、英文文献;(2)重复发表的文献;(3)病例报告或意见、述评、信函、会议摘要、综述、系统评价等;(4)细胞与动物基础实验;(5)无法获取全文或无法通过文中数据进行换算。
1.3 文献筛选与资料提取 由2名研究人员按照上述文献检索策略,根据纳入及排除标准独立检索筛选文献、提取资料,并进行交叉核对。如存在分歧,则通过讨论或交由第3位专业研究人员协助解决。资料提取的内容包括:纳入研究的第一作者及发表年份、国家、研究设计类型、样本量、平均年龄、性别、HI诊断标准、AD诊断标准、结局指标、效应值(95%CI)、校正因素、随访时间。
1.4 纳入研究的偏倚风险 评价由2名研究人员独立对纳入的原始研究文献进行质量评价,采用纽卡斯尔-渥太华量表(NOS)[9]作为评价工具。NOS量表的评价标准包括3个方面:研究人群选择方法、研究人员的可比性以及研究人员暴露因素;共有8个条目,9个给分点,满分共9分。总分7~9分为高质量,4~6分为中质量,≤3分为低质量。质量评价过程中若遇分歧,由双方讨论后决定或由第3位研究人员协助。
1.5 统计学分析 统计学分析采用Review Manager 5.4软件进行。采用Q检验及I2检验进行异质性检验,当P>0.1且I2≤ 50%时,表明各纳入研究之间异质性较小,则采用固定效应模型进行Meta分析;若P≤0.1或I2>50%,表明异质性较大,则采用随机效应模型。根据提取的信息,整理校正后效应值以及95%CI,队列研究中的HR值可看作RR值进行合并。计算合并后的总的效应值及95%CI,二分类变量的效应指标采用RR值进行森林图的绘制。
2 结果
2.1 文献筛选流程及结果 初次共检索3145篇文献,其中PubMed 403篇,Web of Science 1003篇,EmBase 1215篇,Cochrane Library 170篇,CNKI 57篇,万方数据库178篇,VIP 9篇,SinoMed 110篇。剔除重复文献711篇,经过阅读文献题目、摘要及全文后,最终纳入6篇文献[10-15],语言均为英文,共包括9054名研究对象。
2.2 纳入研究的基本特征与偏倚风险评价结果 通过NOS量表的9个得分点对纳入研究进行偏倚风险评价,6项研究评分均>5分,无低质量文献。纳入研究的基本资料信息见表1。按照表1列举的6项研究顺序,各研究的校正因素分别为:(1)年龄;(2)受教育程度;(3)性别、年龄、种族、受教育程度、糖尿病、吸烟和高血压;(4)年龄、社会阶层、焦虑、发病前智力;(5)性别、APOEε4等位基因、受教育程度、基线年龄和心血管危险因素(糖尿病、吸烟、高胆固醇、高血压);(6)年龄、性别、种族、受教育年限、糖尿病、高血压、心脏病、吸烟、卒中和APOE基因。
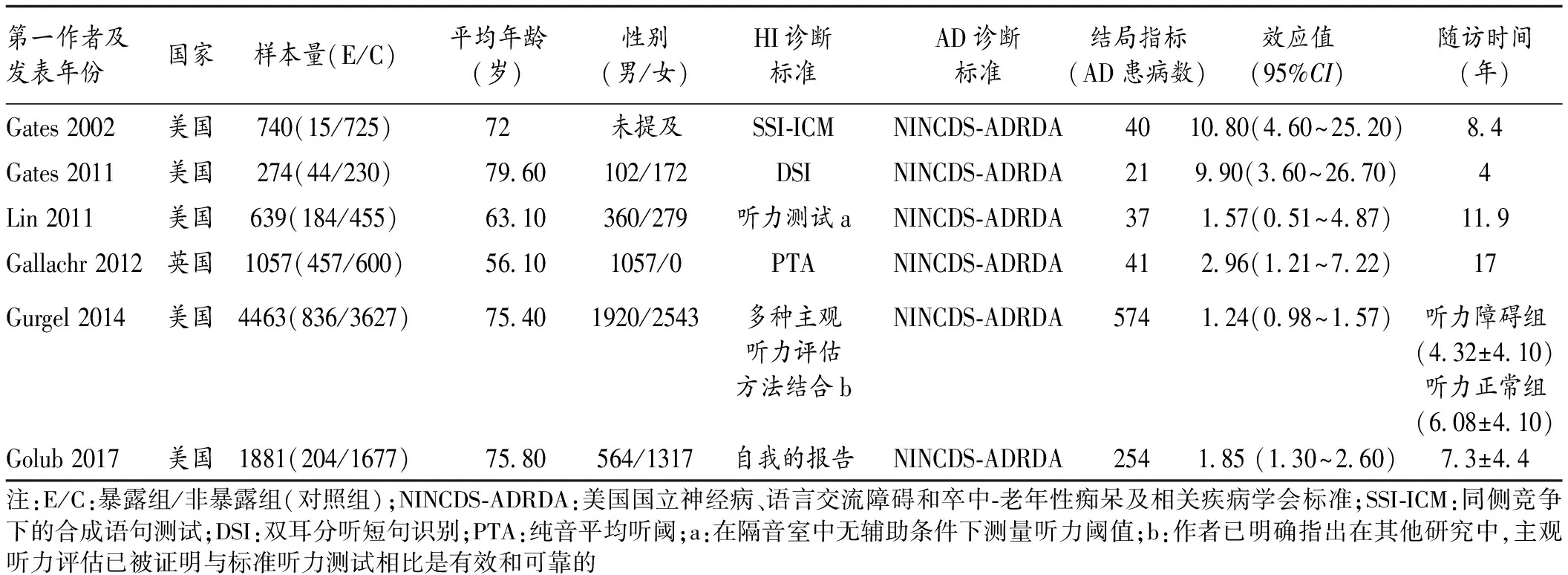
表1 纳入研究的基本信息
2.3 Meta分析结果
2.3.1 HI病人AD发生风险相关性Meta分析:本次研究的6篇文献,经过异质性检验,I2=87%>50%,Q检验中P<0.00001,提示文献之间存在较大的异质性,故选择随机效应模型进行Meta分析。结果显示HI与AD之间的相关性具有统计学意义(RR=3.00,95%CI:1.58~5.70),HI病人发生AD的风险显著高于听力正常者。见图1。除此之外,考虑其他异质性来源可能为年龄和校正因素等,但是纳入的研究校正因素种类较多,无法进一步进行亚组分析。
2.3.2 敏感性分析:逐一剔除本次研究中的任意一篇文献,并不会影响本次研究的结果,表明通过以上随机效应模型进行Meta分析结果稳定性良好。
2.3.3 偏倚检验:通过绘制漏斗图探讨发表偏倚存在与否,本次研究漏斗图对称,未见明显发表偏倚。见图2。
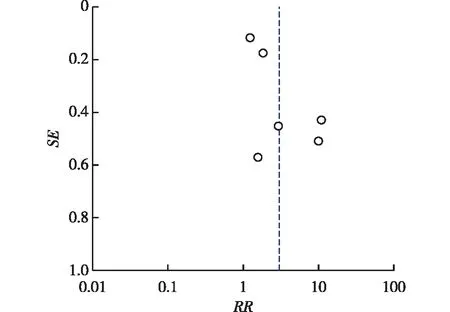
图2 纳入研究的发表偏倚图
3 讨论
自2012年起,痴呆症已被列入世界卫生组织公共卫生优先处理事项。AD报告指出,2019年中国AD患病人数约1000万[16],到21世纪中叶预计人数将超过3000万。
轻度认知功能障碍(mild cognitive impairment,MCI)属于AD的前驱阶段,可在短时间内进一步发展为AD。目前已有研究指出,HI以及听力水平均与MCI以及AD的患病率存在密切关联,存在HI的病人发生MCI以及AD的临床比例明显升高[17]。Davies等[18]报道,相比于正常人群,老年中度HI病人发生认知功能障碍的风险会增高1.4倍,而重度HI病人的认知功能障碍发生风险为正常人群的1.6倍,该学者认为HI会增加认知功能障碍的发生风险,并且可通过措施有效干预、纠正。Golub等[19]也指出,HI与MCI、AD发病率高度相关,改善HI对延缓、预防老年痴呆以及MCI等疾病均具有重要的指导价值。以上学者的研究结果与本次研究结果基本保持一致。但Zheng等[20]在2017年发表的一项Meta分析中指出:HI显著增加MCI的风险,而与AD的风险没有显著差异。
目前,HI与AD之间相关的潜在机制尚不明确,考虑可能有以下几点原因:(1)HI和 AD 之间存在明显的遗传重叠,存在共享的基因组区域。Mitchell等[21]在研究中发现的证据还表明炎症通路在AD中的重要性,但目前的遗传数据并不支持HI是AD的一个可改变的危险因素的假设。也有研究表明,听力损失、认知功能障碍均与C57BL/6J基因表达有关[22]。(2)HI病人的听觉传导通路受损会导致大脑边缘系统、颞叶等其他功能相关脑区及大脑皮层等发生异常改变,进而影响大脑功能,诱发AD[23]。(3)与社会孤立、焦虑抑郁及孤独情绪、社会脱节等有关[7,24]。若病人长期处于听力减弱状态,会减少与他人的交流和沟通,影响社交质量,引起社会性隔离,进而产生抑郁、孤独等负面情绪。(4)HI和认知之间的相互作用可以通过自发的脑活动来反映,认知负荷理论可能是背后的潜在机制[25]。这种代偿效应也可能是HI病人认知能力下降的原因。(5)海马突触退变的发生可能与听力及认知功能下降存在关联[26]。(6)大脑中血管内皮生长因子(vascular endothlial growth factor,VEGF)的表达在正常人和老年性认知功能障碍病人之间存在差异,VEGF在AD病人的颞叶、海马和脑干部位呈低表达,表明其毛细血管功能发生相应改变,研究指出可能是通过调控β-淀粉样蛋白的摄入与代谢,改变病人的颞叶听觉神经中枢,进而对老年性认知功能产生影响,严重者引发HI[27-28]。
本研究存在一定的局限性。(1)最终纳入的原始研究较少,且文献语种为英文,5篇文献来自北美洲的英国,1篇文献来自欧洲的英国,因此存在一定的地域人种差异。(2)6篇文献对于HI的诊断标准不完全一致。(3)HI具有多种类型与临床表现,均可作为验证其与AD相关性的研究思路之一,因此本研究设计方案仍有进一步完善的空间。
综上所述,未来尚需要开展更多大样本、多中心、前瞻性的流行病学调查,对本次研究结果进行验证,同时应该继续探讨HI与MCI以及AD之间相关的机制。对于出现HI的人群,未来应作为临床AD的重点预防对象之一,通过有效的干预、治疗,从而降低AD的发生风险。

