塞来昔布联合化疗对晚期非小细胞肺癌合并慢性阻塞性肺疾病患者的抗炎作用及其机制研究*
唐君媛,张桂新,陈琳,孙雪皎
[广西医科大学附属柳州市人民医院(柳州市哮喘和慢性阻塞性肺疾病诊治及研究重点实验室) 呼吸与危重症医学科,广西 柳州 545006]
肺癌是目前全球癌症相关死亡的主要原因,可能导致肺癌的风险因素主要为吸烟(包括二手烟)、细颗粒物等,非小细胞肺癌(non-small cell lung cancer,NSCLC)约占肺癌总数的80%[1]。NSCLC发病率高,病程短,患者预后差,手术与放疗效果不佳,目前尚无有效的治疗方法[2]。慢性阻塞性肺疾病(chronic obstructive pulmonary diease,COPD)是以持续气流受限为特征的慢性全身性疾病,吸烟是其重要的发病因素。COPD的存在是吸烟者罹患肺癌的最大风险因素,部分患者肺癌合并COPD,其原因可能包括共同存在的危险因素及发病机制[3]。与未合并COPD的肺癌患者相比,合并COPD的早期NSCLC患者的预后不佳。目前,化疗在肺癌治疗领域中仍占主要地位,临床使用的化疗药物在杀伤肿瘤细胞的同时,对某些正常组织细胞也有一定程度的损害[4],部分患者化疗后全身炎症反应增强,影响患者预后[5]。
环氧合酶-2(Cyclooxygenase-2,COX-2)在肺腺癌中上调,COX-2与促进细胞增殖和减少凋亡有关,两者都对侵袭性肿瘤细胞的生长和转移至关重要。最近,有学者发现COX-2抑制剂可以通过抗血管生成、抗炎及促凋亡机制来促进其抗肿瘤作用[6]。塞来昔布是COX-2的选择性抑制剂,塞来昔布能够通过抑制PI3K/Akt信号通路而抑制肿瘤细胞的生长和侵袭。虽然COX-2抑制剂塞来昔布联合化疗被证实在NSCLC的治疗中起到协同作用,能增强化疗药物抗肿瘤的敏感性[7],但对全身炎症反应的影响,目前相关理论依据仍较少,可能与PI3K/Akt信号通路有关[8]。晚期NSCLC合并COPD患者化疗效果欠佳,严重影响生活质量。因此,探索塞来昔布联合化疗是否能减轻晚期NSCLC合并COPD患者的全身炎症反应,并探讨可能的机制,对患者的预后至关重要。
1 资料与方法
1.1 临床资料
选取2021年3月—2022年10月于柳州市人民医院呼吸与危重症医学科或肿瘤科就诊的ⅢB~Ⅳ期NSCLC合并COPD患者45例。NSCLC患者入组标准:①患者均经细胞学与病理学诊断为ⅢB~Ⅳ期NSCLC;②年龄18~75岁;③ECOG评分为0或1分;④临床中具有可测量的病灶;⑤预计生存期3个月以上;⑥具有良好的骨髓储备功能。NSCLC合并COPD的患者须同时满足以下标准:①既往或者现在有10年以上吸烟史,每年至少10包;②患者肺功能检查提示第1秒用力呼气容积与预计值百分比(FEV1%预计值)为30%~50%,且第1秒用力呼气容积占用力肺活量百分比(forced expiratory volume in one second to forced vital capacity ratio,FEV1%)均< 70%,支气管扩张试验阴性;③入选的患者均为重度稳定期COPD患者,若之前有急性加重,至少在1个月之前;④近2周未应用茶碱、大环内酯类药物等抗炎药物;⑤本研究经柳州市人民医院医学伦理委员会批准,所有患者均签署知情同意书。排除标准:①伴有异常的肝肾功能或活动性感染;②预计生存期< 3个月;③处于哺乳期或妊娠期;④伴有第二肿瘤;⑤因为其他原因预期不能完成本研究或研究者认为不应纳入者;⑥其他呼吸道疾病,如支气管哮喘、阻塞性支气管炎、弥漫性多发性气管炎、肺囊性纤维化等;⑦患者有不稳定的心血管病史,如严重的心律失常、心力衰竭、不稳定型心绞痛及心肌梗死等;⑧对实验药物过敏,无法耐受整个研究过程;⑨研究期间因出现其他疾病或者严重不良反应等需要更改治疗方案。
1.2 分组
将入选的45例ⅢB~Ⅳ期NSCLC合并COPD的患者分为常规剂量组(塞来昔布200 mg,2次/d,第1~5天联合化疗)、小剂量组(塞来昔布200 mg,1次/d,第1~5天联合化疗)及化疗组(单独化疗),每组15例。COPD患者的常规治疗方案不变。
1.3 方法
1.3.1 治疗方案 常规剂量组:患者均使用塞来昔布200 mg,2次/d,第1~5天联合化疗;小剂量组:患者均使用塞来昔布200 mg,1次/d,第1~5天联合化疗;化疗组:患者单独化疗。COPD患者的常规治疗方案不变。塞来昔布胶囊[法玛西亚普强(中国)有限公司,规格:200 mg/粒,第1~5天口服]。化疗方案:①化疗前预处理:为减轻药物毒性,入组患者每日需口服叶酸制剂或含有叶酸的复合维生素(350~1 000 μg)。在给药前7 d内,患者须接受1次维生素B12(1 000 μg)肌内注射。使用化疗药物前后进行补充足量液体水化治疗。②化疗:培美曲塞(江苏豪森药业集团有限公司,规格:0.2 g/支,500 mg/m2静脉滴注,第1天用完)联合顺铂或者卡铂。顺铂:南京先声东元制药有限公司,规格:10 mg/支,80 mg/m2静脉滴注,分第1~3天用完。卡铂的用法及用量:按血药浓度-时间曲线下面积(area under the curve,AUC)和肌酐清除率计算卡铂剂量:卡铂(mg)=所设定的ΔAUC [mg/(mL·min)]×[肌酐清除率(mL/min)+25]。AUC取值:取5~7。单次给药,第1~21天为1个周期。COPD患者的常规治疗方案:所有COPD患者按照常规治疗方案,包括吸入性长效抗胆碱能药物、长效的β受体激动剂、吸入性长效抗胆碱能药物+长效的β受体激动剂、吸入性皮质类固醇+长效的β受体激动剂等。所有患者在化疗期间无急性加重表现。
1.3.2 外周血的提取与保存 所有患者分别于治疗前及治疗4个周期后抽取5 mL外周血,4 ℃、3 500 r/min离心5 min,提取上清液置于-80 ℃冰箱冷冻保存,用于检测各组外周血上清液IL-6及TNF-α水平。
1.3.3 外周血炎症因子检测 酶联免疫吸附试验(enzyme-linked immunosorbent assay,ELISA)检测外周血清白细胞介素-6(Interleukin-6,IL-6)及肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)水平,ELISA试剂盒购自美国Linco research公司。
1.3.4 p-Akt、t-Akt蛋白的水平测定 Western blotting检测外周血细胞内PI3K/Akt通路关键蛋白磷酸化Akt(p-Akt)及总Akt(t-Akt)相对表达量。
1.3.5 肺功能的检测 使用肺功能仪于治疗前及治疗4周期后对患者进行肺功能检查,包括第1秒用力呼出气量容积(forced expiratory volume in one second,FEV1)、FEV1%及FEV1%预计值。每次测试时重复检测肺功能2次,取最佳值,2次检查的差值< 5%。
1.3.6 疗效及毒副反应评估 根据实体肿瘤疗效评定标准(RECIST1.1)治疗4个周期后进行评估。目标病灶消失为完全缓解(complete response,CR);目标病灶肿瘤最大径退缩≥ 30%为部分缓解(partial response,PR);目标病灶肿瘤最大径增大20%或有新病灶出现为疾病进展(progressive disease,PD);未达到PR,且不及PD为疾病稳定(stable disease,SD);缓解率(remission rate,RR),临床获益率(clinical benefit rate,CBR)。RR(%)=(CR+PR)病例数/可评估病例总数×100%;CBR(%)=(CR+PR+SD)病例数/可评估病例总数×100%。根据CTCAE 4.03版评估化疗毒副反应。
1.4 统计学方法
数据分析采用SPSS 22.0统计软件。计量资料以均数±标准差(±s)表示,比较用方差分析,进一步两两比较用LSD-t检验;计数资料以构成比或率(%)表示,比较用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 3组患者的一般情况比较
化疗组、常规剂量组、小剂量组患者平均年龄分别为(60.2±2.3)、(63.5±1.6)、(58.9±5.1)岁,3组患者平均年龄比较,经方差分析,差异无统计学意义(F=0.810,P=0.376)。3组患者均为男性且均有吸烟史。
2.2 3组患者临床疗效及毒副反应比较
所有患者顺利完成4周期的治疗,临床评估治疗有效。3组患者均有恶心、呕吐、白细胞下降等药物不良反应。3组患者治疗后RR和CBR的比较,差异均无统计学意义(P>0.05);3组患者不良反应发生率比较,差异无统计学意义(P>0.05)。见表2。
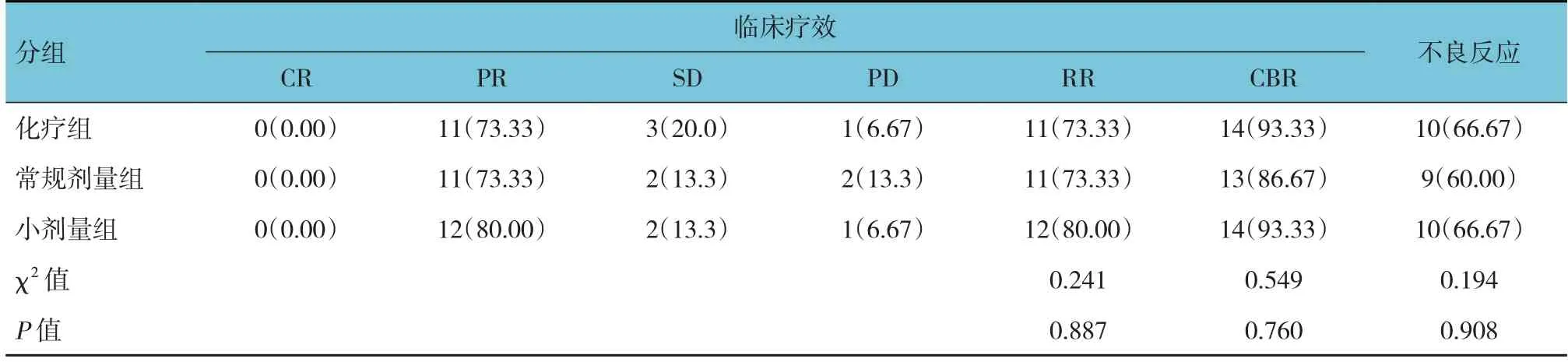
表2 3组临床疗效及毒副反应情况比较 [n=15,例(%)]
2.3 3组治疗前后FEV1、FEV1/%、FEV1%预计值、比较
经4周期治疗后,3组治疗前后肺功能(FEV1、FEV1/%、FEV1%预计值)比较,经方差检验,差异均无统计学意义(P>0.05)。见表3。
表3 3组患者治疗前后肺功能指标比较 [n=15,ng/mL,±s]
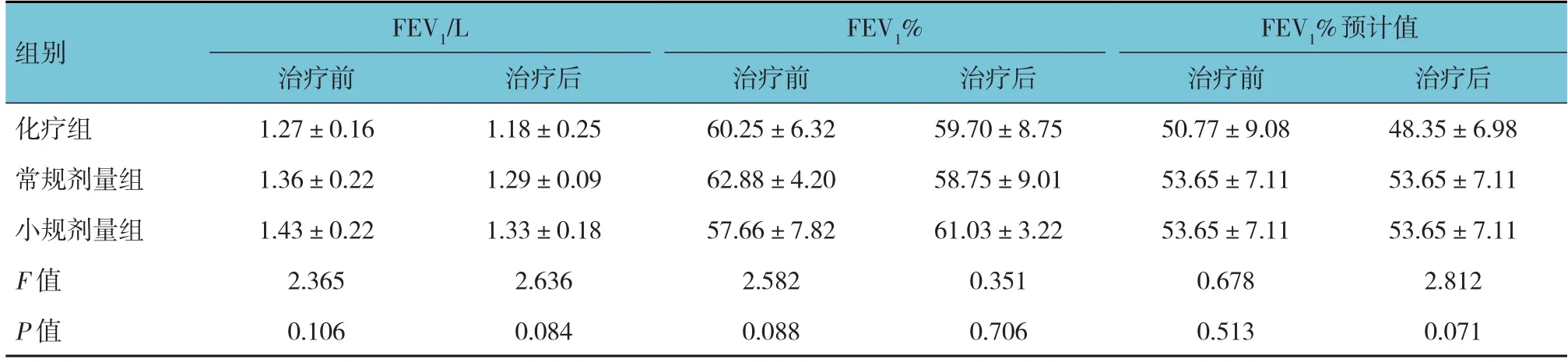
表3 3组患者治疗前后肺功能指标比较 [n=15,ng/mL,±s]
组别FEV1/L治疗后1.18±0.25 1.29±0.09 1.33±0.18 2.636 0.084治疗前1.27±0.16 1.36±0.22 1.43±0.22 2.365 0.106 FEV1%治疗前60.25±6.32 62.88±4.20 57.66±7.82 2.582 0.088治疗后59.70±8.75 58.75±9.01 61.03±3.22 0.351 0.706化疗组常规剂量组小规剂量组F 值P 值FEV1%预计值治疗前50.77±9.08 53.65±7.11 53.65±7.11 0.678 0.513治疗后48.35±6.98 53.65±7.11 53.65±7.11 2.812 0.071
2.4 3组治疗前后IL-6及TNF-α水平比较
治疗后3组患者IL-6比较,差异有统计学意义(P<0.05)。化疗组与常规剂量组比较,差异有统计学意义(P<0.05);常规剂量组与小剂量组比较,差异无统计学意义(P>0.05)。治疗后3组患者TNF-α比较,差异有统计学意义(P<0.05)。化疗组与常规剂量组患者比较,差异有统计学意义(P<0.05),常规剂量组与小剂量组比较,差异无统计学意义(P<0.05)。见表4。
表4 3组患者治疗前后炎症因子的比较 (n=15,pg/mL,±s)
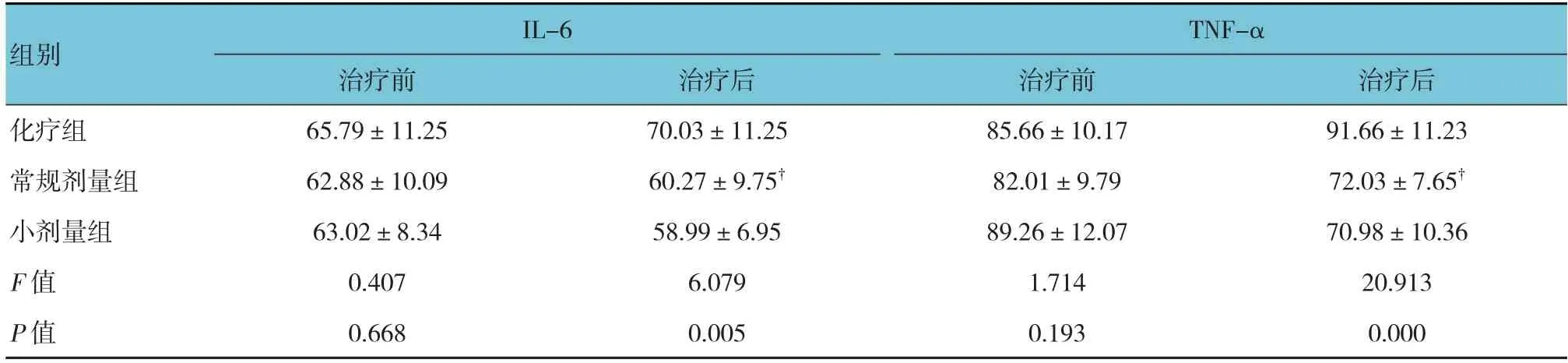
表4 3组患者治疗前后炎症因子的比较 (n=15,pg/mL,±s)
注:†与化疗组比较,P <0.05。
组别IL-6 TNF-α化疗组常规剂量组小剂量组F 值P 值治疗后91.66±11.23 72.03±7.65†70.98±10.36 20.913 0.000治疗前65.79±11.25 62.88±10.09 63.02±8.34 0.407 0.668治疗后70.03±11.25 60.27±9.75†58.99±6.95 6.079 0.005治疗前85.66±10.17 82.01±9.79 89.26±12.07 1.714 0.193
2.5 3组治疗前后外周血细胞内p-Akt、t-Akt蛋白相对表达量比较
治疗4个周期后3组Akt蛋白相对表达量比较比较,差异均有统计学意义(P<0.05)。化疗组与常规剂量组、小剂量组比较,差异均有统计学意义(P<0.05);常规剂量组与小剂量组比较,差异无统计学意义(P>0.05)。见表5和图1。
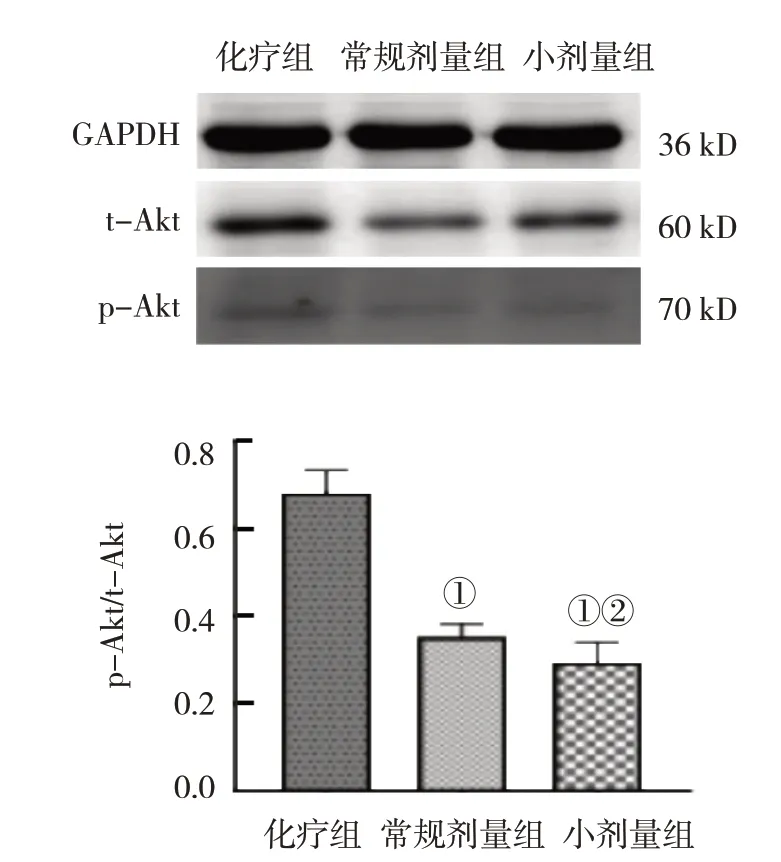
图1 3组患者治疗后外周血细胞内Akt蛋白表达
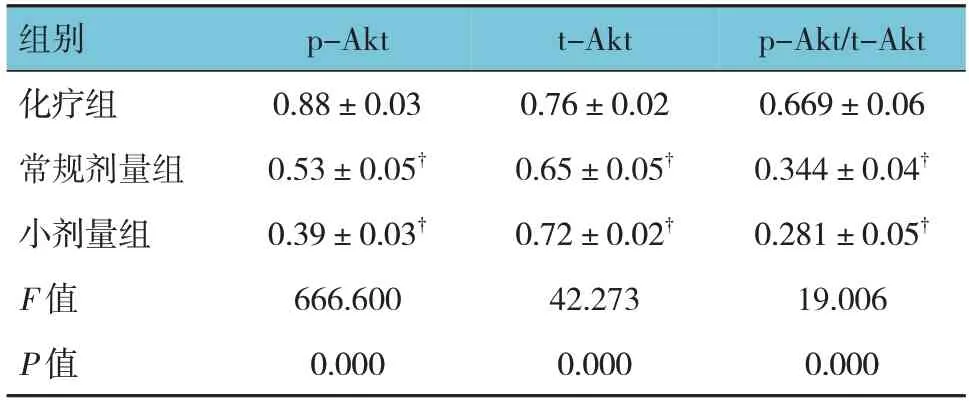
表5 3组患者治疗后外周血细胞内Akt蛋白相对表达量的比较 (n=15)
3 讨论
NSCLC是一种与环境和遗传因素相关且高度异质性的疾病,确诊后的晚期肺癌患者5年生存率<15%,目前尚无有效治疗方法。COPD是肺癌的驱动因素,气流阻塞严重程度是肺癌的一个独立风险因素。国家综合癌症网络(NCCN)建议将铂基化疗作为具有非驱动基因的晚期NSCLC患者的一线药物[9]。然而卡铂加紫杉醇的治疗方案会导致3级或更高的毒性,其潜在的并发症和低于最佳的存活率,使最终化疗效果令人不满意[10]。晚期NSCLC合并COPD患者化疗后全身炎症反应加重,尤其是对于COPD患者,可能导致COPD的急性加重,从而影响化疗药物的应用及患者对治疗的信心。塞来昔布是COX-2的选择性抑制剂,是一种成熟的抗炎药物。越来越多的研究表明,COX-2过度表达与肿瘤发育、肿瘤进展、肿瘤特征及存活率低下有关。选择性COX-2抑制剂可以抑制肺癌细胞的生长,并提高化疗在晚期NSCLC中的疗效[11]。本研究结果表明,经过4周期的治疗,塞来昔布联合化疗较单独化疗未增加药物不良反应,且所有患者临床评估治疗有效。塞来昔布组经过4周期的治疗后,炎症因子IL-6、TNF-α水平明显低于化疗组,塞来昔布联合化疗提高了整体反应率,减轻了患者化疗后的全身炎症反应,改善患者生活质量,提高治疗效果。
ALTORKI等[12]率先将塞来昔布与紫杉醇/卡铂联合用于NSCLC的Ⅱ期临床试验表明,塞来昔布可增加紫杉醇和卡铂的敏感性,明显降低患者的前列腺素E2浓度。NUGENT等[13]使用了塞来昔布联合多西他塞对含铂方案一线化疗失败的晚期NSCLC患者;结果显示,该药物可以显著延长肿瘤进展,且副作用无明显提高。以上研究均提示COX-2抑制剂联合化疗有效且安全,塞来昔布可能是有前途的抗癌药物,同时能减轻患者化疗后全身炎症反应。在一项晚期结直肠腺瘤的临床随机安慰剂对照试验中,接受安慰剂的患者估计累计发病率为17.2%,而塞来昔布200 mg,2次/d治疗的患者为7.8%,塞来昔布400 mg,2次/d治疗的患者为6.3%。为期3年的治疗里,18.8%安慰剂组患者报告了至少1次严重的不良事件,接受200 mg,2次/d塞来昔布的患者为20.4%,接受400 mg,2次/d塞来昔布的患者为23.0%[14],说明使用不同剂量的塞来昔布可能与不良事件风险有关。同样的,本研究结果表明,正常剂量塞来昔布(200 mg,2次/d)与小剂量塞来昔布(200 mg ,1次/d)均能减轻化疗后的全身炎症反应。与单独化疗组相比,使用塞来昔布联合化疗未增加患者的药物不良反应及临床毒副作用。同时在肺功能方面,患者治疗前后并无明显改变。
研究显示,PI3K/Akt通路与NSCLC细胞存活、增殖、凋亡及血管新生调节有关[15]。塞来昔布参与了ERK1/2 MAPK和PI3K/Akt途径,具有抗血管生成作用。烟草烟雾暴露能够导致单核细胞HDAC2表达下降,p-Akt表达升高;PI3K抑制剂能够减轻烟草烟雾暴露下人单核细胞的糖皮质激素抵抗。在PI3K/Akt信号传导通路中,HDACs(主要是HDAC2)的活性显著降低,并能促进COPD的炎症反应。但对于塞来昔布联合化疗减轻晚期NSCLC合并COPD患者的全身炎症反应的相关机制,国内外均无类似研究。为明确可能的抗炎机制,本研究应用Western blotting检测两组患者治疗前后外周血细胞内PI3K/Akt通路关键蛋白(p-Akt及t-Akt)的表达,结果显示常规剂量组和小剂量组治疗4周期后外周血细胞内p-Akt蛋白相对表达量明显低于化疗组,由此证实塞来昔布通过作用于外周血细胞PI3K/Akt通路关键蛋白(p-Akt及t-Akt)的表达提高化疗药物抗肿瘤的敏感性。塞来昔布联合化疗可能通过PI3K/Akt途径诱导细胞凋亡,减轻患者化疗后全身炎症反应,联合治疗的抗肿瘤效果较单独化疗更佳。
综上所述,塞来昔布联合化疗通过抑制PI3K/Akt通路,减少晚期NSCLC合并COPD患者化疗后的炎性介质释放,降低患者化疗后的全身炎症反应。塞来昔布联合化疗较单独化疗未增加药物不良反应,对患者肺功能无明显影响,小剂量塞来昔布与常规剂量塞来昔布无明显差异。在进行研究的过程中,符合入组条件的患者均为男性,同时本研究中所包含的研究例数较少,对数据结果有一定的影响。NSAIDs类药物可能导致不同程度的胃肠道及心血管血栓事件。因此,进一步降低塞来昔布剂量是否具有同样抗炎作用,未来还需要纳入更大病例数进行更深入的探讨。总之,本研究结果为晚期NSCLC合并COPD患者的治疗提供新思路,以期改善患者生活质量,提高疗效,使患者获益。

