铜金属水凝胶的制备及其催化CuAAC反应的实验设计
陈韶蕊, 余旭东
(河北科技大学理学院,石家庄 050018)
0 引言
“点击反应”是以合成碳-杂原子键(C-X-C)为基础的组合化学新方法,其中最具有代表性的是铜催化的叠氮-炔基环加成反应(CuAAC),广泛应用于药物合成、生物缀合和功能材料等领域[1-3]。但是一价铜盐的热不稳定性,很容易发生歧化反应生成Cu(0)和Cu(Ⅱ),且如果铜盐的浓度低会使反应产率较低[4];而含重金属铜离子的水排放到自然环境中,将会严重污染人类赖以生存的地表水和地下水;同时人类吸入过量铜,肝、肾和脑中会沉积过量铜而引起威尔逊症。因此研究高效、可重复利用的铜盐催化剂具有重要的意义。
金属凝胶是通过金属离子与凝胶因子的配位作用组装成的一类特殊的功能材料,其中铜金属凝胶广泛应用于离子视别、化学传感和催化等方面[5-7]。当前应用铜金属凝胶催化CuAAC反应的铜盐价格昂贵,且多是在有机溶剂或混合溶剂中加热回流进行[8-9]。依照当前“省资源、少污染,减成本”的绿色化学的教学理念,本文设计合成了三联吡啶的衍生物,与硫酸铜配位组装得铜金属凝胶,并在室温下以水为溶剂利用铜金属凝胶催化CuAAC反应。利用扫描电子显微镜、X射线衍射仪、电子顺磁共振光谱仪和BET比表面积测试等表征凝胶的形貌及结构,探讨了影响凝胶催化CuAAC反应的原因及催化剂的重复使用的催化效率。
1 实验设计
本文设计的“铜金属水凝胶的制备及其催化CuAAC反应”的实验,其主要过程:①用有机合成的方法制备基于三联吡啶-氮氧化合物的凝胶因子;②用超声和加热-冷却两种作用方式,组装铜金属水凝胶;③用紫外吸收光谱,电子顺磁共振,扫描电子显微镜和X射线衍射对铜金属凝胶进行表征;④将铜金属干凝胶催化CuAAC反应。
2 实验过程
2.1 实验原理
凝胶因子TPA的合成路线如下:
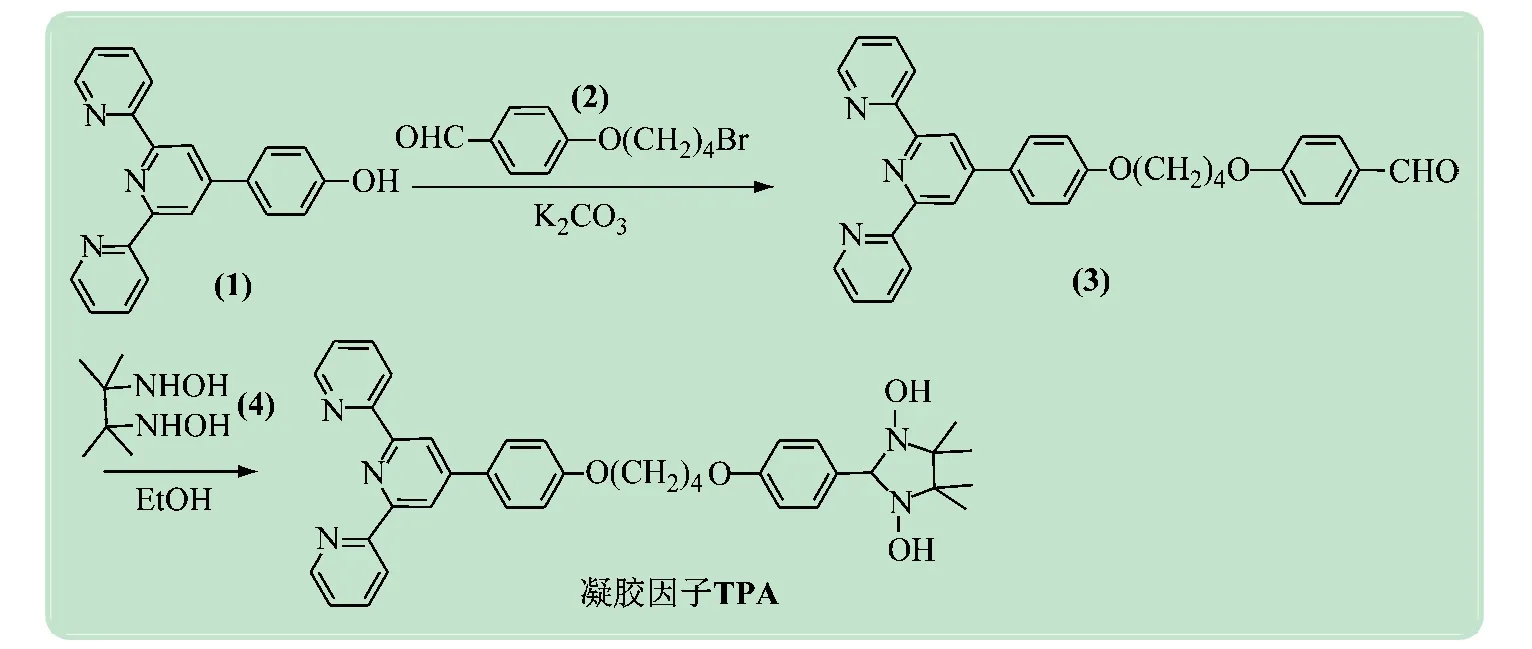
注:(1)表示4-(4-羟基苯基)-2,2';6',2'-三联吡啶;(2)表示4-(4-溴丁氧基)-苯甲醛;(3)表示4-[4-(4-[2,2';6',2']三联吡啶-4'-基-苯氧基)-丁氧基]-苯甲醛;(4)表示2,3-二甲基-2,3-二羟胺基丁烷;凝胶因子TPA表示4' -(4-{4-[4-(4,4,5,5-四甲基咪唑啉-2-基)-苯氧基]-丁氧基}-苯基)-[2,2';6',2']三联吡啶
2.2 实验仪器和试剂
(1)实验仪器。实验涉及的主要仪器:RE-52A旋转蒸发仪;500 兆核磁共振波谱仪(Nuclear Magnetic Resonance Spectrometer,NMR);UH5300 紫外吸收光谱仪(Ultraviolet absorption spectrum,UV-vis);MS-5000 电子顺磁共振光谱仪(Electron Paramagnetic Rresonance,EPR);FE-SEM S-4800 扫描电子显微镜(Scanning Electron Microscope,SEM);AXS D8 X 射线衍射仪(XRay Diffraction,XRD);红外光谱仪(Infrared spectrometer,IR)溴化钾(KBr)压片;薄层色谱(Thin-Layer Chromatography,TLC)。
(2)实验试剂。实验所用试剂主要有碘化钾、碳酸钾、氯仿、苯乙炔、苄基叠氮、五水硫酸铜、乙酸乙酯、二氯甲烷、氘代氯仿,国药集团试剂有限公司;薄层色谱硅板(GF254)和柱层析硅胶75 ~48 nm,青岛海洋化工有限公司;N,N-二甲基甲酰胺(N,Ndimethylformamide,DMF)。
2.3 凝胶因子的制备
(1)中间体(3)的合成及结构表征。将1. 0 g(3.1 mmol)4-(4-羟基苯基)-2,2',6',2'-三吡啶(1)、1.0 g(4.0 mmol)4-(4-溴丁氧基)-苯甲醛(2)、0.1 g(0.6 mmol)碘化钾、0.9 g(6.2 mmol)碳酸钾和40 mL干燥DMF加到100 mL圆底烧瓶中;120 ℃下搅拌12 h,TLC 检测反应完全。加50 mL 水淬灭反应,CH2Cl2萃取(50 mL×3)、水洗(100 mL ×3)、干燥、旋蒸得粗品。柱色谱分离得白色固体(3),产率为60.1%。IR(KBr):3072、2957、1683、1604、1578、1508、1250、790 cm-1;1H NMR(500 MHz,CDCl3)δ:9.89(s,1H,—CHO),8. 73(d,J=4. 5 Hz,2H,Py),8.71(s,2H,Py),8. 67(d,J=7. 5 Hz,2H,Py),7.90-7.87(m,4H,Py),7.84(d,J=8.5 Hz,2H,Ph),7. 37-7. 34(m,2H,Ph),7. 04-7. 00(m,4H,Ph),4.15-4.13(m,4H,—OCH2—),2.05(s,4H,—CH2—)。
(2)凝胶因子TPA 的合成及结构表征。将化合物(3)(0.51 g,1.0 mmol),化合物(4)(0.2 g,1.3 mmol),3-4 滴甲酸和15 mL甲醇/氯仿的混合溶液(体积比2∶1)加到50 mL的圆底烧瓶中,加热回流8 h,冷至室温。过滤得粗产品,氯仿重结晶得白色固体,产率76.8%。m.p. 156-158 ℃;IR(KBr):3514,3051,2929,1607,1546,1246,792 cm-1;1H NMR(500 MHz,DMSO-d6)δ(×10-6):8. 77(d,J=4. 0 Hz,2H,Py),8.67(d,J=12.0 Hz,4H,Py),8.03(t,J=7.5 Hz,2H,Py),7. 88(d,J=8. 5 Hz,2H,Py),7.69(s,2H,—NOH),7.53(t,J=5.5 Hz,2H,Ph),7.37(d,J=8.0 Hz,2H,Ph),7.14(d,J=8.5 Hz,2H,Ph),6.90(d,J=8.5 Hz,2H,Ph),4.47(s,1H,—CH),4. 13(s,2H,—OCH2—),4. 05(s,2H,—OCH2—),1.91(s,4H,—CH2—),1.07(s,6H,—CH3),1.04(s,6H,—CH3)。13C NMR(125 MHz,DMSO-d6)δ(×10-6):160.3,158.5,156.1,155.6,149.8,137.9,134.5,130.1,128.7,124.9,121.4,117. 7,115. 8,114. 1,90. 4,67. 9,67. 6,66.4,25.9,24.9,17.7。
2.4 铜金属水凝胶(Cu-MG)的制备
利用“倒置试管法”构筑凝胶[10],色谱瓶中加入凝胶因子TPA(5 mg,8 μmol)、五水硫酸铜(4 mg,16 μmol)和200 μL 纯水,混合物经超声或加热-冷却后静置5 ~10 min,将试管倒置,保持原来的形状没有坍塌,说明成功制备了凝胶。
2.5 Cu-MG干凝胶催化CuAAC反应
将1.0 mmol苯乙炔、1.2 mmol苄基叠氮、催化剂3 mol%(以铜离子计)和3 mL 溶剂加入圆底烧瓶中,室温下搅拌反应8 ~10 h,加入5 mL水,乙酸乙酯萃取(10 mL ×3),合并有机相,无水硫酸镁干燥、过滤、旋转蒸发得白色粉末状固体。柱色谱分离(VCH2Cl2∶VCH3COOC2H5=10 ∶1)得白色蓬松状固体。m. p. 125 ~127 ℃,与文献值相符[11]。
3 结果与讨论
3.1 Cu-MG的紫外-可见吸收光谱表征
在利用超声和加热-冷却方法制备凝胶的过程中发现了一个现象,加热-冷却制备得到的凝胶是绿色的,而超声制备的凝胶是蓝色的,如图1 所示。

图1 加热-冷却和超声制备的铜金属凝胶
(1)紫外吸收光谱。利用紫外对TPA 的溶液和凝胶进行了表征,如图2 所示。由图2 可知,TPA 溶液的最大紫外吸收峰在367 nm,而TPA/CuSO4溶液和2 种铜金属凝胶Cu-MG 的最大吸收峰均蓝移到347 nm,说明铜离子与TPA 进行了配位作用,而蓝色的Cu-MG在600 nm 处出现了一个宽峰,推测可能是形成了氮氧自由基。
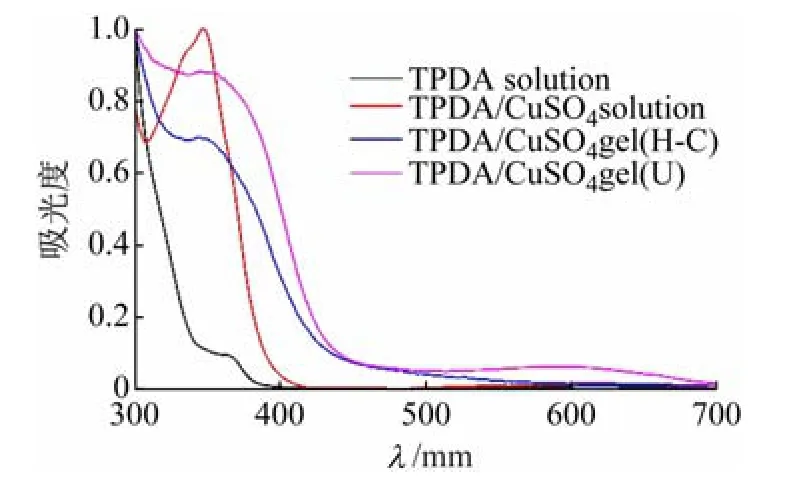
图2 TPA溶液和铜金属凝胶(Cu-MG)的UV-vis
(2)电子顺磁共振谱。图3 所示为铜金属,凝胶的EPR,由图可知,2 种金属凝胶在323 mT 的峰是铜离子的顺磁共振峰[12],而在336 mT 的峰只在Cu-MG(U)凝胶中出现,且g值为2.007,与文献报道的氮氧自由基的g值一致[13],因此确认了正是由于超声产生了氮氧自由基才造成凝胶的颜色变成了蓝色。
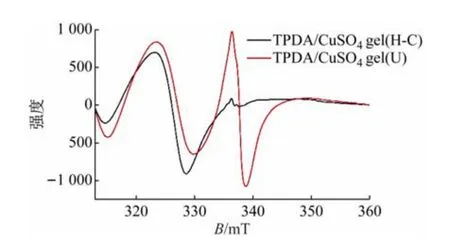
图3 铜金属凝胶(Cu-MG)的EPR共振谱
3.2 Cu-MG的形貌和组装方式表征
图4 所示为SEM 观察铜金属凝胶的微观形貌。由图4(a)、(b)可知,通过加热-冷却得到的铜金属凝胶呈片状花瓣形,而超声得到的金属凝胶呈纤维交织结构。

图4 2 种Cu-MG 的SEM 图 (a、b)Cu-MG(H-C),(c、d)Cu-MG(H-C)
为进一步研究凝胶的聚集方式,进行了XRD 表征,如图5 所示。由图5(a)可知,加热-冷却制备的铜金属凝胶在衍射角3.18°,其层间距d=2.77 nm,大于凝胶因子TPA 的分子长度(2.61 nm)。超声得到的凝胶在衍射角为8.3°、16.2°和23.9°处其d值分别为1.07、0.55 和0.37 nm,其比例关系为1∶1/2∶1/3,表明形成了有序的层状结构。
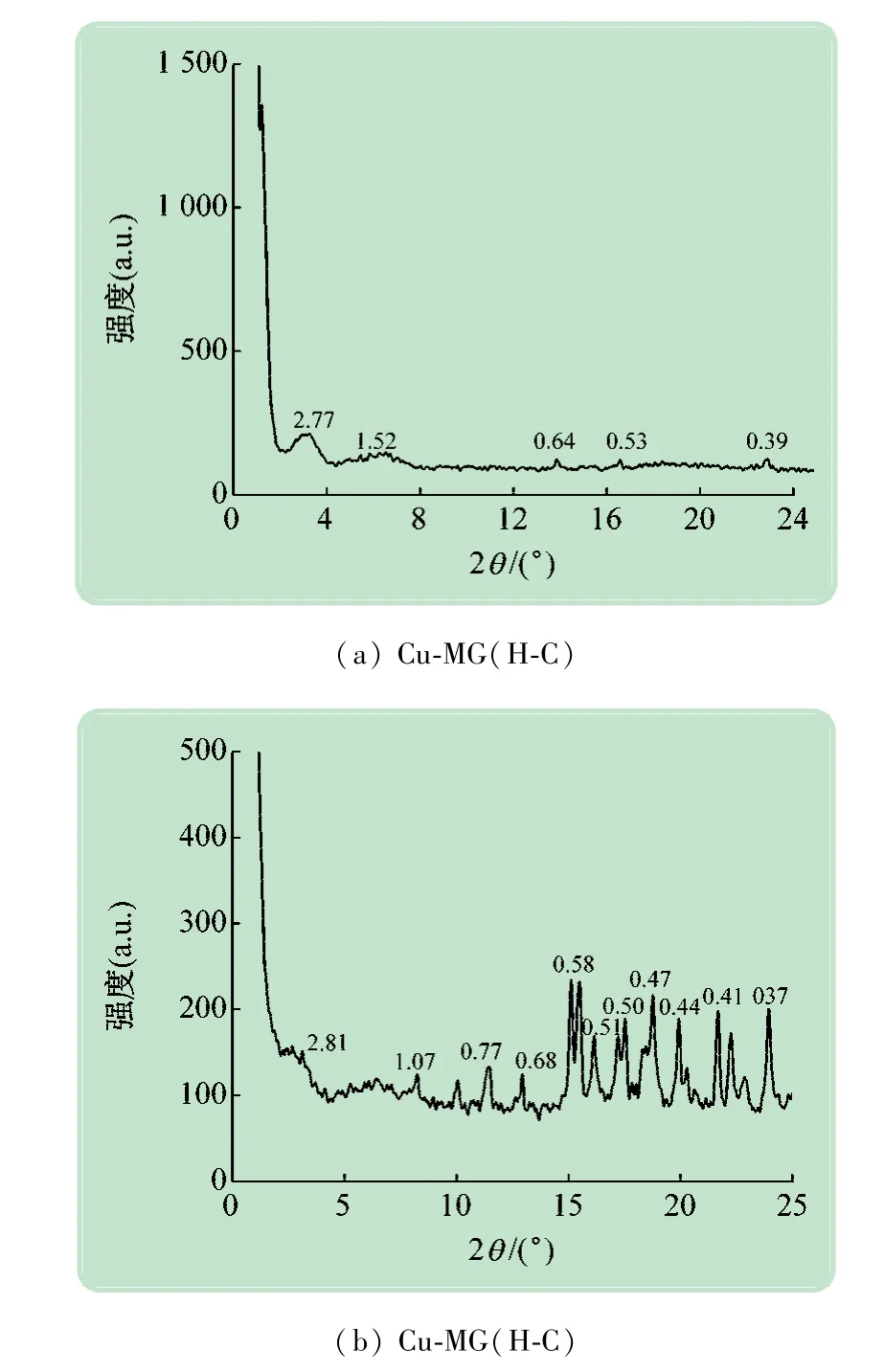
图5 2种Cu-MG的XRD
3.3 金属干凝胶的BET比表面积
将2 种铜金属凝胶冷冻得干凝胶,并在77 K下进行N2的吸附-解吸,如图6 所示。由图可知:加热-冷却得到的铜金属凝胶的比表面积为342 m2/g,超声得到的铜金属凝胶的比表面积为213 m2/g,根据密度泛函理论(NLDFT)计算,可知二者均是介孔材料[14],这一结果与XRD结果一致。
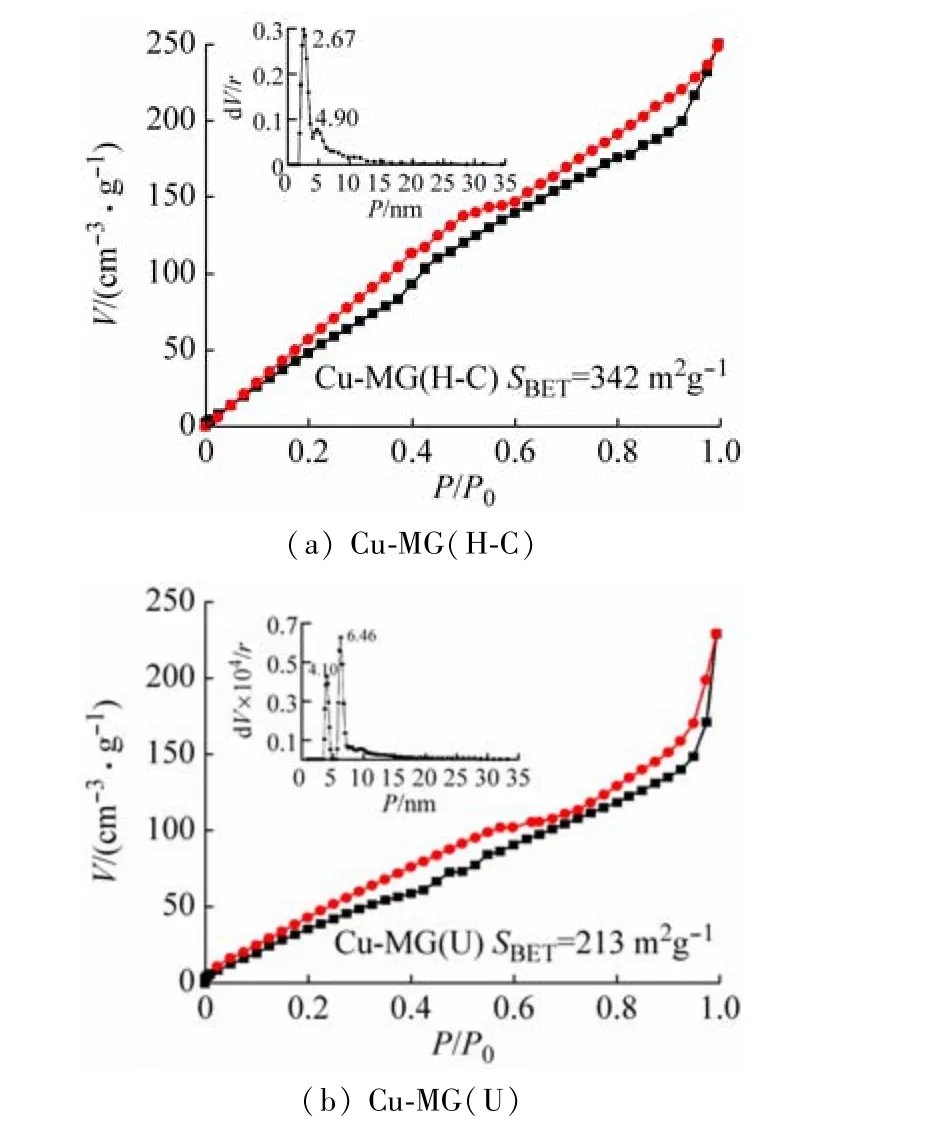
图6 77 K下吸附/解吸等温曲线
3.4 铜金属干凝胶催化CuAAC反应
利用Cu-MG干凝胶催化CuAAC反应,结果见表1所列。以纯水、THF和THF/水的混合溶液做溶剂时,加热-冷却得到的铜金属干凝胶(Cu-MG(H-C))的产率均高于干凝胶(Cu-MG(U))和经典的硫酸铜,用纯水做溶剂时产率最高达78%,且过滤后得到的催化剂经3 次重复使用产率略有降低(见图7)。Cu-MG(HC)干凝胶的催化效率较高的原因可能是由于其比表面积较大(见图6),扩大了催化网络和协同作用从而提高了其催化效率[15]。
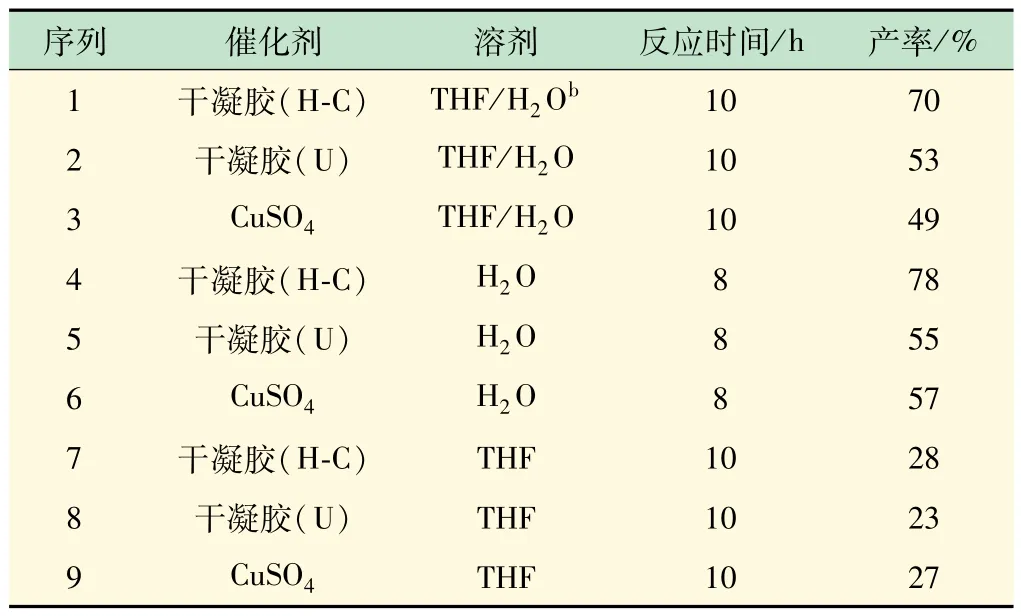
表1 不同催化剂和溶剂条件下的CuAAC反应
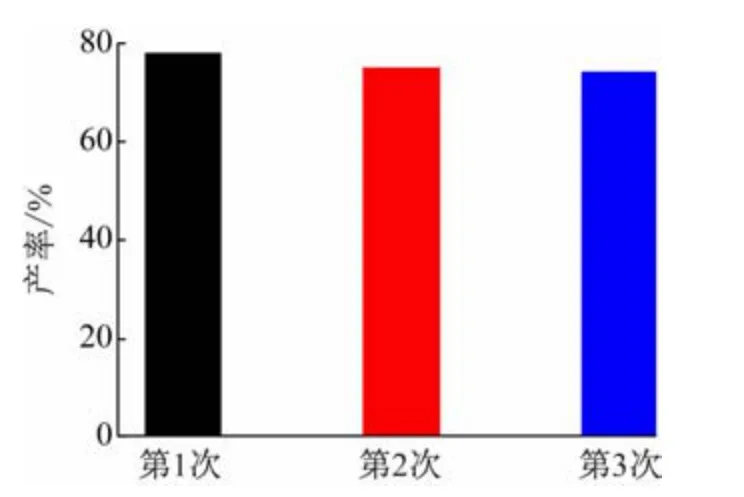
图7 3次重复实验Cu-MG(H-C)干凝胶催化CuAAC 反应的效率
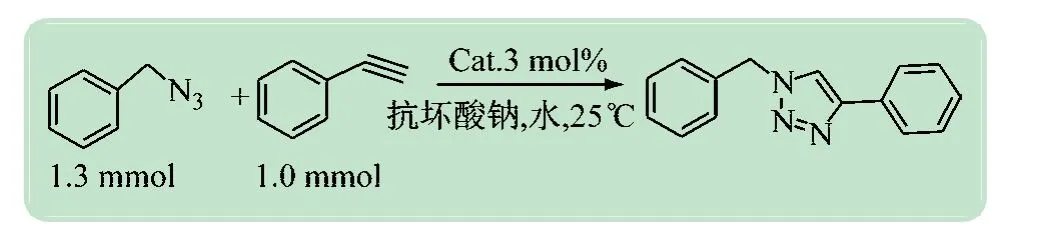
利用苄基叠氮和苯乙炔为模型研究铜金属干凝胶催化CuAAC反应,即:
4 结语
本实验利用有机合成的方法制备了凝胶因子TPA,通过超声和加热-冷却制备了2 种不同颜色的金属凝胶,利用SEM、XRD和EPR对2 种金属凝胶进行了表征,实验结果表明:由EPR 可知超声产生了氮氧自由基造成凝胶颜色变蓝;将铜金属干凝胶应用于催化CuAAC 反应,最高产率达78%。此反应在室温下进行,以水为溶剂,具有操作简单,催化效率高等优点,且催化剂重复使用3 次后催化效率略有降低,这对解决能源短缺和环境污染等具有重要的应用价值。

