硬尖神香草的化学成分研究
刘 畅,孙照翠,夏提古丽·阿不利孜,马国需, ,石磊岭*,张 晶
硬尖神香草的化学成分研究
刘 畅1, 2,孙照翠3,夏提古丽·阿不利孜2,马国需2, 3,石磊岭2*,张 晶1*
1. 吉林农业大学中药材学院,吉林 长春 130118 2. 新疆维吾尔自治区中药民族药研究所,新疆 乌鲁木齐 830002 3. 中国医学科学院 北京协和医学院药用植物研究所,北京 100193
研究硬尖神香草地上干燥部分的化学成分。采用硅胶柱色谱、高效液相色谱技术等进行分离纯化,通过现代波谱学技术对所得化合物进行结构鉴定,并采用MTT比色法对分离得到的化合物进行体外抑制人胃癌HGC-27细胞的活性筛选。从神香草95%乙醇提取物中分离得到9个化合物,分别鉴定为4-(2-羟基异丙基)-环己烷-2-烯-1-酮(1)、(3,4a,5,6)-6-羟基-4a,5-二甲基-3-(丙-1-烯-2-基)-3,4,4a,5,6,7-六氢萘-1(2)-酮(2)、对茴香酸(3)、三裂鼠尾草素(4)、5-羟基-6,7,3,4-四甲氧基黄酮(5)、蓟黄素(6)、--香豆醇乙醚(7)、()--香豆醇γ--甲醚(8)、4-羟基-3-甲氧基乙基肉桂酸盐(9)。其中,化合物1为新化合物,命名为神香草酮A。对化合物1~9进行抗肿瘤活性筛选,结果显示,化合物1、3、8对HGC-27胃癌细胞具有一定的抑制作用,其半数抑制浓度(median inhibition concentration,IC50)值分别为8.76、16.34、25.28 μmol/L。化合物1为新化合物,化合物5~9为首次从该属植物中分到。
硬尖神香草;抗肿瘤作用;神香草酮A;对茴香酸;蓟黄素;()--香豆醇γ--甲醚
神香草为唇形科(Lamiaceae)神香草属L.植物硬尖神香草Boriss.的干燥全草,是维吾尔族民间习用药[1]。神香草是一种亚灌木,高度可达30~60 cm,生长在海拔约1100~1800 m有砾石或干燥的山坡上,主要分布在中国新疆地区、蒙古、哈萨克斯坦和俄罗斯[2]。其维吾尔语称“祖发”,人工栽培者二级干热,气芳香、味苦,有祛痰散风、发汗解毒、抗炎消肿、驱肠内小虫的功效[3]。目前,从神香草属植物中分离得到的化合物主要有萜类、黄酮、酚酸类、苯丙素类、甾类等[4-5]。为了进一步研究神香草的药用物质基础,本研究通过对神香草95%乙醇提取物中的化学成分进行分离,从中获得9个单体化合物,分别鉴定为神香草酮A(hyssopusone A,1)、(3,4a,5,6)-6-羟基-4a,5-二甲基-3-(丙-1-烯-2-基)-3,4,4a,5,6,7-六氢萘-1(2)-酮 [(3,4a,5,6)- 6-hydroxy-4a,5-dimethyl-3-(prop-1-en-2-yl)-3,4,4a,5, 6,7-hexahydronaphthalen-1(2)-one,2]、对茴香酸(-anisic acid,3)、三裂鼠尾草素(salvigenin,4)、5-羟基-6,7,3,4-四甲氧基黄酮(5-hydroxy-6,7,3',4'- tetramethoxy-flavone,5)、蓟黄素(cirsimaritin,6)、--香豆醇乙醚(--coumaryl alcohol ethyl ether,7)、()--香豆醇γ--甲醚 [()--coumaryl alcohol γ--methyl ether,8]、4-羟基-3-甲氧基乙基肉桂酸盐(4-hydroxy-3-methoxy ethyl cinnamate,9)。其中,化合物1为1个新的单萜,化合物5~9为首次从神香草属植物中分到。对化合物1~9进行抗肿瘤活性筛选,结果显示,化合物1、3、8对HGC-27胃癌细胞具有抑制作用,其半数抑制浓度(median inhibition concentration,IC50)值分别为8.76、16.34、25.28 μmol/L。
1 仪器与材料
Bruker Avance III 600型核磁共振波谱仪(德国Bruker公司);赛默飞世(Thermo Fisher)LTQ-ObitrapX液质联用仪(美国Thermo Fisher公司);DLSB-5/10低温冷却液循环泵(郑州长城科工贸有限公司);LC3050N型半制备液相色谱仪(北京创新通恒有限公司);RY C18-A半制备色谱柱(250 mm×10 mm,5 μm,北京中科恩源科技有限公司);RE-2000B型旋转蒸发仪(上海亚荣生化仪器厂);ZF-5型手提紫外分析仪(上海勤科分析仪器有限公司);柱色谱硅胶(创益化工有限公司);薄层色谱硅胶(烟台华阳新材料科技有限公司);常规试剂均为分析纯;娃哈哈水;人胃癌细胞株HGC-27(中国科学院上海细胞研究所);MTT试剂盒(河北费德生物科技有限公司);顺铂(Sigma-aldrich公司)。
神香草于2021年8月采自新疆阿勒泰地区将军山,经新疆中药民族药研究所王果平研究员鉴定为硬尖神香草Boriss,凭证标本号(654301170718057 LY)保存于新疆维吾尔自治区中药民族药研究所标本室。
2 方法
2.1 提取与分离
取神香草10 kg晒干,将干燥全草剪成小段,95%乙醇回流提取3次,每次1.5 h,将提取液合并减压浓缩成浸膏状,得到总浸膏3126 g。总浸膏加水混悬,依次用石油醚、二氯甲烷、醋酸乙酯萃取,分别得石油醚部位191 g、二氯甲烷部位301 g、醋酸乙酯部位121 g。取二氯甲烷部位浸膏经硅胶柱色谱分离,用石油醚-醋酸乙酯(20∶1~5∶1)以及二氯甲烷-甲醇(1∶0~0∶1)梯度洗脱,合并后得到7个流分Fr. 1~7。Fr. 3(9.0 g)进行硅胶柱色谱分离,用石油醚-醋酸乙酯(20∶1~5∶1)以及二氯甲烷-甲醇(1∶0~0∶1)梯度洗脱,合并洗脱液,得到8个组分Fr. 3-1~3-8。其中,Fr.3-4(3.3 g)溶于二氯甲烷时析出黄色针状结晶化合物4(107.3 mg)。Fr. 3-3(2.3 g)经半制备液相色谱分离纯化得化合物3(1.9 mg,R=15.5 min,70%甲醇,2.0 mL/min)。Fr.1(8.5 g)进行硅胶柱色谱分离(200~300目),石油醚-醋酸乙酯(1∶0~0∶1)梯度洗脱,合并相似洗脱液后得到10个组分Fr. 1-1~1-10,Fr. 1-7(0.8 g)经半制备液相色谱分离纯化得化合物7(1.3 mg,R=23.0 min,60%甲醇,2.0 mL/min)、8(1.5 mg,R=17.5 min,2.0 mL/min)。Fr. 4(48.2 g)经硅胶柱色谱分离(200~300目),依次用石油醚-醋酸乙酯(10∶1)以及二氯甲烷-甲醇(1∶0~0∶1)梯度洗脱,合并相似洗脱液得到10个组分Fr. 4-1~4-10。其中Fr. 4-5(4.2 g)经半制备液相色谱分离纯化得化合物6(3.3 mg,R=20.0 min,60%甲醇,2.0 mL/min)。Fr. 4-3(3.8 g)经半制备液相色谱分离纯化得化合物5(2.3 mg,R=20.5 min,60%甲醇,2.0 mL/min)。
石油醚部位浸膏经硅胶色谱柱分离,用石油醚-醋酸乙酯(1∶0~0∶1)及二氯甲烷-甲醇(1∶0~0∶1)梯度洗脱,合并后得到5个流分Fr. 1~5。Fr. 3(15.2 g)经硅胶色谱柱分离(200~300目),经二氯甲烷-甲醇(1∶0~0∶1)梯度洗脱,合并后得到6个组分Fr. 3-1~3-6。Fr. 3-6(1.2 g)经半制备液相色谱分离纯化得化合物2(2.3 mg,R=34.5 min,50%甲醇,2.0 mL/min)。Fr. 3-4(2.1 g)经半制备液相色谱分离纯化得化合物1(3.2 mg,R=30.5 min,30%甲醇,2.0 mL/min)。Fr. 4(39.0 g)经硅胶色谱柱分离(200~300目),经二氯甲烷-甲醇(1∶0~0∶1)梯度洗脱,合并后得到9个组分Fr. 4-1~4-9。Fr. 4-2(2.96 g)经硅胶色谱柱分离(300~400目),经二氯甲烷-甲醇(1∶0~0∶1)梯度洗脱,合并后得到7个组分Fr. 4-2-1~4-2-7。Fr. 4-2-2(0.4 g)经半制备液相色谱分离纯化得化合物9(2.8 mg,R=20.5 min,50%乙腈,2.0 mL/min)。
2.2 细胞毒活性筛选
采用MTT比色法对分离得到的化合物进行体外抑制人胃癌HGC-27细胞株的活性筛选。培养HGC-27胃癌细胞至对数生长期,PBS洗去培养液,用0.25% 胰酶消化离心后用培养基稀释,以6×104个/mL接种于96孔板,每孔150 μL,培养箱中常规培养条件下培养24 h后,加入配制好的化合物和阳性药顺铂继续培养48 h,然后每孔加入MTT溶液(5 mg/mL)10 μL,置于培养箱37 ℃培养4 h后弃去培养液。最后每孔加入150 μL DMSO,室温下避光低速振荡15 min,用酶标仪570 nm波长处测定吸光度()值,根据公式计算药物对细胞的抑制率,并用Excel软件计算IC50值。
抑制率=1-加药/空白
3 结果
3.1 结构鉴定
化合物1:白色固体,HR-ESI-MS/: 191.103 3 [M+Na]+(计算值191.104 8),分子式为C10H16O2。红外光谱中显示该化合物的结构中存在羟基(3450 cm−1)、羰基(1730 cm−1)的特征吸收峰。在化合物1的1H-NMR中,观察到在高场区有3个甲基信号H1.77 (3H, s, H-10), 1.23 (3H, s, H-8), 1.22 (3H, s, H-9)、2个亚甲基信号H2.61 (1H, d,= 15.0 Hz, H-6), 2.45 (1H, d,= 18.0 Hz), 2.19~2.27 (2H, m, H-5, 6)、1个次甲基信号2.04~2.08 (1H, m, H-4),低场区观察到1个双键氢信号6.76 (1H, d,= 6.2 Hz, H-3),归属数据见表1。化合物的13C-NMR谱显示10个碳信号,包括3个甲基碳、2个亚甲基碳、2个次甲基碳(包括1个烯碳信号)以及3个季碳(包括1个酮羰基、1个烯碳信号),其中1个酮羰基碳和2个烯碳组成了1个α,β-不饱和酮200.4 (C-1), 145.2 (C-3), 135.5 (C-2)。由此推测出化合物1的平面结构见图1。
表1 化合物1的1H-NMR和13C-NMR 数据 (600/150 MHz, CDCl3)
Table 1 1H-NMR and 13C-NMRspectral data of compound 1 (600/150 MHz, CDCl3)
碳位δHδC 1 200.4 2 135.5 36.76 (1H, d, J = 6.0 Hz)145.3 42.04~2.08 (1H, m)46.2 5α2.45 (1H, d, J = 18.0 Hz)27.4 5β2.19~2.27 (1H, overlapped) 6α2.61 (1H, d, J = 15.0 Hz)39.8 6β2.19~2.27 (1H, m) 7 77.9 81.23 (3H, s)27.3 91.22 (3H, s)27.6 101.77 (3H, s)15.9

图1 化合物1的结构
化合物1的波谱数据与4-hydroxy-4-(1- hydroxy-1-methylethyl)-cyclohex-2-en-1-one[6]较为相似,不同之处在于,C-2位上存在1个甲基,C-4位上不存在羟基。在HSQC谱图上可以观察到H-4与C-4的氢-碳直接相关信号,表明C-4位为次甲基,同时在HMBC谱图上可以观察到H-10与C-1、C-2、C-3的氢-碳远程相关信号,表明C-2位存在甲基(图2)。在NOSEY谱图上可以发现,H-4与H-5α存在远程相关信号,表明H-4与H-5α共面,指定H-4和H-5α为α取向,则4-羟基异丙基为β取向。为了进一步确定化合物1的绝对构型,测定了其圆二色谱(ECD),采用 [B3LYP/6-311G (d, p), MeOH]水平上的TDDFT方法计算。通过模拟计算,当C-4位为构型时,化合物1的理论计算ECD谱与实际测试图较为一致,进而确定化合物1的立体构型(图3)。因此,鉴定化合物1的结构为4-(2-羟基异丙基)-环己烷-2-烯-1-酮,命名为神香草酮A。
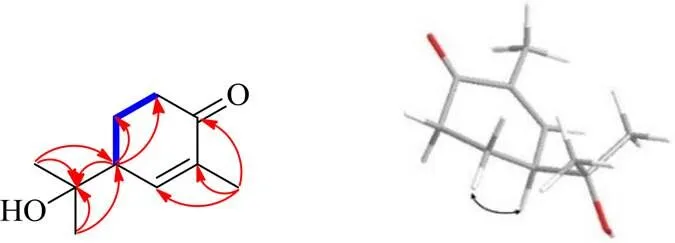
图2 化合物1的主要1H-1H COSY (━) 和HMBC (H→C)相关
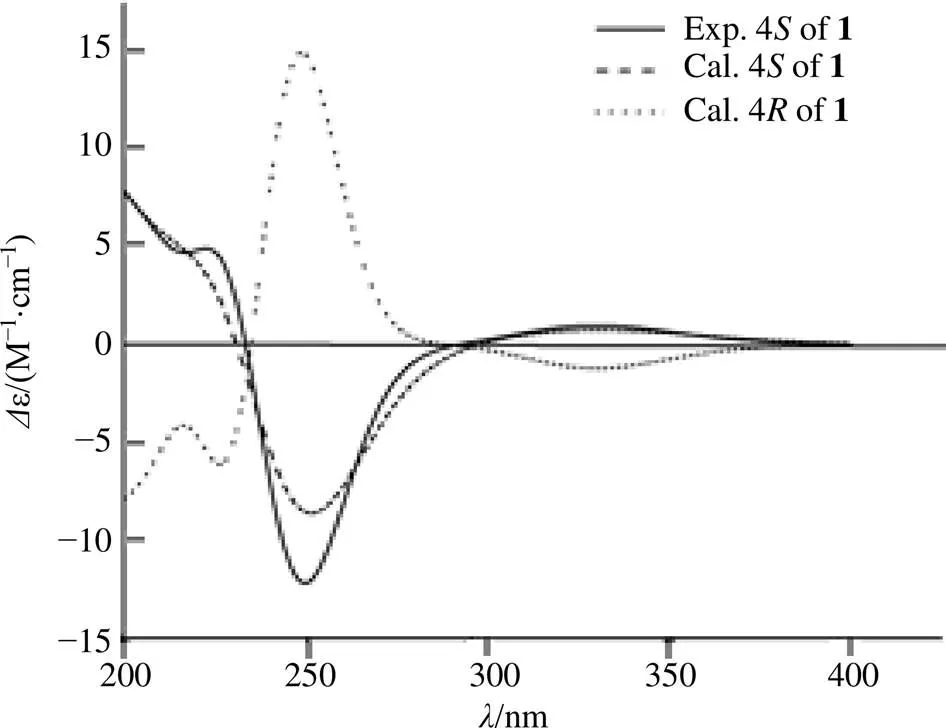
图3 化合物1的ECD实验和计算谱图
化合物2:淡黄色固体,ESI-MS/: 257.15 [M+Na]+,分子式为C15H22O2。1H-NMR (600 MHz, CDCl3): 6.48 (1H, q,= 2.4 Hz, H-1), 4.78 (1H, s, H-13), 4.73 (1H, s, H-13), 3.69~3.71 (1H, m, H-3), 2.64 (1H, d,= 5.4 Hz, H-2), 2.42 (1H, d,= 2.4 Hz, H-8), 2.37 (1H, s, H-7), 2.35 (1H, s, H-8), 2.14 (1H, d,= 2.4 Hz, H-2), 2.00~2.01 (1H, m, H-6), 1.72 (3H, s, H-12), 1.62 (1H, s, H-6), 1.57 (1H, s, H-4), 1.10 (3H, d,= 7.2 Hz, H-15), 0.98 (3H, s, H-14);13C-NMR (150 MHz, CDCl3): 203.3 (C-9), 147.3 (C-11), 144.0 (C-10), 132.1 (C-1), 110.4 (C-13), 69.1 (C-3), 46.2 (C-4), 42.9 (C-8), 41.9 (C-6), 39.0 (C-7), 38.1 (C-5), 35.2 (C-2), 26.0 (C-14), 20.7 (C-12), 11.0 (C-15)。以上数据与文献报道对照基本一致[7],故鉴定化合物2为 (3,4a,5,6)-6-羟基-4a,5-二甲基- 3-(丙-1-烯-2-基)-3,4,4a,5,6,7-六氢萘-1(2)-酮。
化合物3:无色针状晶体(氯仿),ESI-MS/: 175.04 [M+Na]+,分子式为C8H8O3。1H-NMR (600 MHz, CDCl3): 7.98 (2H, d,= 8.6 Hz, H-2, 6), 6.87 (1H, d,= 8.6 Hz, H-3, 5), 3.81 (3H, s, 4-OMe);13C-NMR (150 MHz, CDCl3): 170.7 (C-7), 164.0 (C-4), 132.4 (C-2, 6), 113.7 (C-3, 5), 55.5 (4-OMe)。以上数据与文献报道对照基本一致[8],故鉴定化合物3为对茴香酸。
化合物4:淡黄色晶体(氯仿),ESI-MS/: 351.08 [M+Na]+,分子式为C18H16O6。1H-NMR (600 MHz, CDCl3): 12.71 (1H, s, 5-OH), 7.78 (2H, d,= 8.8 Hz, H-2, 6), 6.95 (2H, d,= 8.8 Hz, H-3, 5), 6.53 (1H, s, H-8), 6.51 (1H, s, H-3), 3.90 (3H, s, 7-OMe), 3.86 (3H, s, 4-OMe), 3.83 (3H, s, 6-OMe);13C-NMR (150 MHz, CDCl3): 182.7(C-4), 164.07(C-2), 162.6 (C-4), 158.7 (C-7), 153.7 (C-5), 153.1 (C-9), 132.6 (C-6), 128.1 (C-2, 6), 123.5 (C-1), 114.5 (C-3, 5), 106.2 (C-10), 104.2 (C-3), 90.6 (C-8), 60.9 (6-OMe), 56.3 (7-OMe), 55.6 (4-OMe)。以上数据与文献报道对照基本一致[9],故鉴定化合物4为三裂鼠尾草素。
化合物5:黄色针状晶体(甲醇),ESI-MS/: 381.10 [M+Na]+,分子式为C19H18O7。1H-NMR (600 MHz, CDCl3): 7.53 (1H, dd,= 8.4, 2.0 Hz, H-6), 7.34 (1H, d,= 2.0 Hz, H-2), 6.98 (1H, d,= 8.5 Hz, H-5), 6.61 (1H, s, H-8), 6.56 (1H, s, H-3), 3.93~3.99 (12H, s, 6, 7, 3, 4-OMe);13C-NMR (150 MHz, CDCl3): 182.7 (C-4), 164.0 (C-2), 158.7 (C-7), 153.3 (C-5), 153.1 (C-9), 152.2 (C-4), 149.3 (C-3), 132.6 (C6), 123.7 (C-1), 120.2 (C-6), 111.1 (C-5), 108.6 (C-2), 106.2 (C10), 104.5 (C-3), 90.6 (C-8), 60.9 (6-OMe), 56.4 (7-OMe), 56.2 (3, 4-OMe)。以上数据与文献报道对照基本一致[10],故鉴定化合物5为5-羟基-6,7,3,4-四甲氧基黄酮。
化合物6:淡黄色晶体(甲醇),ESI-MS/: 337.07 [M+Na]+,分子式为C17H14O6。1H-NMR (600 MHz, DMSO-6): 12.95 (1H, s, 4-OH), 7.98 (2H, d,= 8.7 Hz, H-2, 6), 6.96 (1H, s, H-8), 6.93 (1H, d,= 8.7 Hz, H-3, 5), 6.88 (1H, s, H-3), 3.93 (3H, s, 7-OMe), 3.73 (3H, s, 6-OMe);13C-NMR (150 MHz, DMSO-6): 182.7 (C-4), 164.5 (C-2), 161.7 (C-4), 159.1 (C-7), 153.1 (C-5), 152.5 (C-9), 132.3 (C-6), 129.0 (C-2, 6), 121.5 (C-1), 116.4 (C-3, 5), 105.5 (C-10), 103.1 (C-3), 92.1 (C-8), 60.5 (6-OMe), 56.9 (7-OMe)。以上数据与文献报道对照基本一致[9],故鉴定化合物6为蓟黄素。
化合物7:淡黄色固体,ESI-MS/: 201.09 [M+Na]+,分子式为C11H14O2。1H-NMR (600 MHz, DMSO-6): 7.25 (2H, d,= 9.0 Hz, H-2, 6), 6.71 (2H, d,= 8.2 Hz, H-3, 5), 6.46 (1H, d,= 15.8 Hz, H-7), 6.10 (1H, dt,= 16.0, 6.0 Hz, H-8), 4.01 (2H, dd,= 6.2, 1.2 Hz, H-9), 3.44 (2H, q,= 7.0 Hz, H-10), 1.12 (3H, s, H-11);13C-NMR (150 MHz, DMSO-6): 152.7 (C-4), 132.4 (C-7), 128.1 (C-2, 6), 127.8 (C-1), 123.2 (C-8), 115.3 (C-3, 5), 71.4 (C-9), 64.2 (C-10), 15.6 (C-11)。以上数据与文献报道对照基本一致[11],故鉴定化合物7为--香豆醇乙醚。
化合物8:白色非定形固体,ESI-MS/: 187.07 [M+Na]+,分子式为C10H12O2。1H-NMR (600 MHz, DMSO-6): 7.26 (2H, d,= 8.6 Hz, H-2, 6), 6.72 (2H, d,= 8.6 Hz, H-3, 5), 6.47 (1H, d,= 16.0 Hz, H-1), 6.09 (1H, dt,= 16.0, 6.0 Hz, H-2), 3.97 (2H, dd,= 6.0, 1.4 Hz, H-3), 3.24 (3H, s, 3-OMe);13C-NMR (150 MHz, DMSO-6): 157.2 (C-4), 132.2 (C-1), 128.6 (C-2, 6), 127.8 (C-1), 123.2 (C-2), 115.8 (C-3, 5), 73.6 (C-3), 58.0 (3-OMe)。以上数据与文献报道对照基本一致[12],故鉴定化合物8为()--香豆醇 γ-O-甲醚。
化合物9:黄色油状物,ESI-MS/: 245.08 [M+Na]+,分子式为C12H14O4。1H-NMR (600 MHz, CDCl3): 7.61 (1H, d,= 15.8 Hz, H-7), 7.07 (1H, dd,= 1.8, 8.2 Hz, H-2), 7.03 (1H, d,= 1.8 Hz, H-6), 6.91 (1H, d,= 8.0 Hz, H-5), 6.28 (1H, d,= 16.0 Hz, H-8), 4.25 (2H, q,= 7.2 Hz, H-10), 3.92 (3H, s, 3-OCH3), 1.33 (3H, t,= 7.0 Hz, H-11);13C-NMR (150 MHz, CDCl3): 167.5 (C-9), 147.9 (C-3), 146.7 (C-4), 144.7 (C-7), 127.1 (C-1), 123.1 (C-6), 115.8 (C-2), 114.7 (C-5), 109.2 (C-8), 60.4 (C-10), 55.9 (3-OMe), 14.3 (C-11)。以上数据与文献报道对照基本一致[13],故鉴定化合物9为4-羟基-3-甲氧基乙基肉桂酸盐。
3.2 体外细胞毒活性结果
对神香草95%乙醇提取物分离得到的化合物1~9对人胃癌HGC-27细胞进行细胞活性筛选。结果显示,化合物1、3、8对HGC-27细胞具有一定的抑制作用,其IC50值分别为8.76、16.34、25.28 μmol/L。阳性对照药顺铂的IC50值为3.2 μmol/L。其他化合物均无抑制作用(表2)。
表2 化合物1~9对HGC-27细胞的抑制作用
Table 2 Inhibitory effects of compounds 1—9 on HGC-27 cell
化合物IC50/(μmol·L−1) 18.76 2>50 316.34 4>50 5>50 6>50 7>50 825.28 9>50 顺铂3.20
4 讨论
本研究通过对神香草95%乙醇提取物中的化学成分进行分离,从中获得9个化合物,包括1个单萜、1个倍半萜、3个黄酮以及4个酚酸。其中,化合物1为1个新的单萜,化合物5~9为首次从神香草属植物中分到。现代药理学研究表明,许多萜类化合物具有一定的抗肿瘤、保护胃黏膜等作用[14-16]。因此,对9个化合物进行抗肿瘤活性筛选,结果显示,化合物1、3、8对HGC-27胃癌细胞具有一定的抑制作用,其中,化合物1的IC50值为8.76 μmol/L,表明硬尖神香草中部分化合物可以作为潜在的抗肿瘤药物。神香草作为新疆地区习用药,临床上被广泛应用,但国内外对其疗效机制研究相对不足,因此本研究为更好地开发利用该植物、丰富硬尖神香草化学成分以及探究其有效活性成分奠定了基础,为进一步实现其药用价值提供科学依据。
利益冲突 所有作者均声明不存在利益冲突
[1] 蔡晓翠, 买买提·艾力, 王新堂, 等. 硬尖神香草的化学成分研究 [J]. 中药材, 2021, 44(4): 848-852.
[2] Shomirzoeva O, Li J, Numonov S,. Chemical components ofBoriss.: Isolation and identification, characterization by HPLC-DAD-ESI- HRMS/MS, antioxidant activity and antimicrobial activity [J]., 2020, 34(4): 534-540.
[3] 刘丹, 朱小涛, 向槿, 等. 神香草倍半萜类化学成分研究 [J]. 中草药, 2019, 50(5): 1049-1054.
[4] Wang N, Yang X W. Two new flavonoid glycosides from the whole herbs of[J]., 2010, 12(12): 1044-1050.
[5] Skrzypek Z, Wysokińska H. Sterols and triterpenes in cell culture ofL [J]., 2003, 58(5/6): 308-312.
[6] Ramos F, Takaishi Y, Kawazoe K,. Immunosuppressive diacetylenes, ceramides and cerebrosides from[J]., 2006, 67(11): 1143-1150.
[7] Furukawa M, Makino M, Ohkoshi E,. Terpenoids and phenethyl glucosides from(labiatae) [J]., 2011, 72(17): 2244-2252.
[8] Barbosa-Filho J, Lima C S A, Camorim E L,. Botanical study, phytochemistry and antimicrobial activity of[J]., 2004, 53:221-228.
[9] Abdelhalim A, Karim N, Chebib M,. Antidepressant, anxiolytic and antinociceptive activities of constituents from[J]., 2015, 18(4): 448-459.
[10] El-Bassossy T, Ahmed F, El-Mesallamy A. Phytochemical analysis and biological evaluation ofaerial parts [J]., 2019, 76(5): 815-823.
[11] Sukhirun N, Pluempanupat W, Bullangpoti V,. Bioefficacy of(Zingiberaceae) rhizome extracts, ()--acetoxycinnamyl alcohol, and ()--coumaryl alcohol ethyl ether against(Diptera: Tephritidae) and the impact on detoxification enzyme activities [J]., 2011, 104(5): 1534-1540.
[12] Ly T N, Shimoyamada M, Kato K,. Isolation and characterization of some antioxidative compounds from the rhizomes of smaller galanga (Hance) [J]., 2003, 51(17): 4924-4929.
[13] Yang X, Ying Z M, Liu H R,. A new homoisoflavone fromLand its antioxidant activity [J]., 2019, 33(24): 3500-3506.
[14] Li L, Tao R H, Wu J M,. Three new sesquiterpenes from[J]., 2018, 20(4): 306-312.
[15] 张航, 马家乐, 昝妮利, 等. 沉香中倍半萜类化学成分研究 [J]. 中国中药杂志, 2022, 47(16): 4385-4390.
[16] Crowell P L. Monoterpenes in breast cancer chemoprevention [J]., 1997, 46 (2/3): 191-197.
Study on chemical composition of
LIU Chang1, 2, SUN Zhao-cui3, Xiatiguli Abulizi2, MA Guo-xu2, 3, SHI Lei-ling2, ZHANG Jing1
1. College of Chinese Medicinal Materials, Jilin Agricultural University, Changchun 130118, China 2. Xinjiang Institute of Chinese and Ethnic Medicine, Urumqi 830002, China 3. Institute of Medicinal Plant Development, Chinese Academy of Medical Sciences and Peking Union Medical College, Beijing 100193, China
To study the chemical composition of the above-ground dried parts ofBoriss.The constituents were isolated and purified by silica gel column and high performance liquid chromatography techniques repeatedly, and the resulting compounds were structurally characterized by modern wave spectroscopy techniques to determine the structures of the compounds, and the isolated compounds were screened forinhibitory activity against human gastric cancer HGC-27 cell line using MTT colourimetric assay.A total of nine compounds were isolated from the 95% ethanol extract of. and were identified as: 4-(2-hydroxyisopropyl)-cyclohexane-2-en-1-one (1), (3,4a,5,6)-6-hydroxy-4a,5-dimethyl- 3- (prop-1-en-2-yl)-3,4,4a,5,6,7-hexahydronaphthalen-1(2)-one (2),-anisic acid (3), salvigenin (4), 5-hydroxy-6,7,3,4- tetramethoxy flavone (5), cirsimaritin (6),--coumaryl alcohol ethyl ether (7), ()--coumaryl alcohol γ--methyl ether (8), 4-hydroxy-3-methoxy ethyl cinnamate (9). Wherein, compound 1 is a new compound. The antitumor activity screening of compounds 1-9 showed that compounds 1, 3 and 8 had certain inhibitory effects on HGC-27 gastric cancer cells, and their IC50values were 8.76, 16.34, 25.28 μmol/L, respectively.Compound 1 is a new compound. Compounds 5-9 were first isolated from this genus.
Boriss.; anti-tumor effect; hyssopusone A;-anisic acid; cirsimaritin; ()--coumaryl alcohol γ-- methyl ether
R284.1
A
0253 - 2670(2023)17 - 5481 - 06
10.7501/j.issn.0253-2670.2023.17.002
2023-04-27
中国医学科学院医学与健康科技创新工程(2022-I2M-1-017);新疆维吾尔自治区科技项目计划(2021A03002)
刘 畅(1999—),女,硕士研究生,研究方向为天然产物化学。E-mail: liuc1221@126.com
张 晶(1971—),女,博士生导师,教授,从事天然产物化学研究。E-mail: zhjing0701@163.com
石磊岭(1977—),男,研究员,从事药学研究。E-mail: shileiling163@163.com
[责任编辑 王文倩]

