过硫酸钾氧化法测定海水中总氮的影响因素和解决方法
徐玉珊,刘新杰,张欣欣,陈星光
(荣成市海洋与渔业监测减灾中心,山东荣成 264300)
总氮(Total Nitrogen,TN)指水体中所有含氮化合物中氮的总含量,包括亚硝酸盐氮、硝酸盐氮、无机铵盐、溶解态氨,以及大部分有机含氮化合物中的氮[1]。总氮作为评价海水富营养化的重要指标,是海洋环境监测中的必测参数。目前国际上测定海水中总氮的方法为过硫酸钾氧化法[1],虽然近几年流动注射分析法的应用范围逐渐扩大,但由于仪器设备造价较高,大部分基层实验室还是应用海洋调查规范GB/T 12763.4—2007中的过硫酸钾氧化法进行总氮的测定。过硫酸钾氧化法应用的实验仪器和试剂比较常见,操作也相对简单,但也存在一定的缺点:实验过程相对比较繁琐,对实验条件、试剂、器皿等方面的要求也较为严格。如何降低空白值,提高结果准确度和重现性,经过长时间的实践、摸索和研究,最终总结出下面几个对实验结果非常重要的影响因素和解决方法。
1 实验原理与方法
1.1 实验原理
海水样品在碱性和110~120℃条件下,通过硫酸钾氧化,有机氮化合物被转化为硝酸氮。同时,水中的亚硝酸氮、铵态氮也定量地被氧化为硝酸氮。硝酸氮经还原为亚硝酸盐后与对氨基苯磺酰胺进行重氮化反应,再与1-萘替乙二胺盐酸盐作用,生成深红色偶氮染料,于543 nm 波长处进行分光光度测定[2]。
1.2 实验方法
取25 mL 海水和10 mL 氯化钠溶液于消煮瓶中,加入4 mL 过硫酸钾溶液,放入高压蒸汽灭菌锅中加热消煮,在1.1~1.4 kPa(120~140℃)的条件下,保持30 min。样品冷却后,加入0.5 mL 盐酸溶液后转移到100 mL 容量瓶中。用氯化钠溶液洗涤消煮瓶3次,加入2 mL 四硼酸钠溶液,用氯化钠溶液稀释至标线,混匀。分别量取25 mL 至对应消煮瓶中,加入锌卷和0.5 mL 氯化镉溶液振荡10 min,取出锌卷,加入0.5 mL对氨基苯磺酰胺,5 min 后再加入0.5 mL 1-萘替乙二胺。15 min 后在543 nm 波长处测定溶液吸光值[2]。
2 影响因素与解决方法
2.1 实验室环境
实验室环境对总氮测定结果的影响主要有空气中的污染气体及沉降颗粒等,特别是实验室靠近卫生间[3]、与氨氮等含氮项目在同一实验室内分析或者夏天开空调等环境条件下,都会对样品造成污染,同时使空白值结果偏高。
解决方法:总氮的测定应在无氮实验室内进行,有条件的可以单独设置总氮实验室。
2.2 水样冷却
消解后的水样冷却不完全或冷却方法不正确都会对实验结果产生偏差。因为消解后的水样中有部分氮会以气态形式存在于消解瓶内水层上方[4],若在水样没有完全降至室温时强行打开瓶盖,会使这部分氮游离于空气中,从而造成结果偏低。若强行用冰块、凉水等方式对水样进行降温,会使游离于水层上方的氨气不能完全氧化为硝酸盐氮,从而影响实验结果,降低结果准确度。
解决方法:将水样自然冷却至室温后再进行接下来的实验。若气温过高或时间紧张,可用吹风扇等增加空气流动的方式对水样进行物理降温。
2.3 实验用水
总氮的测定对实验用水的要求非常高,目前大多数实验室使用的是超纯水,部分实验室直接使用购买的,如娃哈哈纯净水等作为纯水使用。本研究通过对实验室现有的两台纯水机(型号分别为Milli-Q 和200QSU001)及娃哈哈纯净水进行比对发现,这两台纯水机现制的超纯水和娃哈哈纯净水都可以达到空白使用要求(≤0.050)(表1)。
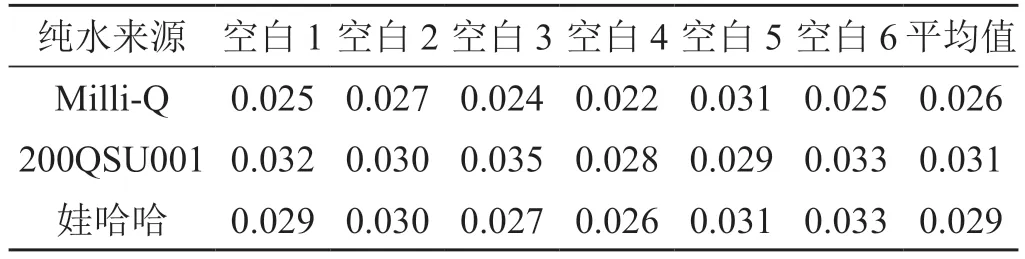
表1 三款纯水的空白值对比
解决方法:尽量选用超纯水机现制的超纯水,如果没有超纯水可以购买娃哈哈等品牌纯净水(使用前先进行空白值测定,合格后方可使用)。
2.4 实验试剂
海水中的总氮测定过程中需要用到很多试剂,但在实际检测过程中发现氢氧化钠、盐酸等试剂纯度对实验结果的影响并不大,但过硫酸钾的纯度则会严重影响实验结果的准确度。主要原因有以下几个。
(1)过硫酸钾中的杂质会影响过硫酸钾与水样的氧化反应,造成结果偏低或偏高。
(2)过硫酸钾纯度不够,造成水样中的氮没有被完全、足量氧化为硝酸氮,从而使结果偏低。
(3)过硫酸钾中可能含有含氮杂质,从而造成结果偏高。
解决方法:一是对过硫酸钾进行重结晶提纯处理。有研究发现,国产的过硫酸钾的总氮含量很高,无法直接进行实验,但对国产的过硫酸钾进行3次重结晶也可使空白值降至0.05以下[5],重结晶具体可参考余浩然等[6]的方法。二是选购进口或纯度更好的试剂。
另外还应注意过硫酸钾的存放和配制温度。因为过硫酸钾是氧化剂,存放时要避免与还原性物质、硫、磷等混合存放,且过硫酸钾容易吸潮,放出氧气,因此最好存放在干燥塔中。同时,因过硫酸钾在60℃以上会发生分解反应,因此在配制时应注意温度不应超过60℃。
表2为使用国产未提纯过硫酸钾、国产提纯后的过硫酸钾、进口未提纯过硫酸钾的空白比对数据。通过数据可以看出,国产提纯后及进口的过硫酸钾都可满足实验要求。

表2 国产未提纯、国产提纯后、进口未提纯过硫酸钾空白比对数据
2.5 实验器皿的选择与处理
目前总氮测定使用的实验器皿主要是玻璃和聚四氟乙烯材质的。聚四氟乙烯材质效果最好,但缺点是价格较高,因此大部分检测机构还是使用玻璃材质。其实,玻璃器皿经正确处理后,精密度和准确度也完全满足实验要求。
解决方法:实验所用所有器皿均提前用体积分数为10%盐酸浸泡24 h 后,再用大量无氮水冲洗干净,方可使用。图1为使用处理后的器皿来测定总氮的标准曲线和空白值。图2为使用未处理的器皿测出的标准曲线和空白值。两者对比可以很明显看出:处理后的标准曲线线性及空白值都较好,而未处理的则出现了高浓度吸光值低或低浓度吸光值高的情况,同时相关系数和空白值也达不到要求。因此,在实验前所有器皿必须严格按照要求处理合格后方可使用。另外,实验器皿的密闭性也同样要注意,避免在消解过程中发生漏液,从而造成实验结果偏低。
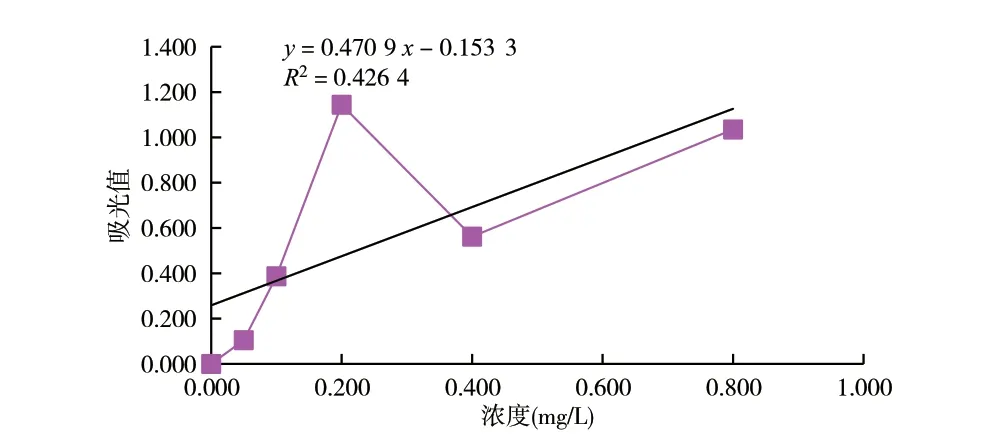
图2 未用盐酸浸泡器皿后的总氮标准曲线
2.6 消解时间
另有研究表明消解时间也会对空白值造成一定影响,从而影响标准曲线的绘制及测定结果的准确度。有研究表明在一定时间范围内,消解时间与空白值成反比,即消解时间越长,空白值相对越低。因为随着消解时间的增长,有机物中的氮向硝酸氮的转化更加彻底,进而使消解后的溶液吸光度降低,最终使溶液的空白值降低[7]。本研究通过多次实验比对发现,消解30 min 基本可以满足实验要求,但为了提高总氮空白值的稳定性,可适当延长消解时间,综合时间成本及实验效果,建议采用45 min 的消解时间最佳。
2.7 仪器设备对实验结果的影响
有相关研究表明,分光光度计的预热时间与曲线的相关性系数有一定的关系,预热时间越长,仪器越稳定,其相关系数越理想,本实验室用的分光光度计型号为普析通用T6,经多次实验摸索发现,仪器预热40 min 左右达到稳定状态,测定结果最佳。不同仪器达到稳定状态的时间不同,可以在实验过程中摸索出自己仪器的最佳预热时间,从而达到最理想的实验效果。
3 结论
测定海水中总氮时应注意:①实验室应为无氮环境;②过硫酸钾应进行重结晶提纯处理或选择进口高纯试剂;③实验用水应选择现制无氮超纯水;④消解后的水样先自然晾凉再进行接下来的操作;⑤实验器皿都应提前用体积分数为10 %的盐酸浸泡24 h 以上;⑥在时间允许的情况下,适当延长消解时间;⑦注意仪器的预热时间。做好以上几点,总氮空白值基本可降到0.050以下,标准曲线相关系数可达到0.995以上,满足实验要求。

