HPLC 法同时测定黄连上清片中栀子苷、黄芩苷的含量
彭玲娜,孙辉,丁野,李文莉,赵桂铃
湖南省药品检验检测研究院,湖南省药品质量评价工程技术中心,湖南 长沙 410001
黄连上清片是由大黄、黄芩、黄柏、栀子等17味中药组成的复方制剂[1]。方中黄连、黄芩、黄柏、石膏清热泻火,燥湿解毒,栀子、大黄清热凉血解毒,引热毒从二便出,共为君药。防风、连翘、荆芥穗、菊花、白芷、川芎、蔓荆子、薄荷疏散风热,共为臣药。佐以旋覆花下气行水,桔梗清热、利咽、排脓,载药上行。甘草调和诸药,为佐使药。诸药合用,泻火止痛,散风清热。临床用于因风热上攻、肺胃热盛、引动肝火上蒸头目所致眼内刺痒交作、见光流泪、白睛红赤、舌苔黄,还适用于急性结膜炎、急性化脓性中耳炎、口热、口臭、口疮、急性牙周炎、冠周炎、急性咽炎等。
该制剂质量标准收载于《中国药典》2020 年版一部,质量标准含量测定项目仅设置了盐酸小檗碱的含量测定,未对处方中的君药栀子和黄芩的含量进行控制,现行标准不能完全反映出投料药材的质量[2],不利于产品的质量把控和批间差异性的评价,可能导致药品的疗效存在差异。因此本研究选择栀子和黄芩中的指标活性成分栀子苷、黄芩苷为研究对象,建立了同时测定两者含量的HPLC 方法,为提高黄连上清片质量标准,控制产品质量提供了科学依据。
1 仪器与试药
1.1 仪器
Waters2698 高效液相色谱仪系统(DAD 检测器、四元梯度泵、自动进样器、柱温箱),分析天平(梅特勒 XS205),超声波清洗机(昆山KQ-300 型)
1.2 试药
栀子苷对照品(批号:110749-201919,纯度:97.1%);黄芩苷对照品(批号:110715-2017,纯度:93.5%);以上对照品均购于中国食品药品检定研究院。乙腈为色谱纯,其他试剂均为分析纯。黄连上清片,A 厂家,批号:210311、210305、210310;B厂家,批号:ZEA2107、ZEA2106、ZEA2105;C 厂家,批号:20210301、20210302、20200504、20200906。
2 实验方法
2.1 色谱条件
色谱柱:Agilient zorbax-C18(250 mm×4.6 mm,5 µm);流动相:以0.2%磷酸溶液为流动相A,以乙腈为流动相B,按表1 进行梯度洗脱;柱温:35 ℃;流速:1.0 mL/min;DAD 检测器;采集波长为250 nm[3-4]。
2.2 对照品溶液的制备
精密称取栀子苷对照品10.15 mg,置10 mL容量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得栀子苷对照品溶液①(0.985 6 mg/mL);精密称取栀子苷对照品3.84 mg,置10 mL 量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得对照品溶液②(0.372 9 mg/mL)。精密量取栀子苷对照品溶液①适量,用甲醇稀释成栀子苷对照品溶液③~⑤(浓度分别为0.098 56、0.019 71、0.001 971 mg/mL)。
精密称取黄芩苷对照品18.18 mg,置50 mL 量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得黄芩苷对照品溶液①(0.340 0mg/mL)。精密量取黄芩苷对照品溶液①适量,用甲醇稀释成黄芩苷对照品溶液②~⑤(浓度分别为0.170 0、0.085 0、0.034 0、0.008 5 mg/mL)。
2.3 供试品溶液的制备
取供试品研细,取粉末约0.5 g,精密称定,置具塞锥形瓶中,精密加入70%甲醇25 mL,称定重量,超声处理(功率300 W,频率50 kHz)30 min,放冷,再称定重量,用70%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。
2.4 阴性对照溶液的制备
按处方称取除黄芩、栀子外的其他药材,按质量标准中的制备工艺制成缺黄芩、栀子的阴性样品,同“2.3”项下的方法制备缺黄芩、栀子的阴性对照溶液。
2.5 测定法
精密吸取对照品溶液、供试品溶液、阴性对照溶液各10 μL,注入液相色谱仪,测定,即得。
3 结果
3.1 专属性检测结果
分别精密吸取栀子苷对照品溶液③、黄芩苷对照品溶液③、供试品溶液及阴性对照溶液各10 μL,注入液相色谱仪,照“2.1”项下色谱条件进行测定,记录色谱图。结果表明,阴性对照溶液色谱图中,在栀子苷和黄芩苷色谱峰相同的保留时间处未出现相同的色谱峰,表明处方中其他药味不会干扰两者的测定。结果见图1~4。
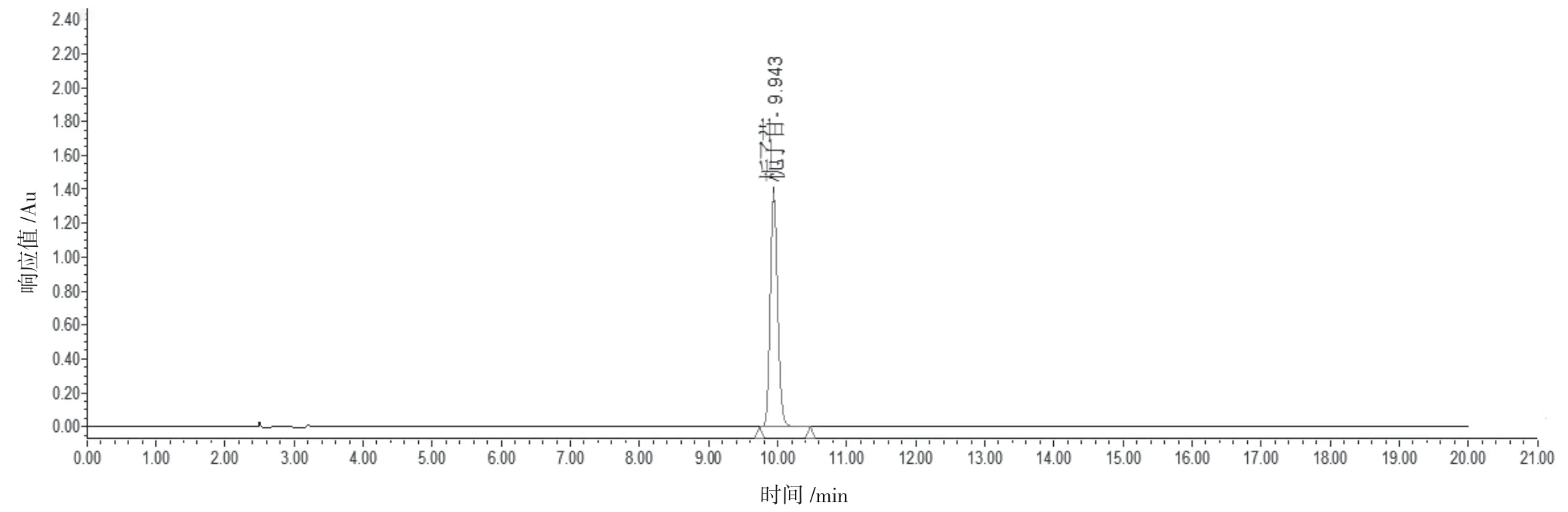
图1 栀子苷对照品色谱图

图2 黄芩苷对照品色谱图

图3 阴性对照溶液色谱图
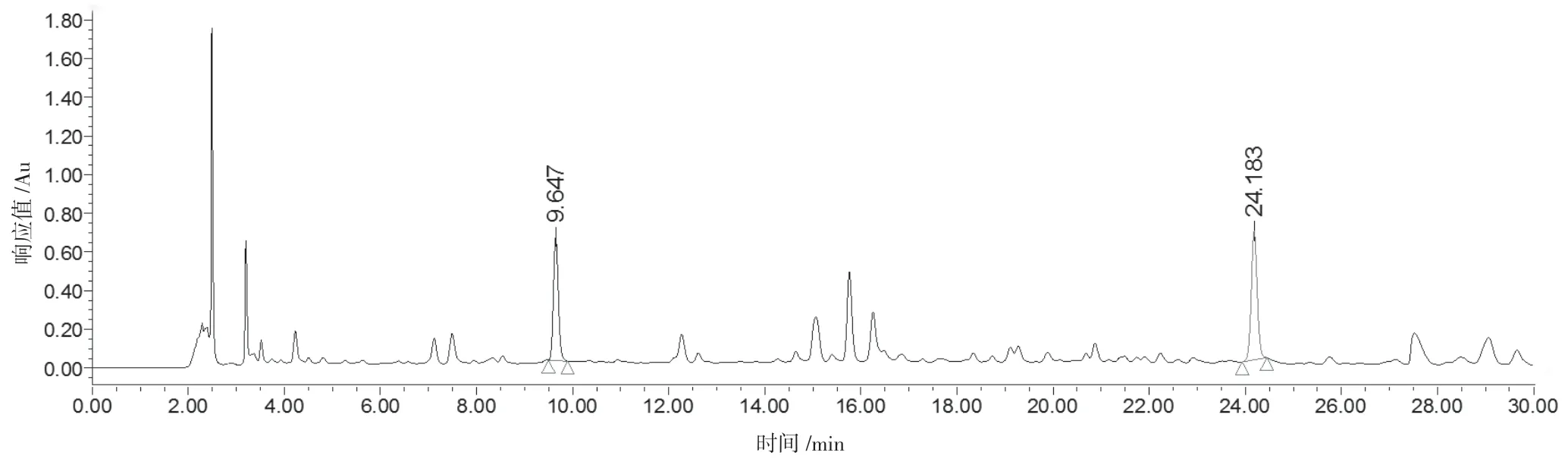
图4 供试品溶液色谱图
3.2 方法学考察
3.2.1 线性关系考察 分别精密吸取栀子苷、黄芩苷对照品溶液①~⑤各10 μL,注入高效液相色谱仪,照“2.1”项下色谱条件测定,记录峰面积。以对照品溶液浓度为横坐标(X),峰面积为纵坐标(Y),分别绘制标准曲线并进行分析,结果见表2,表明栀子苷、黄芩苷在范围内线性关系良好。

表2 栀子苷和黄芩苷的标准曲线方程、相关系数、线性范围
3.2.2 稳定性试验 取同一份样品溶液,分别于配制后的0、6、12、18、24 h,精密吸取10 μL,注入液相色谱仪,测定,结果栀子苷和黄芩苷的峰面积RSD 分别为0.24%、0.71%。表明供试品溶液在配制后24 h 内基本稳定。
3.2.3 重复性试验 取同一批样品(批号:20200504)6 份,按“2.3”项下方法制备供试品溶液,依法测定并计算含量,结果栀子苷和黄芩苷的含量分别为1.80 mg/g,4.60 mg/g,RSD 分别为0.88%、0.70%。表明该方法具有良好的重复性。
3.2.4 回收率试验 精密称取6 份已知含量的样品(批号:20200504)各0.25 g,精密加入相应浓度黄芩苷和栀子苷对照品溶液,同“2.3”项下的方法制成供试品溶液,按“2.1”项下色谱条件进行测定,结果见表3,4。栀子苷和黄芩苷的平均回收率分别为96.67%、100.30%,RSD 分别为0.89%、0.97%,该方法准确度良好。
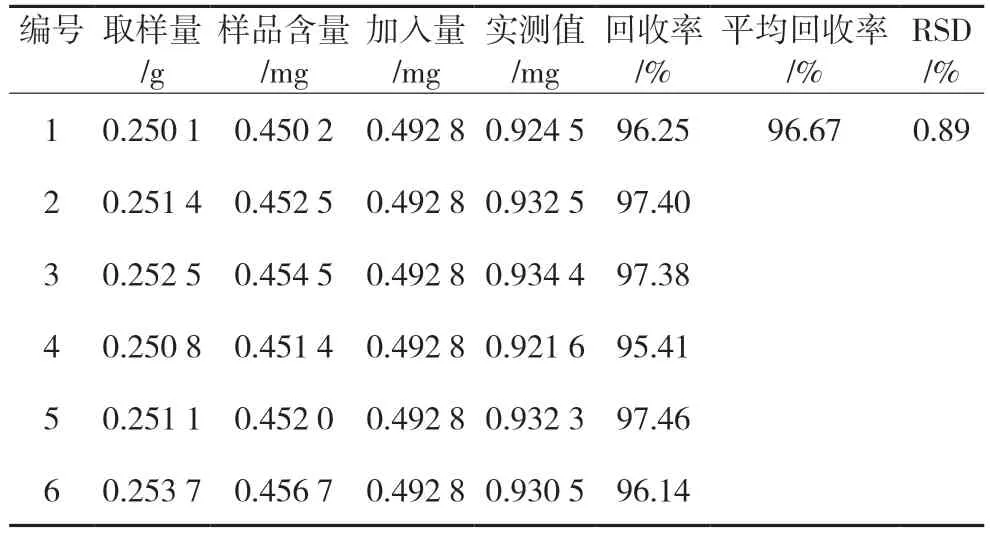
表3 栀子苷回收率试验结果
3.2.5 检测限与定量限 将栀子苷和黄芩苷对照品溶液进行稀释,按上述色谱条件,进行测定。结果当S/N=3 时,栀子苷和黄芩苷的检测限分别为1.02 ng和4.14 ng;当S/N=10 时,栀子苷和黄芩苷的定量限分别为3.06 ng 和12.42 ng。
3.3 供试品含量测定
为考察市面上不同生产企业的黄连上清片的质量差异,按照上述的方法测定10 批次样品中黄芩苷和栀子苷的含量。结果表明,本研究所建立的含量测定方法可用于不同生产厂家产品中栀子苷和黄芩苷的含量测定;不同厂家的产品质量差异较大,在10 批样品中,栀子苷的含量范围为0.45~1.08 mg/片,黄芩苷的含量范围为0.26~1.62 mg/片,见表5。该结果表明,不同生产厂家的制剂工艺、质控水平参差不齐,可能导致产品质量的差异。因此,完善黄连上清片的质量标准极为必要。
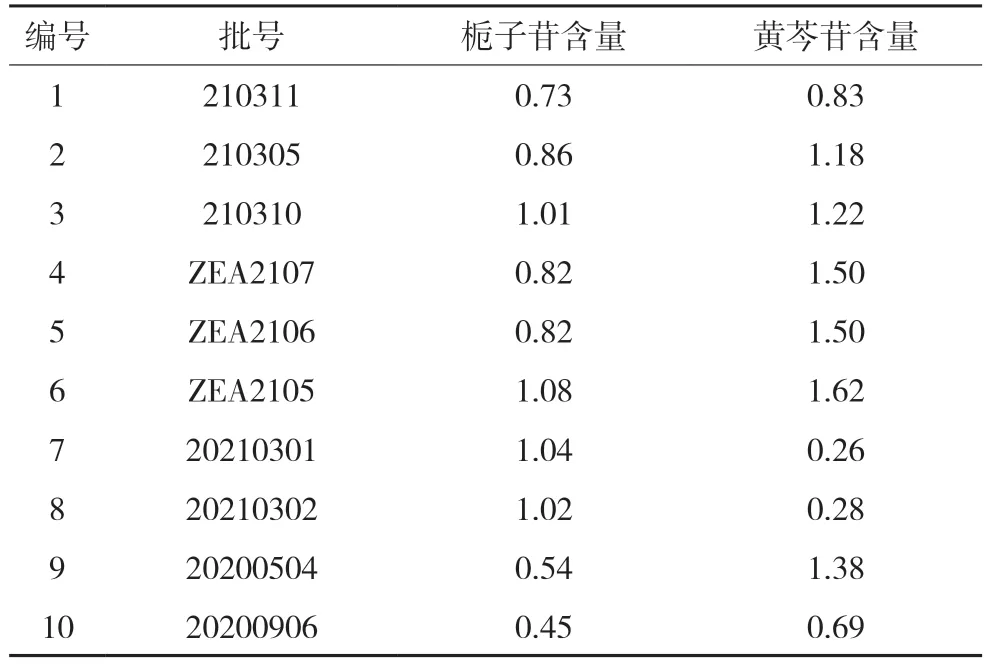
表5 样品含量测定结果 mg/片
4 讨论
4.1 检测波长的选择
本研究采用DAD 检测器,在200~400 nm 范围内对栀子苷和黄芩苷两种成分进行扫描,结果在250 nm 处均有较强的紫外吸收,因此选用250 nm为检测波长。
4.2 流动相的选择
分别考察了甲醇-水、甲醇-磷酸溶液、乙腈-水、乙腈-磷酸溶液等四种洗脱系统,结果乙腈的洗脱能力优于甲醇,水溶液中加入适量的磷酸后可改善峰形和分离度、减少拖尾现象。故最终选择流动相为乙腈-0.2%磷酸溶液[5]。
4.3 提取溶剂和提取方式的选择
采用甲醇、70%甲醇、乙醇、70%乙醇四种不同的溶剂对供试品进行超声提取,结果发现,当溶剂为70%甲醇时,提取效率优于其他溶剂,故最终选择70%甲醇作为提取溶剂。比较超声和回流两种提取方式,结果两种方式的含量测定结果相似,考虑到检验经济学和检测效率,最终选择超声作为提取方式。又分别考察了超声处理时间10 min、30 min、60 min 对含量测定结果的影响,结果超声处理30 min 和60 min 含量结果无明显差别,且均比超声处理10 min 时含量高。故最终选择超声处理时间为30 min[6]。
5 结论
本研究建立了黄连上清片中同时测定栀子苷和黄芩苷的HPLC 含量测定方法,供试品前处理简单,合理;方法准确度高,重复性好,为该药品的质量控制提供了研究依据,对评价黄连上清片的质量稳定性以及有效性均具有十分重要的意义。

