带蒂结膜瓣遮盖与羊膜遮盖术联合羊膜填塞术治疗角膜溃疡穿孔疗效比较
梁宗宝 李维娜 钟福炉
中国人民解放军联勤保障部队第910医院眼科,福建省泉州市 362300
角膜溃疡是一种比较常见的致盲性眼病,虽然大部分患者可以通过药物治愈,但是有些角膜溃疡由于发病机制不明、诊疗过程长、用药不当等因素,致使角膜溃疡经久不愈,甚至发生穿孔。目前治疗角膜溃疡穿孔常用的方法是穿透性角膜移植,但是由于角膜供体材料紧缺,治疗费用较高,使很多角膜穿孔患者得不到及时有效的救治,甚至最后并发感染最终只能行眼内容物剜除术。近年来,随着生物羊膜材料的发展,羊膜被广泛应用于角膜穿孔治疗中,并取得一定的成效[1-2]。同时带蒂结膜瓣也是一种有效治疗角膜溃疡穿孔的方法,其可以将营养物质和生长因子运送到角膜表面,明显提高角膜抗感染能力,阻止角膜进一步溶解,促进角膜溃疡穿孔的修复。本文通过收集42例角膜溃疡穿孔患者,并分别采用角膜溃疡清创+羊膜填塞及带蒂结膜瓣遮盖术和角膜溃疡清创+羊膜填塞及羊膜遮盖术两种手术方式,探索两种不同术式治疗角膜溃疡穿孔效果的差异,报道如下。
1 对象与方法
1.1 观察对象 收集2017年11月—2021年6月确诊的角膜溃疡穿孔患者42例(42眼)。纳入标准:确诊为感染引起的角膜溃疡穿孔,无药物过敏史。排除标准:合并青光眼、葡萄膜炎、玻璃体及视网膜等眼后段疾病;有外伤病史。所有患者入院均行裂隙灯、B超、眼前段OCT、角膜刮片等相关眼科检查。本研究经医院伦理委员会批准,患者均知情同意。按随机对照试验分为两组,每组21例(21眼),两组患者一般资料比较差异均无统计学意义(P>0.05),见表1。角膜溃疡位置是将角膜分为3区,以Ⅰ、Ⅱ、Ⅲ表示,其中Ⅰ区以角膜中心点为圆心,以2mm半径的圆形区,Ⅲ区为靠近角膜缘2mm以内的环形区,Ⅱ区为除Ⅰ和Ⅲ区外剩余的角膜环形区[3]。
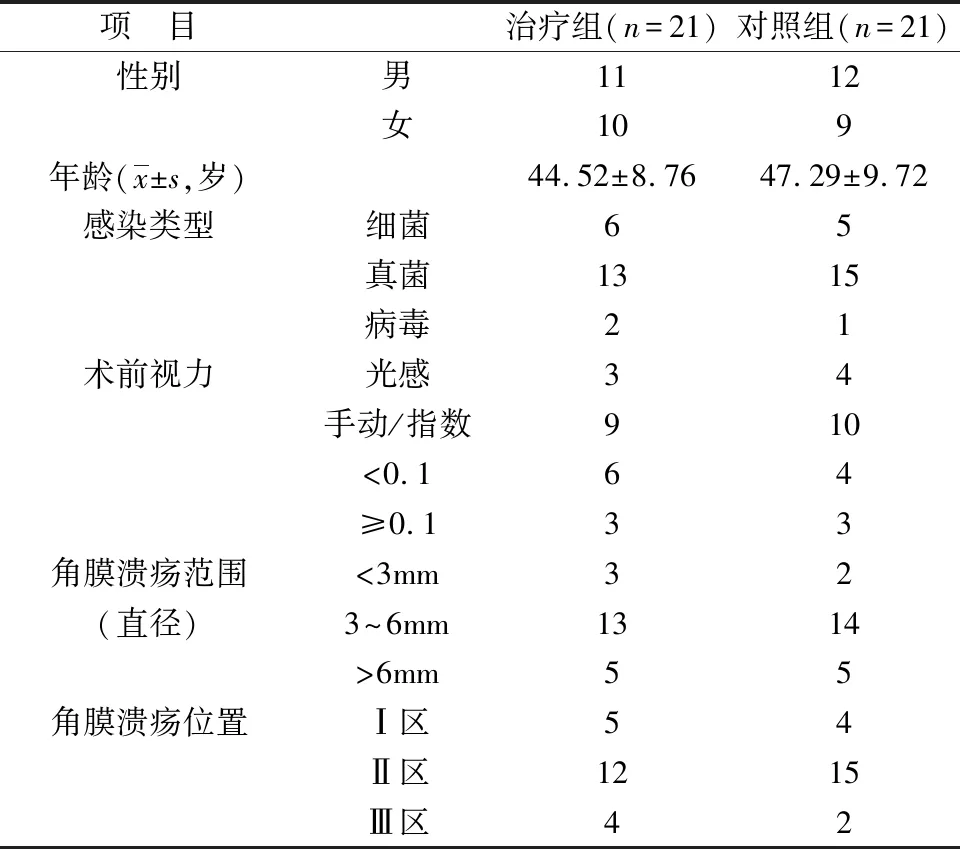
表1 两组患者一般资料比较(n)
1.2 方法 患者入院均根据感染病原菌给予全身及局部抗细菌、抗病毒或抗真菌治疗,待感染控制后手术治疗。患者术前30min均全身静脉滴注20%甘露醇250ml。常规消毒、铺巾,并行球结膜下浸润麻醉,显微镜下用刀片彻底清除角膜病变组织,尽量除去穿孔周围的炎症坏死组织及表面渗出物,从上方正常角膜缘做一穿刺口,沿着穿刺口向前房注入少许粘弹剂使虹膜与溃疡穿孔口的角膜分离。取生物羊膜(江西瑞济生物工程技术有限公司)根据溃疡面积的大小制作成多层植片,凸面朝下,把羊膜填塞于溃疡穿孔区,用10-0尼龙线将填塞的羊膜对位缝合于角膜基质上。其中对照组再取生物羊膜直接覆盖于角膜表面,用10-0尼龙线沿着角巩膜缘外连续缝合羊膜及结膜,并带部分浅层巩膜;其中治疗组根据溃疡面积大小于邻近结膜制作带双蒂结膜瓣,覆盖面积约大于溃疡两侧2mm。如果角膜溃疡穿孔位于中央,则从上方和下方分别取带双蒂结膜瓣,使两条带蒂结膜瓣覆盖面积约大于溃疡两侧2mm,将制作好的带双蒂结膜瓣覆盖于填塞羊膜的溃疡灶上,用10-0尼龙线将结膜瓣间断缝合于角膜浅基质层。然后两组患者均经角膜缘切口用乳酸钠林格注射液(浙江天瑞药业有限公司)冲洗前房粘弹剂,并做穿刺口水密使前房形成。两组患者术后均予结膜下注射妥布霉素2万U,术后加压包扎1d,术后继续局部及全身针对病原菌的药物治疗。
1.3 观察指标 (1)对两组患者术前及术后1和2周的疼痛程度、异物感、畏光症状进行视觉模拟量表(VAS)评分[4],随访时先在卡片上画0~10刻度,分别代表不同程度的不适感,让患者对自身的疼痛程度、异物感和畏光症状进行评分,其中0代表无明显不适,5分为中度不适,10分为极度不适。(2)观察两组患者溃疡愈合时间,判断标准为观察患者溃疡变化,进行荧光染色,无着色为溃疡愈合,记录患者从手术后第1天开始到溃疡愈合时间;(3)记录两组患者术前及术后1个月的视力变化情况。(4)观察两组患者术后角膜治愈情况。

2 结果
2.1 两组患者症状VAS评分及术后1个月视力比较 术前后两组VAS评分差异无统计学意义(t=0.795,P=0.378);术后1周对照组的症状较治疗组减轻明显,差异有统计学意义(t=5.467,P<0.01);术后2周治疗组的症状较对照组减轻明显,差异有统计学意义(t=9.134,P<0.01)。术后1个月,治疗组的视力较对照组提高更明显,差异有统计学意义(χ2=8.719,P<0.05),见表2。

表2 两组患者VAS评分及视力变化比较
2.2 两组患者角膜溃疡愈合时间 对照组患者角膜溃疡愈合时间为12~45d(20.68±8.72)d,长于治疗组的10~34d(15.8±3.88)d,差异有统计学意义(t=8.246,P<0.05)。
2.3 两组患者角膜治愈情况比较 对照组中5眼羊膜植片术后第4~9天出现羊膜卷缩或移位,予重新复位,并缝线固定;术后2周3例患者角膜感染无法控制,溪流征阳性,予重新打开羊膜,再次切除穿孔周围的炎症坏死组织,改行羊膜填塞加结膜瓣遮盖术;术后仍有1例感染无法控制并发眼内炎,予行眼内容物剜除术。治疗组1例患者术后由于结膜瓣回缩暴露其下填塞羊膜,再次行结膜瓣遮盖术,术后溃疡愈合,另有1例观察可见结膜瓣在位,但溪流征阳性,予重新打开结膜瓣,再次切除穿孔周围的炎症坏死组织,重新进行羊膜填塞后溃疡愈合,无穿孔患者。对照组术后角膜治愈率为61.9%(8/21),明显低于治疗组的90.5%(19/21),差异有统计学意义(χ2=4.725,P=0.030)。
3 讨论
角膜直接暴露于空气中,一般受伤导致角膜上皮的屏障被破坏后,角膜基质层便出现脱落、坏死、胶原溶解,最终导致角膜溃疡[5]。角膜溃疡如果炎症无法控制可出现穿孔,穿孔治疗不及时可导致视力丧失、眼内结构破坏,最终导致眼球摘除,如何及时处理穿孔是降低眼内感染及减少相关并发症的关键。羊膜含有丰富的生长因子,可促进上皮细胞的增殖、分化和移行,同时具有抗炎、抗瘢痕和抗新生血管形成的特点,已被广泛应用于临床,特别是用于治疗角膜溃疡穿孔已取得了显著效果。大量研究发现,羊膜填塞用于治疗直径为0.5~3.0mm的角膜溃疡穿孔成功率较高,且羊膜可维持人角膜内皮细胞的形态和功能,故可用于填塞角膜溃疡穿孔[6-7]。同时有研究显示,羊膜填塞可以加快药物吸收,通过直接作用于穿孔的部位,促进感染伤口愈合[8]。
本文通过比较角膜溃疡穿孔患者采用两种不同方法进行治疗,发现随着时间延长,两组患者自觉症状均较术前明显减轻,术后1周对照组症状减轻更明显,术后2周治疗组症状减轻明显,治疗组术后角膜溃疡愈合平均时间和视力恢复情况均明显优于对照组,原因可能有:(1)早期治疗组患者由于角膜溃疡处有带蒂结膜瓣遮盖,凸起明显高于对照组,故患者舒适度较差;(2)术后2周由于对照组覆盖表面羊膜吸收,使填塞的羊膜暴露,患者自觉症状反而加重,但是相对于术前两组患者的舒适度均有所提升;(3)治疗组患者由于溃疡处有带蒂结膜瓣遮盖,带蒂结膜瓣含有结膜丰富的血管,可增加溃疡处角膜的血供,加快药物、各种营养物质及生长因子等向角膜供应,进而促进角膜溃疡的愈合,减少角膜瘢痕形成,使其愈合时间缩短,视力改善明显;(4)治疗组患者由于将带蒂结膜瓣用缝线固定于角膜溃疡处,能使填塞羊膜贴覆紧密,不易脱落,而单纯羊膜遮盖容易引起羊膜卷缩或移位,甚至脱落,需要再次或多次手术,不仅延缓角膜溃疡愈合,而且可导致角膜瘢痕形成,因此治疗组患者愈合时间缩短,角膜治愈率高。
综上所述,在角膜材料缺乏的情况下,两种手术方法均可用于角膜溃疡穿孔的治疗。而采用角膜溃疡清创+羊膜填塞及带蒂结膜瓣遮盖术可以为角膜溃疡穿孔患者提供较好的组织结构,促进溃疡创面的愈合,缩短病程,减少并发症的发生,进而提高患者视力,该方法安全有效、简单实用,可为以后的角膜移植手术创造条件。

