经皮椎体成形术联合抗骨质疏松综合治疗伴有椎体裂隙征的老年胸腰椎压缩骨折*
代凤雷,赵建宁,钱卫庆,俞 宁,段光宇
南京市中医院,江苏 南京 210012
椎体裂隙征(Intravertebral cleft,IVC)是一类特殊的椎体骨质疏松压缩骨折(Osteoporotic vertebral compression fracture,OVCF),也称为骨质疏松性椎体骨折不愈合。随着我国人口老龄化加重,骨质疏松患者越来越多,但随着CT、MRI检查技术的进步,越来越多的IVC在老年骨质疏松性椎体骨折中被筛查出来。IVC表现为脊柱轻微外伤后数周或数月时间没有明显不适,但会逐渐出现腰背部的疼痛,并且疼痛呈持续加重,最后发展到脊柱后凸畸形。该病的发病机制尚不完全清楚,目前大多数研究认为IVC 系椎体缺血性坏死所致。Kim 等[1]研究认为,IVC 的发病机制可能为骨质疏松性骨折后椎体内假关节形成而非椎体缺血性坏死。IVC保守治疗通常予以非甾体抗炎药物联合抗骨质疏松治疗缓解疼痛,但多数患者病史较长,效果不佳。为能有效缓解患者腰背疼痛、减少卧床时间,南京市中医院采用经皮椎体成形术(percutaneous vertebroplasty,PVP)联合抗骨质疏松综合治疗伴有IVC的椎体压缩骨折,并取得了满意的近期疗效,现将结果报告如下。
1 资料与方法
1.1 一般资料
回顾性分析2018年1月—2021年9月南京市中医院接受PVP联合抗骨质疏松综合治疗的37例单阶段伴有IVC的老年胸腰椎压缩骨折患者的临床资料。其中,男11例,女26例;病程2周~7个月,平均病程6.8个月;年龄56~94岁,平均年龄71岁;主要症状为腰背疼痛,尤其是变换体位时疼痛明显,无明显神经根及脊髓损伤症状。纳入标准:(1)符合世界卫生组织(WHO)推荐的原发性骨质疏松诊断标准。(2)符合IVC的影像诊断标准[2〕。①CT提矢状位示椎体内有“真空征”或“裂隙征”。②MRI显示椎体中柱塌陷,硬膜囊受压,T1加权像呈低信号,T2加权像呈高信号、中等信号或混合性改变。排除标准:(1)非骨质疏松患者,双能X 射线骨密度测定T 值>-2.5。(2)伴神经根或脊髓功能损害。(3)存在手术禁忌证,如严重心、肺等内科疾病。本研究经样本医院医学伦理委员会审核批准。
1.2 治疗方法
患者取俯卧位,胸部、髂部垫软枕,腹部悬空保持脊柱过伸,术中持续低浓度吸氧,监护血压、心律、氧饱和度等。C型臂X射线定位病椎,采用单侧或双侧穿刺,1%利多卡因局部浸润麻醉,穿刺点常规选取椎弓根外缘1.5 cm 处,C臂机正侧位监视穿刺针进针点,调整穿刺针角度、位置,穿刺针指向椎体内裂隙,置入工作套管。调制聚甲基丙烯酸甲酯(PMMA)骨水泥至处于拔丝状态时开始推注,不过度追求完全恢复椎体高度,监视下低流量、低压、分次缓慢推注,至椎体内裂隙充盈满意即可。监视发现骨水泥渗漏时停推注骨水泥,旋转拔出穿刺针,穿刺处稍加压后外敷料覆盖,手术结束。术后24 h佩戴护具保护患者起床活动。
规范抗骨质疏松治疗:(1)术后予骨化三醇、碳酸钙长期规范用药,定期复查血钙。(2)对依从性差的患者予唑来膦酸注射液,1次/年静滴,连续3~5年。(3)不能使用唑来膦酸的患者给予阿伦磷酸钠片,1 片/次,1 次/周。(4)予鲑鱼降钙素鼻喷剂,1 次/d,鼻喷。(5)联合中药补肾健骨方剂。(6)腰背肌功能锻炼。指导患者行“飞燕式”腰背肌功能锻炼,3~5 s/个,5~8 个/组,2~3组/d。(7)健康宣讲,适当在日光下户外活动,预防跌倒,戒烟、减少饮酒,增加富含钙质、低盐和适量蛋白质的膳食,多晒太阳和适当户外运动合理饮食,定期随访,复查骨密度。
1.3 评价标准
术前、术后1周及末次(大于半年)随访复查,影像学评估观察局部椎体后凸角(Cobb 角)及椎体前缘高度;并采用疼痛视觉模拟评分(VAS 评分)及Oswestry 功能障碍指数(ODI指数)评估治疗效果。
1.4 统计学方法
采用SPSS 22.0 软件进行统计分析。分别对各组资料进行统计学描述。其中计量资料符合正态分布且方差齐时采用t 检验,组间比较行LSD-t 检验,不符合正态分布且方差不齐时采用秩和检验。计数资料比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
37例患者均完成手术并获得随访,随访时间7~26个月,平均随访时间11.8个月。术前、术后1周、以及末次随访均行正侧位片X 片检查,术后1 d 患者戴腰围护具进行下地行走。
2.1 患者术中、术后不良反应情况
术中9例患者出现骨水泥外漏,渗漏率为24.32%,多为椎体前缘渗漏,但未造成明显的不良后果,未发生有症状的肺栓塞病例。术后腰背疼痛症状多在1个月内明显缓解,半年内仅部分患者留有腰部酸胀感,通过口服抗炎镇痛药、肌松药等药物,联合指导患者腰背肌肉伸屈功能锻炼后好转。
2.2 患者术前、术后1周、末次随访各项指标情况
术后1周及末次随访与术前相比,患者椎体后凸角显著减少、椎体前缘高度显著增加,差异有统计学意义(P<0.05);末次随访与术后1周相比,患者椎体前缘高度略有降低、椎体后凸角稍增加,差异无统计学意义(P>0.05);患者术后1周及末次随访的VAS评分、ODI指数较 术前显著降低,差异有统计学意义(P<0.05),见表1。
表1 患者术前、术后1周、末次随访各项指标情况(±s)
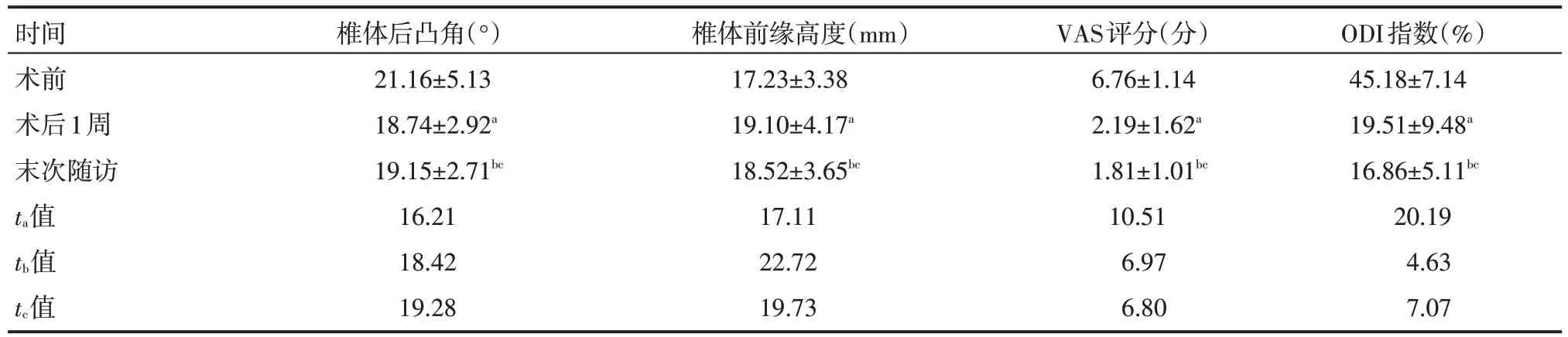
表1 患者术前、术后1周、末次随访各项指标情况(±s)
a表示术后1周与术前比较P<0.05;b表示末次随访较术前比较P<0.05;c表示术后1周及末次随访比较P>0.05。
时间术前术后1周末次随访ta值tb值tc值椎体后凸角(°)21.16±5.13 18.74±2.92a 19.15±2.71bc 16.21 18.42 19.28椎体前缘高度(mm)17.23±3.38 19.10±4.17a 18.52±3.65bc 17.11 22.72 19.73 VAS评分(分)6.76±1.14 2.19±1.62a 1.81±1.01bc 10.51 6.97 6.80 ODI指数(%)45.18±7.14 19.51±9.48a 16.86±5.11bc 20.19 4.63 7.07
3 讨论
伴有椎体裂隙征的老年胸腰椎压缩骨折由Herman Kummell于1895年首次报道,有许多同义词:如“椎体内真空裂隙征”“创伤后椎体骨坏死”或“椎体假关节”等,椎体内裂隙性骨折和骨折不愈合为特点,国内亦称骨质疏松性骨折不愈合。国外报道IVC在老年人群骨质疏松椎体压缩性骨折中的发生率为7%~37%[3],其发病机制可能是在老年人骨质疏松的基础上椎体微骨折,使椎体的血液循环发生损伤,供血障碍后骨小梁缺血坏死,骨重建负平衡,微骨折修复受阻,骨折不愈合,并存在假关节活动,微骨折的损伤与修复过程互相影响作用下使得IVC裂隙征形成。IVC是由骨质疏松、椎体局部缺血坏死、微骨折后的生物力学改变等多种因素作用的结果[4]。IVC患者往往合并骨质疏松症,骨质疏松症是其最被广为认可的一个重要危险因素。骨质疏松患者本身骨质量差,成骨能力弱,骨折处不易愈合,椎体骨折发生后不及时治疗导致骨质量进一步变差,形成恶性循环,导致出现IVC。影像学发现高达10%的骨质疏松性椎体骨折患者出现IVC 改变,随着骨质疏松性椎体骨折椎体压缩越明显,IVC的发生率越高[5]。此病临床表现为外伤或者无明显外伤腰背部疼痛,疼痛呈现为缓慢加重或持续疼痛,翻身等轻微活动即可造成疼痛加重,早期门拍诊摄X片显示椎体无明显压缩或轻微压缩,易造成漏诊,需进一步查CT 及MR 明确诊断。CT 横断面扫描可以发现不规则的结构及明显的硬化线;结合MRI 对诊断的帮助意义最大,MR 显示椎体内出现裂隙时可以发现异常信号的液体征或气体影[6]。
目前治疗IVC的方法并不统一,传统疗法以患者腰背疼痛时卧床休息,口服非甾体抗炎镇痛药或肌松剂,以腰背部软组织疾病方式治疗,患者往往因镇痛药的“欺骗”性而忽视进一步检查及治疗,易造成腰背疼痛的反复发作,病程较长,影响生活质量。伴有IVC的老年胸腰椎压缩骨折是一种进展性疾病,难以自行愈合,如不能及时发现和治疗,椎体进一步塌陷,引起后凸畸形,压迫脊髓和神经,可能会引起瘫痪。IVC的治疗多采用手术干预,对于神经脊髓损害的患者以开放手术居多,包括椎体的截骨、内固定,椎体的融合,椎管的减压等[7]。对不伴有神经脊髓损害的患者椎体成形术为首选[8]。PVP采用骨水泥充填技术,能够显著缓解椎体压缩骨折不愈合所致腰背痛,其作用机制在于骨水泥能增强椎体强度,固定微骨折,避免假关节形成。骨水泥的热效应产生局部高温,灭火病变细胞和神经细胞,降低神经敏感性,以及骨水泥单体对神经细胞具有毒性作用。
在本研究中,37例患者均行PVP手术,单个椎体手术时间约30 min,患者局部麻醉,全程清醒,安全性高,疗效确切。IVC 患者行PVP 手术,容易造成骨水泥的渗漏,术中9例患者出现骨水泥外漏,渗漏率为24.32%,与Elnoamany[9]报道的骨水泥渗漏是常见并发症,其发生率为22%~82%结果一致。骨水泥渗漏由真空裂隙征、病变分期以及骨水泥的注射速度、注入量、注射压力决定。为了减少骨水泥渗漏,应需注意以下几点:(1)术前应仔细阅读影像检查,明确裂隙的部位及椎体的完整性有无破坏,术中穿刺尽量避开破坏的部位。(2)穿刺方向尽量向着裂隙的部位,可在X线透视下调整方向,达到裂隙处,此时可行CT 三维重建,明确穿刺位置。(3)在椎体裂隙靠近终板或椎体前缘,或在椎体有破裂部位先行少量注入骨水泥,可采用边透视边注射,注入后,待骨水泥稍固化形成防漏屏障,再加大注射压力,可边注射边向外拔导管,使骨水泥充分弥散。(4)在椎体后缘及椎弓根无破损,裂隙靠近椎体后缘时,可在裂隙处注入骨水泥后,边拔导管边注射,可注入椎弓根少量骨水泥,形成骨水泥的“锚定”[10]。(5)骨水泥均匀弥散整个椎体能有效预防椎体的再次压缩,但对IVC术中应不追求骨水泥完全弥散到整个椎体,以缓解患者症状为目的,以安全为原则,裂隙周围有明显的硬化骨,骨水泥不能完全弥散,可尝试调整注入骨水泥的部位,也可采用骨填充网袋可“包围”裂隙,使裂隙形成“孤岛”,使得裂隙去神经化。(6)对于椎体后凸成形术,在行球囊扩张时,球囊压力不足以撑开椎体裂隙,是因为在裂隙周围形成硬化骨,再加大球囊压力的同时会引起椎体完整性的破坏,进而增加骨水泥渗漏风险。
IVC的在椎体成形术后能明显改善疼痛,但积极的抗骨质疏松必不可少。骨质疏松症是IVC的发病基础。经积极的抗骨质疏松症治疗,可以提高骨量,促进骨愈合,降低再骨折发生率。本研究发现,患者末次随访的X片显示Cobb角略增加、椎体前缘高度稍降低,说明对于手术能获得椎体即时稳定和改善症状,但随着年龄的增长,骨量的降低,使得椎体继续压缩。在本研究中术后1周与末次随访比较,椎体压缩程度无显著差异,说明积极抗骨质疏松治疗有明显益处。抗骨质疏松治疗以补充钙剂及维生素D为基础,但不建议只服用钙剂及维生素D 治疗骨质疏松,当骨密度明显下降、骨转换标记物显著升高时,应考虑继续抑制骨吸收的双膦酸盐骨质疏松药物或促进骨形成的药物治疗,常用的双膦酸盐类药物如唑来膦酸,阿仑膦酸钠、特立帕肽等[11]。中医认为,伴有椎体裂隙征的老年胸腰椎压缩骨折为“骨萎”范畴,坚持“标本兼顾”“内外兼治”“筋骨并重”的中医药综合疗法在此病上的前景广阔,不仅疗效突出,而且安全、便宜易于患者接受[12]。目前,中药在我国广泛用于原发性骨质疏松,常用的制剂如仙灵骨葆胶囊、骨疏康、左归丸、补正续骨丸等[12]。造成IVC患者腰背部反复疼痛的原因可能是椎体的微骨折刺激末梢神经引起疼痛,也可能为椎体的微骨折造成脊柱的稳定性下降,附着于脊柱的筋膜、肌肉反复刺激损伤引起疼痛。腰背部的肌肉能够保持脊柱的稳定性和平衡性,同时还是脊柱功能和步行功能的基石。本研究发现部分患者术后腰背部酸痛,予以加强腰背肌伸屈功能锻炼,同时给予口服肌松药物乙哌立松,患者症状多能改善。PVP术后疼痛症状明显改善后,需针对腰背部肌肉群力量、协调和稳定进行系统性训练,促进脊柱功能的恢复。这也能说明PVP 术后仍有部分患者出现腰背部疼痛缓解但持续时间长,需逐步加强腰背肌肉锻炼后疼痛逐渐缓解[13-14]。
综上所述,采用PVP结合抗骨质疏松综合治疗伴有椎IVC 的老年胸腰椎压缩骨折患者疗效显著。PVP 能改善腰背部疼痛症状,预防病变进一步加重,此手术方法操作时间短、创伤小、疗效明显,但术中需灵活掌握手术技巧,预防骨水泥渗漏;术后仍需积极的抗骨质疏松治疗,辅以有效的康复锻炼指导及宣教等综合治疗。但由于本研究纳入的病例数有限,需要长期的、多中心、大样本研究来进一步分析IVC的长期疗效。

