基于FAERS的地舒单抗安全警戒信号挖掘与评价*
辛莉 冯焕村 姜琳瑞 许锐佳 张群
(1.南方医科大学第三附属医院药学部,广东 广州 510630;2.中山大学孙逸仙纪念医院药学部,广东 广州 510120;3.广州新华学院药学院,广东 广州 510000)
地舒单抗是一种全人源单克隆抗体(IgG2类),以高度的特异性和亲和力与核因子-κB受体活化因子配体[Receptor activator of nuclear factor-κB(NF-κB)ligand,RANKL]结合,抑制RANKL与其受体核因子-κB受体活化因子(Receptor activator of nuclear factor-κB,RANK)两者之间的结合,以此来抑制破骨细胞的成熟、功能和存活[1]。地舒单抗于2010年5月首次在欧盟上市[2],在国外已经使用超过10年。相关临床研究显示,地舒单抗可提高骨质疏松症患者的骨密度,降低多种骨折的发生概率[3]。2020年7月1日地舒单抗在中国正式商业化上市[4],作为我国首个RANKL抑制剂,被用于骨巨细胞瘤、骨转移[5]和骨质疏松症的治疗。
随着地舒单抗的广泛应用,其上市后的安全监测及评价对指导临床有非常重要的作用。自发呈报是目前进行安全性监测最主要的方法,是发现药物上市后潜在不良事件的重要来源[6-7]。美国FDA不良事件报告系统(U.S. Food and Drug Administration Adverse Event Reporting System, FAERS)由于具有能提供长达20年的大量真实世界信息、数据安全可靠、更新速度快等特点,可用于挖掘药物上市后潜在的不良事件[8-10]。鉴于国内地舒单抗相关不良反应事件(Adverse events,ADEs)的分析鲜少,本研究基于FAERS数据库挖掘安全信号[11-12],分析评估地舒单抗潜在不良事件的可能信号,为今后地舒单抗在临床的使用提供一定参考依据,并为药物安全性评价提供新的思路。
1 资料与方法
1.1 数据来源 本研究所用数据来源于FAERS数据库。FAERS的ADE数据按季度进行更新,数据基于自发呈报系统(Spontaneous reporting system,SRS),即由报告者(患者本人或是医务人员等)自发提交的不良反应事件信息,包括患者身体情况、使用的药品、报告出处、提交时间和国家等信息。所有不良反应事件数据均是采用了国际医学用语词典(Medical Dictionary for Drug Regulatory Activities,MedDRA)的首选语(preferred terms,PT)编码[8,11,13]。
1.2 数据处理 本论文采用Open Vigil 2.1提取FAERS数据库中2010年5月—2021年9月的不良事件报告[14-16]。通过以地舒单抗的通用名“Denosumab”为检索词进行检索,剔除患者信息不全或是患者身份重复的报告,得到地舒单抗的报告数。
1.3 数据挖掘方法 本论文采用比值失衡测量法挖掘安全信号,为当今最常使用的不良反应事件信号挖掘方法,分为频数法和贝叶斯法两种[17-21]。频数法主要包含报告比值比法(ROR法)和比例报告比值比法(PRR法),其中ROR比PRR更加科学、更具说服力[22];贝叶斯法则主要包含贝叶斯判别置信度递进神经网络法(BCPNN法)和伽玛泊松分布缩减法(GPS法)。为减少仅使用一种算法给结果带来的偏差,本论文使用ROR法和BCPNN法对ADE信号进行检测。当ADE信号同时满足ROR法和BCPNN法的信号生成条件时,则将其列为可疑信号。ROR法和BCPNN法的具体计算公式和信号满足条件见表1,其中公式中a,b,c,d 的指代见表2。ROR值与IC值大小表示地舒单抗与对应信号间的统计学关联强度,数值越大则关联性越强。基于比值失衡测量法,对说明书中未提及的高风险信号置信区间作进一步比较,如置信区间越小的说明该信号与该药物的关联性越强[8,22-23]。

表1 2种信息检测方法的检测指标和计算公式
1.4 统计学分析 通过工具BioPortal对不良事件信号挖掘结果按照系统器官分类(system organ class,SOC)进行整理,分析整理数据采用Excel 2019。
2 结果
2.1 ADE报告的基本信息 收集到2010年1月—2021年9月的安全警戒信号共有5147个,患者共270503例,具体情况见表3。在270503例患者的报告中,女性所占比例(72.60%)高于男性(20.10%),年龄主要集中在≥75岁(25.70%);占报告数据前5位的国家分别是美国、日本、加拿大、德国、英国,其中美国报告数占报告总数的65.2%;ADE报告数最多的年份是2018年(60176例)、2017年(55786例)、2016年(31386例)和2019年(27721例),见表3。
2.2 ADE信号分析结果 地舒单抗ADE上报数排序前15的安全警戒信号情况见图1,涉及各类损伤、中毒和手术并发症、肌肉骨骼和结缔组织疾病、全身性疾病及给药部位各种反应、胃肠道疾病、皮肤和皮下组织疾病、外科和医疗程序和代谢和营养疾病,共7个系统器官分类(System organ class,SOC)。上报数最多的不良事件是超说明书用药(29.45%),其次是死亡(14.02%)、下颚骨骨质疏松症(5.41%)和关节痛(3.10%)等,见图1。统计270503份 ADE报告,经ROR和BCPNN 2 种方法共检测出450个ADE信号,剔除重复无关信号,经过整理后得到313个ADE信号,具体见信号筛选流程图2。利用BioPortal工具(https://bioportal.bioontology.org/)查询各ADE信号对照的MedDRA进行SOC,共涉及26个SOC。根据国际医学用语词典(MedDRA),将地舒单抗PT分为26个SOC,见表4。按照报告数排序,排名前五的是各类损伤、中毒和手术并发症(33916例)、肌肉骨骼和结缔组织疾病(28373例)、全身性疾病及给药部位各种反应(15143例)、胃肠道疾病(4748例)、代谢和营养疾病(3215例)。其中,信号数前3位的SOC为重点SOC,包括肌肉骨骼和结缔组织疾病(101个)、医学检查(40个)和胃肠道疾病(37个),在肌肉骨骼和结缔组织疾病的信号数最多,与说明书记录相符。通过合并ROR与BCPNN两法所得数据前100的安全警戒信号得重点安全警戒信号数据表,共80个重合信号。超说明书用药(32274例)为地舒单抗不良事件产生的最主要危险因素,发现异常高风险信号种植体周围炎(ROR=405.01,IC=2.65),但报告数仅6例。另,除说明书中提到的常见各种肌肉骨骼及结缔组织疾病、颌骨坏死及牙科疾病外,发现为高风险且说明书未提及的PT,包括颞下颌关节综合征(ROR=9.83,IC=3.03),下颌脓肿(ROR=23.24,IC=3.88),血液甲状旁腺激素增加(ROR=22.47,IC=4.01),雌激素缺乏症(ROR=80.57,IC=4.60)。见表5。
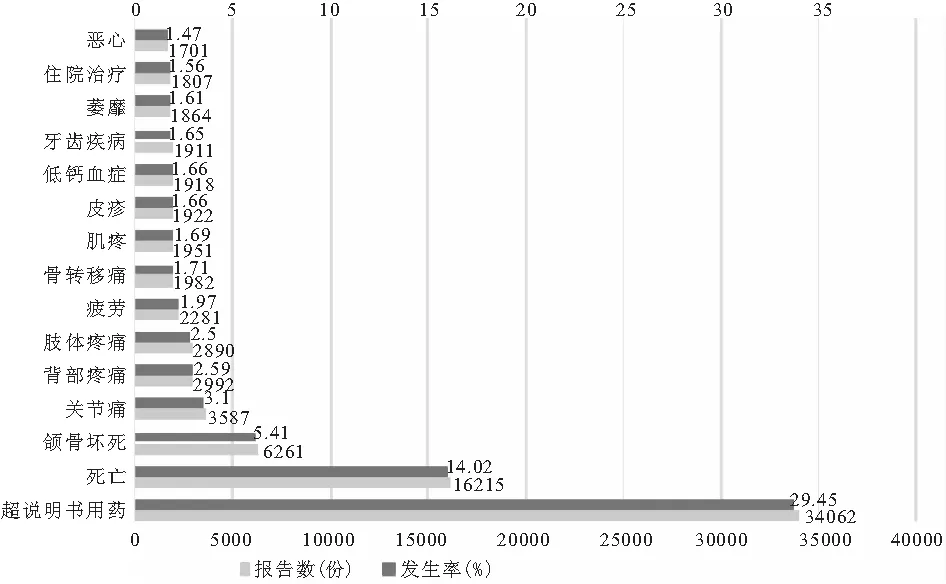
图1 地舒单抗常见的不良事件及其发生率
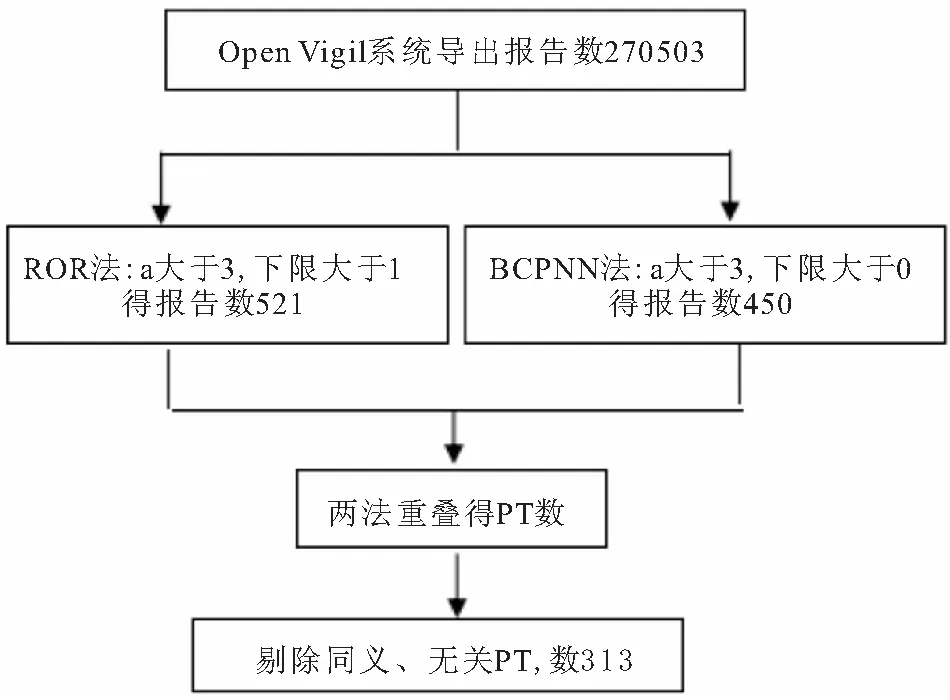
图2 信号筛选流程图
2.3 高风险PT的置信区间 计算2010年—2021年高风险信号中颞下颌关节综合征、下颌脓肿、血液甲状旁腺激素增加和雌激素缺乏症的置信区间,结果见表6。发现从雌激素缺乏症到血液甲状旁腺激素增加到下颌脓肿再到颞下颌关节综合征,置信区间范围逐渐变小,药物与ADE之间的关联性逐渐增强,推测颞下关节综合征较有可能发展成为新的不良反应。
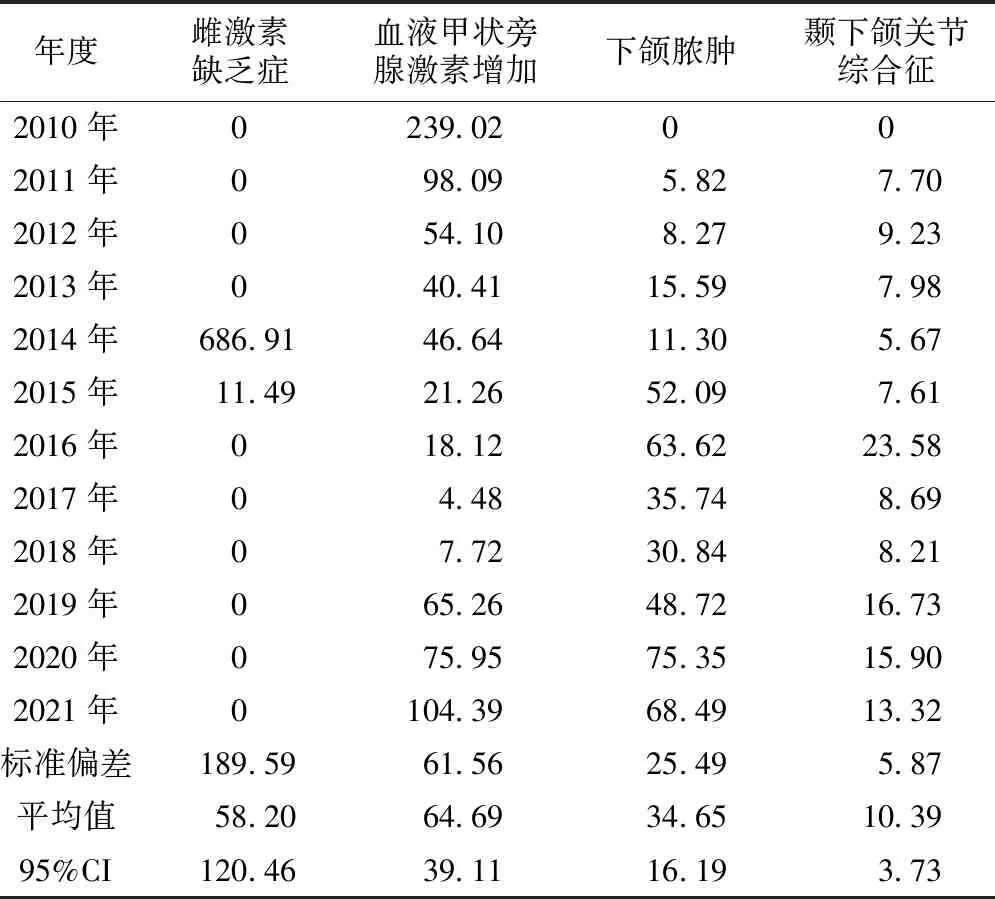
表6 地舒单抗高风险PT的置信区间
3 讨论
由于血液PTH和钙水平需要处于正常范围内才能接受下一剂地舒单抗,因此持续升高的血清PTH可能需要额外的检查来排除病理原因。相关研究发现,年龄的增长与使用地舒单抗的患者PTH升高有关,在无任何病理学的情况下,在降低骨折风险时继续使用地舒单抗可能是安全的,但可能需要进一步研究来证实[25]。也有研究[26]直接指出地舒单抗与注射后最初几个月甲状旁腺激素水平的代偿性增加有关,特别是在慢性肾脏疾病的情况下。本研究发现血清甲状旁腺激素(PTH)增加的强信号,报告数284例。
颞下颌关节综合症是一种影响颞下颌关节和咀嚼肌的疾病,典型特征包括颞下颌疼痛、关节音及下颌运动障碍,可伴有头晕、耳鸣等症状。信号置信区间结果显示颞下颌关节综合症与地舒单抗的关联性较强,报告数达118例,但目前尚无文献报道使用地舒单抗期间出现颞下颌关节综合症相关的不良反应,缺少直接的临床证据支持,但值得进一步研究及关注。在使用地舒单抗治疗期间如发生类似症状,应注意是否为颞下颌关节综合症,及时安慰和教育患者行软性饮食,注意下巴休息,热敷和拉伸疼痛部位,必要时使用非甾体类抗炎药进行干预[27]。
近年来,针对乳腺癌骨转移的患者在化疗的基础上加用地舒单抗,虽然化疗有效,但有可能因颌骨坏死发病,最终导致下颌脓肿而死亡[28]。地舒单抗说明书中提示,接受治疗的患者存在罕见的颌骨坏死报告,应评估风险,本研究同样发现药物相关颌骨坏死信号,且为强信号值,之相关的下颌脓肿报告数达86例。虽下颌脓肿的机制和治疗细节尚不明确,但也提示了使用该药治疗时应密切监测患者用药后反应。
有研究指出,雌激素缺乏初期,骨细胞机械环境和微环境均发生改变,细胞普遍存在凋亡现象,并发生高矿化。在缺乏雌激素的情况下,骨细胞的机械力应答反应受损,加剧破骨细胞的旁分泌调节。近期有研究表明,雌激素缺乏期间骨细胞的变化可能在骨质疏松症的病因学中起到关键作用[29]。而针对本研究发现的高风险信号雌激素缺乏症,报告数68例,提示地舒单抗治疗期间可能导致雌激素水平下降。FDA说明书提及地舒单抗适用于治疗具有骨折高风险的绝经后骨质疏松症的妇女,而绝经后女性卵巢功能衰退,体内雌激素水平急剧下降,考虑使用该药物可能造成的雌激素影响,将增加骨质疏松骨折风险。因此,在使用地舒单抗治疗绝经后患者骨质疏松症时应注意检测雌激素水平,以确定骨细胞靶向治疗抑制再吸收和继发矿化的有效性。
本研究结果显示种植体周围炎出现超强信号值。一项探究抗吸收药物的严重并发症的研究发现,使用地舒单抗治疗伴有骨转移的实体瘤或多发性骨髓瘤时会导致如深部龋齿、颌囊肿和种植体周围炎等众多牙科疾病[30]。但本研究中种植体周围炎事件报告例数仅6例,对该新信号与地舒单抗间的关联性有待进一步研究论证。
随着地舒单抗的快速开发和药品说明书更新的滞后等问题,出现较多超说明书使用案例。有报告显示地舒单抗用于治疗盆腔纤维结构不良等不适合外科手术且尚无有效或推荐的药物治疗的罕见疾病[31]。另有研究表明地舒单抗是青少年佩吉特病,纤维异型增生,Hajdu Cheney综合征和Langerhans细胞组织细胞增生症的潜在治疗选择,因为RANKL / RANK/osteoprotegerin的不平衡与这几种罕见的代谢性骨病的发病机制有关,地舒单抗也已在特定患者中超说明书使用[32]。Dürr等[33]对地舒单抗在动脉瘤性骨囊肿中超说明书使用情况进行案例报告,指出停止治疗后容易出现反弹引起的严重高钙血症,存在相当大的用药风险。临床上超说明用药往往仅基于疾病的发病机制和相关药物的作用机制或潜在药理效应,缺乏充分的临床试验证据,而容易造成不良事件的发生。根据本研究显示,超说明书使用是导致地舒单抗不良事件发生的重大危险因素,规范说明书用药至关重要。各国对普遍存在的超说明书现象实施的相关政策和立法不一[34]。为此,我国也于2022年3月施行的新医师法中首次将超说明书用药写入法条,明确在特殊情况下医师可以采用有循证医学证据的超药品说明书用法,进一步规范临床用药行为。
FAERS 数据库以自发报告的形式收集不良事件报告,可能存在上报人员身份差异、漏报、缺乏患者基本信息和基础用药人口数据等,从而无法得知不良事件报告的确切发生率[17,35];同时,本研究检测结果仅显示了地舒单抗与信号间存在统计学相关性,不一定是因果关系,加之本研究未考虑患者本身的疾病或联合用药等其他因素对ADE信号检测结果的影响,有待研究改进。
本研究通过对地舒单抗上市后的不良事件进行统计分析,利用ROR和BCPNN两种方法共检测出80个重点安全警戒信号,包含50个说明书未提及的新信号,不仅验证了说明书中提及的不良反应和药物警戒中提示的外耳道骨坏死事件,同时挖掘了包括血清甲状旁腺激素增加在内的6个值得关注的风险信号。
4 结论
本研究基于FAERS真实世界信息,运用2种数据挖掘方法与置信区间评价相结合,尽可能减少偏倚,客观地分析了地舒单抗与不良事件的联系。从挖掘出的安全警戒信号显示,地舒单抗超说明书用药情况严峻,安全合理用药工作迫在眉睫,发现的高风险信号显示用药期间需关注患者是否出现颞下颌关节综合征、下颌脓肿、雌激素缺乏症、血液甲状旁腺激素增加等不良事件,早发现早干预,以期降低临床用药风险。

