骨水泥不同分布形态对脊柱骨质疏松骨折单侧PVP手术效果及预后的影响
姜猛,王婷婷,吕科
1.西安国际医学中心医院脊柱外科,陕西 西安 710000;2.陕西中医药大学附属医院骨科,陕西 咸阳 712000
脊柱骨质疏松骨折是由机体骨量降低、骨强度不足、脆性增加造成的,其主要表现为骨质疏松性椎体压缩性骨折[1]。该病多发于老年人群,属于完全性骨折,老年患者在日常活动中轻微损伤即可造成脆性骨折,且骨折后愈合过程缓慢,再次骨折风险大,具有较高的致残率,严重影响其身体健康和生活质量[2-3]。临床针对脊柱骨质疏松骨折治疗有保守治疗和手术治疗,以手术治疗为主。传统手术治疗需切开内固定,创伤大、恢复慢,需再次手术风险大[4]。经皮椎体成形术(PVP)和经皮后凸成形术(PKP)是目前常用治疗该骨折的有效方法。PVP相较于PKP费用较低、操作更简便,得到了临床的广泛应用。据研究报道,PVP创伤小、恢复快、疗效好,相较于保守治疗,术后经早期功能锻炼就可促进患者康复,有助于提高生活质量[5]。骨水泥是PVP主要的填充材料,骨水泥在椎体内的弥散分布情况会对PVP 疗效及预后产生一定的影响,局限、偏态的骨水泥分布状态会导致患者术后疼痛,手术椎体前缘高度丢失,甚至可能再发骨折[6]。但目前针对骨水泥分布对手术的影响尚缺乏统一标准,主要原因是骨水泥分布形态复杂多样。本研究主要通过分析脊柱骨质疏松骨折患者行单侧PVP 手术后骨水泥分布形态,以探讨其对手术疗效与预后的影响,现将结果报道如下:
1 资料与方法
1.1 一般资料 本研究经医院医学伦理委员会批准,回顾性分析2019年3月至2022年3月西安国际医学中心医院收治的80 例脊柱骨质疏松骨折行单侧PVP手术患者的临床资料。纳入标准:(1)临床资料完整,X 线测定腰椎骨密度确诊为骨质疏松症,骨密度T≤2.0;(2)患者年龄≥60 岁,均符合骨质疏松性椎体骨折PVP手术适应证,包括疼痛的骨质疏松性椎体压缩骨折,经药物治疗无效的、与骨坏死相关的疼痛性椎体骨折、不稳定的压缩性骨折、多发性的骨质疏松性椎体压缩骨折、慢性创伤性骨折伴有骨折不愈合或内部囊肿改变、无神经症状的急性创伤性骨折等症状;(3)无PVP手术史及无自发性腰背疼痛;(4)患者及其家属同意并签署知情书。排除标准:(1)肿瘤、感染或其他疾病引起的病理性骨折;(2)具有多发恶性肿瘤性骨折、陈旧性骨折,非跌倒性损伤;(3)脊髓压迫或神经根受损致神经功能障碍者;(4)临床资料不完整,随访失联者。根据X线检查骨水泥分布情况进行分组,其中42例骨水泥分布互相连通的致密型患者纳入观察组,38 例骨水泥分布互相分离的弥散型患者纳入对照组。两组患者的一般资料比较差异均无统计学意义(P>0.05),但ASA 分级组间比较差异具有统计学意义(P<0.05),见表1。
表1 两组患者的一般资料比较[,例(%)]Table 1 Comparison of general data between the two groups[,n(%)]

表1 两组患者的一般资料比较[,例(%)]Table 1 Comparison of general data between the two groups[,n(%)]
项目性别分类t/χ2值0.028 P值0.867年龄(岁)BMI(kg/m2)受伤至手术时间(d)ASA分级男女I级1.492 2.249 1.245 8.752 0.139 0.469 0.455 0.003致伤机制0.0660.796术前合并症Ⅱ级Ⅲ级高处坠落伤交通伤摔伤生活伤其他糖尿病高血压冠心病观察组(n=42)14(33.33)28(66.67)79.33±5.95 22.23±2.35 10.34±3.34 35(83.33)5(11.90)2(2.65)4(9.52)6(14.29)10(23.81)18(42.86)4(9.52)15(35.71)18(42.86)9(21.43)对照组(n=38)12(31.58)26(68.42)81.35±6.15 22.63±2.35 9.36±3.56 20(52.63)16(42.11)2(5.63)3(7.89)5(13.16)12(31.58)16(42.11)2(5.63)15(39.47)13(34.21)9(23.68)0.6280.427
1.2 治疗方法 所有患者均给予单侧PVP术治疗。具体方法:(1)术前行常规X 线检查骨密度情况,根据美国麻醉学医师协会ASA 分级给予患者利多卡因穿刺点周围局部麻醉。(2)取患者俯卧位,胸前及髂前上棘垫枕,脊柱适度过伸位复位。常规碘伏消毒、铺巾后,C 型臂X 线机正侧位透视,确认骨折部位,明确水平位与矢状位的穿刺方向,保持在20°~30°,以棘突为中心确定手术椎体及穿刺点位置并标记。而后,于患者皮肤做长约0.5 cm切口,在X线引导下穿刺针经椎弓根穿入椎体前1/3处,缓慢锤击针尖,正位透视可见针尖位于椎弓根内缘,侧位可见见针尖达椎体后壁,最后再推进2 cm 左右,完成穿刺。然后调制骨水泥,将液压推管连接穿刺套管,推注骨水泥至患者伤椎内,在透视设备监测下,根据患者骨折、椎体形态等情况注入合适骨水泥量,等注入完成后分离装置,完成推注。(3)术中需同时密切监测患者生命体征,在推注完成后观察15 min,确定生命体征稳定后拔出套管,加压包扎,结束手术。(4)术后6~12 h后患者需佩戴支具下床活动,同时给予抗骨质疏松治疗。
1.3 观察指标与评价方法 (1)比较两组患者的手术时间、透视次数和住院时间;测量患者手术前后的前缘、后缘椎体高度,计算前、后缘高度比,并测量术前、术后3 d 局部后凸角(Cobb 角)情况。(2)比较两组患者的骨水泥注入情况,包括术中骨水泥灌注量,以及根据术后X线片观察骨水泥的渗漏情况,并观察两组患者术后再发骨折发生情况。(3)比较两组患者术前、术后1 d、3个月、12个月后的疼痛视觉模拟量表(VAS)评分和Oswestry 功能障碍指数问卷表(ODI)评分,以评价患者的疼痛情况和生活质量。
1.4 统计学方法 应用SPSS19.0统计软件进行数据分析。计量资料以均数±标准差()表示,组间比较采用t检验,计数资料比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者的相关临床指标比较 观察组患者的手术时间短于对照组,差异具有统计学意义(P<0.05),但两组患者的透视次数、住院时间、前后缘高度比、Cobb 角比较差异均无统计学意义(P>0.05),见表2。
表2 两组患者的相关临床指标比较()Table 2 Comparison of relevant clinical indicators between the two groups()

表2 两组患者的相关临床指标比较()Table 2 Comparison of relevant clinical indicators between the two groups()
注:与本组术前比较,aP<0.05。Note:Compared with that in the same group before surgery,aP<0.05.
组别例数手术时间(min)透视次数(次)住院时间(d)前后缘高度比Cobb角(°)观察组对照组t值P值42 38 36.65±8.05 40.76±9.16 2.137 0.035 16.90±4.18 17.03±5.17 0.124 0.901 12.09±5.21 13.12±5.23 0.881 0.380 74.33±5.19 74.42±5.25 0.077 0.938术前13.31±2.21 12.52±2.29 1.569 0.120术后3 d 10.33±2.19a 9.42±2.15a 1.281 0.203
2.2 两组患者的骨水泥注入情况比较 观察组患者的骨水泥灌注量及骨水泥渗漏明显少于对照组,差异均具有统计学意义(P<0.05),但两组患者术后再发骨折数量比较差异无统计学意义(P>0.05),见表3、图1。
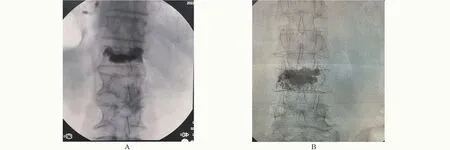
图1 患者正位片Figure 1 Anterior X-ray of patients
表3 两组患者的骨水泥注入情况比较[,例(%)]Table 3 Comparison of bone cement injection between the two groups[,n(%)]
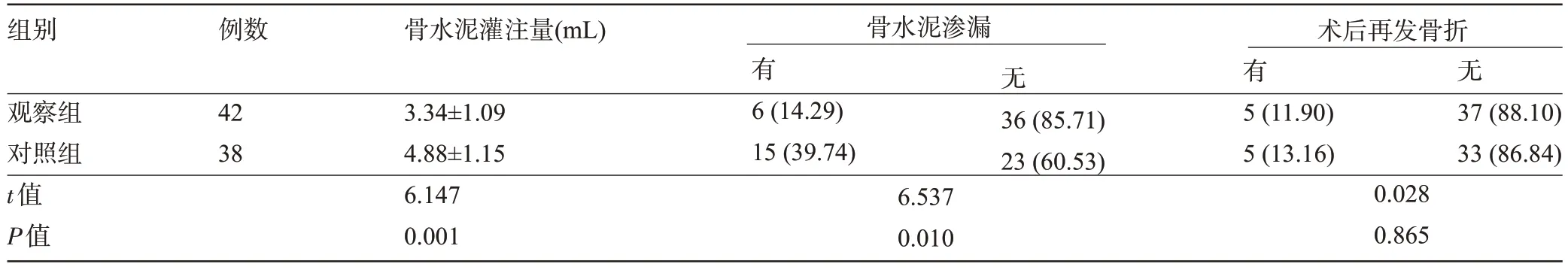
表3 两组患者的骨水泥注入情况比较[,例(%)]Table 3 Comparison of bone cement injection between the two groups[,n(%)]
组别例数骨水泥灌注量(mL)骨水泥渗漏术后再发骨折有无有无观察组对照组t值P值42 38 3.34±1.09 4.88±1.15 6.147 0.001 6(14.29)15(39.74)36(85.71)23(60.53)6.537 0.010 5(11.90)5(13.16)37(88.10)33(86.84)0.028 0.865
2.3 两组患者手术前后的VAS 评分和ODI 评分比较 观察组患者术后1 d、3个月的VAS评分明显低于对照组,术后3个月、12个月的ODI评分明显低于对照组,差异均有统计学意义(P<0.05),见表4。
表4 两组患者手术前后的VAS评分和ODI评分比较(,分)Table 4 Comparison of VAS score and ODI score before and after operation between the two groups(,points)

表4 两组患者手术前后的VAS评分和ODI评分比较(,分)Table 4 Comparison of VAS score and ODI score before and after operation between the two groups(,points)
注:与本组术前比较,aP<0.05,与本组术后1 d比较,bP<0.05,与本组术后3个月比较,cP<0.05。Note:Compared with that in the same group before surgery,aP<0.05;Compared with that in the same group at 1 day after operation,bP<0.05;Compared with that in the same group at 3 months after operation,cP<0.05.
组别例数VAS ODI观察组对照组t值P值42 38术前8.33±0.13 8.56±0.15 0.801 0.425术后1 d 2.35±0.16a 2.76±0.27a 8.355 0.001术后3个月1.37±0.13ab 1.97±0.52ab 7.236 0.001术后12个月0.93±0.03abc 0.95±0.15abc 0.846 0.400术前57.57±8.16 59.76±7.27 1.262 0.210术后1 d 20.87±7.16ab 21.77±7.22ab 0.559 0.577术后3个月12.47±4.16ab 17.86±9.27ab 3.409 0.001术后12个月11.21±3.63abc 16.97±8.50abc 4.008 0.001
3 讨论
PVP 是临床治疗脊柱骨质疏松骨折的常用手术方法,通过经皮单侧或双侧穿刺将骨水泥注入伤椎内,从而增强伤椎骨强度,有助于缓解伤椎疼痛,同时,骨水泥的注入有助于防止伤椎出现压缩,增强脊柱的稳定性[7]。随着技术发展和进步,针对脊柱骨质疏松骨折临床发展出骨填充网袋椎体成形术、PKP和经皮弯角椎体成形术等手术治疗,但PVP因其技术成熟、经济实用、操作简便等优势仍被广泛选择。但PVP存在一定的局限性,术中骨水泥弥散分布形态可能造成术后出现骨水泥泄露、术后邻近再发骨折等并发症,但国内缺乏统一标准[8]。
尽管临床针对不同椎体内骨水泥分布状态提出了不同的评价标准,但由于研究目的不同PVP术后骨水泥分布对术后疗效及预后的影响尚无统一评价标准。本研究根据80 例患者术后X 线检查在椎体内分布、凝固的不同密度和形态分为两组,一组为致密型分布,主要指患者术后骨水泥呈现为成团型分布,骨水泥之间互相连接;另一组主要为弥散型分布,主要指患者术后骨水泥呈现为互相分离的状态。分析形成这两大类的原因,可能在于本研究纳入的样本均为骨质疏松骨折性患者,骨质疏松严重程度、骨水泥稀稠情况、推注压力等多因素影响所致,当患者骨质疏松较严重,加大压力推注较稀的骨水泥,骨水泥可能分散快,形成比较分散的状态,反之则由于椎体内形成局部有限的空间,导致骨水泥在X线下呈现致密成团形态[9-10]。另外,本研究分析形成两种骨水泥分布形态还可能与单侧推注过程中患者伤椎部位范围大小相关。本研究结果显示,观察组患者手术时间短于对照组,骨水泥灌注量、骨水泥渗漏、术后再发骨折数量均少于对照组,差异有统计学意义(P<0.05),观察组患者与对照组透视次数、住院时间、前后缘高度比、Cobb角比较差异无统计学意义(P>0.05)。这提示临床对骨折患者行单侧PVP手术具有显著效果,且不同的骨水泥形态均有助于改善患者伤椎前缘、后缘高度比,恢复椎体高度,矫正后凸畸形,从而恢复椎体序列和稳定性,增强骨折椎体的稳定性和强度。但分析致密型组手术时间少于弥散组主要原因可能在于在透视手术下,术者可直接观察到水泥分散情况,当观察到水泥过分弥散时,术者为减少并发症可放慢推注速度,从而造成手术时间的延长[11-12]。两组骨水泥灌注量、骨水泥渗漏的差异原因可能在于弥散组因其伤椎注入水泥范围大,所需骨水泥量略多;同时因弥散组往往骨小梁腔隙相对大,水泥扩散快,推注速度过快或推注压力过高,都会导致骨水泥渗漏的风险增加[13-14]。两组均出现了术后再发骨折,可能与骨水泥的注入增加了椎体的强度和刚度,力学负荷转移至椎体,加上骨水泥本身可对椎体产生机械性刺激,杠杆作用下使椎体产生应力集中,椎间盘刚度增加,增加再发骨折的风险[15]。
有研究指出,相互连接的骨水泥相较于相互分离的骨水泥更有助于缓解疼痛。本研究结果证实了这一结论。本研究结果显示两组术后1 d、术后3 个月、12 个月的ODI 评分、VAS 评分较术前均大幅度降低,差异有统计学意义(P<0.05)。可见PVP手术中高温骨水泥对神经末梢和炎症介质的影响,使骨折患者术后疼痛均有所缓解,在缓解疼痛的同时恢复了通过固定伤椎骨折,增加伤椎力学稳定性,辅助一定程度的早期功能锻炼,有助于促进患者康复,从而提高患者生活质量[16]。同时,观察组在术后1 d 和术后3 个月的VAS评分低于对照组,术后3个月、12个月ODI评分观察组低于对照组。分析其原因,致密型骨水泥在相互连接状态下可以填充患者伤椎出断裂的骨小梁,承担轴向应力,从而有助于微骨折处的稳定,同时有助于阻断骨小梁对神经末梢的疼痛刺激,相较于弥散型骨水泥,能够更大程度减少患者伤椎疼痛[17]。还有研究指出,骨水泥的弥散不均匀分布可能导致伤椎负载不均匀,降低手术椎体稳定性,导致骨小梁出现微动和偏倚现象,增加患者术后疼痛。因此,本研究认为可通过提高术者手术熟练程度,注意调整骨水泥注射时黏稠度性状,在拉丝期进行推注,以便在推注过程中更好结团,形成致密型分布。同时术者应适当控制骨水泥的灌注量,选用较优质的骨水泥作为手术填充材料,在手术操作中注意穿刺针的进针位置及角度,阻断骨小梁的不良刺激,同时控制骨水泥注射速度,能够一定程度上减少骨水泥弥散和泄露。
综上所述,PVP 术后不同的骨水泥形态均能够有效缓解脊柱骨质疏松骨折患者疼痛,恢复脊柱的生物力学稳定性。骨水泥分布形态影响手术效果及预后情况,互相连通的致密性分布相较于弥散型分布在手术时间上更短,且减少骨水泥渗露,显著改善患者疼痛状况。但本研究仍存在一定不足,一是本研究样本数量有限,纳入样本均为单侧PVP 手术的患者,考察骨水泥分布形态影响可考虑纳入双侧穿刺样本使研究结果更加全面,二是本研究基于X线检测状态下的骨水泥分布分组,可考虑采用CT 三维重建进一步分析骨水泥分布类型,同时本研究采用回顾性分析资料,随访时间为1年,需进行多中心及前瞻性的大样本病例深入研究,使结果更加可靠。

