哈密市非洲猪瘟疫情监测与传播风险评估
张国新,杨 帆,张志新,张婉琪,张晓晓,玉努斯·阿不都,马春江,*
( 1. 哈密市动物疫病预防控制中心,新疆 哈密 839000 ; 2. 伊州区动物疫病预防控制中心,新疆 哈密 839000 )
非洲猪瘟是由非洲猪瘟病毒(African swine fever virus,ASFV)引起家猪、野猪感染的一种急性、热性和高度致死性传染病[1],也是全球当前威胁养猪业最重要的动物疫病之一。世界动物卫生组织(OIE)将其规定为必须报告的一种传染性动物疾病[2],我国将其列为一类动物传染病。截至目前,非洲猪瘟仍缺乏商业疫苗和有效药物,严重威胁养猪业的发展[3]。ASFV 传播途径主要有接触传播、软蜱叮咬或经食物传播等[4],家猪、野猪、疣猪等宿主动物对ASFV 易感,但症状只在家猪和野猪中显现,病程较短,病死率接近90%~100%[5]。ASFV 为非洲猪瘟病毒科非洲猪瘟病毒属的双链DNA 病毒,是迄今为止蜱传病毒中唯一已知的DNA 虫媒病毒[6]。自1921 年非洲猪瘟疫情首次在肯尼亚发现以来,ASFV 已从非洲蔓延到欧洲、亚洲、北美洲、南美洲等60 多个国家和地区[5],且仍呈流行扩大趋势[7-8]。截至2020 年12 月底,中国已有31 个省(市、自治区)发生了173 起非洲猪瘟疫情,累计死亡和扑杀生猪约101.1万头,不仅给养猪业带来巨大损失,还严重威胁我国猪肉生产和粮食安全[9]。
近年来,非洲猪瘟在新疆乌鲁木齐、哈密等地陆续发生,严重威胁当地生猪养殖业的发展。为进一步了解哈密市非洲猪瘟疫情发生后,疫点、疫区、流行病学关联区域、受威胁区及其他区域ASFV 的污染程度,本研究对哈密市非洲猪瘟疫情发生后的不同风险区域的风险因素进行病原学监测和分析,为今后非洲猪瘟疫情防控提供参考。
1 材料与方法
1.1 样品采集和区域监测
2022 年2 月哈密市伊州区发生非洲猪瘟疫情期间在全市范围内开展全覆盖监测,参照农业农村部印发《非洲猪瘟疫情应急实施方案(第五版)》的通知划分各区域,监测范围覆盖疫点、疫区、受威胁区、流行病学关联区域及其他区域的生猪养殖场户、屠宰场、商超肉铺、运输车辆等各风险区域,在哈密市31个生猪养殖场户和2个生猪屠宰场共采集样品3 398份。
1.2 仪器与试剂
实时荧光定量PCR仪购自美国ABI公司;组织研磨仪购自法国BertinTechnologies公司;核酸提取仪及核酸提取试剂盒购自西安天隆公司;非洲猪瘟荧光PCR试剂盒购自洛阳莱普生信息科技有限公司。
1.3 检测方法
本试验依据《非洲猪瘟诊断技术》(GB/T 18648—2020),采用实时荧光定量PCR(quantitative real-time PCR,qPCR)法进行检测。
1.4 数据统计与分析
试验数据采用Graph Pad Prism软件进行统计学分析。P<0.05 表示差异显著,P<0.01 表示差异极显著,P>0.05 表示差异不显著。
2 结果与分析
2.1 不同风险区域非洲猪瘟病原学检测结果(见表1)

表1 不同风险区域非洲猪瘟病原学检测结果Tab.1 Results of aetiological detection of African swine fever in different risk areas
由表1 可知,在哈密市不同风险区域的3 398 份样品中,ASFV核酸阳性样品65份,阳性率为1.91%。其中疫点检测样品167份,50份为病毒核酸阳性,阳性率为29.94%;流行病学关联区域检测175份,10份为ASFV核酸阳性,阳性率为5.71%;疫区检测样品289份,5份为病毒核酸阳性,阳性率为1.73%;受威胁区检测样品415份均为阴性;其他区域2 352份样品均为阴性。
2.2 不同风险区域非洲猪瘟病原学检测阳性率(见表2)
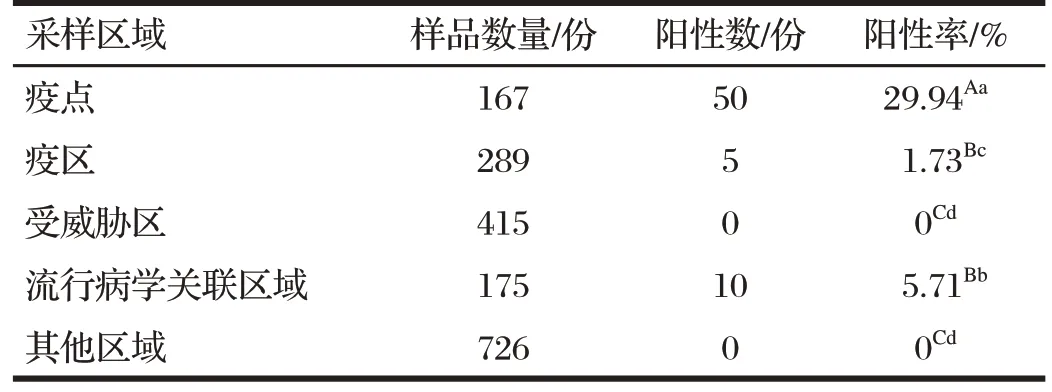
表2 不同风险区域非洲猪瘟病原学检测阳性率Tab.2 Positive rate of aetiological detection of African swine feverin different risk regions
由表2可知,疫点ASFV阳性率最高为29.94%,极显著高于疫区、受威胁区、流行病学关联区域以及其他区域的阳性率(P<0.01);疫区ASFV 阳性率为1.73%,极显著高于受威胁区、其他区域的阳性率(P<0.01),显著低于流行病学关联区域的阳性率(P<0.05);受威胁区ASFV 阳性率为0,极显著低于流行病学关联区域的阳性率(5.71%)(P<0.01);流行病学关联区域ASFV 阳性率极显著高于其他区域的阳性率(P<0.01)。
从疫点检测结果来看,ASFV感染猪的抗凝血、分泌物和组织中均检出ASFV核酸阳性,阳性率分别为100.00%、100.00%和87.50%。从疫区和流行病学关联区域的检测结果来看,在饲料和环境样品中检出ASFV 核酸阳性。结果显示,人员、车辆、工具、环境或饲料等风险因素可能是引发非洲猪瘟疫情的主要原因之一。
3 讨论
ASFV结构复杂,基因组庞大,迄今为止全球共报告了24 种ASFV 基因型,其中20 种分离自家猪,但只有5 种猪适应基因型(Ⅰ、Ⅱ、Ⅷ、Ⅸ、Ⅹ)的病毒在各地广泛传播[10]。基因Ⅰ型是传播最广泛的ASFV,也是唯一在非洲边界以外不同时期传播和确立的毒株[11]。基因Ⅷ型、Ⅸ型和Ⅹ型病毒在非洲具有很长的历史,而基因型Ⅸ型和Ⅹ型在东非占主导地位,在中非有一定的传播,但迄今为止没有进一步传播[12]。基因Ⅱ型病毒最初在莫桑比克发现,随后在欧洲和亚洲广泛传播,现在已传播到全球[13]。目前,中国以基因Ⅱ型病毒流行为主,与东欧和俄罗斯流行的病毒密切相关[14]。2021 年,中国报告了基因Ⅱ型和基因I 型ASFV的出现[15]。有研究指出,缺乏早期监测系统、蜱虫媒介监测、生猪异地调运环节检测、屠宰环节检测以及使用不安全的猪血饲料和泔水等因素可能是该病毒在中国31个省份的迅速传播的主要原因[16]。尽管最初ASFV表现出了极高的遗传稳定性,然而2020年有研究报告了多个ASFV变异株的出现,变异病毒的产生有可能导致具有新特征的ASFV毒株出现,可能会在未来显著影响ASFV的流行[17]。
与其他病毒相同,ASFV的传播也需要传染源、传播途径、易感动物等3 个基本条件。软蜱和野猪是ASFV 的主要储存宿主和传播媒介,家猪、野猪、疣猪等被感染病毒的蜱叮咬而感染[18],使该病毒在蜱-野猪中长期存在且难以根除,并在一定条件下感染家猪,引起疫情暴发。通常,发病猪和带毒猪是ASFV 的主要传染源,病猪组织和体液中含有高滴度的病毒,可经唾液、尿液、粪便和分泌物等排出体外。接触传播、经食传播和软蜱叮咬传播是ASFV 的主要传播途径[19],易感猪可通过与发病猪经口鼻直接接触,或接触病猪的排泄物、血液以及被污染的圈舍、器具、车辆等发生感染,也可因被携带ASFV 的软蜱叮咬或食入污染的饲料、饮水、泔水等感染。此外,由于ASFV对外界环境具有极强的抵抗力,可在血液、粪便、未熟的猪肉制品、腌肉和泔水中长期存活,在冻肉中可存活数年甚至数十年[20],导致该病毒在自然界的长期存在,严重威胁野猪和家猪等易感动物。因此,要控制病毒传播,必须做到尽早检测,发现病毒源头和传播风险因素,及时切断非洲猪瘟的传播链。
尽管安全有效的疫苗是应对当前非洲猪瘟疫情防控的关键手段,但是由于ASFV基因组庞大、结构复杂、基因型多样,导致尚无有效的药物或商品疫苗可用[21]。目前,该病的防控主要依赖严格的动物检疫、“拔牙”、净化、扑杀和无害化处理等程序。此外,由于ASFV高度稳定,对外界环境抵抗力较强,传播途径和风险因素复杂多样,给非洲猪瘟的有效防控带来了巨大挑战。因此,全面了解ASFV传播风险因素对于有效控制该病传播至关重要[22]。然而不同地区猪感染ASFV 的类型和风险因素尚不清楚,不同传播途径的传播风险如何也缺乏研究资料。在整个ASFV传播过程中,主要的潜在风险因素决定了ASFV 在野猪或家猪中的区域传播[23]。
有研究发现,ASFV可通过不同途径引入并传播,如生猪和猪肉产品贸易,跨区、跨境调运,野猪及蜱虫媒介,使用被污染的饲料及泔水喂猪,未经有效消毒的受污染运输车辆或从业者等均是ASFV 的传播途径[16,24]。ASFV 能够在饲料中保持传染性,猪可通过食用受污染的饲料传播。Niederwerder 等[25]研究发现,ASFV DNA 在几乎所有的饲料中均有很高的稳定性,其传染性在豆粕中最稳定,在4.44 ℃下至少能够保持112 d,提示饲料中ASFV传播的风险不容忽视。猪血作为一种重要的蛋白质来源,常作为猪和其他动物的添加饲料。有研究通过qPCR 检测及ASFV的全基因组测序发现辽宁省、河北省部分公司生产的猪血饲料被ASFV污染,且ASFV基因组与我国猪携带的ASFV样本的基因组相同[26],提示猪血饲料可能是ASFV 传播的一个重要来源。本研究对不同风险因素进行分析发现,除感染猪的血液及组织传播风险最高外,携带病毒的人员和车辆的传播风险较高,其次是受污染的饲料。
4 结论
本研究结果表明,通过对不同风险区风险因素的定时监测与分析,可为预防和控制非洲猪瘟疫情流行提供切实有效的建议。生猪、饲料、猪肉产品以及运输环节均可能是导致ASFV 传播的重要因素。因此,有必要加强对传染源和风险因素的定时监测,包括对野猪和蜱虫媒介的监测,对养殖场、转运车辆、易感动物的监测,对水源、饲料等风险因素的监测。应严禁疫点、疫区及流行病学关联区域生猪及生猪产品的调运,加强其他区域的市场调运环节和屠宰环节的检疫监管力度,严禁养殖场(户)使用有污染风险的饲料(猪源性蛋白饲料、泔水等)喂猪,以有效降低非洲猪瘟疫情的传播风险。

