西妥昔单抗联合XELOX方案治疗晚期结肠癌患者的疗效及对其血清NLR、TSGF和TRlM72的影响
廖盛欢,毛英,易双,蔡思敏,袁云(江西省新余北湖医院,江西 新余 338000)
结肠癌是我国常见消化道肿瘤疾病,其发病与饮食、遗传息息相关,高脂肪、高动物蛋白与低纤维饮食都会增加结肠癌的发病几率;此外,家族性息肉病、遗传性非息肉结肠癌的错配基因携带者也会增加结肠癌的患病风险[1]。早期的结肠癌常以排便习惯的改变与粪便形状的变化为主,后来可转变为定位不准确的持续隐痛,中晚期结肠癌则表现为贫血或者肠梗阻等。目前针对结肠癌的化疗方案以XELOX最为常见,该方案具有较好的临床疗效,但是其毒副作用也较为明显,包括抑制淋巴细胞与骨髓细胞造成三系减少,增加结肠癌患者其他疾病的患病风险[2]。西妥昔单抗是一种靶向治疗药物,可以与正常细胞和多种癌细胞表面的表皮生长因子(EGF)受体特异性结合,并竞争性阻断EGF和其他配体(如TGF-α)的结合,从而阻断细胞内信号转导途径、抑制癌细胞的增殖、诱导癌细胞的凋亡、减缓肿瘤生长[3]。相较于常规化疗药物,靶向药物具有毒副作用小、效果好及明显延长结肠癌患者生存期的优势,因此在各种癌症的治疗中得到了广泛的应用。本研究利用西妥昔单抗联合XELOX方案治疗晚期结肠癌患者,观察其临床疗效,报道如下。
1 资料与方法
1.1临床资料 通过便利抽样法连续选取入院时间在2022年1月-2022年11月之间的晚期结肠癌患者75例为研究对象,纳入标准:①经结肠镜和病理切片检查证实为结直肠癌,临床分期为Ⅲ、Ⅳ期,影像学检查证实存在复发、转移;②Karnofsky评分(KPS)>60分,预计生存期不低于3个月;③年龄>18周岁;④无化疗禁忌证;⑤符合伦理学标准,并获得结肠癌患者及家属的知情同意,签署知情同意书。排除标准:①有早期结直肠癌手术史;②伴有心、肺、脑、肝、肾等关键脏器功能异常者;③有其他部位原发恶性肿瘤或活动性感染者;④合并精神疾病、智力异常、认知异常等无法正常沟通交流者。应用随机数字表法分为研究组(n=38,西妥昔单抗联合XELOX方案治疗)和对照组(n=37,XELOX方案治疗),两组结肠癌患者治疗前年龄、性别、癌胚抗原(CEA)、TNM分期、病灶最大直径差异无统计学意义(P>0.05),见表1。

表1 两组结肠癌患者基线资料比较
1.2方法 对照组结肠癌患者均采用XELOX方案治疗,第1天应用奥沙利铂130mg/m2;第1-14天应用卡培他滨片1000mg/m2,2次/d;治疗14d后休息7d,21d为1个疗程,共治疗3个疗程。研究组在对照组基础上给予西妥昔单抗治疗,每次先使用抗组胺药物对过敏反应与输液反应予以预防后再给予西妥昔单抗,初始剂量400mg/m2,静脉滴注2h;之后每周给予维持剂量250mg/m2,静脉滴注1h,直至病情进展或副作用难以耐受或因经济原因而停用,化疗时常规给予盐酸昂丹司琼静脉点滴预防呕吐。
1.3观察指标 ①化疗3个周期后,根据《实体瘤疗效评价标准(RECIST)指南1.1版》评价比较两组治疗有效率。疗效评价标准:完全缓解(CR)即靶病灶消失;部分缓解(PR)即基线靶病灶直径之和减少>30%;病情稳定(SD)即基线靶病灶直径之和减少20%-30%;病情进展(PD)即基线靶病灶直径之和减少<20%或有新病灶出现;治疗有效率采用客观缓解率(ORR)表示,ORR=CR率+PR率,疾病控制率(DCR)=CR率+PR率+SD率。②两组化疗前、化疗1个疗程、2个疗程和3个疗程均取空腹肘静脉血4mL,以3500r/min离心5min,收集血清,置于-20℃冰箱快速冷冻备用,行批量检测。采用罗氏公司Cobas6000自动生化分析仪及其公司配套试剂盒、质控品、标准品进行血清中性粒细胞计数与淋巴细胞计数比值(NLR)、肿瘤特异性生长因子(TSGF)和三重基序家族蛋白(TRIM72)水平检测,具体操作严格按照试剂盒说明书进行。③统计治疗期间化疗毒副反应发生情况,包括白细胞减少、血小板减少、口腔黏膜炎、消化道反应、转氨酶水平异常、手足综合征、脱发、神经毒性。
2 结果
2.1两组近期疗效比较 化疗3个疗程时,研究组客观缓解率为73.68%,高于对照组的51.35%(P<0.05);研究组3个疗程时疾病控制率相较对照组差异无统计学意义(P>0.05),见表2。

表2 两组结肠癌患者客观缓解率比较
2.2两组化疗前后NLR、TSGF和TRIM72水平比较 两组化疗前NLR、TSGF和TRIM72水平比较,差异无统计学意义(P>0.05);两组化疗1个疗程之后,TRIM72水平相较化疗前升高(P<0.05);两组化疗2个疗程时,TRIM72水平高于化疗1个疗程,且化疗3个疗程时高于化疗2个疗程(P<0.05);研究组化疗3个疗程时NLR、TSGF低于对照组,TRIM72水平高于对照组(P<0.05);两组间NLR、TSGF化疗1个疗程、2个疗程时比较,差异无统计学意义(P>0.05),见表3。
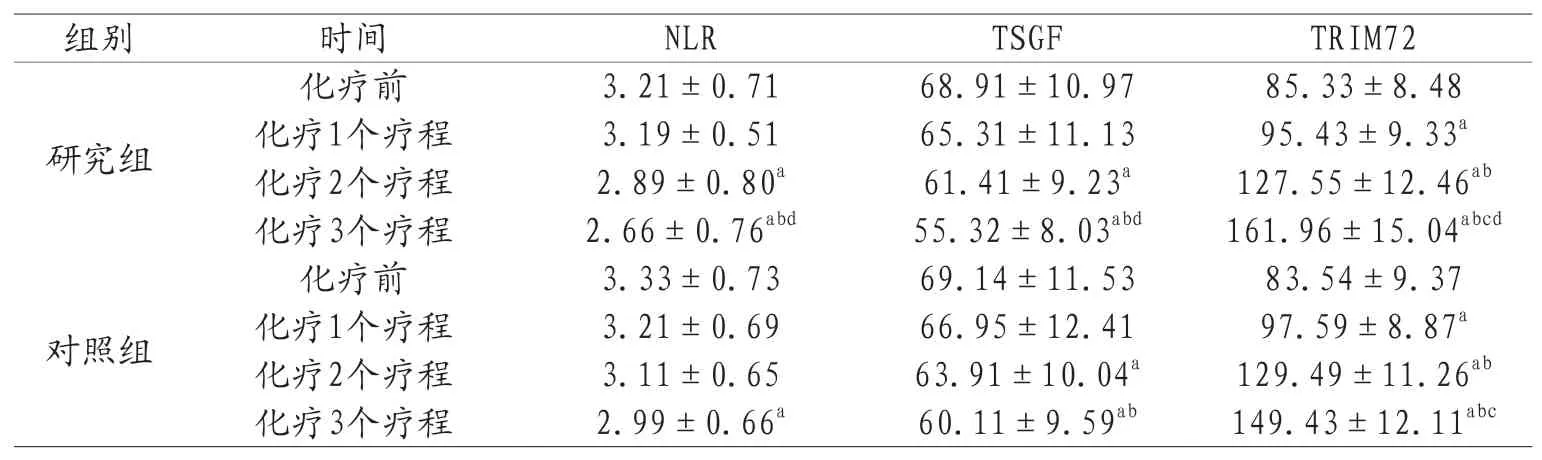
表3 两组结肠癌患者NLR、TSGF、TRIM72水平各疗程变化比较
2.3两组毒副作用发生率比较 化疗3个疗程时,研究组白细胞减少、血小板减少、口腔黏膜炎、消化道反应、转氨酶水平异常、手足综合征、脱发、神经毒性发生率与对照组比较,无统计学差异(P>0.05),见表4。
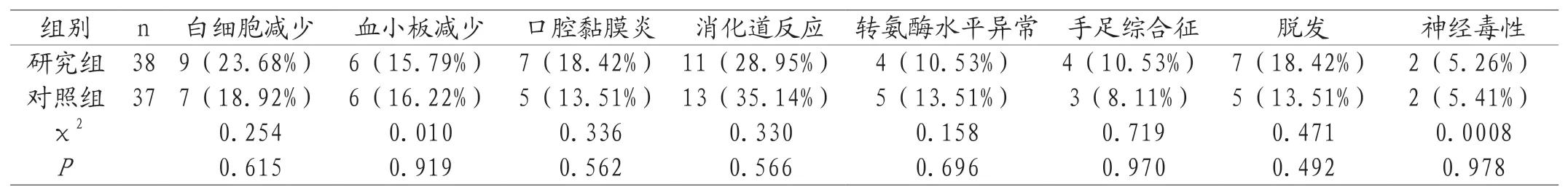
表4 两组结肠癌患者毒副作用发生率比较
3 讨论
对于晚期结肠癌患者来说,受癌症的直径、侵袭范围过大等因素影响,手术难度大大增加,加上病灶转移和癌症晚期导致的结肠癌患者抵抗力、手术耐受能力大大下降,手术的风险成倍增加[4]。目前药物化疗往往作为晚期结肠癌的首选,对于有条件进行结肠癌根治术的结肠癌患者,药物化疗也能降低结肠癌根治术后局部复发风险。奥沙利铂属于铂类抗肿瘤药物,奥沙利铂具有明显的抑制DNA合成作用,可抑制肿瘤细胞的增殖,从而发挥治疗癌症的特性[5]。卡培他滨属于5-氟尿嘧啶(5-FU)的前体药物,可以竞争性抑制dUMP转变为脱氧胸腺嘧啶核苷酸(dTMP),使胸腺嘧啶核苷酸合成受阻,从而抑制了DNA的合成,促进肿瘤细胞凋亡。奥沙利铂+卡培他滨一起使用能起协同作用,该方案是目前治疗晚期结直肠癌的一线化疗方案,但疗效仍不甚理想,在治疗过程中还会抑制淋巴干细胞、骨髓分化,降低结肠癌患者的免疫力,增加患者感染、出血风险,影响患者生存质量[6]。
靶向药物能够特异性结合癌症或者肿瘤的基因表达的位点,通过减少原癌基因的表达实现抑制肿瘤或癌症细胞生长的目的。表皮生长因子受体EGFR是肿瘤生长的关键靶点,西妥昔单抗作为表皮生长因子特异性抑制剂,能够特异性抑制肿瘤的生长。西妥昔单抗在单独使用及与其他药物联合使用时都能发挥其疗效,该药是针对人表皮生长因子受体的一种单克隆抗体,能竞争性抑制表皮生长因子及其相关受体,从而阻止其磷酸化获得活性,切断胞内信息传导通路,控制癌细胞增殖来发挥其效果。本研究发现,研究组经过3个疗程的化疗之后,结肠癌患者客观缓解率均有所升高,秋玉珍[7]等人指出西妥昔单抗联合XELOX化疗方案治疗晚期结肠癌能进一步提升近期化疗效果,本研究结果与其结果一致。此外,研究组与对照组的化疗毒副作用比较,差异无统计学意义,说明西妥昔单抗联合XELOX化疗方案不会增加常规XELOX化疗方案的毒副作用,余峰彬[8]等人的研究发现西妥昔单抗联合XELOX方案可提高结肠癌术后肝转移患者临床疗效及改善功能状态,且并未增加不良反应,本研究结果与其一致。
在近期研究中发现,TRIM72基因的敲除会使非小细胞肺癌转移能力大大增强,肝癌细胞的体外转移同样与TRIM72基因的敲除有一定关系;有研究表明血清TRIM72在结肠癌中水平降低,可能是结肠癌诊断和预后的潜在生物标志物[9]。TSGF能反映周边毛细血管、恶性肿瘤发生恶性增殖的情况,随肿瘤形成、生长,转移至外周血液,当结肠癌患者予以靶向联合化疗治疗时,TSGF水平得到明显改善。靶向联合化疗治疗可以有效降低结肠癌患者血清中TSGF水平,相较于常规化疗手段,对于改善患者预后水平效果显著。相关研究[10]表明,当患者淋巴细胞减少时,其血液处于高凝状态,其血液中的血小板数量与红细胞异质性都会增加,NLR水平也进一步降低。本研究发现,虽然XELOX方案也能在3个疗程之后降低结肠癌患者血清NLR、TSGF水平(P<0.05),但是在第三个疗程结束后,在XELOX方案上增加西妥昔单抗相较常规XELOX方案更能降低结肠癌患者NLR、TSGF水平,而TRIM72水平在3个疗程之后,西妥昔单抗联用XELOX相较常规XELOX方案提升更多(P<0.05),钟丽萍[11]等人也发现西妥昔单抗的应用能显著改善患者NLR水平,本研究与其结果一致。
综上所述,西妥昔单抗联合XELOX化疗能给结肠癌患者带来更好的疗效,同时抑制患者肿瘤增殖,增加患者体内抑癌基因表达,同时不会产生更多不良反应。

