单中心真实世界数据分析:表皮生长因子受体常见和少见突变型非小细胞肺癌靶向治疗疗效比较
王玉颖,燕 翔,董周寰,魏子涵,管静芝解放军医学院,北京 0085;解放军总医院第五医学中心肿瘤医学部,北京 0009;解放军总医院第一医学中心病理科,北京 0085;北京大学人民医院胸外科,北京 000
肺癌是全世界范围内发病率和死亡率最高的恶性肿瘤,非小细胞肺癌(non-small cell lung cancer,NSCLC)约占肺癌的85%。表皮生长因子受 体(epidermal growth factor receptor,EGFR)是NSCLC 最常见的驱动突变之一,以酪氨酸激酶抑制剂(tyrosine kinase inhibitors, TKIs)为代表的靶向治疗显著改善了NSCLC 患者的预后,是这类患者的标准治疗方法[1]。根据突变位点不同,EGFR突变型NSCLC 分为常见突变和少见突变,常见突变包括第19 号外显子缺失突变和第21 号外显子L858R 点突变,约占EGFR 突变型NSCLC 的80% ~ 90%。其余EGFR 第18 ~ 25 号外显子的各种突变类型均归为EGFR 少见突变,约占10%[2]。既往研究表明,少见突变具有较强异质性,与常见突变相比,少见突变患者靶向治疗疗效欠佳[3-5]。前瞻性随机临床研究通常不纳入少见突变人群,由于队列规模不平衡,真实世界研究也很少直接比较不同类别EGFR-TKIs 对常见与少见EGFR 突变患者的疗效。本研究对不同类别EGFR-TKIs 在EGFR 常见、少见突变型NSCLC 患者中的有效性进行回顾性分析,总结不同EGFR-TKIs 在EGFR常见、少见突变患者中的疗效,以期为临床决策提供更多证据。
资料与方法
1 资料 收集2019 年8 月1 日 - 2021 年12 月31 日在解放军总医院第一医学中心病理科进行二代测序(next generation sequencing,NGS)的不可手术的NSCLC 患者临床资料。纳入标准:(1) 病理类型为腺癌,临床分期按照AJCC 第7 版肺癌分期标准为Ⅲb ~ Ⅳ期;(2) NGS 检测提示存在EGFR突变;(3) 初治患者,既往未接受化疗及免疫治疗,原发病灶无手术及放疗指征;(4) EGFR-TKIs单药治疗;(5)基线资料完整,按照实体瘤疗效评估标准,至少有1 个可测量评估病灶。排除标准:(1)合并其他恶性肿瘤;(2) 合并20 T790M 突变;(3) EGFR 常见及少见复合突变;(4) EGFR-TKIs 联合治疗;(5)治疗过程中无法耐受不良反应而中途停药;(6) 病历资料不完整或失访;(7) ECOG 评分≥3 分。
2 研究方法 治疗及分组:满足入组标准患者每日口服一代(吉非替尼250 mg,1 次/d;埃克替尼125 mg,3 次/d)、二代(阿法替尼40 mg,1 次/d;达克替尼45 mg,1 次/d)或三代(奥西替尼80 mg,1 次/d;阿美替尼110 mg,1 次/d) EGFR-TKIs 治疗,直至疾病进展、发生不可耐受的不良反应或死亡。按照NGS 结果,19 DEL 和21 L858R 纳入EGFR 常见突变组,其余满足纳排标准的患者纳入EGFR 少见突变组,患者开始EGFR-TKIs 治疗前完善基线检查,进行胸腹部CT、颅脑MRI、骨扫描检查并记录可测量病灶大小。患者体力状态(performance status,PS) 按照Zubrod-ECOG-WHO评分标准进行评分(5 分法):0 分,患者活动能力完全正常;1 分,患者可以自由走动,进行一般家务活及工作,但不能从事较重的体力活动;2 分,患者生活能自理,但丧失工作能力,日间一半以上时间可以起床活动;3 分及以上,生活仅能部分自理、生活不能自理、死亡。
随访: 建立随访档案,患者每4 ~ 8 周复查1 次胸部CT 及常规实验室检查,治疗过程中出现转移相关临床症状则进行头颅MRI、腹部CT 或骨扫描等检查。每次复查后评价疗效和疾病进展情况。所有患者最长随访3 年,随访截至2022 年8 月1 日,汇总其无进展生存期(progression-free survival,PFS)。
3 疗效评价 近期疗效采用客观有效率(objective response rate,ORR)、疾病控制率(disease control rate,DCR)进行评价,中期疗效指标根据患者的PFS 进行评价。按照实体瘤评价标准(RECIST1.1)进行近期疗效评价,评价指标包括完全缓解(complete response,CR)、部 分缓解(partial response,PR)、疾病稳定(stable disease,SD) 和疾病进展(progressive disease,PD)。中期疗效评价指标为PFS。 PFS 为EGFR-TKIs 治疗开始到疾病进展或患者死亡的时间。在没有达到PFS 的情况下,数据被归为删失(时间截至最后1 次随访)。
4 统计学处理 采用SPSS 26.0 软件进行统计学分析。采用χ2检验或Fisher’s 精确概率检验评估两组患者临床参数间差异;Kaplan-Meier 生存曲线分析患者PFS,log-rank 检验评估组间差异;Cox单因素、多因素回归分析不同临床参数与PFS 之间的关联。P<0.05 为差异有统计学意义。
结果
1 患者一般资料 截至末次随访时间,共收集138 例不可手术的EGFR 突变型NSCLC 患者,39 例患者未满足纳入标准,其中合并其他恶性肿瘤3 例,合并20 T790M 突变8 例,EGFR 常见及少见复合突变4 例,EGFR-TKIs 联合治疗6 例,ECOG 评分≥3 分5 例,病历资料不完整或失访13 例,共99 例患者纳入本研究。所有患者临床上均证实为局部晚期、复发或转移性NSCLC,研究中包括了通过放疗或神经外科手术控制的脑转移瘤患者。45 例(45.5%)患者体力状态良好,ECOG评分为0 分;54 例(54.5%)患者体力状态一般,其中ECOG 评分为1 分43 例,2 分11 例。常见突变79 例(79.8%),少见突变20 例(20.2%)。常见突变患者中19 DEL 突变36 例(45.6%),21 L858R 突变43 例(54.4%)。少见突变患者中18 G719A/S/C/X突变7 例(35.0%),18 DEL 突变1 例(5.0%),19 L747P 突变2 例(10.0%),第20 号外显子插入突变(20 INS) 2 例(10.0.%),21 L861Q 突 变6 例(30.0%),另2 例少见突变复合突变,分别为18 G719C + 20 S768I (5.0%)、18 G719A + 21 L861Q(5.0%)。除EGFR-TKIs 类别(P<0.05)外,两组患者一般临床特征差异均无统计学意义(P>0.05)。见表1、表2。
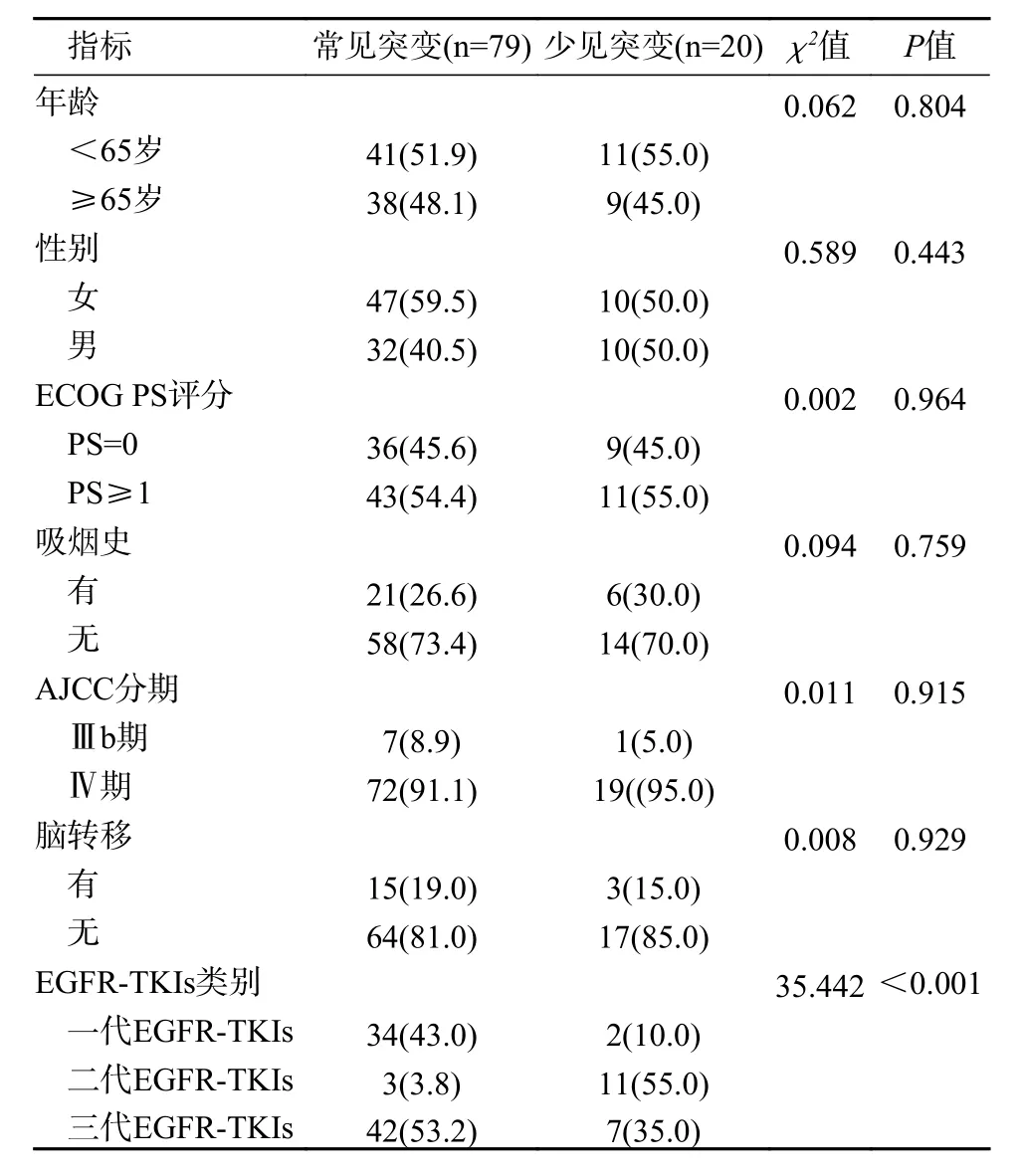
表1 NSCLC 患者人口学及临床特征(例,%)Tab. 1 Demographics and clinical characteristics of the NSCLC patients (n, %)

表2 99 例NSCLC 患者EGFR 基因突变类型T ab. 2 Types of EGFR gene mutations in 99 NSCLC patients
2 疗效分析 EGFR 常见突变组患者接受TKIs治疗的临床反应:50 例(63.3%)PR,24 例(30.4%)SD,5 例(6.3%) PD,ORR 和DCR 分别为63.3%和93.7%。少见突变组7 例(35.0%) PR,6 例(30.0%)SD,7 例(35.0%) PD,ORR 和DCR 分别为35.0%和65.0%。常见突变疗效优于少见突变(P<0.05)。见图1。
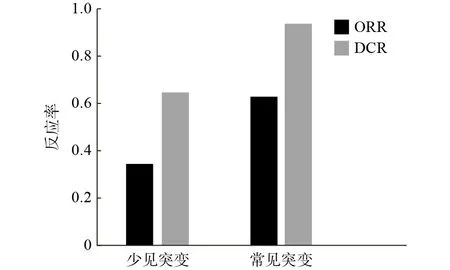
图1 EGFR 常见、少见突变型NSCLC 患者靶向治疗疗效Fig.1 Effect of targeted therapy in patients with common or rare EGFR mutations
3 生存分析 汇总各组患者的PFS,经Kaplan-Meier 生存分析和log-rank 检验,结果如下:常见突变组中位PFS 为13.3 个月,少见突变组中位PFS 为6.0 个月(P=0.006),中位随访时间14.6个月(图2)。应用一代EGFR-TKIs 治疗的常见突变组中位PFS 为12.0 个月,少见突变组中位PFS 为2.7 个月(P=0.139)(图3)。应用二代EGFRTKIs 治疗的常见突变组中位PFS 为13.3 个月,少见突变组中位PFS 为11.8 个月(P=0.497)(图4)。应用三代EGFR-TKIs 治疗的常见突变组中位PFS 为14.0 个月,少见突变组中位PFS 为2.0 个月(P=0.001)(图5)。
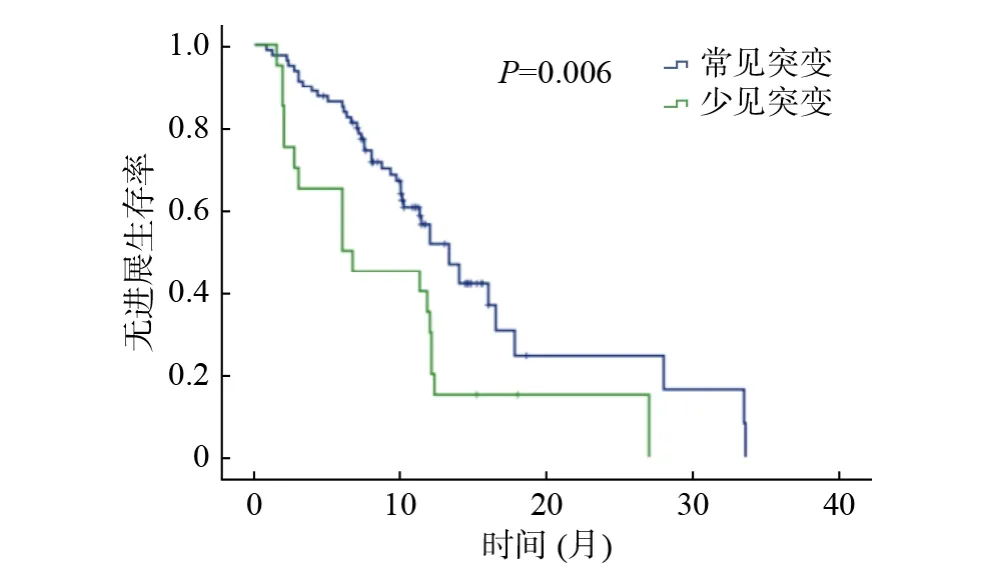
图2 EGFR 常见、少见突变型NSCLC 患者生存分析Fig.2 Progression free survival of the NSCLC patients with common or rare EGFR mutations

图3 接受一代EGFR-TKIs 治疗患者生存分析Fig.3 Progression free survival of the patients treated with firstgeneration EGFR-TKIs
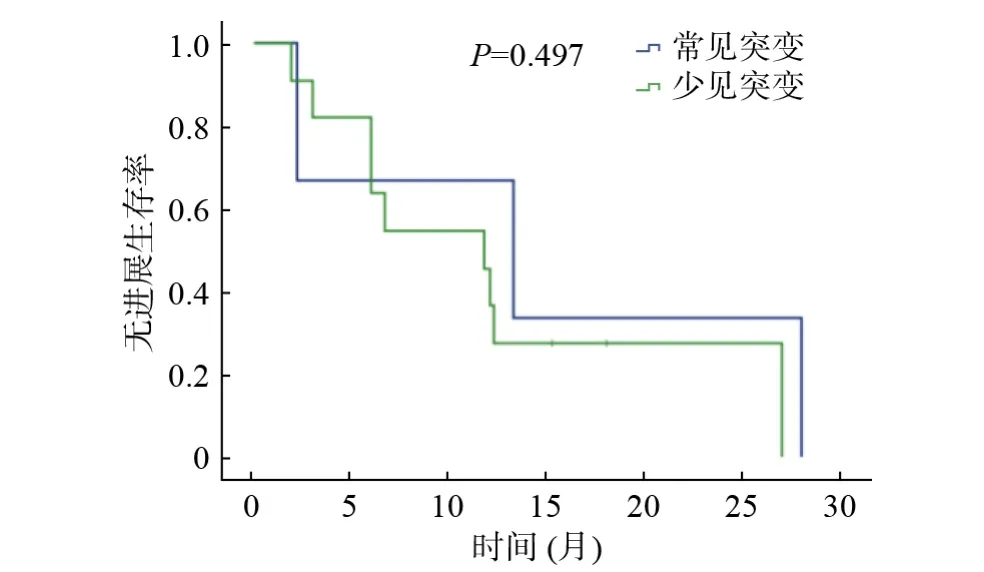
图4 接受二代EGFR-TKIs 治疗患者生存分析Fig.4 Progression free survival of the patients treated with secondgeneration EGFR-TKIs
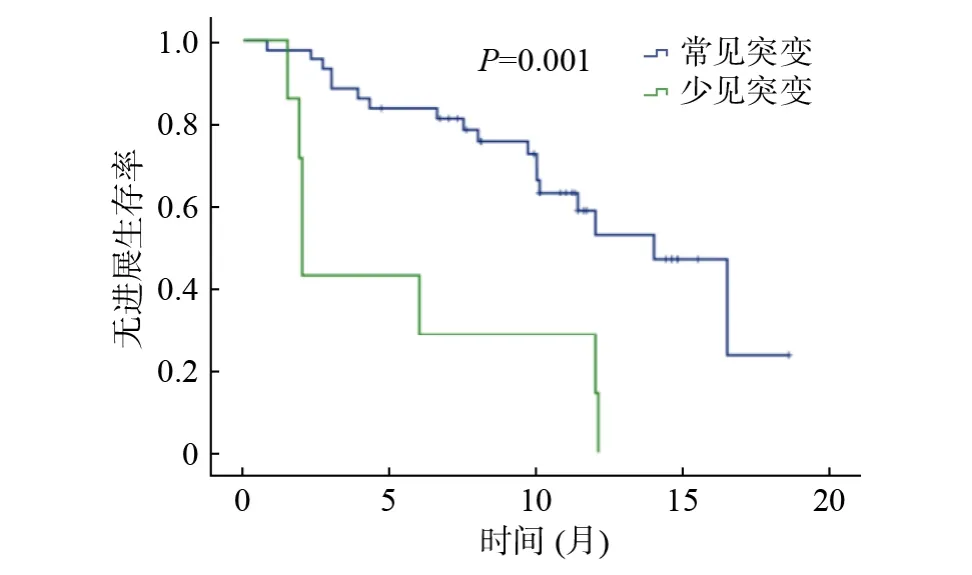
图5 接受三代EGFR-TKIs 治疗患者生存分析Fig.5 Progression free survival of the patients treated with thirdgeneration EGFR-TKIs
4 EGFR 突变型NSCLC 患者预后影响因素分析
单因素Cox 回归分析提示EGFR 突变类型与NSCLC 患者PFS 相关(P=0.008),EGFR 少见突变患者疾病进展风险高于常见突变患者(HR=2.129;95%CI:1.216 ~ 3.728)。多因素Cox 回归分析同样提示EGFR 少见突变患者疾病进展风险高于常见突变患者(HR=3.816;95%CI:1.790 ~ 8.135;P=0.001)。见表3。
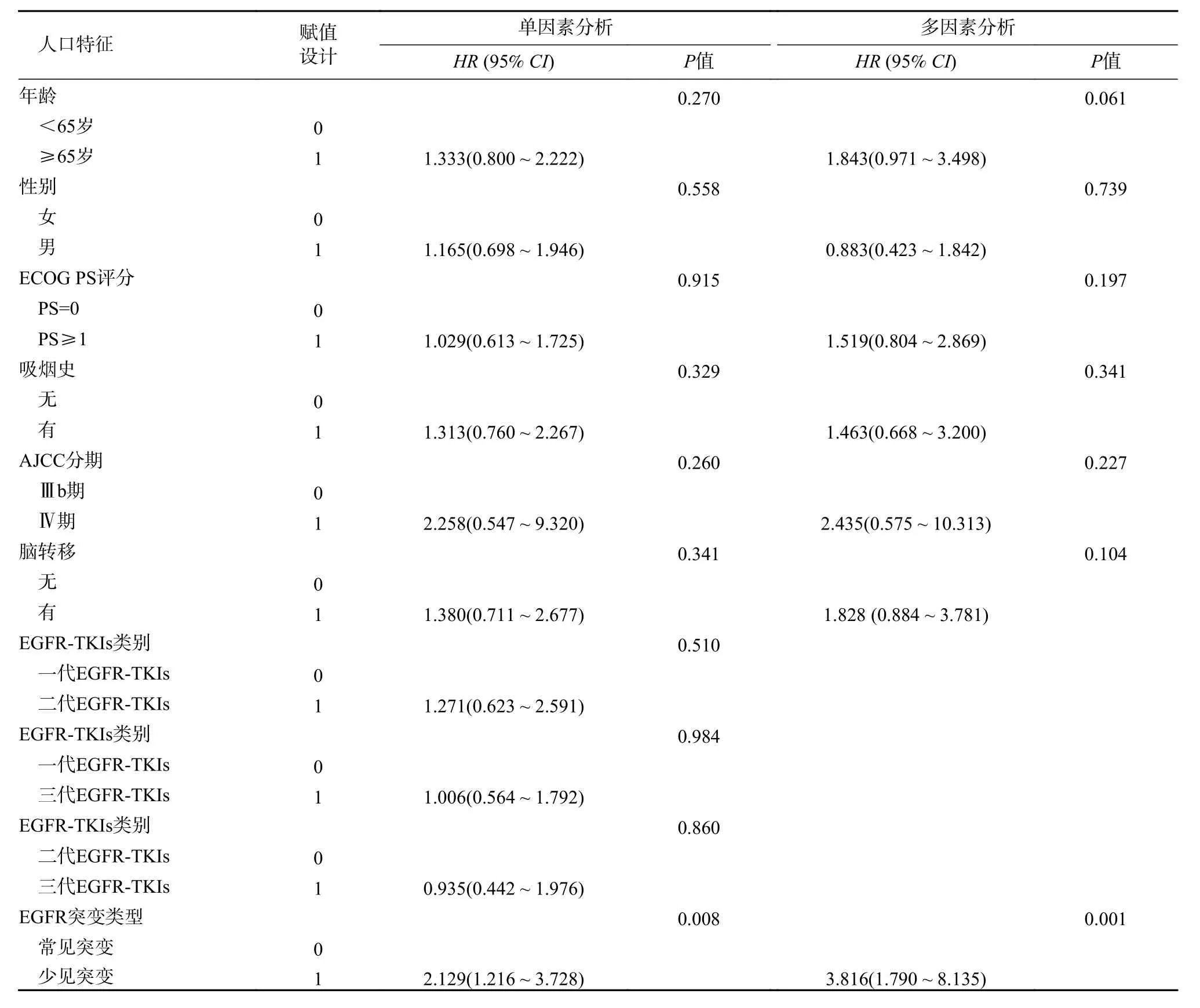
表3 Cox 单因素、多因素回归分析不同临床参数与预后的关系Tab. 3 Univariate and multivariate Cox regression analysis of the relationship between different clinical parameters and prognosis
讨 论
几十年来,IPASS、ENSURE、CONVINCE 等临床研究陆续表明,与化疗相比,一代EGFRTKIs 可明显改善EGFR 突变型NSCLC 患者的ORR和PFS。早期受制于基因突变检测技术,EGFR 少见突变很少被发现,EGFR 常见突变患者成为肺腺癌患者中EGFR-TKIs 治疗的优势人群。但接受一代EGFR-TKIs 治疗的患者中位总生存期(overall survival,OS) 并未显示出明显优势,同时获得性耐药也限制了长期疗效[6-9]。与激酶发生共价结合的不可逆性二代EGFR-TKIs 的出现,显著提高了患者的生存获益。LUX-LUNG3 研究显示,二代EGFR-TKI 阿法替尼可显著降低19 DEL 患者的死亡风险,相比化疗OS 有显著提高(33.3 个月vs21.1 个月)[10]。ARCHER 1050 结果显示,相比于吉非替尼,二代EGFR-TKI 达克替尼可延长患者OS(34.1 个月vs27.0 个月)[11]。同时随着二代测序技术的广泛应用,越来越多的EGFR 少见突变被鉴定出来[12]。然而真实世界数据显示,EGFR 少见突变具有较高异质性,对EGFR-TKIs 反应存在巨大差异。一、三代EGFR-TKIs 对少见突变患者疗效并不理想,只有G719X、S768I、L861Q 三类少见突变FDA 批准使用阿法替尼。针对20 T790M耐药突变而研发的三代EGFR-TKI 奥西替尼在NSCLC 患者一线治疗中也显示出了很好的疗效。FLAURA 研究显示,与一代相比,三代EGFR-TKIs奥西替尼一线治疗ORR 相似,中位PFS 有所提高(18.9 个月vs10.2 个月),OS 显著延长(38.6 个月vs31.8 个月)[13]。然而令人遗憾的是,上述大部分临床随机对照试验都将EGFR 少见突变排除在外,也没有对EGFR 常见、少见突变进行疗效对比,EGFR 少见突变的治疗无证可循。
本研究比较了EGFR-TKIs 一线治疗EGFR 常见与少见突变型NSCLC 患者的疗效。常见突变患者应用一代、二代、三代EGFR-TKIs 均可获益,其中应用三代EGFR-TKIs 治疗的患者中位PFS 最长,本研究的结果与上述大型临床研究结果基本一致。值得注意的是,本研究结果显示少见突变患者应用二代EGFR-TKIs 疗效最好,一代、三代疗效较差。Ⅱ期临床研究KCSG-LU15-09 结果显示,一代EGFR-TKIs 治疗少见突变患者疗效极差,ORR 仅20% 左右[14]。LUX-Lung2、3、6 三项临床试验结果显示,G719X、S768I 和L861Q三种少见突变的患者接受二代EGFR-TKI 阿法替尼的ORR 分别为77.8%、56.3%和100.0%,中位PFS 分别为8.2 个月、15.2 个月和12.3 个月,由此FDA 批准阿法替尼用于治疗上述突变[10]。KCSG-LU15-09 临床研究同时评估了奥希替尼对EGFR 少见突变患者的疗效,ORR 为50%,中位PFS 为8.2 个月[14]。但本研究中接受三代EGFRTKIs 治疗的少见突变患者中位PFS 只有2 个月,20 INS 等其他少见突变患者的纳入可能导致结果产生了偏倚。本研究表明,EGFR-TKIs 的选择对少见突变患者的疗效和预后影响较大,少见突变患者治疗首选二代EGFR-TKIs,三代EGFR-TKIs对少见突变患者的疗效仍需大型前瞻性临床研究进行验证。
本研究中有18 例患者基线即具有脑转移,15 例为常见突变,3 例为少见突变。既往研究表明,奥西替尼更容易通过血脑屏障,对具有脑转移的EGFR 常见突变型NSCLC 患者疗效更好[15]。在常见突变组,合并脑转移的患者中,5 例应用一代EGFR-TKIs,10 例应用三代EGFR-TKIs,应用三代EGFR-TKIs 的患者中位PFS 略有延长(11.4 个月vs8.0 个月,P=0.786)。在少见突变组,合并脑转的患者中,1 例应用二代EGFR-TKIs,2 例应用三代EGFR-TKIs,应用二代EGFR-TKIs 的患者中位PFS 时间更长(6.7 个月vs1.9 个月,P=0.225)。与常见突变不同,少见突变合并脑转移患者应用二代EGFR-TKIs 疗效更好,但由于样本量少,结果可能存在偏倚。
EGFR 少见突变对EGFR-TKIs 的选择性极高,同一外显子的不同位点突变对EGFR-TKIs反应都可不同。以20 INS 突变为例,通常认为20 INS 为EGFR-TKIs 耐药突变[16]。此类突变患者靶向治疗难度大。本研究纳入的2 例20 INS 突变患者(S768_D770dup,A767_V769dup)对靶向治疗反应均表现为早期进展。然而深入研究发现,虽同为20 INS 突变,其中A763_Y764insFQEA 和D770delinsGY 突变患者却在应用奥西替尼治疗时较其他突变患者具有更长的中位PFS (4.2 个月vs2.2 个月,P=0.164)[17]。同代EGFR-TKIs 之间的疗效也不尽相同,Li 等[18]对比了二代EGFR-TKIs阿法替尼与达克替尼用于少见突变患者的疗效,结果显示达克替尼的ORR 显著高于阿法替尼(60.5%vs26.7%,P=0.008),但两者的中位PFS 无统计学差异(12.0 个月vs10.0 个月,P=0.305)。由于样本量有限,未能将EGFR-TKIs、患者突变类型进一步细分,需要进一步研究建立包含所有EGFR 突变及其对不同EGFR-TKIs 治疗个体反应的数据库,用来为每一个特定的EGFR 突变提供临床决策依据,优化EGFR 突变患者尤其是少见突变患者的治疗方案。
本研究的局限性主要在于:(1)本研究为回顾性临床研究,不能消除偏倚;(2) 患者来自单中心,EGFR 少见突变样本量较少,后续需要扩大样本量继续验证;(3)本研究中的部分数据在末次随访时未达到PFS 这一中期观察指标,在进行统计分析时属于删失数据;(4)本研究入组的大部分患者尚未达到OS 这一远期观察指标,后续会继续进行随访。尽管这些因素在一定程度上削弱了本研究结论的准确性和可靠性,但本研究为针对不同代EGFR-TKIs 对EGFR 常见突变、少见突变患者治疗疗效开展的一项临床评估,对EGFR 突变型NSCLC 患者一线临床治疗选择以及少见突变患者后续研究方向具有一定的提示意义。
作者贡献王玉颖:论文选题,数据的收集、整理及分析,完成论文初稿及修改;燕翔:论文选题与构思,方法设计与指导,监督指导,论文修改;董周寰:论文选题,数据收集与整理;魏子涵:数据收集与整理,论文修改;管静芝:论文选题与构思,方法设计与指导,监督指导,论文修改。
利益冲突所有作者声明无利益冲突。
数据共享声明本篇论文相关数据可依据合理理由从作者处获取,Email:jzjz1970@hotmail.com。

