异叶三宝木的二萜成分及抗菌活性研究
岑祥妮, 范艺灜, 刘浩文, 李佳莹, 王川林, 刘平怀
异叶三宝木的二萜成分及抗菌活性研究
岑祥妮, 范艺灜, 刘浩文, 李佳莹, 王川林, 刘平怀*
(海南大学化学工程与技术学院,海口 570228)
为研究异叶三宝木()的二萜成分及其抗菌活性,采用硅胶柱层析、凝胶柱层析、高效液相色谱对萃取物进行分离纯化,结合现代波谱技术对所得化合物进行结构鉴定,并通过牛津杯法和2倍稀释法检测化合物对革兰氏阴性菌大肠杆菌()以及革兰氏阳性菌肺炎双球菌()的生长抑制活性和MIC值。从异叶三宝木中分离得到了6个化合物,包括5个二萜类, 1个木脂素类,分别鉴定为trigonochinene E (1)、neoboutomannin (2)、6,9-- dedimethyltrigonostemone (3)、stelltian B (4)、3,4-secosonderianol (5)、biondinin A (6)。化合物1、2、3、5对大肠杆菌有抑制作用,MIC值分别为9.375、18.75、18.75、18.75g/mL。化合物2、3、4、6为首次从该种植物中分离得到,化合物4为首次从该属植物中分离得到。除化合物4外,其他化合物都有一定的抗菌活性,且化合物1、2、3对大肠杆菌抑制作用强于阳性对照硫酸卡那霉素。
异叶三宝木;二萜类;大肠杆菌;肺炎双球菌
大戟科(Euphorbiaceae)三宝木属()植物全世界有50~80种,主要在热带和亚热带的亚洲地区分布[1], 我国现有10种,分别为三宝木()、孟仑三宝木()、长梗三宝木()、黄花三宝木()、异叶三宝木()、剑叶三宝木()、长序三宝木()、白花三宝木()、丝梗三宝木()和黄木树(),主产于海南、云南、贵州以及广西、广东等南部省区[2]。异叶三宝木是海南特有植物,生长于低、中海拔的山谷密林之中,高1~2 m;叶子长12~35 cm,宽4~ 10 cm,其果序梗长1~8 cm,有长约2 cm的宿存萼片和苞片,且均呈现披针形状;蒴果与球形近似[2]。三宝木植物在海南当地用来治疗平喘病,在东南亚地区还可作为杀菌防腐剂,解毒剂,化痰止咳制剂[3–4]。三宝木植物的主要化学成分为萜类[5–6](二萜及其二聚体)、甾体类、木质素和生物碱类。现代药理研究结果表明,三宝木植物具有抗病毒[7]、抗肿瘤[8]、抗炎镇痛[9]、抗菌[10]和其他生物活性。近10年来,国内外从三宝木植物中分离出了100多个新二萜类化合物[5],绝大多数表现出显著的生物活性。异叶三宝木是海南岛的特有灌木,目前对这种三宝木的化学成分和药理活性研究较少,为进一步开发异叶三宝木的药用价值,明确其活性物质基础,本文对其化学成分及其抗菌活性进行系统研究。
1 材料和方法
1.1 材料和仪器
材料于2021年12月采自海南省五指山市,经海南大学刘平怀教授鉴定为异叶三宝木()的枝条,样品保存于海南大学化学工程与技术学院药食同源生化工程实验室。革兰氏阴性菌大肠杆菌() ATCC8739以及革兰氏阳性菌肺炎双球菌() ATCC8576均保存于海南大学化学工程与技术-40 ℃冰箱。
BSZ-100自动部分收集器(上海琪特仪器); Bruker Avance III 600型核磁共振波谱仪(德国布鲁克);紫外检测器(大连依利特); DAD1024二极管阵列检测器(大连依利特);色谱柱为SB-PHENYL (9.4 mm× 250 mm, 5m, Agilent);实验室超纯水机(上海和泰仪器); Waters UPLC-QTOF 液质联用仪(美国Waters公司); Sephadex LH-20凝胶(上海源叶);硅胶(青岛海洋化工);旋转蒸发仪(艾卡仪器);石油醚、二氯甲烷、乙酸乙酯、色谱甲醇等试剂(西陇科学)。
1.2 提取与分离
异叶三宝木枝条阴干,取干燥枝条5.0 kg以95%乙醇加热回流提取3次,减压浓缩得到乙醇浸膏145 g。浸膏用水混悬,依次石油醚、二氯甲烷、乙酸乙酯萃取,得到石油醚浸膏9.9 g,二氯甲烷12 g, 乙酸乙酯6.4 g。取石油醚段萃取物(9.9 g)进行硅胶柱层析洗脱[石油醚׃乙酸乙酯(1׃0~0׃1)], TLC合并共得到6个流分(E1~E6)。取流分E5 (2.4 g)用Sephadex LH-20凝胶,二氯甲烷׃甲醇=1׃1洗脱, TLC 合并得到5个流分(E5-1~E5-5),取流分E5-2 (23 mg)进行液相纯化,流动相为甲醇:0.1%甲酸水=80׃20, 分离得到高纯度化合物1 (2.1 mg)。取流分E6 (1.5 g)用Sephadex LH-20凝胶,二氯甲烷:甲醇=1:1洗脱,TLC合并得到6个流分(E6-1~E6-6),取流分E6-4 (18.4 mg)进行液相纯化,流动相为80%甲醇,分离得到高纯度化合物2 (1.6 mg)。取乙酸乙酯段萃取物12 g进行硅胶柱层析洗脱[二氯甲烷׃甲醇(1׃0~ 0׃1)],TLC合并共得到6个流分(F1~F6)。取流分F1 (3.2 g)进行硅胶柱洗脱,TLC合并得到6个流分(F1-1~F1-6),取流分F1-3 (1.2 g)用Sephadex LH-20凝胶,二氯甲烷׃甲醇=1׃1洗脱,TLC合并得到5个流分(F1-3-1~F1-3-5)。取流分F1-3-2进行液相纯化,液相条件为70%甲醇,分离得到高纯度化合物3 (1.2 mg),流分F1-3-4用70%甲醇HPLC纯化, 分离得到高纯度化合物6 (1.5 mg)。取流分F2 (2.6 g)进行凝胶柱层析分离,TLC合并得到5个流分F2-1~ F2-6,流分F2-4 (32 mg)用HPLC [甲醇:0.1%甲酸水=80׃20]洗脱,分离得到高纯度化合物4 (2.4 mg)和5 (1.8 mg)。化合物1~6化学结构如图1。
1.3 结构鉴定
化合物1 白色粉末;ESI-MS: 321 [M + Na]+,分子式C18H18O4。1H NMR (600 MHz, CDCl3):8.08 (1H, s, H-14), 7.79 (1H, s, H-11), 7.65 (1H, s, H-1), 6.89 (1H, s, H-6), 4.06 (6H, d,= 4.2 Hz, 2- OMe, 7-OMe), 2.56 (3H, s, H-16), 2.46 (3H, s, H-15);13C NMR (151 MHz, CDCl3):100.27 (C-1), 144.65 (C-2), 143.39 (C-3), 116.44 (C-4), 127.54 (C-5), 96.18 (C-6), 152.35 (C-7), 123.54 (C-8), 131.34 (C-9), 119.90 (C-10), 106.02 (C-11), 153.50 (C-12), 118.97 (C-13), 124.53 (C-14), 16.19 (C-15), 11.19 (C-16), 55.21 (2- OMe), 55.93 (7-OMe)。上述数据与文献[11]报道的基本一致,故鉴定为trigonochinene E。
化合物2 橙色固体;ESI-MS: 529 [M + Na]+,分子式C32H26O6。1H NMR (600 MHz, DMSO-6):10.57 (1H, s, 11-OH, 11′-OH), 7.93 (1H, s, H-13, 13′), 7.13 (1H, s, H-10, 10′), 6.77 (1H, s, H-5, 5′), 2.20 (3H, s, H-14, 14′), 1.43 (3H, s, H-15, 15′), 1.32 (3H, s, H-16, 16′);13C NMR (151 MHz, DMSO-6):133.19 (C-1, 1′), 204.33 (C-2, 2′), 45.39 (C-3, 3′), 160.00 (C- 4, 4′), 121.05 (C-5, 5′), 183.11 (C-6, 6′), 123.58 (C-7, 7′), 129.66 (C-8, 8′), 151.52 (C-9, 9′), 111.81 (C-10, 10′), 160.23 (C-11, 11′), 130.03 (C-12, 12′), 129.68 (C-13, 13′), 16.26 (C-14, 14′), 22.46 (C-15, 15′), 23.60 (C-16, 16′)。上述数据与文献[12]报道的基本一致, 故鉴定为neoboutomannin。
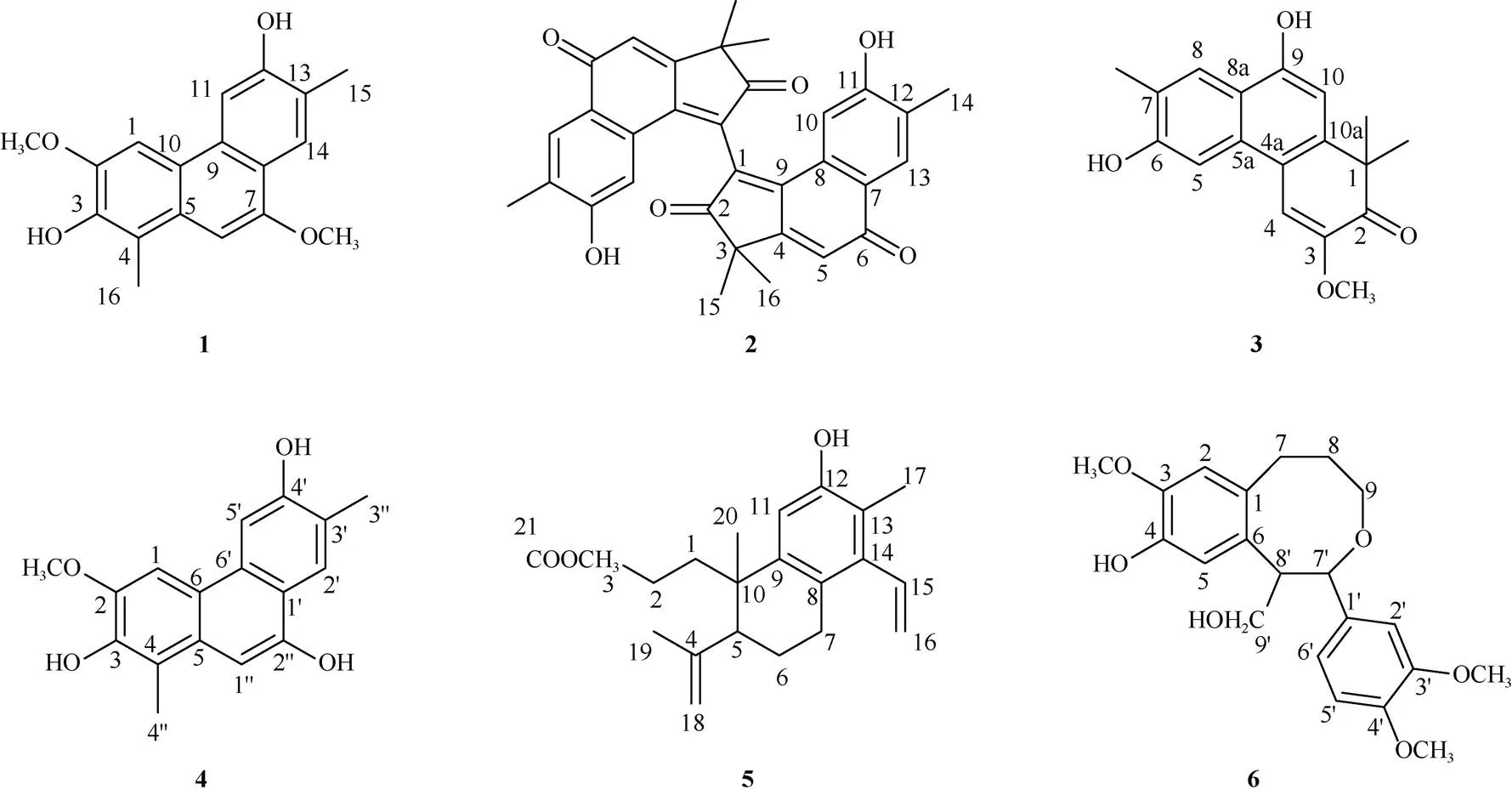
图1 化合物1~6的结构
化合物3 深黄色晶体;ESI-MS: 321 [M +Na]+,分子式C18H18O4。1H NMR (600 MHz, CD3OD):7.94 (1H, s, H-8), 7.45 (1H, s, H-5), 7.42 (1H, s, H-4), 6.75 (1H, s, H-10), 3.89 (3H, s, -OMe), 2.36 (3H, s, 7-Me), 1.47 (6H, s, 1-Me);13C NMR (151 MHz, MeOD):50.14 (C-1), 201.81 (C-2), 148.04 (C-3), 115.08 (C-4), 114.25 (C-4a), 104.47 (C-5), 133.43 (C-5a), 157.31 (C-6), 127.05 (C-7), 125.14 (C-8), 119.99 (C-8a), 155.45 (C-9), 105.06 (C-10), 144.61 (C-10a), 55.90 (3-OMe), 28.80 (1-Me), 16.85 (7-Me)。上述数据与文献[13]报道的基本一致,故鉴定为6,9--dedimethyltrigonostemone
化合物4 白色粉末;ESI-MS: 307 [M + Na]+,分子式C17H16O4。1H NMR (600 MHz, CD3OD):7.93 (1H, s, H-1), 7.70 (1H, s, H-5′), 7.67 (1H, s, H- 1″), 4.03 (3H, s, 2-OMe), 2.50 (3H, s, H-4′′), 2.36 (3H, s, H-3″);13C NMR (151 MHz, MeOD):96.66 (C-1), 144.86 (C-2), 144.39 (C-3), 127.90 (C-4), 118.16 (C- 5), 120.93 (C-6), 120.29 (C-1′), 124.93 (C-2′), 125.58 (C-3′), 156.29 (C-4′), 105.21 (C-5′), 106.34 (C-1″), 153.23 (C-2″), 16.78 (C-3″), 11.52 (C-4″), 55.52 (2- OMe)。上述数据与文献[14]报道的基本一致,故鉴定为stelltian B。
化合物5 淡黄色油状物;ESI-MS: 351 [M + Na]+,分子式C21H28O3。1H NMR (600 MHz, CD3OD):6.66 (1H, s, H-11), 6.62 (1H, dd,= 18.0, 12.0 Hz, H-15), 5.51 (1H, dd,= 12.0, 2.4 Hz, H-16), 5.12 (1H, dd,= 18.0, 2.4 Hz, H-16), 4.94 (1H, m, H-18), 4.71 (1H, d,= 1.2 Hz, H-18), 3.58 (3H, m, H- 21), 2.72 (1H, ddd,= 16.8, 4.8, 3.0 Hz, H-2, 7), 2.49 (1H, m, H-2, 7), 2.40 (1H, dd,= 12.0, 3.0 Hz, H-2, 7), 2.22 (1H, m, H-2, 7), 2.20 (3H, s, H-17), 1.98 (2H, m, H-1, 6), 1.85 (2H, m, H-1, 6), 1.79 (3H, m, H-19), 1.45 (1H, m, H-5), 1.20 (3H, m, H-20);13C NMR (151 MHz, MeOD):36.23 (C-1), 29.52 (C-2), 176.33 (C-3), 141.99 (C-4), 48.00 (C-5), 26.14 (C-6), 30.42 (C-7), 127.06 (C-8), 140.07 (C-9), 42.02 (C-10), 112.28 (C-11), 154.77 (C-12), 121.19 (C-13), 148.44 (C-14), 135.729 (C-15), 119.76 (C-16), 13.28 (C-17), 114.69 (C-18), 23.20 (C-19), 28.31 (C-20), 52.03 (C-21)。上述数据与文献[15]报道的基本一致,故鉴定为3,4- secosonderianol。
化合物6 无色油状;ESI-MS: 397 [M + Na]+,分子式C21H26O6。1H NMR (600 MHz, DMSO-6):6.94 (2H, d,= 9.0, 2.4 Hz, H-2′, 5′), 6.87 (1H, dd,= 9.0, 2.4 Hz, H-6′), 6.68 (2H, s, H-2, 5), 5.45 (1H, d,= 6.6 Hz, H-7′), 3.77 (2H, s, H-9), 3.75 (3H, d,= 4.8 Hz, H-9′, -OH), 3.73 (9H, d,= 2.4 Hz, 3-OMe, 3′-OMe, 4′-OMe,), 3.70 (1H, m, H-8′), 2.58 (2H, m, H-7), 1.69 (2H, m, H-8);13C NMR (151 MHz, DMSO-6):128.89 (C-1), 111.59 (C-2), 143.36 (C- 3), 145.47 (C-4), 109.63 (C-5), 134.12 (C-6), 34.78 (C- 7), 31.58 (C-8), 62.98 (C-9), 135.15 (C-1′), 112.36 (C- 2′), 148.71(C-3′), 148.44 (C-4′), 116.44 (C-5′), 118.05 (C-6′), 86.66 (C-7′), 53.45 (C-8′), 60.20 (C-9′), 55.65 (3-OMe), 55.53 (3′-OMe), 55.46 (4′-OMe)。上述数据与文献[16]报道的基本一致,故鉴定为biondinin A。
1.4 抗菌活性测试
采用牛津杯法检测化合物1~6的抑菌圈直径, 将活化好的大肠杆菌和肺炎双球菌接种于50 mL三角瓶中,160 r/min摇菌12 h,将两种菌用无菌生理盐水稀释,与0.5麦氏比浊管比色,配制浓度为5×105CFU/mL的试验菌液。吸取菌液100L涂布在平板上,待菌液吸收后将牛津杯放置于表面,在杯中加入100L 2 mg/mL的各待检样品,阳性对照为2 mg/mL硫酸卡那霉素,空白对照用DMSO溶液。
采用2倍稀释法[17],配制待测样品初始质量浓度为2 mg/mL,依次用营养肉汤稀释使其浓度减半,通过设置浓度梯度验证其对试验菌作用,其浓度梯度依次为:2、1、0.5、0.25、0.125、0.062 5、0.031 2、0.015 6、0.007 8 mg/mL。在96孔板的A1~A9行中,依次各加入20L被稀释成系列浓度的药液[18],在各孔内加入所制备菌接种物均为180L;第1至9孔的最终药物浓度均在加入时浓度的基础上稀释10倍,分别为200、100、50、25、12.5、6.25、3.12、1.56、0.78g/mL。阳性对照组为硫酸卡那霉素,营养肉汤设置为空白对照,37 ℃恒温培养箱培养数小时(大肠杆菌16~18 h,肺炎双球菌7~9 h)。MIC值由同一排孔中最后1个澄清的孔对应浓度和第1个浑浊的孔对应浓度取平均值,即MIC=(最后1个澄清的孔对应浓度+第1个浑浊的孔对应浓度)/2。
2 结果和讨论
2.1 异叶三宝木化学成分分析
从异叶三宝木的石油醚、二氯甲烷萃取部位分离得到6个化合物,包括5个二萜类(化合物1~5)和1个木脂素类(化合物6),分别鉴定为trigonochinene E (1)、neoboutomannin (2)、6,9--dedimethyltrigono- stemone (3)、stelltian B (4)、3,4-secosonderianol (5)和biondinin A (6)。化合物2、3、4、6为首次从该种植物中分离得到,化合物4为首次从该属植物中分离得到。
2.2 化合物对大肠杆菌生长抑制活性
牛津杯法检测化合物trigonochinene E (1)、neo- boutomannin (2)、6,9--dedimethyltrigonostemone (3)、3,4-secosonderianol (5)对大肠杆菌生长有抑制作用,抑菌圈直径和抑菌程度分别为12.2 (中敏感)、14.7 (中敏感)、13.7 (中敏感)和4.2 mm (低敏感),阳性对照硫酸卡那霉素为11.7 mm,中等敏感程度。微量肉汤稀释法测定的最小浓度分别为9.375、18.75、18.75、18.75g/mL, 阳性对照为18.75g/mL。
2.3 化合物对肺炎双球菌生长抑制活性
化合物trigonochinene E (1)、biondinin A (6)对肺炎双球菌生长有抑制作用,抑菌圈直径分别为9.2和4.2 mm,抑菌程度均为低敏感。阳性对照硫酸卡那霉素为12.2 mm,为中等敏感程度。微量肉汤稀释法测定的最小浓度分别为9.375和150.0g/mL, 阳性对照为1.170g/mL。
二萜类化合物具有广谱的抗菌活性,其抑菌机制是通过破坏菌体的细胞壁和细胞膜,影响其代谢途径,或与其细胞表面的蛋白结合,阻止营养吸收,从而抑制生长导致细菌死亡[19]。trigonochinene E (1)、3,4-secosonderianol (5)、neoboutomannin (2)等二萜物质对多种细菌和真菌具有抗菌作用。Trigono- chinene E (1)对幽门螺杆菌(SS1)、金黄色葡萄球菌(ATCC25923)、表皮葡萄球菌(ATCC12228)、藤黄微球菌(ATCC9341)、白色念珠菌(ACTT1600)、石膏小孢子菌()具有抑菌效果,抗金黄色葡萄球菌、表皮葡萄球菌作用强于阳性对照木兰醇,对石膏小孢子菌抑制效果强于阳性对照土荆皮乙酸[11]。3,4-secosonderianol (5)浓度为1g/50L带药滤纸片具有抗金黄色葡萄球菌活性,抑菌圈直径为13.8 mm[20]。Neoboutomannin (2)对金黄色葡萄球菌、变形杆菌()、粪肠球菌()、白色念珠菌、热带念珠菌()和近平滑念珠菌()有活性[12]。MIC值分别为3.12、25、3.12、6.25、1.56、1.56g/mL。本研究结果表明,从异叶三宝木分离的5种二萜物质中trigonochinene E (1)、neoboutomannin (2)、6,9-- dedimethyltrigonostemone (3)、3,4-secosonderianol (5)的抗菌效果较为优异,与前人[11]研究结果相符。
异叶三宝木是海南特有的热带植物,本研究结果进一步丰富了异叶三宝木中的化学成分及其抗菌活性药理研究,对于热带植物的开发与利用具有重要的意义。
[1] WU D L. Flora of Guangzhou, Tomus 5 [M]. Guangzhou: Guangdong Science and Technology Press, 2003: 379. [吴德邻. 广东植物志, 第5卷 [M]. 广州: 广东科技出版社, 2003: 379.]
[2] Delectis Florae Reipublicae Popularis Sinicae, Agendae Academiae Sinicae Editta. Florae Reipublicae Popularis Sinicae, Tomus 44(2) [M]. Beijing: Science Press, 1996:162–169. [中国科学院中国植物志编辑委员会. 中国植物志, 第44卷第2分册 [M]. 北京: 科学出版社, 1996: 162–169.]
[3] XU J B, YUE J M. Recent studies on the chemical constituents ofplants [J]. Org Chem Front, 2014, 1(10): 1225–1252. doi: 10.1039/c4qo00161c.
[4] CHEN H D, YANG S P, HE X F, et al. Trigochinins A-C: Three new daphnane-type diterpenes from[J]. Org Lett, 2010, 12(6): 1168–1171. doi: 10.1021/ol9028995.
[5] WANG B W, YU M, FENG J, et al. Study progress on chemical constituents and biological activities ofgenus [J]. China J Chin Mat Med, 2020, 45(19): 4589–4597. [王博闻, 郁萌, 冯剑, 等. 三宝木属植物化学成分及其药理活性研究进展 [J]. 中国中药杂志, 2020, 45(19): 4589–4597. doi: 10.19540/j.cnki.cjcmm.20200710.601.]
[6] WANG B W, ZUO A X, MA G X, et al. Chemical constituents of[J]. Chin Trad Herb Drugs, 2021, 52 (20): 6157–6162. [王博闻, 左遨勋, 马国需, 等. 剑叶三宝木的化学成分研究 [J]. 中草药, 2021, 52(20): 6157–6162. doi: 10.7501/j.issn. 0253-2670.2021.20.004.]
[7] ZHANG L, LUO R H, WANG F, et al. Daphnane diterpenoids isolated fromas HIV-1 antivirals [J]. Phytochemi- stry, 2010, 71(16): 1879–1883. doi: 10.1016/j.phytochem.2010.08.008.
[8] YANG C. Study on antitumor active constituents inMerr. et Chun [D]. Yangzhou: Yangzhou University, 2022. [杨超. 长序三宝木中抗肿瘤活性成分的研究 [D]. 扬州: 扬州大学, 2022. doi: 10.27441/d.cnki.gyzdu.2022.001965.]
[9] XU J, PENG M Q, SUN X C, et al. Bioactive diterpenoids from: Structures, NO inhibitory activities, and interactions with iNOS [J]. Bioorg Med Chem Lett, 2016, 26(19): 4785–4789. doi: 10.1016/j.bmcl.2016.08.026.
[10] TANG G H, HE H P, GU Y C, et al. 3,4-secoditerpenoids from[J]. Tetrahedron, 2012, 68(47): 9679–9684. doi:10.1016/j.tet.2012.09.052.
[11] YIN S, SU Z S, ZHOU Z W, et al. Antimicrobial diterpenes from[J]. J Nat Prod, 2008, 71(8): 1414–1417. doi: 10.1021/np800256x.
[12] TENE M, TANE P, DE DIEU TAMOKOU J, et al. Degraded diter- penoids from the stem bark of[J]. Phytochem Lett, 2008, 1(2): 120–124. doi: 10.1016/j.phytol.2008.06.003.
[13] LI S F, HE H P, HAO X J. Three new phenanthrenone constituents from[J]. Nat Prod Res, 2015, 29(19): 1845–1849. doi: 10.1080/14786419.2015.1009066.
[14] YAO C H, SHA X S, SONG H L, et al. Two new compounds from the aerial parts ofand their cytotoxic activity [J]. Phytochem Lett, 2021, 42: 134–137. doi: 10.1016/j.phytol.2020.09.009.
[15] CRAVEIRO A A, SILVEIRA E R. Two cleistanthane type diterpenes from[J]. Phytochemistry, 1982, 21(10): 2571– 2574. doi: 10.1016/0031-9422(82)85259-X.
[16] MA Y L, HAN G Q. A novel neolignan, biondinin A, fromPamp [J]. Chin Chem Lett, 1992(2): 121–122.
[17] JIANG N, LIU X P, TENG J X, et al. Inhibitory effects ofRehd. et Wils. leaf extract againston potato and its control efficacy on potato bacteria wilt [J]. Plant Prot, 2008, 34(2): 58–60. [姜宁, 刘晓鹏, 滕建勋, 等. 紫油厚朴叶提取物对马铃薯青枯病菌的抑制作用及防病效果 [J]. 植物保护, 2008, 34(2): 58–60. doi: 10.3969/j.issn.0529-1542.2008.02.015.]
[18] ZHONG C C, ZHAO J T, FAN Y, et al. Research progress on ultrasonic extraction of total flavonoids fromL. and its anti- bacterial activity [J].J Harbin Univ Commerc (Nat Sci), 2019, 35(6): 651–653. [钟楚楚, 赵晋彤, 范宇, 等. 超声提取夏枯草总黄酮及抑菌活性研究 [J]. 哈尔滨商业大学学报(自然科学版), 2019, 35(6): 651–653. doi: 10.3969/j.issn.1672-0946.2019.06.003.]
[19] WEI C L, CUI P W, XIAO J, et al. Research progress of natural diterpenoids with antibacterial activity [J]. Chin Trad Patent Med, 2022, 44(7): 2240–2249. [韦春玲, 崔培梧, 肖瑾, 等. 具有抗菌活性的天然二萜类化合物研究进展 [J]. 中成药, 2022, 44(7): 2240–2249. doi: 10.3969/j.issn.1001-1528.2022.07.030.]
[20] GU H G. Isolation, identification and bioactive secondary metabolites of the endophytic fungi from[D]. Aral: Tarim University, 2013. [古海刚. 角果木内生真菌分离、鉴定及其生物活性次生代谢产物研究 [D]. 阿拉尔: 塔里木大学, 2013.
Chemical Constituents and Antibacterial Activities of
Cen Xiangni, Fan Yiying, Liu Haowen, Li Jiayin, Wang Chuanlin, Liu Pinghuai*
(School of Chemical Engineering and Technology, Hainan University,Haikou 570228, China)
To understand the chemical constituents and antibacterial activities of, six compounds, including five diterpenoids and one lignan, were isolated and purified by silica gel column chromate- graphy, gel column chromatography and high performance liquid chromatography. Based on spectroscopic data, their structures were identified as trigonochinene E (1), neoboutomannin (2), 6,9--dedimethyl trigonostemone (3), stelltian B (4), 3,4-secosonderianol (5), biondinin A (6). The inhibitory activity and MIC values of compounds against a Gram-negative bacterium,, and a Gram-positive bacterium,, were detected by Oxford Cup method and double dilution method. Compounds 1, 2, 3 and 5 had inhibitory effects onwith MIC values of 9.375, 18.75, 18.75 and 18.75g/mL, respectively. Compounds 2, 3, 4, and 6 were isolated fromfor the first time, and compound 4 was isolated fromgenus for the first time. Except compound 4, all the other compounds had certain antibacterial activity, and compounds 1, 2 and 3 had stronger inhibitory effect onthan Kanamycin sulfate positive control.
; Diterpenoids;;
10.11926/jtsb.4753
2022-11-22
2023-01-10
海南省重点研发计划项目(ZDYF2020169)资助
This work was supported by the Key Research & Development Program in Hainan (Grant No. ZDYF2020169).
岑祥妮(1997年生),女,硕士研究生,研究方向为天然产物研究与开发。E-mail: cenxiangni@163.com
通讯作者 Corresponding author.E-mail: twlph@163.com

