多模式血液管理措施下血友病关节炎与股骨头坏死初次全髋关节置换术围术期失血风险比较:回顾性队列研究
陈 波,徐溢明,彭慧明,冯 宾,刘冠墨,王雪晴,翁习生
1海口市人民医院 中南大学湘雅医学院附属海口医院骨科,海口 570208 2上海市第六人民医院 海口骨科与糖尿病医院骨科,海口 570728 3中国医学科学院北京协和医院骨科,北京 100730
全髋关节置换术(total hip arthroplasty,THA)可减轻患者疼痛、提高生活质量,是治疗终末期髋关节疾病的有效措施,该方法技术成熟、医疗费用经济,被誉为“世纪手术”,但围术期失血问题不容忽视[1]。文献显示,THA围术期总失血量可达1510 mL,其中隐性失血量471 mL[2-3]。Carling等[4]研究发现,18%的THA患者围术期需接受异体输血治疗。血友病患者由于凝血因子减少或缺乏导致凝血功能异常,血友病骨关节炎(hemophilia arthritis,HA)患者THA围术期失血风险明显增加[5],既往曾被视为骨科大手术的相对禁忌人群。近年来随着血液管理措施的优化,该状况才得以改善[6]。回顾性研究表明,HA患者接受THA治疗后中远期预后令人鼓舞,关节功能得到明显改善且假体存活率高[7-8]。本研究团队既往比较了HA患者与单纯骨关节炎患者全膝关节置换术(total knee arthroplasty,TKA)围术期失血风险,发现前者出血量增多[9],随后本中心进一步优化血液管理,实行多模式血液管理措施[10]。在此背景下,相较于非血友病患者,HA患者THA围术期失血及异体输血风险是否增加尚无报道。本研究针对上述问题进行了探究,以期为临床优化血液管理提供借鉴。
1 资料与方法
1.1 研究对象
本研究为回顾性队列研究,研究对象为2010年1月—2022年6月于北京协和医院接受单侧THA治疗的HA患者(HA-THA组)及按性别进行1∶3匹配的股骨头坏死(osteonecrosis of the femoral head,ONFH)患者(ONFH-THA组)。HA-THA组纳入标准:确诊为HA,并接受初次单侧THA术(全身麻醉,采用后外侧入路,使用生物型固定假体,假体摩擦界面均为陶瓷-陶瓷)。排除标准:(1)同期行其他类型/部位的骨科手术;(2)未采用多模式血液管理措施;(3)研究相关临床资料不完整者。
ONFH-THA组纳入标准:(1)ONFH诊断明确,并接受初次单侧THA,术式同HA-THA组;(2)入院时间与HA患者相近,主刀医师与HA患者相同,并按照性别与HA患者进行1∶3匹配。排除标准:同HA-THA组。
本研究已通过北京协和医院伦理审查委员会审批(审批号:S-K921),并豁免患者知情同意。
1.2 研究方法
1.2.1 多模式血液管理措施
ONFH-THA组:(1)使用氨甲环酸[11-13]:切皮前5~10 min予1 g氨甲环酸静脉滴注,关闭切口前予1~2 g氨甲环酸局部应用。(2)若无禁忌,术中采取控制性降压措施,将平均动脉压控制在基础值的70%。(3)使用促红细胞生成素:术后第1天开始皮下注射促红细胞生成素 10 000 IU/d(联合静脉输入蔗糖铁100~200 mg/d),连续3 d。若术前合并贫血,术前即开始使用。(4)术后异体输血:依据《临床输血技术规范》[14]及临床实践,血红蛋白(hemoglobin,Hb)>100 g/L时可不进行输血;Hb<80 g/L时进行输血;Hb处于80~100 g/L时,结合患者年龄、贫血程度、心肺代偿功能、代谢情况综合考虑是否输血。
HA-THA组:围术期不予以药物预防性抗凝[12],而采用机械预防,余血液管理措施同ONFH-THA组。此外,HA-THA组患者予以凝血因子替代治疗[15]:(1)甲型血友病患者首选基因重组FⅧ制剂,所需剂量(U)=体质量(kg)×(所需达到的血浆 FⅧ:C 水平%-实际测量的血浆FⅧ:C 水平%)÷2。由于 FⅧ的半衰期为 8~12 h,首次输注后应每 8~12小时再次输注首剂量的50%,以维持FⅧ:C 水平,防止出血等并发症产生。术后继续输注凝血因子,将术后1~3 d、4~6 d、 7~14 d FⅧ:C分别保持在所需浓度的>80%、40%~80%、30%~60%。(2)乙型血友病患者采用活化凝血酶原复合物(activated prothrombin complex concentrates,APCC)进行替代治疗。
1.2.2 术后处理
两组患者术后均加压包扎伤口,保持患肢外展中立位,术后给予抗生素预防性治疗1 d;均鼓励早期进行主动踝泵和直腿抬高练习,复查髋关节正侧位X线确认假体位置及大小,合适后可完全负重下床活动。HA-THA组患者视情况可放置引流管,并于术后24 h内拔除。ONFH-THA组不放置引流管,常规进行静脉血栓栓塞症预防性治疗。
1.2.3 观察指标
根据电子病历系统收集患者年龄、体质量指数、手术部位(左/右侧)、术前美国麻醉医师协会(American Society of Anesthesiologists,ASA)分级、术前凝血功能、术后引流量、手术时间、住院时间等基本资料。(1)主要结局指标:围术期失血情况。包括术前与术后红细胞压积(hematocrit,Hct)水平及其变化、总失血量、隐性失血量、异体输血与大出血患者的比例。其中总失血量根据手术前后Hb、Hct进行计算[16],隐性出血量为总失血量-显性失血量(术中失血量+术后引流量)。大出血定义为24 h内Hb下降≥20 g/L或输入异体红细胞2 U及以上[17]。(2)次要结局指标:术后并发症发生情况(截至术后6个月)。
1.3 样本量估算
根据文献报道,一般人群行初次THA术的异体输血率为22.2%[2-3],假设HA患者异体输血率的相对危险度为2,ONFH-THA组与HA-THA组样本比例为1∶3,在检验水准α为0.05、检验效能(1-β)为80%的条件下,经计算HA-THA组与ONFH-THA组分别所需病例为39例、117例。
1.4 统计学处理
采用SPSS 26.0软件进行统计学分析。年龄、隐性失血量、总失血量等正态分布计量资料以均数±标准差表示,组间比较采用t检验;手术时间、住院时间等非正态分布计量资料以中位数(四分位数)表示,组间比较采用Mann-WhitneyU检验。异体输血率、大出血率等计数资料以频数(百分数)表示,组间比较采用卡方检验或Fisher确切概率法。双侧检验,以P<0.05为差异具有统计学意义。
2 结果
2.1 一般临床资料
共入选符合纳入与排除标准的HA-THA患者26例,ONFH-THA患者76例(受病例数限制未严格按照1∶3的比例)。两组均为男性患者,术前ASA分级均为Ⅱ级。HA-THA患者中,甲型血友病25例,乙型血友病1例;术后留置引流管9例,均于术后24 h内拔除。
与ONFH-THA组比较,HA-THA组年龄更低,术前活化部分凝血活酶时间更高,手术时间与住院时间均更长(P均<0.05),见表1。
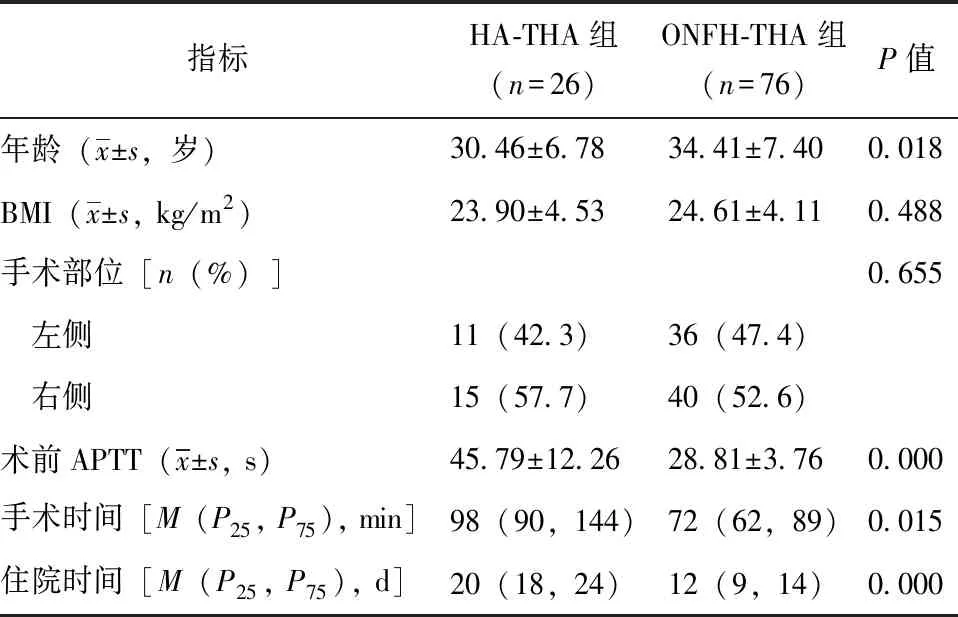
表1 HA-THA组与ONFH-THA组一般资料比较
2.2 两组失血相关指标比较
相较于ONFH-THA组,HA-THA组术后第3天Hb、Hct水平更低,术后Hb与Hct下降量、大出血率更高,总失血量更多(P均<0.05),见表2。
HA-THA组、ONFH-THA组输注浓缩红细胞总量分别为14 U、12 U。HA-THA组25例甲型血友病患者平均消耗FⅧ因子13021.2 U(范围:8100~19 210 U),1例乙型血友病患者消耗APCC 17 600 U。相较于ONFH-THA组,HA-THA组异体输血率更高(P<0.05),见表2。
2.3 两组并发症比较
HA-THA组血肿形成3例、下肢静脉血栓形成1例、伤口愈合不良3例、术中股骨距骨折1例、短暂性神经麻痹1例;ONFH-THA组下肢静脉血栓形成2例、伤口愈合不良2例、泌尿系统感染2例。给予冷敷、抗凝、骨折处固定、伤口引流、抗感染治疗等针对性干预后均恢复正常。HA-THA组并发症发生率显著高于ONFH-THA组(34.62% 比7.89%,P=0.000)。
3 讨论
本研究基于回顾性队列研究,探究了行单侧THA治疗的HA患者围术期失血风险,结果显示相较于ONFH-THA组,HA-THA组总失血量更多[(1927.08±956.59)mL比(1475.88±924.43)mL],大出血率(38.46%比14.47%)、异体输血率(15.38% 比3.95%)以及并发症发生率(34.62% 比7.89%)均更高,提示HA患者行THA治疗时失血风险仍较高,需进一步优化血液管理措施。
3.1 HA增加THA围术期失血风险
HA患者接受THA治疗的报道最早见于1967年,研究者多采用冷冻血浆应对围术期出血风险,由于此类患者较少见,相关病例多为个案报道[18-19]。Kleiboer等[20]研究表明,HA患者行单侧THA治疗时异体输血风险是TKA的1.76倍(95% CI:1.68~1.83),进一步明确了THA治疗时的失血风险。本研究团队既往报道了14例接受THA并予以凝血因子替代治疗HA患者的失血情况,结果显示总失血量、显性失血量和隐性失血量均值分别为3543 mL、1435 mL和2110 mL,但该研究纳入了进行一期多关节置换的病例,未对单侧THA是否增加输血风险进行分析[21]。近年来,多位研究者针对HA患者THA围术期失血风险是否较非HA患者增高的问题进行了探究。2016年Kapadia等[22]报告了332例血友病患者及按1∶3比例匹配的996例非血友病患者行关节置换术(包括THA和TKA)时的输血情况,结果显示血友病患者输血率高于对照人群(15.06%比9.84%,P=0.012);经多元回归分析校正混杂因素后,血友病患者接受任何类型输血、异体输血、自体输血的风险均增高,但该研究并未对THA和TKA加以区分。2019年Wang等[23]收集了中国台湾地区2000—2015年121例血友病患者和194 026例非血友病患者的临床资料,经倾向评分匹配和多元回归分析后显示,HA患者THA术后输血风险显著升高(HR=5.262,95% CI:3.0442~ 6.565,P<0.001),该结论在Gillinov等[24]的研究中得到了进一步验证,即血友病患者THA术后90 d内异体输血的风险较非血友病患者增加。但上述研究未报道多模式血液管理方案的应用情况。
为进一步降低HA患者行THA治疗期间出血风险,北京协和医院制定了多模式血液管理措施,包括术前红细胞动员(使用促红细胞生成素)[10],围术期使用氨甲环酸[11],术中控制性降低血压,术后使用促红细胞生成素等,并提倡HA患者THA围术期不常规使用药物进行预防性抗凝[12],旨在通过多种优化措施,合力减少围术期出血,保障HA患者手术安全。本研究基于26例HA患者及与之相匹配的76例ONFH患者诊疗数据,首次对在多模式血液管理措施下HA患者THA围术期失血风险进行了评估,结果显示相较于ONFH-THA组,HA-THA组总失血量、大出血率、异体输血率均增高,提示在血液管理策略优化的情况下,HA患者THA围术期失血量仍较多,笔者认为主要与以下原因相关:(1)凝血功能障碍:尽管HA患者均予以成熟且有效的凝血因子替代治疗,但其凝血功能仍无法达到正常水平,以致出血风险增加;(2)HA-THA组髋关节病变更为严重,创伤更大、手术时间更长,以致出血量更多;(3)虽然放置引流管是否增加THA围术期失血风险尚存争议[25],但笔者认为该措施可能在一定程度上增加了HA-THA组失血量,其原因包括两方面:①引流液本身即包含血液成分;②引流可减少血肿形成,以致局部压力减小、失血量增加。
3.2 HA增加THA围术期并发症
HA患者THA围术期并发症主要包括出血相关并发症(血肿形成)以及非出血相关并发症(如静脉血栓形成、感染等)。Nelson等[10]针对39例血友病患者的研究显示,THA围术期血肿形成率为7.6%。倾向性评分结果显示,与非血友病患者比较,血友病患者THA术后发生严重不良事件、轻微不良事件、深静脉血栓形成与肺栓塞、急性肾损伤的风险均增加,假体5年存活率降低(91.9%比95.3%,P=0.009)[24]。但亦有研究者持不同观点。本研究团队针对2002—2012年21例血友病患者进行了长期随访(包含行一期多关节置换术的病例),患者出院时均无假体松动、感染或其他并发症发生,术后随访113个月(范围:5~15年),假体存活率为100%,均未进行翻修手术[8]。大样本研究表明,相较于非血友病患者,血友病患者行THA治疗1年后感染率未显著增高(8.11%比3.38%,P=0.206),且两组30 d与90 d并发症发生率、1年感染率、再次手术率及死亡率均无显著差异[23]。本研究HA-THA组围术期血肿形成率为11.54%,较文献结果稍高[10],总体并发症发生率显著高于ONFH-THA组(34.62% 比7.89%),可能与本研究HA病例病情复杂、术后未常规抗凝治疗有关。
本研究局限性:研究对象均为男性,且均为后外侧入路手术。有研究显示相比传统后外侧入路,直接前入路可降低THA术后出血风险[26],故结果外推需谨慎,尚需开展多中心大样本前瞻性研究进一步评估HA患者THA围术期失血风险。
综上,虽然临床可通过规范的凝血因子替代治疗方案及多模式血液管理措施降低HA患者THA围术期失血风险,但相较于ONFH患者,其失血及异体输血风险仍较高。临床需进一步优化血液管理策略,保障此类人群围术期安全。
作者贡献:彭慧明负责研究设计,数据统计分析及论文撰写;陈波负责研究设计,数据收集及整理;徐溢明负责数据统计分析;冯宾、刘冠墨、王雪晴参与数据收集;翁习生负责研究设计及论文修订;所有作者均对论文进行了审阅。
利益冲突:所有作者均声明不存在利益冲突
志谢:感谢赵丽娟老师提供了原始资料及其在资料检索方面提供的帮助

