基于质量源于设计理念优化黄柏提取工艺
陈希宇,张庆明,张兴德,3,5*,谢 辉,刘永海,狄留庆,5,郁红礼,3,4
(1.南京中医药大学 药学院,江苏 南京 210023 ;2 东部战区总医院 药剂科,江苏 南京 210002;3.江苏省中药炮制重点实验室,江苏 南京 210023 ;4.江苏省经典名方工程研究中心,江苏 南京210023 ;5.江苏省中药高效给药系统工程技术研究中心,江苏 南京 210023)
黄柏为芸香科植物黄皮树Phellodendron chinenseSchneid.干燥树皮,习称“川黄柏”,其性寒,味苦,归肾、膀胱经,具有清热燥湿、解毒疗疮功效[1]。研究报道,黄柏具有抗炎、抗菌、抗氧化、心血管保护和免疫调节等多种药理作用[2-4],在临床上应用甚广。黄柏含有多种化学成分,包括生物碱类、黄酮类、酚酸类以及挥发油等,而生物碱类含量约占2.1% ~8.3%,是黄柏的主要活性成分。2020 年版《中国药典》(一部)收录含黄柏的64 种成方制剂,多为单一检测指标,不能很好地保证含黄柏制剂的质量及有效性。如今黄柏提取大多采用水提或醇提,2021 年印发的《中药配方颗粒质量控制与标准制定技术要求》[5]中黄柏配方颗粒的提取工艺为加水煎煮,滤过;在标准汤剂的制备中是加水浸泡,回流提取两次[6];在复方制剂如复方黄柏液涂剂中则为加水煎煮三次[1]。可见目前中药提取多凭借经验,工艺要求并不明确,不能达到良好的控制效果,需要将经验控制向基于模型控制的方向转变。
近十年来,“质量源于设计”(QbD)这一概念被普遍作用于中医药领域和制药空间。此理念强调借助控制所用原材料的质量和生产产品的具体过程质量,使药品质量稳定可靠。设计空间法已被证明为可以保证实际提取工艺过程中的动态性,其通过深入理解生产制造过程中工艺参数的相互作用从而保持质量均一。有助于结合产品质量属性控制目标成分,不仅可以在误差方面减少损失,还可以提高工艺参数和产品质量之间的关联性[7-8]。此前已有研究分别采用指标叠加法和Monte Carlo 法[9-10]求得中药生产工艺的设计空间。本研究基于QbD 理念筛选出关键工艺参数(CPPs)和关键质量属性(CQA),并建立黄柏提取关键工艺参数与质量属性的定量数学模型,采用两种设计空间法方法优化工艺,保证药品质量的同时为相关制剂进一步开发提供依据。
1 仪器与材料
1.1 药物与试剂
黄柏(批号:201101,四川启隆中药饮片有限公司;批号:210714,南京海源中药饮片有限公司)均经南京中医药大学陈建伟教授鉴定为黄皮树Phellodendron chinenseSchneid.的干燥树皮;盐酸小檗碱对照品(批号:MUST-20073011,纯度:98.96%)、盐酸黄柏碱对照品(批号:MUST-20072610,纯度:99.16%)、绿原酸对照品(批号:MUST-21070910,纯度:99.40%),均购自成都曼思特生物科技有限公司;甲醇、乙腈、磷酸(色谱纯,MORCK 公司);蒸馏水(广州屈臣氏食品饮料有限公司)。
1.2 主要仪器
岛津AUW120D 型分析天平(日本岛津有限公司);CAV64C 型电子分析天平(海奥豪斯有限公司);KQ-500B 型超声清洗机(昆山市超声仪器有限公司);Waters 2695 型高效液相色谱仪、2998 型DAD 检测器、自动进样器(美国 Waters 公司);ZNHW 型恒温电热套(上海力辰科技有限公司);FW100 型高速粉碎机 (天津市泰斯特仪器有限公司)。
2 方法与结果
2.1 黄柏提取液的制备
取黄柏饮片10 g,精密称定,转移至圆底烧瓶中,加入适量水,按照提取对应参数进行加热回流,滤过后减压浓缩至100 mL 容量瓶中定容,即得。
2.2 小檗碱、黄柏碱、绿原酸的含量测定
2.2.1 对照品溶液制备 取盐酸小檗碱、盐酸黄柏碱、绿原酸对照品适量,精密称定,加甲醇溶液制成含盐酸小檗碱95.5μg/mL、盐酸黄柏碱45.7μg/mL、绿原酸12.8μg/mL 的混合对照品溶液。
2.2.2 供试品溶液制备 取“2.1”项下黄柏提取液,经0.45 μm 微孔滤膜滤过,作为供试品溶液。
2.2.3 色谱条件 Hedera ODS-2 柱 (4.6 mm×250 mm,5μm);流动相为乙腈(A)-0.2%磷酸水溶液(B),梯度洗脱70 min,洗脱程序见表1,流速为1.0 mL/min;检测波长为230 nm;柱温为25℃ ;进样量为10μL;其中,理论塔板数以各成分计不低于5 000,分离度大于1.5,阴性无干扰,色谱图见图1。
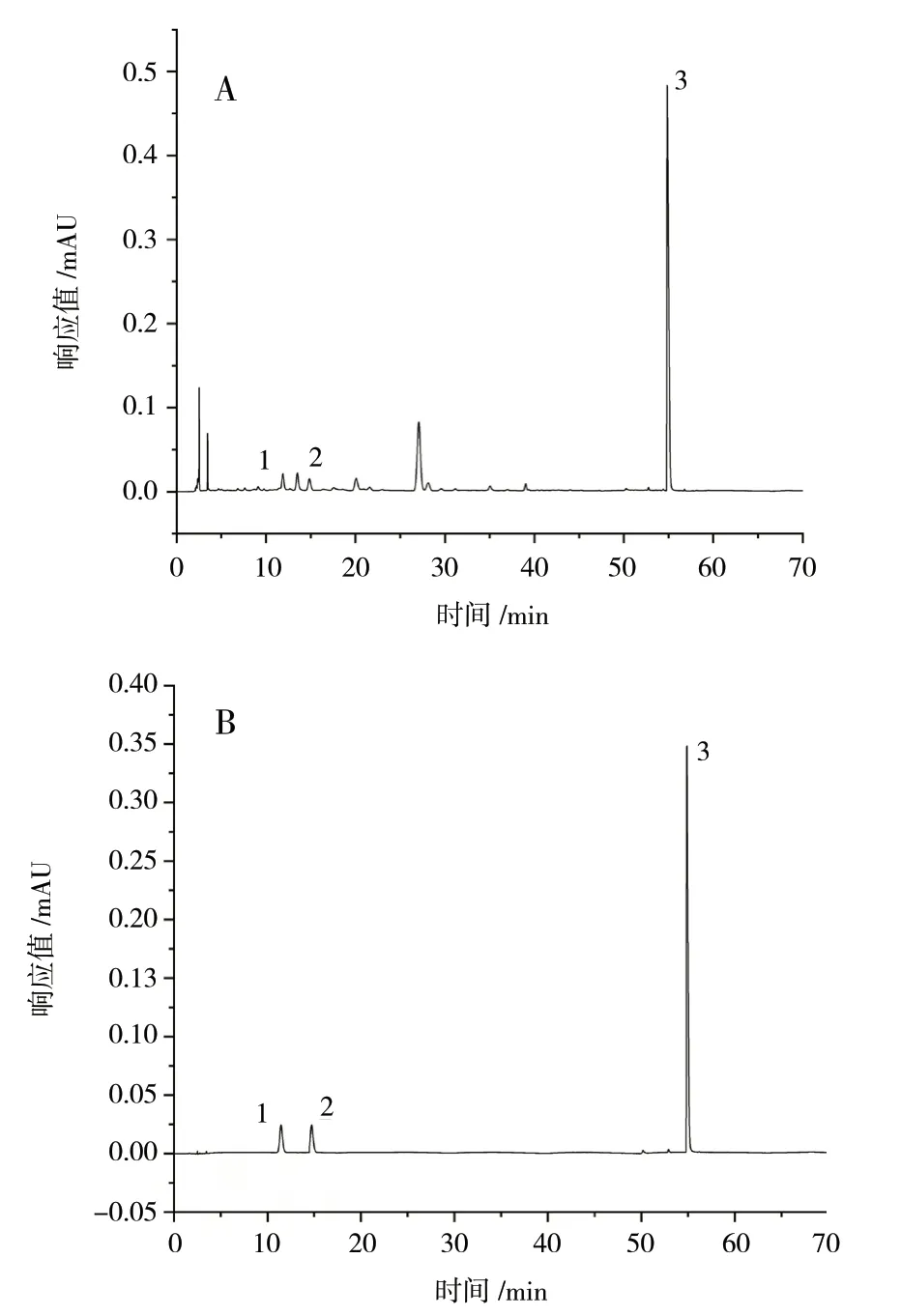
图1 供试品溶液(A)和混合对照品溶液(B)的HPLC 图Fig.1 HPLC chromatogram of test substance and mixed control

表1 梯度洗脱程序Tab.1 Gradient elution
2.2.4 专属性试验 精密移取“2.2.1”项下混合对照品溶液和“2.2.2”项下供试品溶液各10μL,按“2.2.3”项下条件进行含量测定,结果表明供试品色谱峰与对照品色谱峰的保留时间一致对应,色谱图见图1。
2.2.5 线性关系考察 取“2.2.1”项下混合对照品溶液,用甲醇稀释成不同质量浓度的一系列混合对照品溶液,按“2.2.3”项下色谱条件进行测定,以对照品质量浓度(X,μg/mL)为横坐标,峰面积(Y)为纵坐标,得线性回归方程,结果见表2。

表2 线性回归方程Tab.2 Linear regression equations
2.2.6 精密度试验 精密移取“2.2.1”项下对照品溶液10μL,按“2.2.3”项下色谱条件,连续进样测定6 次,记录峰面积,计算绿原酸、盐酸黄柏碱、盐酸小檗碱的峰面积的 RSD 分别为1.29%、2.22%、0.66%,结果表明仪器精密度良好。
2.2.7 稳定性试验 精密称取“2.1”项下黄柏饮片适量,按“2.2.2”项下方法制备供试品溶液,分别在 0、2、4、8、12、16、20、24 h 后分别进样10μL,按“2.2.3”项下色谱条件进样测定,记录峰面积。结果表明,绿原酸、盐酸黄柏碱、盐酸小檗碱峰面积的RSD 分别为1.98%、3.87%、1.16%,表明供试品溶液在室温下放置24 h 基本稳定。
2.2.8 重复性试验 精密称取“2.1”项下黄柏饮片6 份,按“2.2.2”项下方法制备供试品溶液,“2.2.3”项下色谱条件进样测定,记录绿原酸、盐酸黄柏碱、盐酸小檗碱峰面积并计算其含量。计算得绿原酸、盐酸黄柏碱、盐酸小檗碱含量RSD 分别为2.36%、2.99%、1.19%,表明该方法重复性良好。
2.2.9 加样回收率试验 精密称取已测定绿原酸、盐酸黄柏碱、盐酸小檗碱含量的黄柏饮片6 份,分别添加饮片中等量的混合对照品溶液,按“2.2.2”项下方法制备供试品溶液,按“2.2.3”项下色谱条件进样测定,记录峰面积。计算得绿原酸、盐酸黄柏碱、盐酸小檗碱的平均回收率分别为96.94%、97.26%、99.55%,RSD 分别为 2.86%、1.08%、1.06%。
2.2.10 样品测定 取“2.2.2”项下制备的供试品溶液按“2.2.3”项下色谱条件进行测定。
2.3 提取率的测定
按“2.2”项下方法分别测定提取液小檗碱、黄柏碱、绿原酸的提取率,提取率= [(提取液中有效成分浓度×提取液体积)/加入药材质量]×100%。
2.4 干膏率测定
精密量取实验所得黄柏提取液50 mL,置于已恒重的蒸发皿中,水浴蒸干,于105 ℃烘箱中干燥3 h,置干燥器中冷却至室温后,称定记录质量并计算干膏率。干膏率=mV/50M,式中,m为每50 mL 提取液的干膏质量(mg);V为总提取液体积(mL);M为饮片质量(mg)。
2.5 CQA 和CPPs 的确定
2020 年版《中国药典》(一部)收录含黄柏的64种成方制剂,除去丸剂、散剂、膏剂等无需提取的制剂且未明确质量评价指标成分的成方制剂外,剩余31 种成方制剂。通过对以盐酸小檗碱和黄柏碱为检测成分的8 种黄柏提取工序进行分类,发现仅以盐酸小檗碱为检测指标占总成方制剂的26%;提取工艺中62%为水煎煮提取,平均时间为1 ~ 2 h。因此选取水提工艺并且考虑包括盐酸小檗碱的多成分检测。根据前期研究经验及文献分析将小檗碱提取率(Y1)、黄柏碱提取率(Y2)、绿原酸提取率(Y3)以及干膏率 (Y4)作为CQA。对黄柏提取过程中所涉及的设备、工艺参数、管理程序和饮片因素采用鱼骨图分析,从而确定影响提取工艺的可能关键工艺参数并进行初步评价,结果见图2。
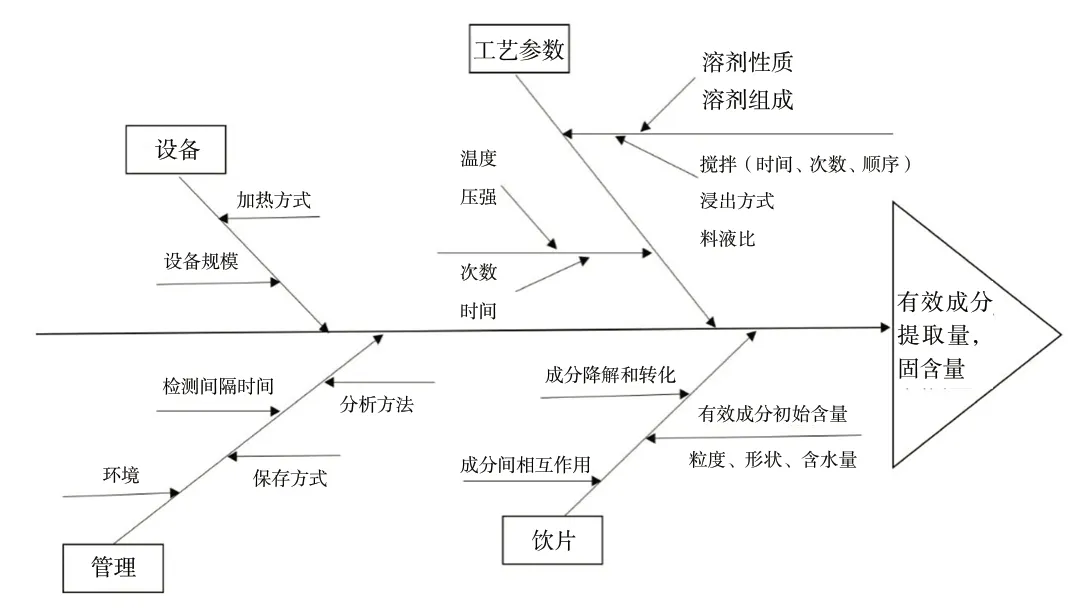
图2 提取工艺鱼骨图Fig.2 Fishbone diagram of the extraction process
利用 Minitab 17 软件对提取温度(X1)、提取时间(X2)、提取次数(X3)、浸泡时间(X4)、加水倍量(X5)、饮片批次(X6)进行 Plackett-Burman 实验设计,Plackett-Burman 实验设计与结果见表3。

表3 Plackett-Burman 实验条件及结果Tab.3 Plackett-Burman experimental design and results
分别以Y1~Y4对X1~X6进行线性回归,得回归方程Y1= -1.57 + 0.045 37X1+ 0.0212 8X2-0.399X3+ 0.005 17X4+0.003 1X5- 0.167X6;Y2= 0.027 5 + 0.001 784X1+0.001 174X2- 0.013 6X3+ 0.000 277X4- 0.010 90X5-0.009 4X6;Y3= -0.162 + 0.003 823X1+ 0.001 671X2-0.034 2X3- 0.000 584X4+ 0.005 33X5+ 0.001 1X6;Y4=-14.07 + 0.174 5X1+ 0.087 2X2+ 4.14X3+ 0.026 4X4+0.038X5+ 0.98X6。
方差分析见表4,可知模型总体P值均小于0.05,即Y1~Y4对X1~X6显著。由图3 标准化效应所得Pareto 图可知参数为X1、X2、X3时可影响较多效应值。因此根据方差分析和Pareto 图可筛选出提取温度(X1)、提取时间(X2)、提取次数(X3)作为本研究中的关键工艺参数(CPPs)进行后续实验。

图3 Pareto 图(响应为综合评分,α= 0.055)Fig.3 Pareto diagram (response value is a comprehensive score, α= 0.055)
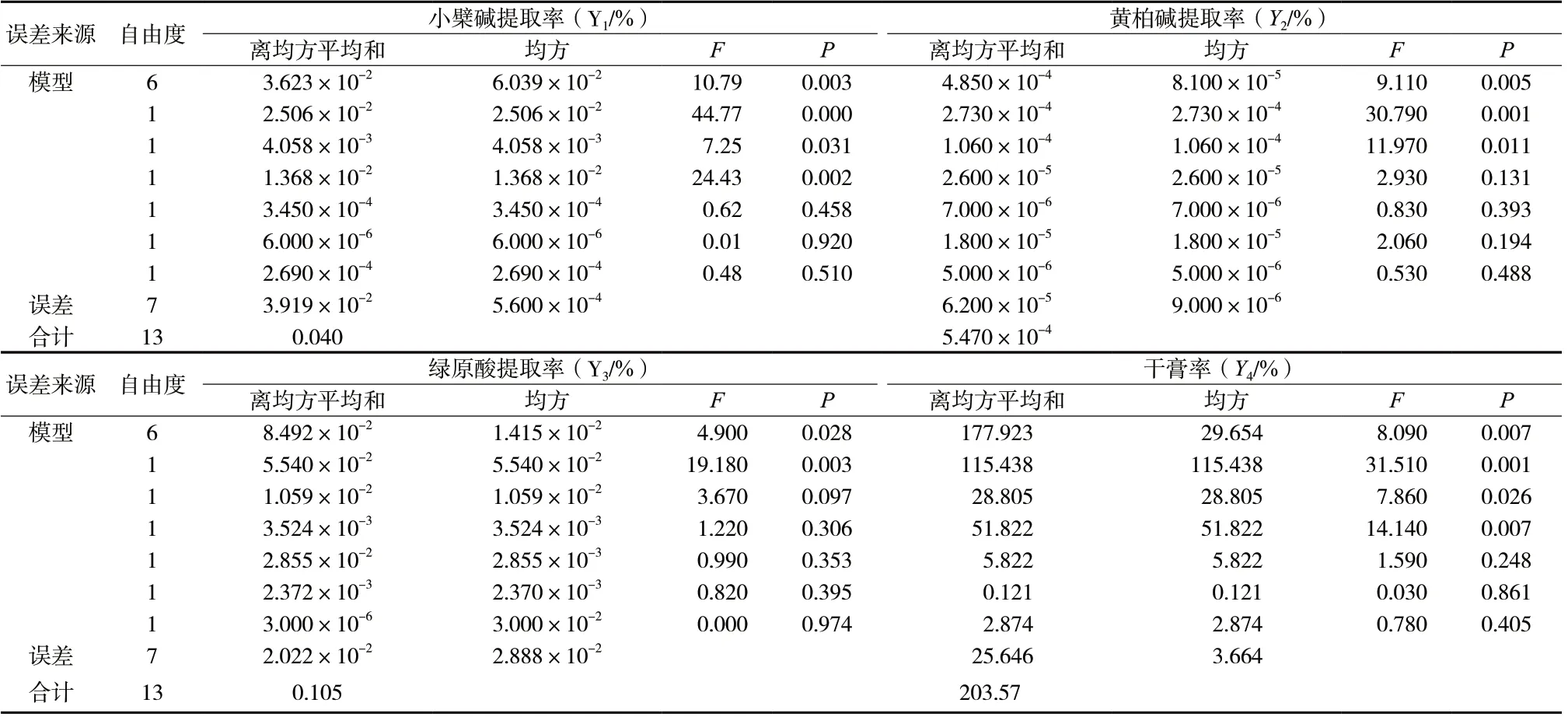
表4 方差分析Tab.4 Analysis of variance
2.6 Box-Behnken 实验设计
为考察提取温度(X1)、提取时间(X2)、提取次数(X3)对黄柏饮片提取工艺的影响程度,设置单因素实验,以小檗碱、黄柏碱、绿原酸得率为指标,对提取工艺中的提取温度(60、80、100℃)和提取时间(30、60、90、120、150 min)进行单因素考察,发现60℃到100℃小檗碱黄柏碱提取率呈上升趋势,而绿原酸提取率80℃发生转折,温度可能影响绿原酸的溶出与降解,在30 min 到150 min 小檗碱提取率分别在60 min 和120 min 发生转折,因此确定因素水平为提取温度80、90、100℃,提取时间60、90、120 min,提取次数1 次、2 次、3 次,见图4。利用软件Design-Expert12 中Box-Behnken 设计三因素三水平实验,中心点重复五次,得到17 组实验条件,实验设计与结果见表5。
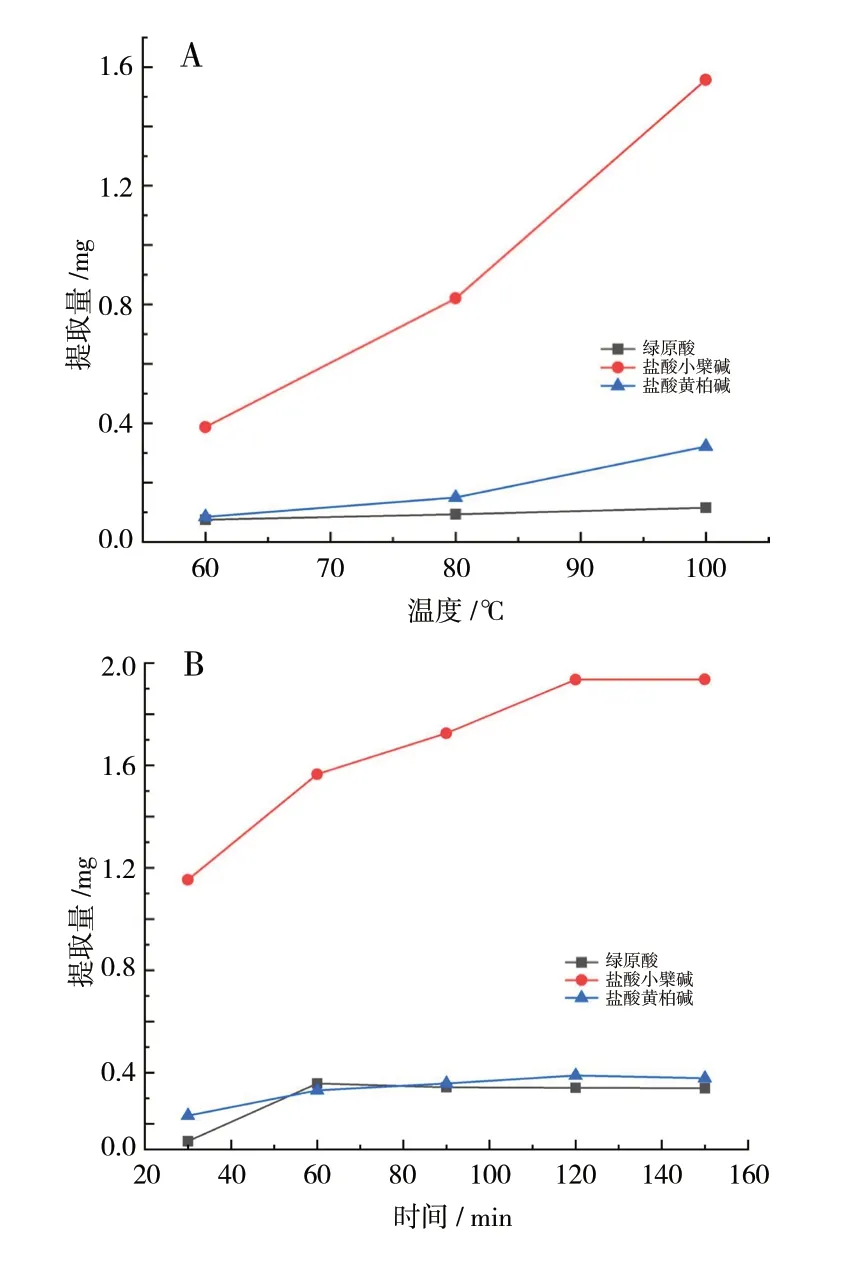
图4 不同因素对绿原酸、小檗碱、黄柏碱提取量的影响Fig.4 Effects of different factors on the extraction of chlorogenicacid berberine and phellodendrine
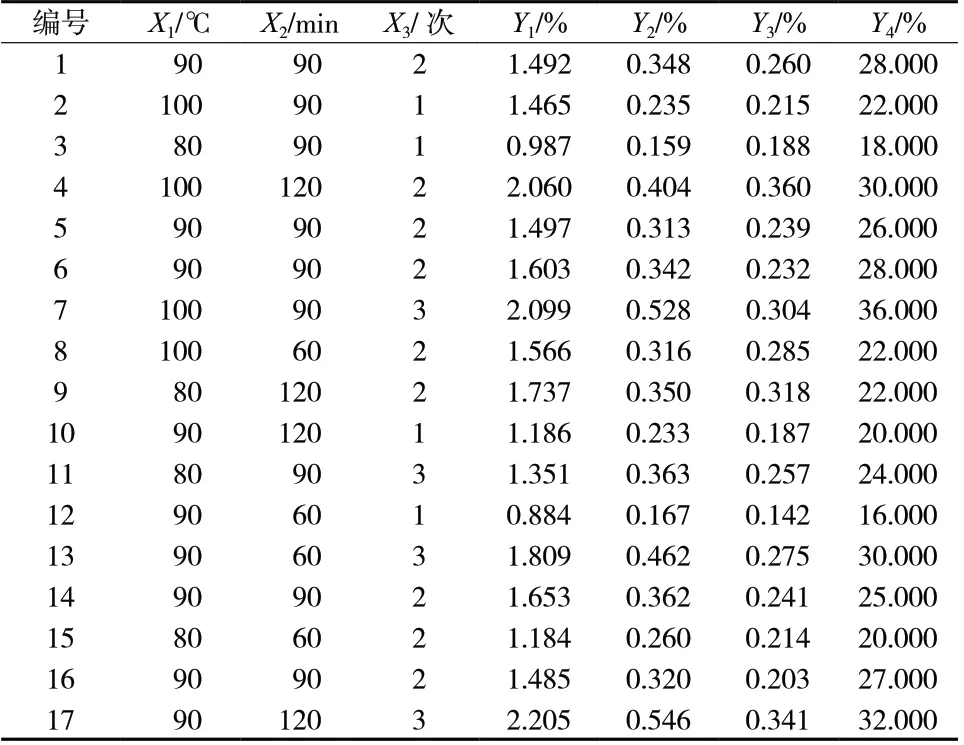
表5 Box-Behnken 试验设计与结果Tab.5 Box-Behnken experimental design and results
2.7 模型的建立与评价
使用软件Design-Expert12 对结果进行模型拟合利用2 阶多项式模型对 4 个CQAs(盐酸小檗碱提取率、盐酸黄柏碱提取率、绿原酸提取率、干膏率)及对应的CPPs(提取时间、提取时间、提取次数)进行方程拟合。得到回归方程如下:Y1= 1.01 - 0.026X1-0.003 5X2+ 0.062X3+ 0.000 226+ 0.000 076-0.093 1- 0.000 049X1X2+ 0.006 75X1X3+ 0.000 78X2X3;Y2= -1.35 + 0.031 8X1- 0.001 41X2- 0.083X3- 0.000 176+0.000 015+ 0.001 9- 0.000 002X1X2+ 0.002 23X1X3+0.000 150X2X3;Y3= 2.46-0.054 1X1-0.002 42X2+0.099X3+ 0.003 20+ 0.000 30- 0.026 0-0.000 24X1X2+ 0.005 0X1X3+ 0.000 175X2X3;Y4= -133.8 +3.08X1+ 0.15X2- 6.75X3- 0.02- 0.002 778-+0.005X1X2+ 0.2X1X3- 0.016 7X2X3。方差分析见表6。

表6 回归模型方差分析Tab.6 Analysis of variance of regression model
由表6 可知小檗碱提取率、黄柏碱提取率、绿原酸提取率、干膏率的回归总模型P值均小于0.01,方差极显著,失拟值P值不显著,表明所建模型有统计学意义。R2adj和R2均较高说明相关性较好,且回归模型能充分描述提取工艺的过程,精密度均大于4,说明该模型拟合较好。根据Design-Expert12 件优化模块下的 Graphical 选项所得的黄柏水提取最佳工艺的预测值为提取时间120 min,提取温度100℃,提取次数1.83 次,在此条件下绿原酸提取率为0.334%,盐酸黄柏碱提取率为0.397%,盐酸小檗碱提取率为1.942%,干膏率为28.99%。结合实际确定提取工艺为100 ℃下提取2 次,每次提取120 min。
2.8 设计空间的建立
2.8.1 工艺评价指标范围设置 通过综合文献报道结果并考虑实际生产经验[12-13]确定关键工艺评价指标的可接受范围及达标概率,见表7。
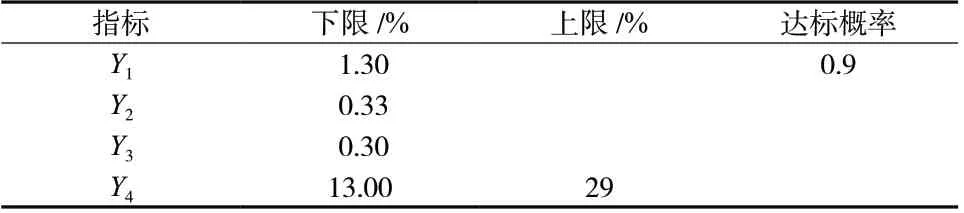
表7 工艺指标下限及达标概率要求Tab.7 The control limits of process indices
2.8.2 指标叠加法 使用Mintab 20 软件作图,四个指标设定上限和下限,然后将能达到表7 评价指标的工艺参数范围叠加,叠加后所得部分即为设计空间。采用指标叠加法计算设计空间。结果见图5。
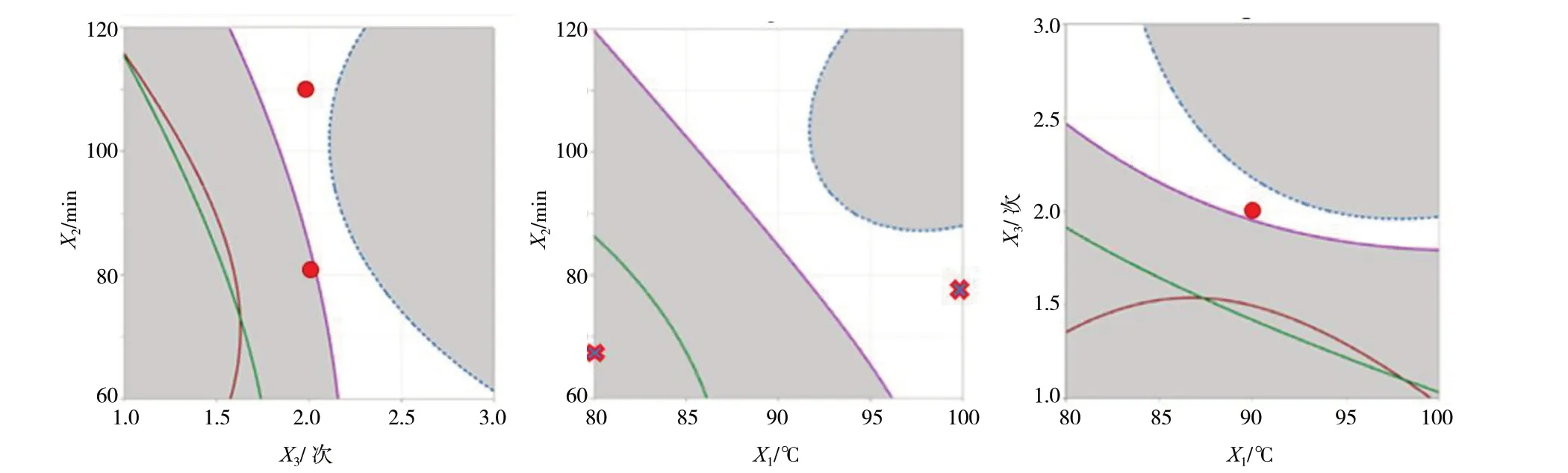
图5 多指标叠加法所得设计空间图Fig.5 Design space obtained by the overlapping method
2.8.3 Monte Carlo 法 采用蒙特卡洛法计算达标概率,设定计算模拟10 000 次,以meshgridm 命令绘制二维设计空间图来统计所有达到概率阈值要求的工艺参数组合,计算采用Matlab R2020a 编程。采用达标概率法计算设计空间结果见图6。分别选取阀值0.9 和0.8的点(2,80,90)、(2,110,90)以及阈值为0 的两点(1,70,80)、(1,110,100)两组实验测定盐酸小檗碱、盐酸黄柏碱、绿原酸、干膏率,结果显示,点1、2 的各项指标与点3、4 相比均较高,验证结果见表8。由验证结果可知此法建模可满足一定的指标预测,且在设计空间内的工艺参数可以保证提取液各成分质量的动态稳定。
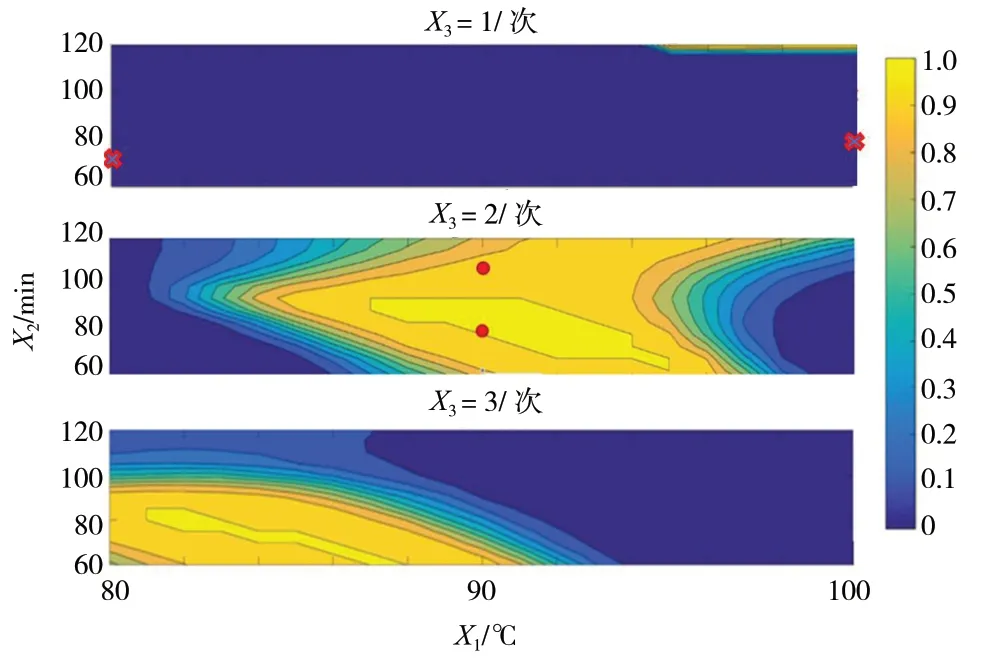
图6 Monte Carlo 法所得设计空间图Fig.6 Monte Carlo method design space diagram
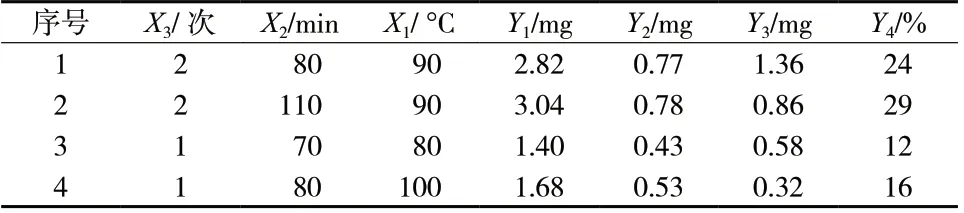
表8 设计空间结果验证表Tab.8 Verification of design space results
3 讨论
在之前的黄柏提取工艺优化研究报道中,多以盐酸小檗碱或生物碱作为考察指标[14],2020 年版《中国药典》中以盐酸小檗碱和盐酸黄柏碱两种成分作为评价黄柏药材质量的指标,为保证中药产品质量一致性,需要对中药制剂前处理工艺的开端即中药提取进行更加全面的质控。黄柏作为临床常用中药,生物碱类和酚酸类成分为提取液中含量较多的成分且与多种药理效应相关联[15]。刘洋等[16]证明了黄柏抗感染的药理作用与盐酸小檗碱抑菌作用具有一致性。黄柏碱可显著抑制免疫效应,降低机体炎症因子水平,发挥免疫调节作用[17]。黄柏中的酚酸类成分绿原酸,不仅可以调节细胞炎症因子的表达,亦具有抗氧化抗病毒的作用[18]。这三者药理活性与黄柏的传统药效均具有一定的相关性,故选择盐酸小檗碱、盐酸黄柏碱、绿原酸为评价指标,出膏率亦为评价提取液质量的重要指标。
当可接受达标概率的阈值为0.9 时,指标叠加法所得区域大于Monte Carlo 法所得设计空间。对比两种方法可以发现指标叠加法只能描述是否达标的绝对值,而Monte Carlo 法所得设计空间能描述所有指标均能达标的概率的渐变过程。虽然ICH 指导原则《Q8(R2):药品研发》中并未明确规定设计空间应达到的概率,但对于工业验证,Peterson 根据三批次工业经验,提出在达标概率大于0.80 时,设计空间已经足够可靠[19]。本研究在达标概率0.9 的条件下结合生产实践[20-21],确定黄柏提取工艺操作空间为提取2 次,温度87 ~ 95 ℃,时间70 ~ 100 min。
4 结论
本研究通过鱼骨图选出6 个工艺参数,结合筛选实验确定了关键工艺指标为提取温度、提取时间和提取次数。配合Box-Behnken 实验设计探究 CPPs 和CQA 的相关性,采取了两种不同的设计空间算法比较并获取适宜的黄柏提取工艺操作空间。在中药提取过程中借鉴了质量源于设计的理念,从多指标成分角度更全面的优化了黄柏提取工艺并分析优化算法的优劣,从而能更好地解决中药原材料与关键质量属性、工艺参数之间的关系,达到提升中药制剂生产质量的目的。

