饲用五环三萜提取物的致突变试验
张 媛 肖宜容 陈怡梦 陈 新,2 张雨梅,2
(1.扬州大学兽医学院,江苏 扬州 225009;2.江苏省动物重要疫病与人兽共患病防控协同创新中心,江苏 扬州 225009)
细菌耐药性的产生是医学界面临的重要问题,减少及禁止抗生素在畜禽养殖中的使用已经成为必然趋势。寻找天然动植物、海洋生物或利用生物技术发现抗菌药物替代品,增强机体免疫功能迫在眉睫[1]。中草药具有良好的药用价值,可部分替代抗生素,因此受到广泛关注[2]。研究发现,在植物中广泛存在的萜类化合物具有多样的药理作用[3]。三萜类物质具有不易挥发、性质稳定的特点,是很多中草药的主要活性成分[4]。五环三萜类物质具有广泛的生物学活性和药理作用,如抗炎[5]、降血糖[6]、抗肿瘤[7]、抗寄生虫[8]等。本研究的受试物有效成分主要包括山楂酸[9]、科罗索酸[10]、桦木醇、白桦脂酸、齐墩果酸、熊果酸等。使用山楂酸治疗腹泻型肠易激综合征具有较好的治疗效果[11]。熊果酸可以维护肠道稳态和机体健康[12]。小檗碱齐墩果酸盐有助于仔猪的生长发育,可有效缓解仔猪感染产肠毒素大肠杆菌后的体重减轻[13]。从茶籽中提取的五环三萜类化合物可以提高畜禽生产性能,增强免疫力[14]。以三萜类为主要活性物质的糖萜素添加在饲料中,可有效提高肥育猪生长性能,增强免疫力,降低谷草转氨酶活性。目前,关于该提取物遗传毒性研究的报道较为少见。本文参照GB 15193.4—2014 食品安全国家标准中细菌回复突变试验、小鼠骨髓细胞微核试验及精子畸变试验的方法,评价五环三萜提取物是否具有的致突变性,为五环三萜提取物作为饲料添加剂的安全性评价提供参考。
1 材料与方法
1.1 试验材料
1.1.1 试验菌株
依据GB 15193.4—2014 中推荐组合,选取鼠TA97、TA98、TA100、TA102 和TA1535 菌株,购自Molecular Toxicology Inc 公司。菌株储存于-80 ℃或平板短期保存于4 ℃,备用。按GB 15193.4—2014 方法对菌株进行生物学特性鉴定。
1.1.2 试验动物
Wistar 大鼠,雄性,5~6 周龄;ICR 小鼠,24~35 g。试验动物由扬州大学兽医学院比较医学中心提供。动物生产许可证号:SCXK(苏)2017-0004;使用许可证号:SYXK(苏)2017-0044。
1.1.3 试剂及仪器
五环三萜提取物成分为科罗索酸、桦木醇、山楂酸、白桦脂酸、齐墩果酸、微甲酸和熊果酸,含量≥90.0%(20191101),由湖南先伟生物有限公司提供。200 mg/mL多氯联苯溶液、沙门氏菌细菌培养基,按GB 15193.4—2014 中要求配制。阳性诱变剂:1,8-二羟基蒽醌(S52025-379,德国Sigma 公司)、叠氮钠(200001012,沈阳化学试剂厂)、2-氨基芴(26238B,美国Sigma-Aldrich公司)、敌克松(10112926,上海晶纯试剂有限公司),均为分析纯。
SG603A 生物安全柜(美国BAKER 公司)、SX-500高压灭菌器(日本TOMY 公司)、BSA223S 电子天平(赛多利斯科学仪器(北京)有限公司)、GHP 系列隔水式恒温培养箱(上海一恒科学仪器有限公司)、UXF30086V 超低温冰箱(美国Thermo Fisher 公司)、培养皿(南通苏品实验器材有限公司)。
1.2 试验方法
1.2.1 鼠伤寒沙门氏菌回复突变试验
1.2.1.1 代谢活化系统(S9)
Wistar大鼠,雄性,5~6周龄。多氯联苯玉米油溶液(200 g/L)按体重(500 mg/kg)腹腔注射。5 d 后处死大鼠,取肝脏,按GB 15193.4—2014 细菌回复突变试验中大鼠肝S9的制备方法进行。
1.2.1.2 增菌培养
各试验菌接种于5 mL营养肉汤培养基中,振荡培养条件:37 ℃、100 次/min,10 h。按照要求每毫升菌株培养物中应等于或大于1×109~2×109活菌数。
1.2.1.3 预试验(点试验法)
受试物剂量设置为50.00、10.00、2.00、0.40、0.08 g/L 溶液,另外设置的阴性对照(灭菌水、DMSO)和阳性对照组。每个剂量均设置有代谢活化系统(+S9)和无代谢活化系统(-S9)两个系列,每个剂量组2个平行,每皿受试品溶液点样10 μL。
1.2.1.4 正式试验(平板掺入法)
受试物设置5 个剂量组,分别为0.008、0.040、0.200、1.000、5.000 mg/皿;另设DMSO对照组、灭菌水阴性对照及阳性对照组。每个剂量组都包括+S9和-S9两个系列,每个剂量组3 个重复。制备底层培养基平板(10 mL/皿),取2 mL顶层培养基倒入5 mL无菌EP管中,加入100 μL 配置好的菌液,试验组加10 μL 受试物,未处理对照组加10 μL 生理盐水,DMSO 对照组加入10 μL DMSO,阳性对照组加入相应的诱变剂,-S9 组加入500 μL 生理盐水,+S9 组加入500 μL S9 混合液。混匀顶层培养基,倒入铺好底层培养基的平板上使其均匀分布,平放凝固后倒置培养,经37 ℃培养48 h,计数菌落数。
1.2.2 小鼠骨髓细胞微核试验
50只ICR小鼠,25~35 g,雌、雄各半。受试物设置1.25 、2.50、5.00 g/kg BW 3 个剂量组,设环磷酰胺阳性对照组及灭菌水阴性对照组。给药2次,间隔24 h。环磷酰胺对照组腹腔注射给药一次。第二次给药6 h后解剖小鼠,取股骨,用注射器吸取小牛血清冲出骨髓细胞进行推片,待涂片风干后使用甲醇固定,姬姆萨染色后镜检。每只小鼠计数1 000 个嗜多染红细胞(PCE),计算其中含微核的细胞数目,并计数200 个红细胞,计算嗜多染红细胞(PCE)与正常红细胞(NCE)的比值。
1.2.3 小鼠精子畸变试验
30~35 gICR雄鼠50只,设置1.25、2.50、5.00 g/kg BW 3个剂量组,并设环磷酰胺阳性对照组及灭菌水阴性对照组。灌胃染毒,共给药5次,每次给药间隔24 h。阳性对照组按40 mg/kg BW进行环磷酰胺腹腔注射。于第一次给药后35 d解剖小鼠,取两侧附睾,在生理盐水中剪碎并吹打混匀,吸取过滤后的悬浮液制片,使用甲醇固定,2%伊红染液染色。在油镜下观察精子形态,每只小鼠检查精子800条,统计精子畸变率和畸变种类。
1.3 数据统计与分析
采用GraphPad Prism 5.0 软件进行数据统计分析。两独立样本之间比较采用t检验,多组别采用单因素方差分析,结果用“平均值±标准差”表示,P<0.05差异显著。
2 结果与分析
2.1 Ames 试验结果
预试验结果显示,受试物各剂量组对5 种试验菌无明显抑菌作用。
正式试验结果显示,受试物各剂量组中5 种试验菌的菌株表现正常,阳性对照试验及各菌株验证试验反应符合要求。受试物Ames 试验两次重复试验结果见表1 和表2。由表1 及表2 可知,受试物在每皿0.008~5.000 mg/皿剂量范围内,有或无S9 时,5 种试验菌的平均回变菌落数均在阴性对照的两倍以内,无剂量-反应关系,并且两次重复结果一致。
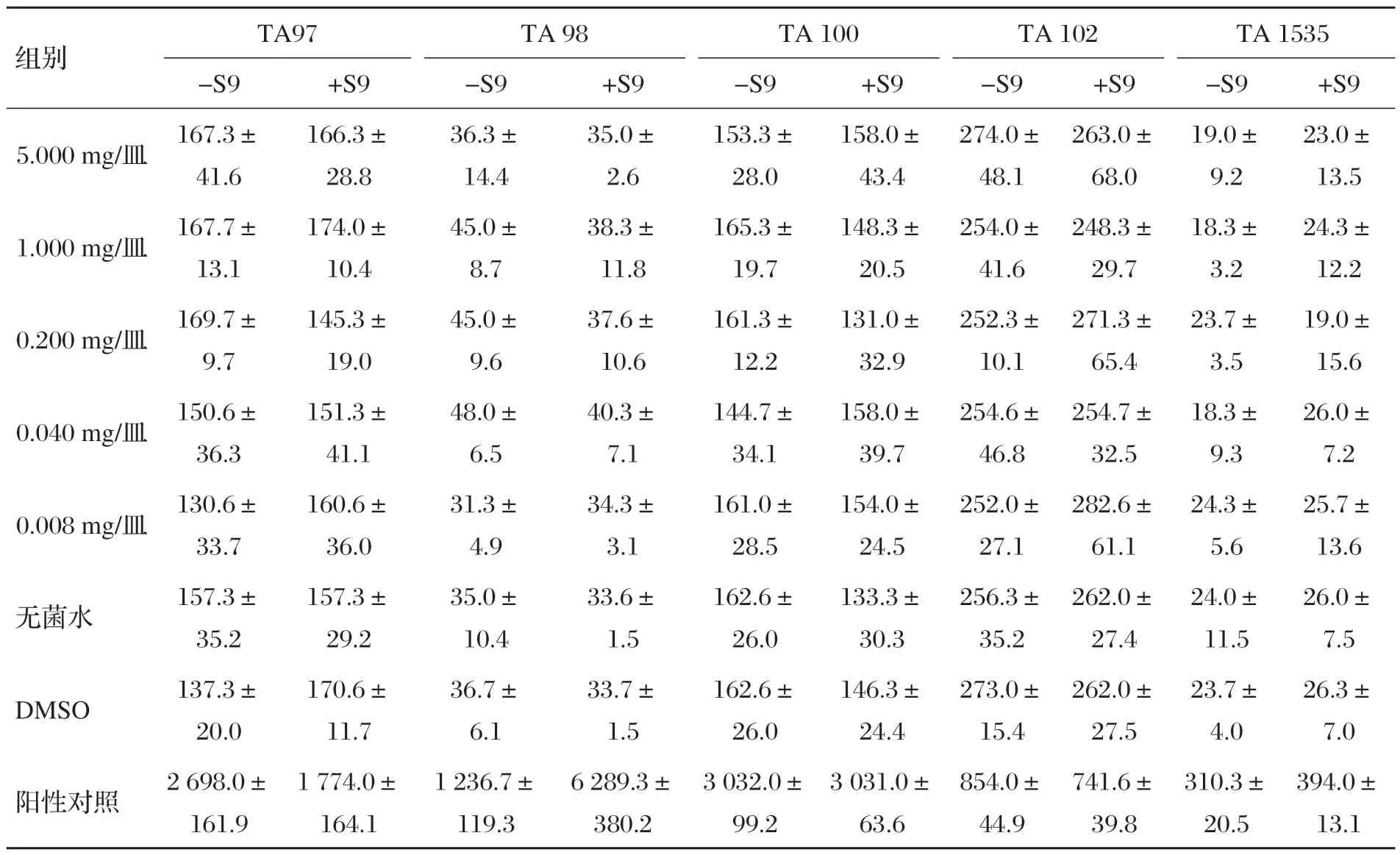
表1 五环三萜提取物对鼠伤寒沙门氏菌回复突变试验结果的影响(第一次)

表2 五环三萜提取物对鼠伤寒沙门氏菌回复突变试验结果的影响(第二次)
2.2 小鼠骨髓细胞微核试验
五环三萜提取物的小鼠骨髓细胞微核试验结果见表3。由表3可知,各试验组嗜多染红细胞与正常红细胞的比值(PCE/NCE)在0.6~1.2范围内,且阳性对照组微核率显著高于阴性对照组,表明本试验方法结果可靠。五环三萜提取物各剂量组与阴性对照组的嗜多染红细胞微核率均小于5%,且无显著差异性(P>0.05),表明受试物小鼠骨髓细胞微试验结果为阴性。

表3 五环三萜提取物对小鼠骨髓细胞微核试验结果
2.3 小鼠精子畸变试验
五环三萜提取物的小鼠精子畸变率结果见表4,畸变精子类别统计结果见表5。由表4可知,阳性对照组精子畸变率显著高于阴性对照组(P<0.05),表明本试验方法可靠。五环三萜提取物各剂量组的精子畸变率与阴性对照组相比无显著差异(P>0.05)。

表4 五环三萜提取物对小鼠精子畸变率的影响

表5 五环三萜提取物对小鼠精子畸变试验各类精子畸变百分率 单位:%
由表5可知,各组间畸变类别无显著差异(P>0.05),表明受试物的小鼠精子畸变试验结果为阴性。
3 讨论
在饲料中添加萜类提取物可以增强动物的免疫应答及抗病能力,在畜禽养殖中具有潜在的应用价值[15]。急性毒性和亚慢性毒性试验结果表明,在饲料中添加五环三萜提取物是相对安全的[16]。本文采用Ames试验、小鼠骨髓细胞微核试验及小鼠精子畸变试验,从体外基因突变、体细胞和生殖细胞危害3 个方面对五环三萜提取物的致突变作用进行评价,进一步为五环三萜提取物作为饲料添加剂的安全性提供依据。
3.1 五环三萜提取物对鼠伤寒沙门氏菌回复突变试验结果的影响
本试验中,在试验剂量下五环三萜提取物的Ames试验中受试物各剂量组中5 种试验菌的菌株生长正常,阳性对照试验及各菌株验证试验反应合格。受试物在各剂量范围内,有或无S9 时,5 种试验菌的平均回变菌落数均在阴性对照的两倍以内,未见剂量-反应关系,表明五环三萜提取物不具有致微生物(细菌)的基因突变作用。Ames 试验是一种在体外进行的致突变实验法,可以快速、便捷地检测受试物引起的点突变。菌株(突变型)与受试物接触,如果菌株(突变型)重新成为野生型菌株,表示其发生了回复突变从而体现出受试物具有致突变性。Ames试验结果的判定是在一种及多种试验菌株得到阳性结果,则认为受试物是致突变物;当所有试验菌株均得到阴性结果,认为受试物是非致突变物。若在无活化系统(-S9)时得到阳性结果,说明受试物是直接致突变物。若在有活化系统(+S9)时为阳性结果,表明受试物是间接致突变物。目前,有研究表明,某些五环三萜类也不具有致突变性,如沙棘叶科罗索酸[17]浓缩物的Ames试验结果也表明其不具有致突变性[18]。
3.2 五环三萜提取物对小鼠骨髓微核细胞率的影响
本试验中,在试验剂量条件下五环三萜提取物未增加小鼠骨髓细胞微核率,表明在该试验条件下五环三萜提取物不具有对小鼠体细胞的遗传毒性。小鼠骨髓细胞微核试验是用于反映受试物是否会引起染色体或有丝分裂损伤是否具有体细胞致突变作用,是从细胞水平上检测受试物是否具有体细胞遗传毒性的一种方法。在细胞的有丝分裂过程中,无着丝粒的染色体片段或者因纺锤体受损而丢失的整个染色体,会在细胞分裂后期仍留在子细胞的胞质内形成微核。在小鼠骨髓中PCE 数量较充足,微核易辨别且微核自发率低因此可作为理想的试验动物。有研究发现,楤木叶中分离出的多种五环三萜类皂苷,在小鼠骨髓微核试验中也表现为无致突变性,并且能明显抑制由环磷酰胺诱发的小鼠骨髓细胞的遗传毒性,表明五环三萜类皂苷可保护由化学诱变剂引起的染色体断裂,具有抗突变作用[19]。
3.3 五环三萜提取物对小鼠精子畸变率的影响
在本试验中,在试验剂量下小鼠精子畸变试验结果为阴性,表明五环三萜提取物不具有对小鼠生殖细胞的遗传毒性。小鼠精子畸变试验中精子形态的改变提示着相关基因发生改变,将受试物给予雄性动物后,如果受试物具有遗传毒性会使精子形态出现折尾、香蕉头、无钩、胖头和无定形头等变化,从形态学角度直接观察受试物对精子产生的影响,来检测受试物对雄性生精细胞的致突变作用,从而判断其对生殖细胞是否具有潜在的致突变性。人参皂苷属于三萜类皂苷,是人参、刺玫果、黄芪等中药材中的主要活性成分之一,在对其进行小鼠精子畸变试验发现其未诱发小鼠精子畸形率增高不具有致畸作用,活性氧引起的小鼠精原细胞氧化损伤可以被人参皂苷所缓解[20]。
4 结论
本试验中,五环三萜提取物对Ames试验、骨髓细胞微核试验及精子畸变试验的试验结果表明其不具有致基因突变作用。

