维A 酸类制剂对皮肤的刺激作用及其影响因素分析
祝霞
(本溪市中心医院皮肤科,辽宁 本溪 117000)
维A 酸类制剂常用于皮肤疾病的治疗,其可影响上皮细胞的增殖、分化,并且可抑制皮脂的分泌,临床常用于治疗银屑病、痤疮等[1]。但是维A 酸类制剂易对皮肤产生刺激,这种刺激作用在最初使用时较为严重[2,3],而目前关于维A 酸类制剂对皮肤的刺激作用的影响因素、机制尚未明确。基于此,本研究旨在探讨维A 酸类制剂对皮肤的刺激作用及其影响因素,现报道如下。
1 资料与方法
1.1 一般资料
选取2019 年1 月—2021 年12 月本院招募的37例受试者。采用随机方法分为试验药受试者和对照药受试者,其中试验药组30 例痤疮受试者中男2 例、女28 例;年龄23~56 岁,平均年龄(38.62±0.66)岁。对照组7 例健康受试者中男1 例、女6 例;年龄24~55 岁,平均年龄(38.65±0.68)岁。两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究经医院医学伦理委员会审核通过,患者知情同意,并签署知情同意书。
1.2 入选标准
纳入标准:①受试者身体健康;②能配合完成该研究;③非哺乳期或者妊娠期女性或者男性;④年龄大于18 岁。排除标准:①存在精神障碍患者不配合该次研究或者中途退出的患者;②使用过影响该研究的药物存在精神障碍患者;③局部皮肤有特应性皮炎、湿疹、银屑病等皮肤病者使用过影响该研究的药物;④局部皮肤有特应性皮炎、湿疹、银屑病等皮肤病者;⑤哺乳期或者妊娠期女性。
1.3 方法
①根据双盲法将上述受试者分为对照组以及试验药组,其中试验药组根据药物不同分为a 组[0.1%阿达帕林凝胶(达芙文)(黑龙江福和制药集团股份有限公司;国药准字H20056871,规格:0.1%)]、b 组[0.025%维A 酸霜剂(0.025%维特明)(山东良福制药有限公司;国药准字H37023768,规格:0.1%)]、c 组[0.05%维A 酸霜剂(0.05%维特明)(山东良福制药有限公司;国药准字H37023768,规格:0.1%)]、d 组[0.025%维A 酸霜剂(0.025%迪维霜)(山东良福制药有限公司;国药准字H37023768,规格:0.1%)]、e 组[0.1%维A 酸霜剂(0.1%迪维霜)(山东良福制药有限公司;国药准字H37023768,规格:0.1%)]、f 组[0.03%维胺酯乳膏(邦力痤疮王)(中美天津史克制药有限公司;国药准字:H10930064,规格:2%)]6组,药物均采购于该院药房。对照组为白凡士林(山东赤兔马医疗科技有限公司;生产批号:CP2019,规格:50 ml)。各组给药方法以及受试时间相同。②给药方法和受试时间:每周每种药品进行3 次24 h 的斑贴试验、1 次72 h 的斑贴试验。观察3 周。每周前4 天将6 种药物、对照药白凡士林分别置于7个铝制小室内,每个小室内在受试者背部贴上0.2 g药品,在24 h 后去掉药物,30 min 后将结果记录下来,并对受试者的背部情况进行照相保存。每周第5 天进行上述方法,但是观察时间改为72 h 后(下周的第1 天)。为控制研究变量,每次斑贴试验需要在同一处皮肤处进行,同时为了避免影响研究结果,在受试期间受试者禁止淋浴、游泳等。
1.4 观察指标
观察各组受试者平均累计刺激指数(MC Ⅱ)(C Ⅱ为每个受试者3 周内进行的每个药的刺激评分之和/评分次数。MC Ⅱ为所有受试者的C Ⅱ之和/受试人数);局部皮肤反应;不良事件发生情况;维A 酸类制剂对皮肤的刺激作用的单因素分析;维A酸类制剂对皮肤的刺激作用的多因素分析。
1.5 统计学方法
采用SPSS 22.0 统计学软件分析处理数据,符合正态分布的计量资料以(±s)表示,组间差异比较采用t检验;计数资料以[n(%)]表示,影响因素采用Logistic 多元回归分析,组间差异比较采用χ2检验,P<0.05 为差异有统计学意义。
2 结果
2.1 各组平均累计刺激指数比较
b 组平均累计刺激指数高于其他各组(P<0.05);e 组平均累计刺激指数高于a 组、f 组、d 组和对照组(P<0.05);d 组平均累计刺激指数高于对照组(P<0.05);对照组平均累计刺激指数低于f 组、a 组,但与c 组相近(P>0.05),见表1。
表1 各组平均累计刺激指数(MC Ⅱ)(±s)
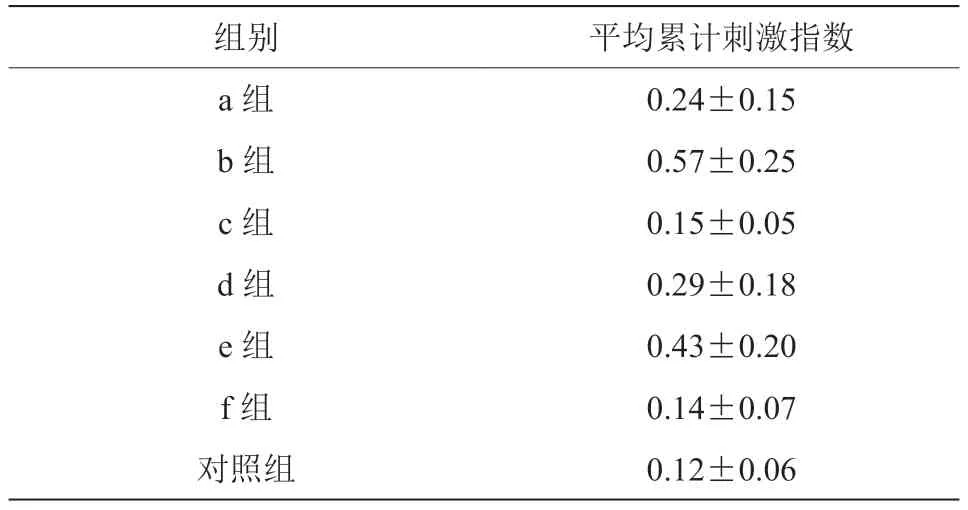
表1 各组平均累计刺激指数(MC Ⅱ)(±s)
组别 平均累计刺激指数a 组 0.24±0.15 b 组 0.57±0.25 c 组 0.15±0.05 d 组 0.29±0.18 e 组 0.43±0.20 f 组 0.14±0.07对照组 0.12±0.06
2.2 各组局部皮肤反应情况
b 组在第15 天时出现渗液1 例,第12 天时出现水疱1 例;d 组在第4、5、8、10 天时均出现渗液1 例;f 组在第2、5、9 天时均出现水疱1 例;其他组并未见皮肤反应。
2.3 维A 酸类制剂对试验药组皮肤刺激作用的单因素分析
维A 酸类制剂对皮肤的刺激作用中,基质的性质对其并没有影响作用(P>0.05),但维A 酸类制剂的剂量、种类、浓度、患者使用时间对皮肤的刺激作用较大(P<0.05),见表2。
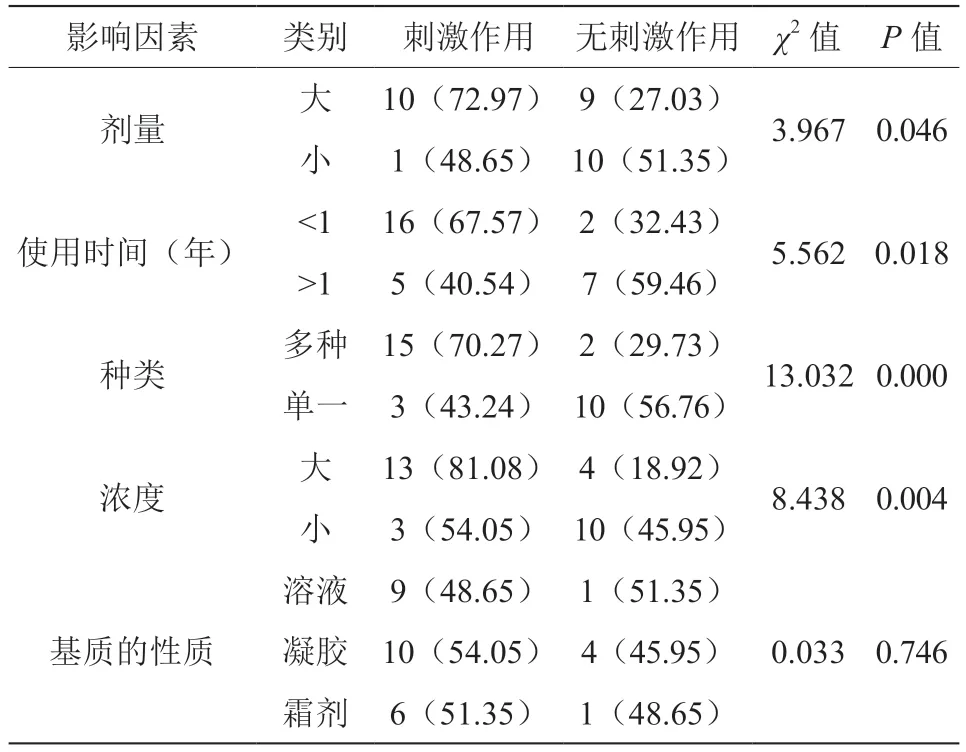
表2 维A 酸类制剂对试验药组皮肤刺激作用的单因素分析[n(%)]
2.4 维A 酸类制剂对试验药组皮肤刺激作用的多因素分析
以维A 酸类制剂的剂量、种类、浓度、患者使用时间为因变量,经Logistic 多元回归分析显示,维A 酸类制剂的剂量、种类、浓度、患者使用时间为影响维A 酸类制剂对皮肤的刺激作用的主要因素,见表3。
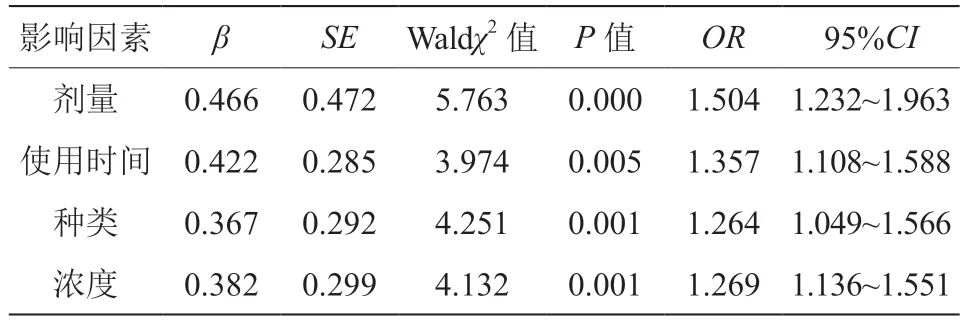
表3 维A 酸类制剂对试验药组皮肤刺激作用的多因素分析
3 讨论
3.1 维A 酸类制剂的常用药物及其现状研究
维A 酸类制剂是治疗皮肤疾病的常用药物,包括第一代的维A 酸、异维A 酸、维胺酯,其中口服异维A 酸对于治疗痤疮最为有效[4,5];第二代的依曲替酸、依曲替酯主要用于治疗银屑病[6]。张大维等[7]研究表明,异维A 酸可以直接杀灭痤疮丙酸杆菌,其作用机制可能为增加细胞通透性、降低细胞膜电位,从而破坏细菌细胞结构,最终促进其死亡。丁娟等[8]研究表明,清热散结片联合异维A 酸软胶囊、克拉霉素缓释片治疗寻常型痤疮的临床效果较为明显,对于改善患者的痤疮效果显著,能够抑制炎症反应,降低血清IL-17 水平,改善皮肤病生活质量指数,且不良反应少。
3.2 维A 酸类制剂对皮肤的刺激作用的结果分析
本研究中对于皮肤刺激作用最小的为0.03%维胺酯乳膏(f 组),其在20 天的刺激作用明显低于0.1%迪维霜(b 组),且组间差异较为明显(P<0.05)。并且0.03%维胺酯乳膏(f 组)相比于0.025%迪维霜(e 组)、0.05%维特明(d 组)明显较小(P<0.05)。b 组在第15 天时出现渗液1 例,第12 天时出现水疱1 例;d 组在第4、5、8、10 天时均出现渗液1 例;c 组在第2、5、9 天时均出现水疱1 例;其他组并未见皮肤反应,表明使用阿达帕林凝胶的刺激作用不仅小于同样浓度的第一代的迪维霜,而且也小于浓度低于它的第一代维A 酸类制剂,说明第3 代维A酸类制剂的刺激性相对较小,对于皮肤的安全性相对较高。其作用机制可能为第3 代的阿达帕林在和维A 酸受体结合时是有选择性的,主要是选择性地与RARβ 受体结合,也可以选择性地和RARγ 受体结合,但是第1 代维A 酸可以和RAR 的3 种受体结合。另外,第1 代维A 酸属于一种长链有机酸,但是阿达帕林为一种较为中性的分子,因此其结构存在一定的差异性[9]。同时,维A 酸类制剂对皮肤的刺激作用由于与RARα 受体有关,因此具有特异性。但其一方面通过表皮细胞中的LC、T 淋巴细胞、ICAM-1、E-选择素等这些炎症细胞或者因子发挥作用,另一方面通过使细胞的通透性增加、细胞膜电位降低,达到破坏细菌细胞结构的效果,进而促进其死亡。另外,at-RA、RAR 激动剂可以修复老化皮肤、增加Ⅰ和Ⅲ型的胶原蛋白方面的表达,维A 酸受体对于皮肤的刺激作用的机制参与了该过程,并且RAR 在其中起了非常重要的作用[10]。
本研究中通过探讨维A 酸类制剂对皮肤的刺激作用的影响因素可知,维A 酸类制剂的剂量、种类、浓度、患者使用时间为影响维A 酸类制剂对皮肤的刺激作用的主要因素。因此,在使用维A 酸类制剂时要严格按照说明使用,提高用药的安全性,减少不良反应的发生[11]。维A 酸类制剂对皮肤的刺激作用的影响因素中的基质的种类并不是其影响因素,说明维A 酸类制剂的刺激作用是维A 酸类制剂本身存在的一种反应,反应的一过性也是维A 酸类制剂自身所决定的,在出现刺激作用时无须停药,等过段时间会自行消退[12]。
3.3 结论和不足
维A 酸类制剂对皮肤的刺激作用受维A 酸类制剂的剂量、种类、浓度、患者使用时间影响,要合理用药,减少对皮肤的刺激作用。但是本研究由于探究的时间有限,未进行维A 酸类制剂对皮肤的刺激作用的剂型、不同用药途径是否对于皮肤刺激作用存在影响,在今后研究中会重点关注维A 酸类制剂对皮肤的刺激作用的影响因素,从而使研究更加具有全面性。

