市售11种煎煮类中药饮片微生物污染情况考察
杨昊,周爽,杨戈,庞庆林,张蕾
(江苏省食品药品监督检验研究院,国家药品监督管理局化学药品杂质谱研究重点实验室,江苏 南京 210019)
中药饮片是指药材经过炮制后可直接用于中医临床或制剂生产使用的药品[1]。中药饮片绝大部分来源于动物、植物或矿物,炮制方法有净制、切制、蒸煮、发酵等,其自身的这些特点导致其微生物载量居高不下,所以中药饮片的卫生质量一直是风险隐患之一。近年来,随着中医药行业在世界临床医学地位和国际影响力进一步提升[2],中药饮片的质量控制越发重要。但《中国药典》2020年版仅对中药提取物、直接口服及泡服饮片等做了微生物限度规定,而临床应用最广的煎煮类饮片未规定限度标准[3]。煎煮类中药饮片品种繁多、炮制方法多样,短时间内难以制定统一标准。本研究通过分析11种煎煮类中药饮片的微生物污染情况,研究多种类别饮片的微生物负载水平,为今后《中国药典》中药饮片微生物限度标准的制修订提供数据支撑,为监管工作的开展提供技术支持。
1 仪器与材料
1.1 仪器 生物安全柜(Thermo,AII级);生化培养箱(Memmert IF450PLUS和HHP400);显微镜(Nikon Eclipse 55i);VITEK2全自动细菌鉴定系统(Biomerieux,Vitek 2 compact15);水浴恒温振荡器(Memmert WNB45)。
1.2 试剂 胰酪大豆胨琼脂培养基(批号:20170108)、胰酪大豆胨液体培养基(批号:20170102)、沙氏葡萄糖肉汤培养基(批号 :20160112)、沙氏葡萄糖琼脂培养基(含抗生素)(批号:20170120)、肠道菌增菌液体培养基(批号:20160701)、紫红胆盐葡萄糖琼脂培养基(批号:20160728)、麦康凯琼脂培养基(批号:20151012)、麦康凯液体培养基(批号:20161222)、RV沙门菌增菌液体培养基(批号:20151019)、木糖赖氨酸脱氧胆盐琼脂培养基(批号:20160327)、三糖铁琼脂培养基(批号:20161016),均为干粉培养基,按《中国药典》2020年版(四部)通则[4]进行配制、灭菌,培养基适用性检查均合格。MUG培养基(批号:161225),沙门氏菌干制生化鉴定盒(批号:161124),大肠埃希氏菌干制生化鉴定盒(批号:161104),以上购自北京陆桥技术有限公司。
1.3 试验样品 中药饮片购自医院、市各大药房(南京大华中药店、益丰大药房、乐富来大药房、先声再康药店等)、饮片厂、药企等。来源于不同产地,均为植物类,有根类、茎类、花类、果实类、种子类等,共11个品种101批次,详见表1。
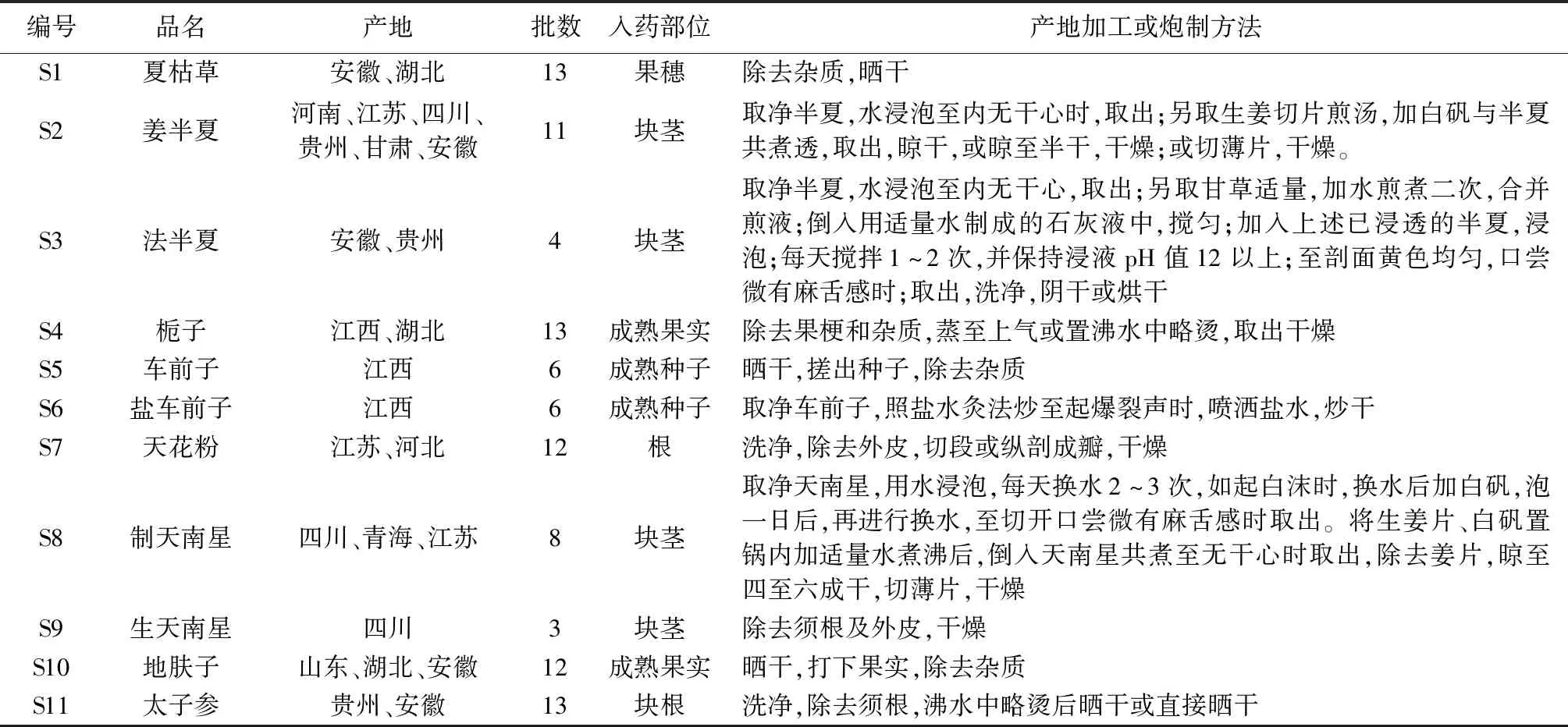
表1 11种煎煮类中药饮片样品信息
1.4 菌种和菌液制备 大肠埃希菌[CMCC(44102)]、乙型副伤寒沙门菌[CMCC(B)50094]、铜绿假单胞菌[CMCC(B)10104],以上菌种购自中国医学细菌管理保藏中心,均为第3代,经菌种验收合格。
2 方法
本试验的所有培养基和101批饮片样品均按照《中国药典》2020年版(四部)通则1108“中药饮片微生物限度检查法”进行了培养基适用性试验和中药饮片的方法适用性试验。结果表明,培养基均符合要求,且饮片样品的方法适用性良好。
2.1 供试液制备 取25 g供试品,加入225 mL胰酪大豆胨液体培养基,制成1∶10供试液,45 ℃水浴振荡不少于15 min。
2.2 需氧菌总数TAMC,霉菌和酵母菌总数TYMC和耐热菌NAIRE的测定方法按照《中国药典》 2020 年版(四部)通则1108“中药饮片微生物限度检查法”。取1∶10供试液1 mL及5~7个连续稀释级10倍递增稀释,每个稀释级制备2个平皿,以TSA和含0.1‰氯霉素的SDA注皿,培养至规定时长得到TAMC和TYMC。另取1∶10供试液于冷水中,加热煮沸30 min,迅速冷却后,同TAMC测定法进行耐热菌数测定。结果以常用对数形式表示。
2.3 控制菌的检查
2.3.1 耐胆盐革兰阴性菌检查 参照《中国药典》2020年版(四部)通则1108“中药饮片微生物限度检查法”进行耐胆盐革兰阴性菌检查。取相当于0.1、0.01和0.001 g……(连续5~7个稀释级)的预培养供试液及其稀释液。
2.3.2 大肠埃希菌检查 取“2.1”项下1∶10的供试液10 mL,参照《中国药典》2020年版(四部)通则1108“中药饮片微生物限度检查法”检查大肠埃希菌。
2.3.3 沙门菌检查 参照《中国药典》2020年版通则1108“中药饮片微生物限度检查法”检查沙门菌。
2.4 微生物限度判定参考标准 《美国药典》(USP43)、《欧洲药典》(EP10.0)、《日本药典》(JP17)中对与煎煮类中药饮片相当的植物药(天然药物)的微生物限度标准做了规定,结果见表2。

表2 USP43、EP10.0和JP17中植物药(天然药物)微生物限度标准
2.5 统计学方法 利用统计学SPSS 13.0软件对数据结果进行统计与分析。
3 结果
3.1 中药饮片中需氧菌总数(TAMC)的检查结果 101批饮片样品的lgTAMC(需氧菌总数的lg值)均值为3.6,小于6.0,表明中药饮片样品的需氧菌总数总体水平符合美国、欧洲和日本药典标准;lgTAMC的最大值在7.2,说明有部分样品超出美国、欧洲和日本药典标准,为不合格饮片样品。lgTAMC的最大值与最小值差为5.9,表明饮片受微生物污染程度差距相当大。以101批中药饮片的需氧菌总数的对数值为横坐标、lgTAMC频率为纵坐标,画出直方图和分布曲线(见图1),由图可知101批中药饮片中,90%lgTAMC值小于6.0,符合美国、欧洲和日本药典标准。以中药饮片品种为横坐标、需氧菌总数的对数值为纵坐标作箱式图(结果见图2),由图2可知,姜半夏(S2)lgTAMC值为1.3~2.3、法半夏(S3)lgTAMC值为2~2.4、栀子(S4)lgTAMC值为2.1~2.8、生天南星(S9)lgTAMC值为2.3~2.8,表明这4个品种微生物污染水平低,且批间差异小,质量稳定;制天南星(S8)lgTAMC值为2.1~6,该品种污染微生物的批间差异最大,质量最不稳定;盐车前子(S6)的lgTAMC值相较车前子(S5)的lgTAMC值明显降低,对S6和S5两种中药饮片进行独立样本T检验,P<0.05存在显著性差异,表明饮片样品的炮制工艺如盐炒等加热炮制工艺可降低TAMC生物负载;地肤子(S10)lgTAMC值为4.1~7.2,在本次检测的所有饮片样品中最高,均值与中位数也高出其他所有饮片样品,表明其TAMC生物负载相当高,部分样品超出了美国、欧洲和日本药典标准,即不符合三国药典标准。

图1 101批中药饮片样品lgTAMC分析

图2 中药饮片不同品种lgTAMC分析
3.2 中药饮片霉菌和酵母菌总数(TYMC)检查结果 101批饮片样品的lgTYMC(霉菌和酵母菌总数的lg值)均值为2.3,中位数为1.9,低于4.0,表明中药饮片样品的TYMC总体水平符合美国、欧洲和日本药典标准;lgTYMC的最大值在5.7,说明也有部分样品超出美国、欧洲和日本药典标准,为不合格饮片样品。lgTYMC的最大值与最小值差为5.2,表明饮片受微生物污染水平差距相当大。以101批中药饮片的霉菌和酵母菌总数的对数值为横坐标、lgTYMC频率为纵坐标,画出直方图和分布曲线(见图3);可知101批中药饮片中,80%lgTYMC值小于5.0,符合《欧洲药典》和《日本药典》标准,65%lgTYMC值小于4.0,符合《美国药典》标准。以中药饮片的品种为横坐标、lgTAMC值为纵坐标,作箱式图(见图4)。由图4可知,在11种中药饮片的lgTYMC均值中仅有1批(地肤子S10)超过4.0,表明这11种中药饮片的TYMC生物负载相对较低。生天南星(S9)和太子参(S11)的lgTYMC值在1.0~1.9之间,表明这两个品种TYMC污染水平较低,批间差异小,质量稳定;天花粉(S7)的lgTYMC值在1.3~3.9之间,表明其TYMC污染水平批间差异大,质量最不稳定;盐车前子(S6)的lgTYMC值相较车前子(S5)的lgTYMC值明显降低,对S6和S5两种中药饮片进行独立样本T检验,结果与TAMC生物负载情况一样,P值<0.05,存在显著性差异,表明饮片样品的炮制工艺如盐炒等加热炮制工艺可降低中药饮片TYMC生物负载;地肤子(S10)lgTYMC值为3.0~5.7,在本次检测中远高出其他饮片样品,表明其TYMC生物负载相当高, lgTYMC的中位数为4.2,即一半以上的地肤子饮片不符合《美国药典》标准。
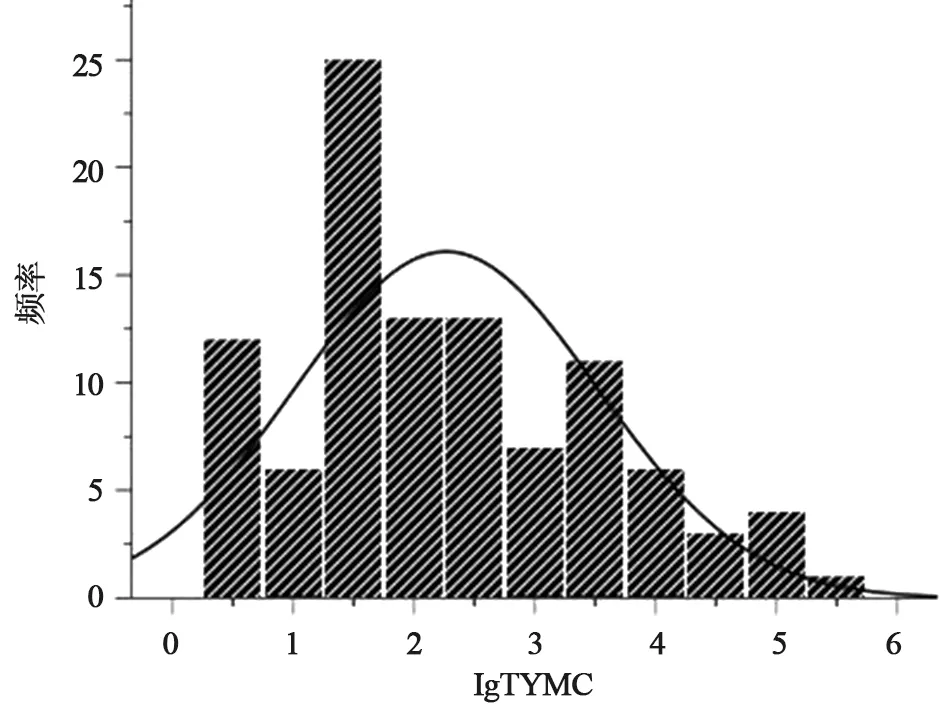
图3 101批中药饮片样品lgTYMC分析

图4 中药饮片不同品种lgTYMC分析
3.3 中药饮片耐热菌数(NAIRE)检查结果 101批饮片样品的lgNAIRE(耐热菌总数的lg值)均值为1.5,中位数为1.3,整体水平较之lgTAMC值均有大幅下降,平均下降2~3个数量级。以101批中药饮片的耐热菌总数的对数值为横坐标、lgNAIRE频率为纵坐标,画出直方图和分布曲线(见图5);以中药饮片品种为横坐标、耐热菌总数的对数值为纵坐标作箱式图(见图6)。由图5及图6可知,中药饮片样品按《中国药典》方法在经过100 ℃ 30 min处理后所有样品仍有耐热菌检出,但与未热处理的需氧菌数相比有明显下降,热处理后35%左右的lgNAIRE值在1.0以下,65%以上的lgNAIRE值降到2.0以下,仅有不足5%饮片样品的lgNAIRE值大于5.0。可见热处理对该11个品种的中药饮片lgNAIRE均有一定的降低作用。对部分污染较为严重的中药饮片进行了耐热菌的分离鉴定,鉴定结果显示,耐热菌大部分为芽孢杆菌,车前子中检出嗜热芽孢杆菌、枯草芽孢杆菌、地衣芽孢杆菌和环状芽孢杆菌等;地肤子中检出嗜热芽孢杆菌和枯草芽孢杆菌;天花粉中检出枯草芽孢杆菌、解淀粉芽孢杆菌和地衣芽孢杆菌。这些芽孢杆菌本身耐热性强,不易被杀灭,因此热处理对该类菌灭活效果不理想,仍有细菌毒素等潜在安全风险存在的可能性。现行各国药典对耐热菌的控制均未有相关规范和检查标准,这也是中药饮片质量标准长久以来难以确定的难点之一,煎煮类中药饮片日常服用时也仅通过简单的煎煮,还是存在一定的生物安全风险,因此中药饮片中的耐热菌污染需引起足够重视,健全相关法规。

图5 101批中药饮片样品lgNAIRE分析
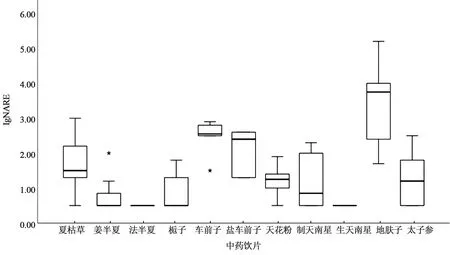
图6 中药饮片不同品种lgNAIRE分析
3.4 中药饮片控制菌检查结果 《中国药典》2020年版(四部)通则1107“微生物限度标准”中对直接口服及泡服饮片的控制菌作出相关规定:不得检出大肠埃希菌(1 g或1 mL);不得检出沙门菌(10 g或10 mL);耐胆盐革兰阴性菌应小于104cfu(1 g或1 mL)。对中药提取物和煎煮类中药饮片未作规定。本实验以此标准为参考判定依据。
3.4.1 耐胆盐革兰阴性菌(G-) 对耐胆盐革兰阴性菌计数结果(G-)进行分析统计,G-计数结果<10 cfu·g-1以lg值0.5计,10 cfu·g-1< G-<102cfu·g-1以lg值1.5计,102cfu·g-1< G-<103cfu·g-1以lg值2.5计,以此类推,做箱式图(见图7)。由图7可知,姜半夏(S2)、法半夏(S3)、生天南星(S9)的lgG-值较低,大部分的G-<10,盐车前子(S6)、制天南星(S8)的lgG-值相对较低,大部分的G-<102;夏枯草(S1)、栀子(S4)、太子参(S11)的lgG-值较高(G-<104),符合《中国药典》2020年版(四部)通则1107中同类标准规定(直接口服及泡服饮片);车前子(S5)、天花粉(S7)、地肤子(S10)的lgG-值很高(G-<105),其中车前子有2批、天花粉有2批、地肤子有9批结果G->104,不符合《中国药典》2020年版(四部)通则1107中同类标准规定(直接口服及泡服饮片)。此外,lgG-值与lgTAMC值存在一定的正相关性,即lgTAMC值较高的中药饮片,一般lgG-值也较高。对紫红胆盐平皿上分离出的耐胆盐革兰阴性菌进行鉴定,其中车前子中检出阴沟肠杆菌、伤口埃希菌、泛菌属以及肺炎克雷伯菌等;地肤子中检出阴沟肠杆菌、泛菌属和阪崎肠杆菌;天花粉中检出阴沟肠杆菌、泛菌属和肺炎克雷伯菌,均为致病菌或条件致病菌[4-7]。
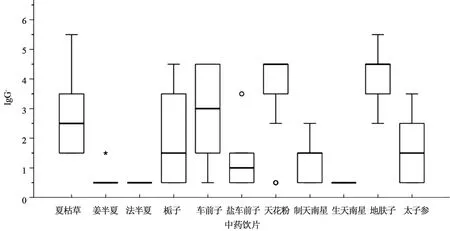
图7 中药饮片不同品种lgG-分析
3.4.2 大肠埃希菌、沙门菌 101批中药饮片中有13批检出大肠埃希菌,包含夏枯草、车前子和地肤子;检出沙门菌的为地肤子3批,且其中2批同时检出大肠埃希菌。从本次实验结果也可以看出,地肤子中药饮片这一品种生物负载较高,TAMC、TYMC、NAIRE及G-也均高于其余品种的中药饮片,这也与该品种的自身特点及炮制工艺有关。
4 讨论
本研究通过对11个品种共计101批煎煮类中药饮片进行微生物污染程度的考察,初步建立了相关品种的微生物负载数据库。这11个品种的中药饮片均为煎煮类,《中国药典》2020年版(四部)通则仅对中药提取物和直接口服及泡服饮片做了微生物限度标准的规定,煎煮类中药饮片还未出台相关微生物限度标准。在现行各国药典标准中,USP、EP、JP对与煎煮类中药饮片相当的植物药(天然药物)的微生物限度均有规定,其中美国对使用前用沸水处理的植物产品工艺要求不同[4],故USP43制订的标准较为严格,微生物限度比JP17和EP10.0低了1个数量级。上述101批中药饮片符合USP标准的为52批,合格率仅为51.5%;符合EP10.0和JP17标准的为99批,合格率98.0%。这些饮片问题项目主要体现在需氧菌总数、霉菌和酵母菌总数及耐胆盐革兰阴性菌的微生物负载较高。
从药材类别来看,矿物药的微生物负载较低,植物药和动物药微生物负载较高,植物药和动物药的微生物负载无显著性差异,这与微生物的生长过程中受药材成分影响相关,不同种类微生物对药材种类有选择特异性[8];对植物药,通常全草类、花粉类、种子类、块根类中药饮片微生物负载较高,皮类、茎类、果实类中药饮片微生物负载相对较低;中药饮片中有抑菌成分的品种微生物负载较低[9];不同产地加工及炮制方法对微生物的污染情况也有影响,直接切制、晒干的中药饮片微生物负载较高,煮制、炒制和蒸制等涉及热炮制工艺的中药饮片微生物负载较低,如本研究中的车前子和盐车前子(热炮制工艺)的微生物负载就存在显著性差异(P<0.05)。
中药作为我国古代文化传承的瑰宝,我国药典中收载的药材品种要远远多于国外药典,目前已有直接口服及泡服中药饮片标准,但煎煮类中药饮片还缺少相关标准限度进行监管,微生物风险长期存在。煎煮类中药饮片涉及面广,日常需求量大,因此煎煮类中药饮片微生物污染数据的积累和微生物危害的风险评估工作更加迫在眉睫。作为中药大国,我们目前应多积累国内各中药饮片相关的微生物污染数据,分析各个品种的微生物负载水平和影响因素[10],才能在中药饮片各个环节的关键点进行把控,指导完善饮片的合理加工炮制、企业的规范生产、流通环节的科学储运等,为完善中药材监管打下基础。这是中国药典的中药标准引领国际中药发展的必经之路[11],也是中药走向世界的关键。

