直接抗病毒药物对持续病毒学应答慢性丙型肝炎患者肝纤维化的影响
严景全 刘娟 卢雪兰 蓝云翠 林占洲
HCV感染是造成肝硬化、门静脉高血压甚或是肝细胞癌常见病因[1]。流行病学研究表明,HCV病例中超三成会发展为肝硬化,而这其中约25%的病例存在进展为肝细胞癌的风险。治疗后持续病毒学应答(SVR)意味着肝脏组织学改善,同时还包括肝功能乃至于生活质量的恢复[2-4]。既往CHC治疗方案是以IFN为基础的,治疗后肝纤维化状态能够得到缓解,不过该方案副作用多、耐受性差,临床适用性受到限制[5]。随着直接抗病毒药物(DAAs)陆续获批,CHC治疗后SVR率得到逐步攀升[6-7]。有关DAAs治疗CHC肝纤维化改善的表现尚待查证,本次研究即探究该问题,旨在为临床抗HCV治疗疗效提供信息。
资料与方法
一、研究对象
选取2018年1月—2021年12月期间本院首诊并接受入院规范化治疗的CHC患者104例,男性65例,女性39例,年龄(45.6±11.2)岁 。CHC诊断符合要求[8],且获得SVR。排除标准:①合并HBV、肝寄生虫、HIV感染;②并发其他局灶性、弥漫性慢性肝病;③治疗终止、病毒转阴后复发。
二、治疗方法
DAAs治疗方案包括索磷布韦联合达拉他韦/维帕他韦/利巴韦林,具体服用方案参考既往文献[6]。SVR定义为抗HCV结束至少12周后复测HCV DNA阴性(低于50 IU/mL)。
三、肝纤维化评价
收集病例资料,于DAAs治疗前后,对纳入CHC病例进行肝纤维化评价,包括肝纤维化指标(APRI、FIB-4)、肝脏硬度值(LSM)。LSM测定设备购自于Echosens公司(法国)。
四、统计学方法
采用SPSS 24.0处理数据。根据资料类型,采用t检验、单因素方差分析或卡方检验比较;Logistic二元回归分析进行单因素、多因素分析。P<0.05为差异有统计学意义。
结 果
一、DAAs治疗前后各项指标变化
与DAAs治疗前比较,治疗后CHC患者WBC、PLT、ALT、AST、TBil、APRI、FIB-4及LSM均明显改善(P<0.05)。
二、肝纤维化指标变化值比较
根据病史、检验指标及影像学资料,将CHC分为慢性肝炎(n=67)、代偿期肝硬化(n=22)及失代偿期肝硬化(n=15)等肝病状态,比较三组DAAs治疗前后肝纤维化指标的变化值,发现APRI、FIB-4及LSM治疗前后变化值差异具有统计学意义(P<0.05)。
三、LSM影响因素分析
参考既往文献建议[9],与治疗前比较,慢性肝病患者治疗后LSM检测值降低>30%定义为LSM改善。以CHC患者DAAs治疗后LSM是否改善作为应变量(赋值0=未改善,1=改善),对治疗前各项指标进行单因素分析,发现治疗前ALT、AST、APRI与LSM改善相关。多因素分析显示,治疗前ALT、AST是LSM改善的独立影响因素。
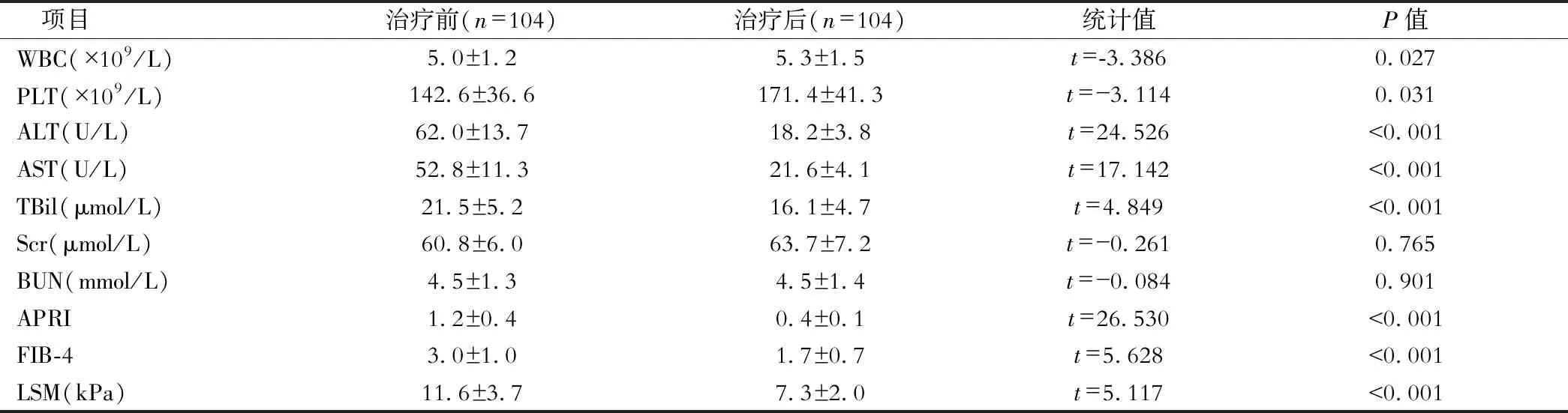
表1 DAAs治疗前后CHC患者各项指标比较
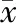
表2 DAAs治疗前后CHC患者肝纤维化指标变化值(±s)比较
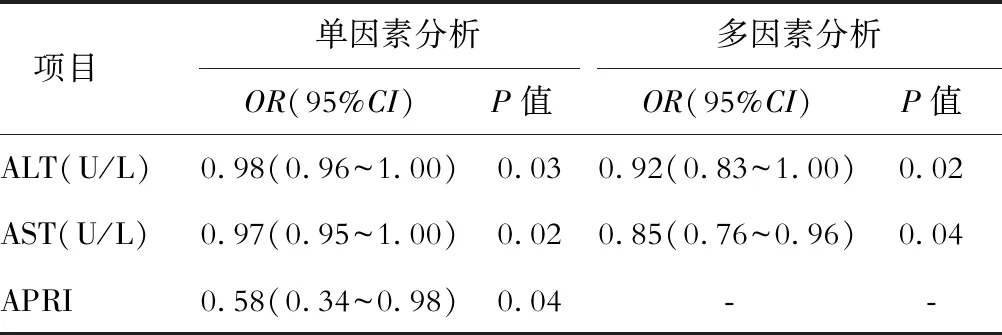
表3 CHC患者治疗后LSM改善的影响因素分析
讨 论
CHC病情较为隐匿,尚无预防性疫苗问世。随着DAAs相关药物相继问世,正在开辟HCV治疗的新时代[10-11]。根据国内HCV防治指南推荐,DAAs可用于治疗失代偿期肝硬化、肾功能不全以及对IFN敏感性差或存在禁忌等CHC病例。据统计,现有多种DAAs药物品种有待审批上市。多年来,以IFN联合利巴韦林的抗HCV方案被广泛用于CHC病例的临床治疗。相较于传统治疗策略,DAAs单药或联合方案对于CHC患者肝脏组织学状态改变的研究尚处在论证阶段。
HCV感染介导病毒蛋白调控信号及代谢途径,同时间接刺激宿主产生抗病毒细胞免疫反应,致使肝实质慢性炎症形成,加速肝纤维化进程。相较于治疗前肝脏穿刺活检结果,在以IFN为基础策略进行治疗后,约半数病例肝脏组织学状态得到明显改善[12-13]。鉴于IFN治疗相关不良反应、耐受性等方面考量,其临床应用已逐步退出市场。检索DAAs相关发表文献,得出经DAAs治疗清除HCV,患者肝纤维化程度显著改善,不过考虑到服用时间较短等问题,尚需要大规模前瞻性研究加以论证。本次研究也得出类似结果,相较于治疗前,DAAs治疗后各项检验指标均得到改善。
影响CHC治疗后肝纤维化改善因素较多。近年来,众多研究、指南指出,基于弹性超声成像检测LSM值可以有效评价肝脏状态。Tag-Adeen等[14]报道,治疗前ALT、AST、TBil以及LSM是CHC患者LSM改善程度的独立预测指标。Chan等[15]指出,基线ALT水平、HCV基因型与CHC病例LSM改善显著相关。本次研究借鉴既往文献建议,定义CHC患者DAAs治疗后LSM值降低>30%为LSM改善,评价影响LSM改善相关影响因素,logistic二元回归分析显示,治疗前ALT、AST为LSM改善独立影响因素,这些与既往研究结论是类似的。
综上所述,应用DAAs治疗CHC能够有效改善患者肝纤维化程度,一旦HCV感染确诊,应尽早开展抗HCV治疗,阻止病情进展。
利益冲突声明:所有作者均声明不存在利益冲突。

