281例儿童眼部毛母质瘤的临床及病理分析
刘泽源,高 燕,陶 丹
(昆明市儿童医院眼科,云南 昆明 650000)
毛母质瘤是一种良性肿瘤,起源于毛囊的毛基质细胞,多位于真皮深部与皮下脂肪交界处。此类肿瘤最初被Malhherb 在1880 年描述为“钙化上皮瘤”[1]。1949 年,Lever 和Griesemer 提出此类肿瘤起源于毛发基质细胞。1961 年,Forbis 和Helwig 建议将此类肿瘤命名为“毛母质瘤”[2]。毛母质瘤临床较少见,发病原因及机制尚不明确。此病的发生可能与编码β-catenin 连环蛋白的CTNNB1 基因突变有关。本文回顾性分析2017 年1 月至2022 年9 月于我院眼科就诊的281 例眼部毛母质瘤患儿的病理资料,旨在探讨儿童眼部毛母质瘤的临床和病理学特点。
1 临床资料与方法
回顾性分析2017 年1 月至2022 年9 月于我院眼科就诊的281 例眼部毛母质瘤患儿的病理资料。这些患儿术前均完善胸片、心电图、血常规、尿液分析、粪便分析、凝血全套、肝肾功、传染病四项等相关检查,确认无手术禁忌后在全麻下行手术切除治疗。281 例患儿中有男性151 例,女性130 例;年龄为4 个月12 天至15 岁9 个月。全部病理标本均采用10% 甲醛溶液固定,行常规石蜡包埋、切片,常规染色。对患儿的性别、年龄、发病部位、肿物大小、病理光镜下所见细胞情况进行统计分析。
2 结果
患儿的发病年龄范围为4 个月12 天至15 岁9 个月,按照以下年龄区间分类(表1):婴儿期(0 岁~1 岁)35 例(12.5%),幼儿期(2 岁~3 岁)111 例(39.5%),学龄前期(4 岁~6 岁)77 例(27.4%),学龄期(7岁~12 岁)46 例(16.4%),青春期(13 岁~18 岁)12 例(4.3%)。患儿中有男151 例(53.7%),女130例(46.3%);男女构成比为1.16:1。

表1 毛母质瘤发病年龄统计结果
281 例病例中毛母质瘤的最多发病部位(见表2)是眼睑162 例(57.7%), 包括上眼睑139 例(49.5%),下眼睑23 例(8.2%)。其他还包括眉弓73 例(26.0%)、眶周45 例(16.0%)、结膜1 例(0.4%)。发病眼别:双眼眶周1 例(0.4%),右眼129 例(45.9%),左眼151 例(53.7%)。
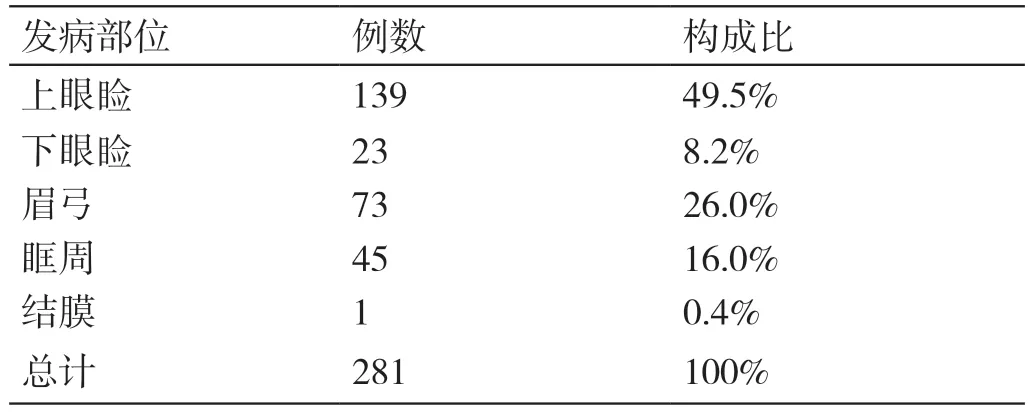
表2 毛母质瘤发生部位
281 例病例中有伴其他部位增生毛母质瘤3 例:左眼下睑毛母质瘤合并右眼眶周皮样囊肿1 例,左眼上睑毛母质瘤合并颅顶皮下毛母质瘤1 例,左眼上睑鼻侧毛母质瘤合并左眼颞侧化脓性肉芽组织炎1 例。本组病理标本大部分都是完整的,送检病理标本中最小毛母质瘤大小为0.1 cm×0.1 cm×0.1 cm,最大毛母质瘤大小为2.0 cm×1.5 cm×1.3 cm。本研究中毛母质瘤的最小直径为0.1 cm,最大直径为2.0 cm,平均直径为0.6 cm。
281 例病例的光镜下细胞组成如下:嗜碱性细胞(毛母质细胞)262 例(93.2%)、影细胞281 例(100%)、钙化灶268 例(95.4%)、多核细胞246 例(87.5%)、炎性细胞116 例(41.3%)。同时有嗜碱性细胞、影细胞、钙化灶、多核细胞、炎性细胞共存者109 例(38.8%),嗜碱性细胞、影细胞、钙化灶、多核细胞共存者121例(43.1%)。见表3。

表3 光镜下细胞分类
3 讨论
毛母质瘤是一种儿童群体常见的皮肤浅表良性肿瘤,位于真皮深部或皮下,与皮肤粘连,瘤体多样,大多单发,极少多发。有研究指出,毛母质瘤多为石灰渣样硬度的坚实结节,病程长,很少引起不适,极小部分患儿诉病灶疼痛或有分泌物。位于真皮深层的毛母质瘤其表面偶尔有界限清楚的血管、溃疡或分泌物,这可能是由其覆盖的皮肤变薄、破溃,瘤体内钙化物外排所致[3-5]。该肿瘤是一种常见的需切除的儿童皮肤肿瘤,在相关病理诊断中其占浅表良性肿瘤的10%[6]。偶尔可见穿通性毛母质瘤、水疱型毛母质瘤及巨大型毛母质瘤等罕见类型[7-14]。本研究中男女构成比为1.16:1,男性多于女性, 与以往大部分学者报告不同[3-4,12]。毛母质瘤可发生在任何年龄阶段,但会在0 岁~10 岁及51 岁~60 岁出现发病双峰值[13]。本报道中毛母质瘤的发病年龄主要在幼儿期,平均3.98 岁,12 岁以前发病者占95.7%。这与相关国内外报道一致。邓维等[7]的研究显示,233 例毛母质瘤患儿的发病高峰为1 岁~4 岁(约占94.41%)。登篓旭等[12]报道称,46 例眶周毛母质瘤患儿的平均发病年龄为3.6 岁。Hassan 等[8]报道称,66% 的毛母质瘤发生在10 岁以下的儿童群体。韩国学者Hu 等[9]报道称,165 例眶周毛母质瘤患儿中发病年龄在10 岁以内的占93.3%。本研究发现281 例病例中毛母质瘤的最多发病部位是眼睑179 例(64.5%), 包括上眼睑139 例(49.5%),下眼睑23 例(8.2%)。其他还包括眉弓73例(26.0%)、眶周45 例(16.0%)、结膜1 例(0.4%)。这与国内外一些学者的研究一致[7,10-12,15-22]。国外学者常采用细针穿刺法对毛母质瘤进行术前针吸细胞学诊断,针吸细胞可见毛母质瘤中的影细胞、嗜碱性细胞、钙化灶等[17]。进行此检查时,患儿通常无法有效配合,故需要进行全身麻醉。毛母质瘤在超声检查中最常见的特征是钙化和低回声边缘。彩色多普勒超声是诊断和评估毛母质瘤的常用工具,其相关诊断结果与病理检查基本一致[18-19]。此检查对患儿配合度的要求较低,故可作为毛母质瘤的首选诊断方法。毛母质瘤在CT上表现为软组织密度影、混杂密度影、高密度影及不同类型的钙化。在检查部位特殊及彩色多普勒超声不能判断时可选用CT 检查。毛母质瘤在MRI T2WI 和T2WI+FS 中呈特征性网状和环状高信号表现。上述表现可提示病变与周围组织的关系。但是,MRI 检查也存在检查费用高昂等缺点[11,19-21]。病理检查是诊断毛母质瘤的金标准。在光镜下可见毛母质瘤由影细胞、嗜碱性细胞和过渡细胞组成。影细胞位于瘤团的中央,胞质呈强嗜酸性,胞核消失,边界清楚。嗜碱性细胞小,处于瘤团周边,大小均匀,有活跃的核分裂情况,但无病理性核分裂。介于二者之间的是过渡细胞,其早期形态类似于嗜碱性细胞,晚期形态类似于影细胞[16,23-24]。部分毛母质瘤病例的瘤体内有钙化灶甚至伴有骨化形成(主要见于病程较长的患儿)。在穿孔性毛母质瘤中,肿物穿孔的表皮挤压到皮肤表面为其主要特征。在大疱性毛母质瘤中,还可发现淋巴水肿及淋巴管扩张[15,25-26]。本研究中281 例患儿的毛母质瘤中未见骨化细胞,但均有影细胞。
本研究中毛母质瘤的最小直径为0.1 cm,最大直径为2.0 cm,平均直径为0.6 cm,无巨大型毛母质瘤。毛母质瘤不能自行吸收,会继续生长,引起皮肤溃疡及感染。若包膜破裂易引起局部感染,在进行手术治疗前可使用抗生素抗感染,手术过程中应注意保护皮肤,确保动作轻柔、剥离完全。完整切除毛母质瘤及其包膜是预防其复发的关键,术后应使用生理盐水冲洗术腔,本研究中无复发病例。

