鱼腥草素钠鼻喷雾剂的喷雾特性评价
王淼,贾青,吴陈亮*(1. 安徽中医药大学药学院,合肥 20012;2. 南通市海门长三角药物高等研究院,江苏 海门 2261;. 上海欧米尼医药科技有限公司,上海 20120)
鱼腥草素钠(sodium houttuyfonate),化学名为十二酰乙醛亚硫酸氢钠,是三白草科植物蕺菜的有效成分——癸酰乙醛与亚硫酸氢钠的加成物,其生物活性和药理作用与癸酰乙醛相似,研究发现其具有抗炎、抑菌、抗病毒、抗肿瘤、保护心血管等[1]作用。目前,临床上以鱼腥草素钠为原料开发了鱼腥草素钠片和鱼腥草素钠栓,片剂主要用于治疗慢性支气管炎及其他上呼吸道感染性疾病,栓剂用于治疗子宫颈糜烂。
近年来,鼻腔给药由于起效迅速、给药方便、无肝脏首过效应、生物利用度高以及脑靶向作用等特点,成为国内外制剂领域研究的热点[2]。目前尚未见以鱼腥草素钠为原料制备鼻喷雾剂的相关报道。本研究以鱼腥草素钠为原料开发了鱼腥草素钠鼻喷雾剂,拟用于治疗鼻腔局部炎症。参照《中国药典》、美国药典和美国食品药品监督管理局(Food and Drug Administration,FDA)相关指南,对自制的鱼腥草素钠鼻喷雾剂的启动/再启动、递送剂量均一性、雾滴粒径分布(激光衍射法、撞击器法)、喷雾模式和羽流几何学等喷雾特性指标进行评价,为后续鱼腥草素钠鼻喷雾剂的工业化开发奠定基础。
1 材料
1.1 仪器
XSR205DU/AC(分析天平,精度:十万分之一,梅特勒-托利多仪器有限公司);LC-20A型高效液相色谱仪[岛津国际贸易(上海)有限公司];Andersen级联撞击器(英国Westech Instrument公司);HELOS/BF型激光粒度仪(德国Sympatec公司);Mighty Runt自动喷射器(美国Innovasystem公司);SprayVIEW激光成像系统(美国Proveris Scientific公司);Millipore纯水系统(默克密理博贸易有限公司);鼻腔液体药用喷雾泵(规格:100 μL,深圳博纳精密给药系统股份有限公司);低硼硅玻璃管制螺口瓶[双峰格雷斯海姆医药包装(镇江)有限公司]。
1.2 试药
鱼腥草素钠对照品(中国食品药品检定研究院,批号:100247-202102,含量:99.4%);鱼腥草素钠鼻喷雾剂(自制,批号:221129-1,规格:32 μg/喷、30喷/瓶);鱼腥草素钠(西安皓泽生物科技有限公司,批号:HZ210706,含量:99%);亚硫酸氢钠(成都华邑药用辅料有限公司,批号:20200901);无水葡萄糖(潍坊盛泰药业有限公司,批号:w20200401);依地酸二钠(南京化学试剂有限公司,批号:181114082c,含量:100.2%);山梨酸钾(成都华邑药用辅料有限公司,批号:20220701,含量:100.2%);甲醇(色谱纯,上海星可高纯溶剂有限公司);10%四丁基氢氧化铵水溶液(分析纯,国药集团化学试剂有限公司);水为去离子水。
2 方法与结果
2.1 鱼腥草素钠含量测定
2.1.1 色谱条件[3]色谱柱:Xtimate C8色谱柱(4.6 mm×250 mm,5 μm);流动相:甲醇-水-10%四丁基氢氧化铵水溶液(65∶35∶0.35,V/V/V);检测波长:280 nm;柱温:30℃;流速:1.0 mL·min-1;进样量:20 μL;稀释液:甲醇-水(70∶30,V/V)。
2.1.2 溶液配制
① 取鱼腥草素钠对照品约50 mg,精密称定,置100 mL量瓶中,用稀释液溶解并稀释至刻度,摇匀,作为对照品储备液。精密量取对照品储备液0.5 mL置250 mL量瓶中,用稀释液稀释至刻度,摇匀,作为对照品工作液。
② 取供试品1瓶,有雾喷出后喷废3喷。将药瓶垂直向上放置,使泵的喷头恰好插入一垂直倒立的25 mL量瓶中,揿压泵1次,迅速直立量瓶,使药液流入量瓶底部。用稀释液稀释至刻度,摇匀,作为供试品工作液。
③ 参照“2.2”项下方法制备不含鱼腥草素钠的鼻喷雾剂,并按照供试品工作液配制过程配制空白辅料溶液。
2.1.3 专属性考察 分别取对照品工作液、供试品工作液、空白辅料溶液,按“2.1.1”项下色谱条件进样,记录色谱图(见图1)。结果显示空白辅料溶液色谱图中无色谱峰与鱼腥草素钠峰重叠,对照品工作液和供试品工作液中主峰保留时间一致,表明该方法专属性良好。

图1 方法专属性考察的高效液相色谱图Fig 1 HPLC chromatogram of method specificity
2.1.4 线性关系考察 用稀释液逐级稀释对照品储备液,制备成质量浓度分别为0.05、0.10、0.20、0.49、0.98、1.57、1.96 μg·mL-1的对照品溶液,按“2.1.1”项下色谱条件进样分析。以质量浓度(X,μg·mL-1)为横坐标,峰面积(Y)为纵坐标,绘制标准曲线,得到鱼腥草素钠的回归方程:Y=8.600×104X+6.152×102(r=0.9999)。结果表明,鱼腥草素钠在0.05~1.96 μg·mL-1内与峰面积线性关系良好。
2.1.5 重复性考察 平行制备6份供试品工作液,按“2.1.1”项下色谱条件进样分析,记录峰面积。以外标法计算鱼腥草素钠含量,含量RSD为1.6%,表明该分析方法重复性良好。
2.1.6 回收试验 平行配制9份空白辅料溶液,分别加入“2.1.2”项下对照品工作液1.3、1.6、1.9 mL,得到鱼腥草素钠低、中、高质量浓度(1.02、1.25、1.49 μg·mL-1)供试品工作液,按“2.1.1”项下色谱条件进样分析,计算回收率。低、中、高质量浓度供试品的回收率分别为99.94%、99.71%、99.88%,RSD分别为0.25%、0.19%、0.20%,表明该方法准确度符合要求。
2.2 鼻喷雾剂的制备
精密称取鱼腥草素钠0.16 g,用适量水溶解;精密称取亚硫酸氢钠1.00 g、无水葡萄糖20.00 g、依地酸二钠0.05 g和山梨酸钾0.65 g至适量水中,搅拌溶解,合并鱼腥草素钠溶液和辅料溶液,并用水定量至500 g,搅拌均匀。量取药液5 mL置低硼硅玻璃管制螺口瓶中,盖上鼻腔液体药用喷雾泵,即得。
2.3 启动/再启动
启动/再启动采用重量法和HPLC法进行测试。取鱼腥草素钠鼻喷雾剂3瓶,以相同的力触发鼻喷雾剂至有液滴喷出,开始记录喷射重量和次数,至喷射重量稳定,结果见图2。由图2可知,该鼻喷雾剂喷射1喷后,从第2喷开始,每喷的喷射重量在目标喷量(100±10)mg,从第4喷开始保持稳定。为保证给药剂量的准确性,本研究中的鼻喷雾剂在初次给药时,需至少喷废3喷。

图2 鱼腥草素钠鼻喷雾剂启动时喷射重量变化Fig 2 Changes in shot weight of sodium houttuyfonate nasal spray during priming
将启动后的样品于室温条件下垂直放置,分别间隔0、2、4、7、14 d进行再启动测试,采用HPLC法测试递送剂量,每个间隔时间测试3喷,结果见表1。由表1数据可以看出,间隔14 d时,第1喷递送剂量的平均值超出了标示量的85%~115%,说明放置了14 d的鼻喷雾剂,再次给药时不能立刻递送出准确剂量。因此,在超出7 d的使用周期后再次给药前应至少喷废1喷。
表1 再启动测试结果( ±s,n=3)Tab 1 Repriming test ( ±s,n=3)

表1 再启动测试结果( ±s,n=3)Tab 1 Repriming test ( ±s,n=3)
递送剂量/%间隔时间/d第1喷第2喷第3喷0103.91±2.34103.40±2.69103.90±1.89 2100.78±3.44101.34±1.90101.77±2.27 4101.07±2.68 99.54±4.47 99.54±4.83 7 96.71±2.58 97.67±1.33 98.72±1.45 14 81.88±11.53 95.27±2.00 97.05±1.87
2.4 递送剂量均一性
递送剂量均一性是多剂量鼻喷雾剂的主要质量标准之一,包括瓶间递送剂量均一性和瓶内递送剂量均一性。递送剂量均一性采用HPLC法进行测试。
取样品1瓶,有雾喷出后喷废3喷。将药瓶垂直向上放置,使泵的喷头恰好插入一垂直倒立的25 mL量瓶中,揿压泵1次(第1喷),迅速直立量瓶,使药液流入量瓶底部。用稀释液稀释至刻度,摇匀。重复测定10瓶,共10个测定结果,作为瓶间递送剂量均一性。10个测定结果的平均值为104.85%,RSD为1.5%,其中最大值为106.58%,最小值为101.84%。
取样品1瓶,有雾喷出后喷废3喷。测试每瓶前段(第1喷)和后段(第30喷)的递送剂量。重复测定5瓶,共10个测定结果,作为瓶内递送剂量均一性。10个测定结果的平均值为105.12%,RSD为1.8%,其中最大值为108.48%,最小值为102.79%。
瓶间和瓶内递送剂量均一性共20个测定结果中,平均值均在标示量的85%~115%,且全部测定值均在标示量的80%~120%,表明该鼻喷雾剂给药剂量稳定、准确。
2.5 雾滴粒径分布(激光衍射法)
研究中采用自动喷射器进行触发,使用激光粒度仪进行雾滴粒径分布测试,主要考察D10、D50、D90、Span值和小于10 μm雾滴百分比。
取样品5瓶,有雾喷出后喷废3喷。将样品固定于自动喷射器上,并将自动喷射器置于激光与镜头中央,使激光束能够穿过喷射范围的中心。分别测定3 cm和6 cm(鼻喷泵喷头顶端距离激光源中心的垂直距离)下的雾滴粒径分布,在有效喷次内,每个样品初始段和末段每个距离分别测定3次。
鼻腔定量喷雾泵的一次触发可分为形成期、稳定期和消退期3个阶段[4],这3个阶段的雾滴粒径分布有很大区别。鱼腥草素钠鼻喷雾剂雾滴粒径随时间变化如图3所示。

图3 鱼腥草素钠鼻喷雾剂喷雾过程Fig 3 Course of sodium houttuyfonate nasal spray
形成期由于是触发开始阶段,雾化压力和喷雾流速较低,所以形成的雾滴粒径较大;之后雾滴粒径变小,进入稳定期,此时雾化压力和喷雾流速处于最优状态,形成的雾滴粒径较小且最稳定;最后由于定量室变空,雾化压力和流速降低,雾滴粒径变大,从而进入消退期。通常稳定期形成的雾滴粒径均一且稳定,与药物的治疗效果密切相关,因此本研究对稳定期的雾滴粒径分布进行测定和分析。
2020年版《中国药典》要求鼻用喷雾剂喷出后的雾滴粒子绝大多数应大于10 μm[5]。鼻喷雾剂雾滴粒径分布结果如表2所示,雾滴粒径主要集中分布在14~82 μm,初始段和末段雾滴粒径分布无明显区别(P>0.05),符合《中国药典》对鼻用喷雾剂的要求。
表2 鱼腥草素钠鼻喷雾剂雾滴粒径分布( ±s,n=3)Tab 2 Droplet/particle size distribution of sodium houttuyfonate nasal spray ( ±s,n=3)

表2 鱼腥草素钠鼻喷雾剂雾滴粒径分布( ±s,n=3)Tab 2 Droplet/particle size distribution of sodium houttuyfonate nasal spray ( ±s,n=3)
距离/cm编号D10/μmD50/μmD90/μm小于10 μm雾滴百分比/%Span值初始段-3114.36±0.1832.21±0.2469.44±1.605.35±0.401.71±0.03 2 16.26±0.1136.24±0.3577.74±0.793.49±0.111.70±0.01 3 17.17±0.2537.16±0.5779.36±1.413.03±0.161.67±0.01 4 16.76±0.2937.79±0.4781.05±0.673.32±0.211.70±0.02 5 15.73±0.1535.22±0.2275.36±0.954.29±0.271.69±0.01初始段-6117.66±0.3738.06±0.3567.50±0.143.91±0.421.31±0.02 2 18.40±0.1239.58±0.2171.75±0.183.88±0.181.35±0.01 3 19.55±0.0739.97±0.1571.83±1.113.19±0.321.31±0.02 4 18.50±0.1939.64±0.1872.82±0.323.93±0.021.37±0.02 5 17.45±0.1838.04±0.3268.58±1.863.85±0.361.34±0.03末段-3115.37±0.2333.81±0.4671.98±1.244.36±0.421.67±0.02 2 16.76±0.3338.52±1.3282.40±1.473.15±0.321.70±0.03 3 16.75±0.3037.49±0.6881.05±2.263.14±0.371.71±0.02 4 17.07±0.0338.62±0.1081.95±0.422.78±0.131.68±0.01 5 15.82±0.1034.97±0.1474.18±0.443.76±0.231.67±0.01末段-6116.75±0.1336.81±0.0161.73±0.215.50±0.161.22±0.01 2 18.57±0.1239.73±0.2573.24±1.223.71±0.231.38±0.02 3 19.03±0.2139.76±0.4170.21±0.912.79±0.301.29±0.01 4 18.81±0.1340.51±0.2975.29±4.423.08±0.401.39±0.10 5 17.93±0.3638.37±0.2767.41±0.893.51±0.161.29±0.02
2.6 雾滴粒径分布(撞击器法)
通过Andersen级联撞击器(Andersen Cascade Impactor,ACI)对喷雾的空气动力学粒径分布进行研究,主要考察小于9 μm雾滴中药物含量,从而判断进入气管等下呼吸道的药物量百分比。
在F层放上玻璃纤维滤纸,将撞击器各部件按顺序组装好,调整流速为(28.3±1.4)L·min-1。用适宜的橡胶接头将5 L圆底玻璃烧瓶(侧面带有直径1.5 cm小孔)与ACI的进口端(锥口)连接起来。取样品3瓶,有雾喷出后喷废3喷,每瓶测试10喷。用250 mL稀释液清洗回收圆底玻璃烧瓶、橡胶接头、负1层及其接收盘,作为大于9 μm雾滴的供试品;用50 mL稀释液清洗回收0~6层和含滤纸的F层,作为小于9 μm雾滴的供试品。分别经0.45 μm 亲水滤膜过滤,取续滤液,按“2.1.1”项下色谱条件进样分析。结果显示,3瓶样品的回收率分别为101.0%、100.9%、99.3%,大于9 μm雾滴中药物含量均为100.0%,小于9 μm雾滴中药物含量均未检出,表明几乎无药物进入气管等下呼吸道。
2.7 喷雾模式和羽流几何学
采用SprayVIEW激光成像系统进行喷雾模式和羽流几何学测定,结果见图4。根据预实验结果确定仪器的各项参数,设置自动喷射器触发速度和加速度分别为:45 mm·s-1和2500 mm·s-2。取样品3瓶,有雾喷出后试喷3次。将鼻喷泵固定于自动喷射器上,分别测定喷雾模式和羽流几何学,每个样品测定3次。喷雾模式测试结果以Dmax、椭圆率和喷雾面积表示(见表3)。羽流几何学测试结果以喷雾角度和喷雾宽度表示(见图5及表4)。
表3 鱼腥草素钠鼻喷雾剂喷雾模式( ±s,n=3)Tab 3 Spray pattern of sodium houttuyfonate nasal spray ( ±s,n=3)

表3 鱼腥草素钠鼻喷雾剂喷雾模式( ±s,n=3)Tab 3 Spray pattern of sodium houttuyfonate nasal spray ( ±s,n=3)
距离/cm编号Dmax/mm椭圆率喷雾面积/mm2 3120.95±0.241.146±0.010304.2±5.1 220.89±0.421.143±0.015297.5±6.5 320.16±0.241.136±0.011278.2±6.7 6136.00±0.601.237±0.019836.5±23.7 234.65±0.671.174±0.021808.0±17.5 334.57±0.411.187±0.038768.1±28.2
表4 鱼腥草素钠鼻喷雾剂羽流几何学( ±s,n=3)Tab 4 Plume geometry of sodium houttuyfonate nasal spray( ±s,n=3)

表4 鱼腥草素钠鼻喷雾剂羽流几何学( ±s,n=3)Tab 4 Plume geometry of sodium houttuyfonate nasal spray( ±s,n=3)
编号喷雾角度/°喷雾宽度/mm 1 35.2±0.238.31±0.22 2 34.5±0.237.55±0.22 3 31.1±0.433.37±0.44
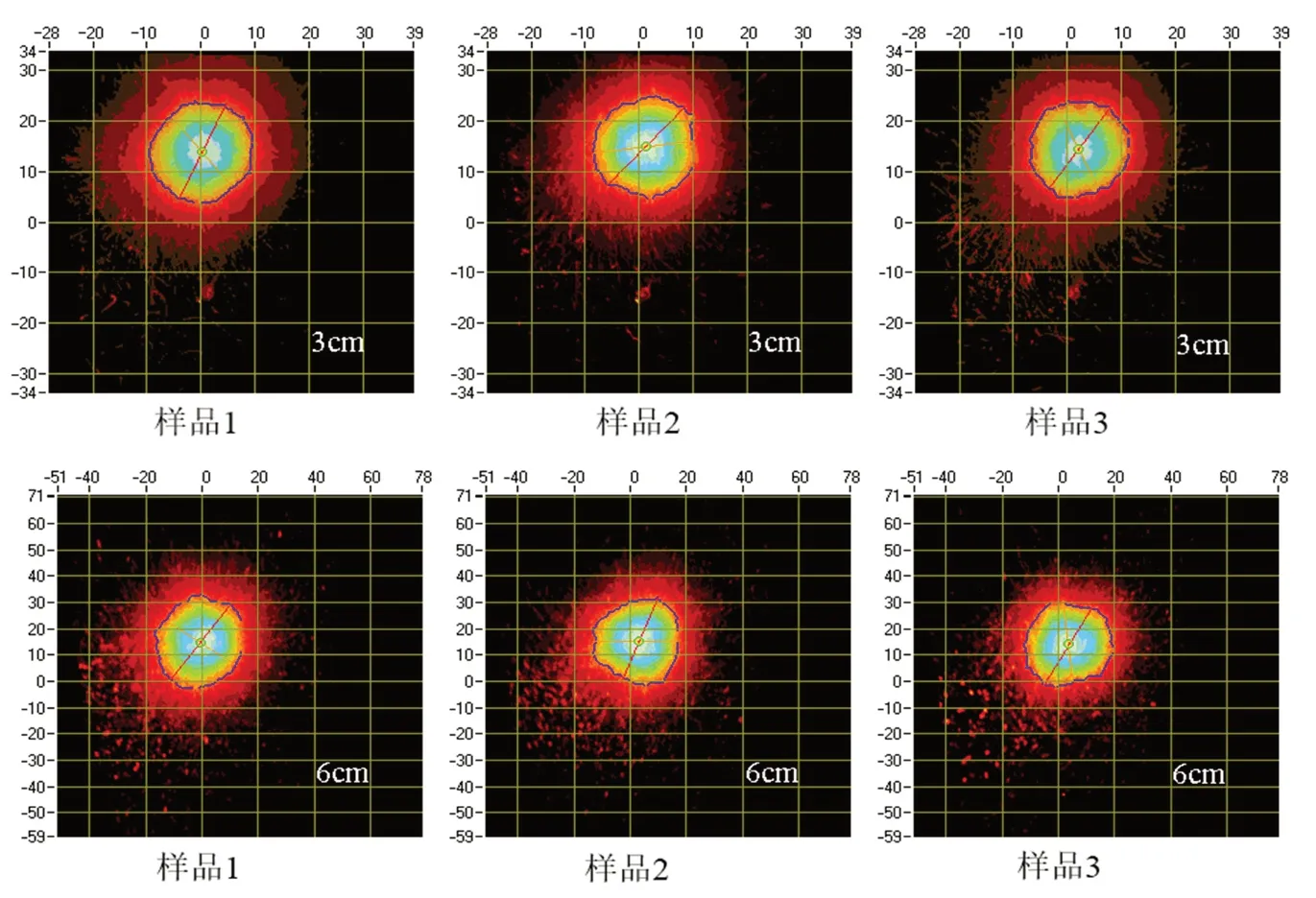
图4 不同样品在不同检测距离下的喷雾模式照片Fig 4 Spray pattern images of different samples at different detection distances

图5 不同样品的羽流几何学照片Fig 5 Plume geometry images of different samples
由图4可知,不同检测距离下鼻喷雾剂的喷雾形状都比较规则,接近圆形,且随着检测距离的增加,喷雾形状无明显变化。检测距离为3 cm和6 cm的样品的椭圆率也无明显变化,RSD分别为1.0%、3.1%,表明该鼻喷雾剂重现性较好,在各个方向上的分布比较均匀,有利于药液在鼻腔中的沉积。
由图5可以看出,鱼腥草素钠鼻喷雾剂的喷雾以鼻喷泵喷头为原点,呈扇形分布。由表4可知,喷雾宽度与检测距离为6 cm的Dmax值一致,表明喷雾形状比较规则。该鼻喷雾剂的喷雾角度为31°~35°,RSD为5.8%,表明该鼻喷雾剂重现性较好。
3 讨论
将药物递送至鼻腔是一个复杂的过程,它取决于许多参数,如喷雾产生的原理、鼻喷装置、处方设计以及患者因素等[6]。FDA建议通过递送剂量、体外沉积等[7-8]方面对鼻喷雾剂的体外特性进行评价。多剂量鼻喷雾剂产品,为保证其在使用期间递送剂量的准确性和稳定性,需对产品的启动/再启动、递送剂量均一性进行考察。递送剂量是评估产品使用过程中实际递送剂量与标示量差异的重要指标。递送剂量均一性反映了同一批次间不同鼻喷雾泵递送剂量的差异。通过对递送剂量均一性的控制,保证了药品使用过程中递送剂量的准确性,避免了单次剂量过高超过安全剂量,或者单次剂量过低达不到有效剂量。
鼻喷雾剂的喷雾特性对药物的吸收和疗效有很大影响,特别是雾滴粒径分布和喷雾模式。鼻喷雾剂的雾滴粒径分布[9-10]与药物在鼻腔中的分布与沉积密切相关。雾滴粒径太大,易被鼻黏膜表面的纤毛清除;粒径太小,药物会随呼吸进入肺部。因此,采用激光衍射法对喷雾的雾滴粒径分布进行测试。除此之外,为保证药物在鼻腔中的沉积,同时尽可能减少雾滴进入肺部的风险,采用撞击器法来检测鼻喷雾剂到达肺部的微小粒子的概率。喷雾模式和羽流几何学是评价喷雾性能的重要指标,主要描述鼻喷雾剂在经鼻喷装置雾化后的气溶胶形态。
雾滴粒径分布(激光衍射法)测试中,检测距离为3 cm和6 cm的雾滴粒径分布数据有细微差异,可能是因为测试过程中雾滴发生了聚集、蒸发、二次破裂等[11]原因。检测距离为3 cm的D10和D50相对于6 cm小,可能是因为慢速的雾滴在到达激光束之前会在短距离内沉降,另外,本研究中的鼻喷雾剂为水溶液制剂,雾化过程中高速的较小雾滴由于蒸发作用而造成粒径较小;而检测距离为3 cm的D90相对于6 cm大,可能原因为检测距离为6 cm的雾滴相对于3 cm处更分散,大雾滴不易发生聚集,故雾滴粒径相对较小。
鼻喷雾剂药液的流变学性质也会影响其喷雾特性,例如:随着药液黏度的增加,喷雾雾滴会增大,而喷雾面积和喷雾角度会减小[12-13]。本研究中制剂黏度为3.54×10-3Pa·s,与纯水黏度相当,改变辅料用量,制剂黏度无明显变化,故未深入探究黏度对鱼腥草素钠鼻喷雾剂喷雾特性的影响。
本研究参照《中国药典》、美国药典以及FDA发布的相关指南,对鱼腥草素钠鼻喷雾剂的启动/再启动、递送剂量均一性、雾滴粒径分布(激光衍射法、撞击器法)、喷雾模式和羽流几何学进行了评价。结果表明,该鼻喷雾剂的递送剂量均一性、雾滴粒径分布均符合《中国药典》的要求,具有良好的喷雾形态。本研究中的喷雾特性评价指标对鱼腥草素钠鼻喷雾剂的后续工业化开发具有一定的指导意义。

