非编码RNA对昼夜节律调控的研究进展
李海朋 冯玛莉
山西省中医药研究院,山西太原 030000
DNA 中的遗传信息通过RNA 被传递给蛋白质,少数基因组被用于编码蛋白质,剩余不能编码蛋白质的转录本则被称为非编码RNA(non-coding RNA,ncRNA)[1]。ncRNA 可分为基础结构型RNA和调控型RNA,本文探讨的ncRNA 为调控型RNA。ncRNA 分为长链ncRNA(long ncRNA, lncRNA)、微小RNA(microRNA,miRNA)和环状RNA(circular RNA,circRNA)等。它们参与生物个体的发育与分化、生殖、细胞凋亡和细胞重编程[2]。
随着人们的压力越来越大,昼夜节律紊乱,导致与昼夜节律相关疾病,如心脏病、溃疡等发病率也随之上升。因此,深入了解昼夜节律运行机制对于疾病预防和有效干预至关重要。本文将从昼夜节律、miRNA、lncRNA 及circRNA 四方面探讨ncRNA 对昼夜节律的影响。
1 昼夜节律
昼夜节律是指光敏感生物协调自己的生理和行为,以适应地球时间(24 h)的日常变化[3]。昼夜节律系统主要由两部分组成:服务时钟和客户时钟。服务时钟位于下丘脑的视交叉上核(suprachiasmatic nucleus,SCN)上,客户时钟以互锁转录/翻译反馈环(translation feedback loop,TTFL)的形式嵌入几乎每个细胞中。此外细胞外囊泡(extracellular vesicle,EV)作为蛋白质和ncRNA 的重要细胞间载体,携带同步信号,并根据服务时钟校正客户时钟[4]。
光刺激通过视网膜向下丘脑传递,SCN 直接响应光刺激而重置其时钟阶段。哺乳动物的TTFL 为:蛋白脑和肌肉芳烃受体核转位蛋白1(brain and muscle Arnt-like 1,Bmal1)和昼夜运动输出周期蛋白(circadian locomotor output cycles kaput,clock)相互结合形成异源二聚体,复合物与周期蛋白(period homolog,per)、促进隐花色素(cryptochrome homolog,cry)中的E-box 调节元件结合。但per和cry 在表达成熟时,会形成新的蛋白复合物,抑制Bmal1 和clock 活动。当per 和cry 的mRNA 水平下降时,per-cry 复合物降解,开始新的循环,形成生物钟[5]。除核心回路外,还有两个子回路,它们与核心回路协同完成振荡。第一个由视黄酸受体相关的孤儿受体(retinoic acid receptor-related orphan receptor,ROR)和孤儿核激素受体(reverseerythroblastosis,Rev-erb)组成。Rev-erb 和Ror 与Ror 结合元件(retinoic acid receptor-related orphan receptors elements,Rore)竞争性结合,Rev-erb 抑制Bmal1 和clock 的表达,而ROR 反而激活clock和Bmal1。第二个由D-box 相关蛋白组成,包括D-box 结合蛋白(D-box binding protein,DBP)、促甲状腺激素胚胎因子(thyrotroph embryonic factor,TEF)和肝白血病因子(hepatic leukaemia factor,HLF)。这些蛋白质和核因子与白细胞介素3 调节蛋白(nuclear factor interleukin-3-regulated protein,NFIL3)相互作用[4]。翻译后进行的磷酸化、乙酰化、糖基化和次酰化等修饰在TTFL 的动力学中同样起着关键作用,尤其是per 和cry 的蛋白的磷酸化对于一个完整的生物钟周期是不可或缺的[6]。TTFL的转录和转录反馈循环通路存在于每个细胞中,在组织器官中也存在生物钟调控模式。
2 miRNA对昼夜节律的影响
miRNA 是由约22 个核苷酸构成的小ncRNA分子,可调控基因表达和作为多种基本细胞过程的关键调控因子,如细胞凋亡、分化、增殖等[7]。miRNA 参与昼夜节律调控况情见图1。
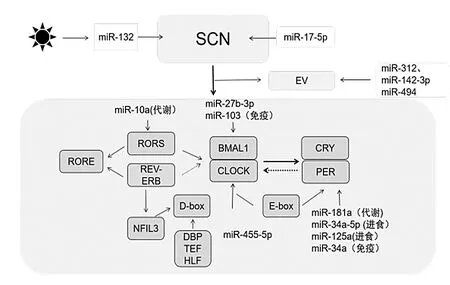
图1 哺乳动物的TTFL 构成及miRNA 对TTFL 的影响
2.1 对SCN的影响
SCN 接收光信号后与中枢神经系统和非中枢神经系统器官进行通信,将客户时钟与环境时间同步[8]。光诱导的miR-132 可减弱重置或夹带时钟的能力,它的直接靶标是参与染色质重塑和翻译控制的基因,这些基因的协调调节是miR-132 依赖性调节per 基因表达和时钟夹带的基础。并证明miR-132/212 的基因消融改变了夹带的周期和SCN中per2 表达的光周期[9]。与肿瘤相关的miR-17-5p在小鼠的SCN 中有节奏地表达,它的增加和减少均会导致cry1 水平的增加和自由运行期的缩短,miR-17-5p 通过与clock 相互作用,在检查和稳定生物钟周期方面发挥重要作用[10]。
神经内分泌通路控制SCN 诱导的外周效应,包括自主神经系统的神经末梢诱导肾上腺素/去甲肾上腺素的释放、下丘脑-垂体-肾上腺轴诱导肾上腺释放糖皮质激素和激活松果体诱导褪黑激素释放[11]。其中褪黑激素是调节日常和季节性节律的关键激素,有研究发现miR-7 在猪松果体细胞中特异性表达并调节褪黑激素的合成[12]。
2.2 对TTFL的影响
对TTFL 的调控表现在对核心基因和核心钟基因转录翻译后修饰的影响。miRNA 对转录翻译的影响如上文所示:miR-132 的直接靶标是参与染色质重塑和翻译控制的基因,从而影响昼夜节律。miRNA 对核心钟基因调控的机制为与其3’-非翻译区(3’-UTR)的互补区域结合,抑制它们的翻译并增强mRNA 的降解。例如miR-455-5p 与clock的3’-UTR 结合并调节其稳定性[13];同样荧光素酶报告显示miR-27b-3p 以剂量依赖性方式抑制Bmal1 的3’-UTR 活性,降低了Bmal1 的蛋白表达水平并损害了内源性Bmal1[14]。miRNA 对核心钟基因的影响,在不同的组织会产生不同的生物节律,比如代谢、进食、先天免疫和休息运动等生物节律。
2.2.1 代谢节律 肝脏的昼夜节律在维持代谢稳态中起重要作用。miR-10a 调节各种肝脏代谢基因,直接抑制RORA 的表达,下调Bmal1 的表达,同时抑制了脂质合成基因、脂肪酸合酶、糖异生、蛋白质合成和胆汁酸合成,这些导致昼夜节律紊乱和肝损伤[15]。同样miR-181a 增加了脂肪的产生,在永生化骨髓来源的基质细胞以及原发性患者脂肪来源的基质细胞脂肪生成过程中发现,miR-181a 通过靶向per3 产生了脂肪[16]。
2.2.2 进食节律 当进食规律改变时,生物钟基因会相应的改变。白天进食时改变了per1 的峰值,并且在切除80%小肠的小鼠发现miR-125a 的含量增加[17]。在研究前额叶皮层中的外围昼夜节律振荡器参与食物奖励诱导活动的机制实验中,发现miR-34a-5p 在大鼠的前额叶皮层诱导节律时钟基因表达,尤其是per2 和clock,改变大鼠的进食规律[18]。
2.2.3 免疫 昼夜节律紊乱会增加肝细胞癌、肺癌和结肠直肠癌等癌症发生的概率。per1 通过在细胞周期、生长和凋亡过程抑制细胞生长,miR-34a将per1 作为靶标可控制细胞生长和死亡平衡并降低肿瘤的生长[19]。Bmal1 诱导miR-103 的表达,对大鼠脑动脉钙通道的昼夜节律进行调节,改变大鼠脑血管收缩力,从而增强大鼠的免疫力[20]。
2.2.4 睡眠节律 强烈的压力和记忆会改变动物的快速眼动睡眠,所以在休克的动物发现其基底外侧杏仁核的miRNA 表达改变和快速眼动睡眠减少。将miR-221 显微注射到中基底外侧杏仁核中,减弱了快速眼动睡眠的减少[21]。将小鼠植入生物遥测单元,连续记录脑电图/肌电图生物电位3 d。发现与对照小鼠相比,miR-155 敲除小鼠的非快速眼球运动、快速眼球运动睡眠次数和脑电波慢波反应均降低[22]。
2.3 对EV的影响
EV 是一组异质的细胞衍生的膜结构,包括外泌体、微泡和凋亡小体。外泌体和微泡存在于生物体液中,参与多种生理和病理过程。EV 现在被认为是细胞间通信的额外机制,允许细胞交换蛋白质、脂质和遗传物质[23]。
最近发现EV 会影响昼夜节律系统。首先EV调节促使per 乙酰化的沉默调节蛋白1[24]、调节cry和Bmal1/clock[25]。小鼠血清中的miR-494、miR-152和miR-494 在介导外周昼夜节律振荡器节律性中发挥作用,现发现这3 种miRNA 在微泡中富集。并且miR-142-3p 通过囊泡运输在细胞之间进行交流,当抑制囊泡运输时,整体时钟基因节律会被改变[11]。
3 lncRNA对昼夜节律的调控
lncRNA 是一类长度至少为200 个核苷酸的线性RNA 转录本,虽然lncRNA 的数量远大于miRNA,但其调控基因表达的机制尚不完全清楚。与miRNA 类似,lncRNA 在视网膜、肝脏和松果体中呈昼夜节律性或差异性表达。在对恒定黑暗和恒定光照条件下,斑马鱼幼虫下分别有269 和309 个lncRNAs 显示昼夜节律[26]。
lncRNA 可以靶向钟基因影响昼夜节律。结肠炎相关的lncRNA(Lnc-UC)可通过组蛋白3降低自身基因沉默活性,增强Rev-erb 转录和表达。Lnc-UC的循环表达由Bmal1 通过E-box 元件产生,这些将生物钟与结肠炎联系起来。并且发现Lnc-UC 敲除的小鼠昼夜节律紊乱和对结肠炎敏感[27]。用非酒精性脂肪性肝病啮齿动物模型进行lncRNA 微阵列,发现lncRNA,例如FLRL1、FLRL6 和FLRL2 参与了昼夜节律,其中干扰FLRL2 表达会影响Bmal1的表达,此外FLRL2 还参与Bmal1 介导的非酒精性脂肪性肝病发病机制[28]。TCONS_00044595 在松果体中高度富集,并具有节律性。它受抑制时可以减轻糖氧剥夺条件下培养的松果体细胞和缺氧缺血性脑损伤后松果体体内的clock 激活。miR-182 可以调节松果体时钟表达,并靶向TCONS_00044595和clock 影响昼夜节律[29]。
4 其他ncRNA
circRNA 是一组具有共价闭合连续环的ncRNA,可作为miRNA 海绵,包含数个与一个或多个不同的miRNA 互补的结合位点,并在转录后的基因调控中发挥作用[30]。现也发现部分circRNA 可调节昼夜节律。首先circRNA 具有昼夜节律性,将松果体进行转录组分析后获得了40 个差异表达的circRNA,其中20 个circRNA 在白天显著上调,20 个circRNA 在夜间显著上调[31]。CircR-WNK2 存在于大鼠的松果体、视网膜和脑中,并且在松果体和视网膜中高表达。通过竞争性内源性RNA 机制参与调节褪黑激素的分泌。当circR-WNK2 敲低时,miR-328a-3p 表达上调并抑制芳香胺-N-乙酰基转移酶mRNA 表达。现其他ncRNA 对昼夜节律的调控尚未发现。
5 小结
本文从服务时钟、客户时钟和EV 三方面讲述了miRNA 对昼夜节律的影响。miRNA 对SCN 调控主要通过miR-132 减弱重置或夹带时钟。光通过视网膜被传递到SCN,经过处理和整合后,再通过激素和自主神经系统将环境信息传递到外周组织的子时钟中。不同的组织的昼夜节律主要依靠TTFL 来完成。miRNA 可以调控哺乳动物的代谢、进食、先天免疫、和休息运动节律等。EV 作为蛋白质和ncRNA 的重要细胞间载体,EV 会携带ncRNA 影响昼夜节律。后续不仅要检测EV 携带的其他昼夜节律相关分子,而且要验证这些分子的具体功能及miRNA 对其影响。
目前lncRNA 调控昼夜节律的机制还不完全清楚,但有学者认为lncRNA 的调节机制与miRNA的类似[32]。miRNA 的节奏表达通常由核心时钟驱动,核心时钟基因形成互锁转录反馈回路。这些转录因子也被证明可以调节lncRNA 的节律表达。lncRNA 调节昼夜节律的机制是否与miRNA 一致需要进一步探讨。其他ncRNA 对昼夜节律的影响的研究较少,后续也可进一步研究其他ncRNA 对昼夜节律的调控。

