视神经纤维层厚度分析在利奈唑胺中毒性视神经病变中的应用价值
张彦坤 关艳 田净净 翟静洁
利奈唑胺(Linezolid,Lzd)是一种应用于严重革兰阳性球菌感染,同时具有良好的抗结核分枝杆菌作用的药物,临床应用广泛,是耐药结核病治疗方案中的核心药物之一。随着利奈唑胺治疗时间的增加,其引起视神经病变等不良反应的风险也持续上升,而国内外文献报道多为个案,我院作为河北省传染病医院,收治耐药结核病患者较多,本研究对我院耐药结核病患者应用Lzd所致视神经病变患者视神经纤维层厚度变化规律进行分析,对视神经不良反应做到早期发现,避免不可逆视力丧失,以期为Lzd的临床合理用药提供参考依据。
1 资料与方法
1.1 一般资料 纳入2018年9月至2020年9月就诊于我院的确诊为耐多药结核病(multiple drug resistant tuberculosis, MDR-TB )的42例患者作为病例组,按照抗 MDR-TB 的治疗指南,其中包含利奈唑胺用药治疗的患者:年龄18~60岁,平均(35.98±2.73)岁。同期纳入采用初治肺结核抗结核治疗方案为HRZE(异烟肼片、利福平胶囊、吡嗪酰胺片、乙胺丁醇胶囊)的42例患者作为对照组,均排除外伤、疾病、药物所致的视神经损伤,双侧视功能正常,眼压<21 mm Hg,其中男21例,女21例;年龄18~60岁,平均(31.84±2.81)岁。2组性别比、年龄差异无统计学意义(P>0.05)。
1.2 纳入与排除标准
1.2.1 纳入标准:①研究中均接受包含利奈唑胺在内的抗结核治疗,既往未接受过利奈唑胺治疗;②治疗前和视功能正常;③治疗前治疗中均采用光学相干断层扫描技术(OCT)测量RNFL厚度;④诊断明确,临床资料完整。
1.2.2 排除标准:①中枢神经系统疾病;②其他药物中毒性视神经病变;③内眼手术史;④其他影响视功能的眼病;⑤哺乳期或妊娠期女性。
1.3 方法 对照组和病例组患者均接受最佳矫正视力、裂隙灯显微镜下眼前节检查、眼底镜检查、眼压、眼底照相等眼科常规检查。用OCT测量对照组常规抗结核治疗和病例组加用利奈唑胺抗结核治疗前、治疗1个月、治疗6个月及停药2个月时的RNEL厚度。被检者正常瞳孔大小,坐位,额部紧贴额托,下颌在下颌托内,仪器旁刻度线与被检者外眦呈水平线。调整为视神经扫描模式,扫描深度为2 mm,横向分辨率为10 μm,轴向分辨率为5 μm,调节OCT注视点位置,嘱被检者注视前方米字线中央,使视盘介于显示器上眼底图像正中央。调节患眼与OCT扫描镜头的前后距离直至产生视盘扫描断层图,根据患者实际情况调节屈光度,待出现清晰断层图。将扫描圆环的内环套住视盘,长时间按住扫描按钮,短按扫描按钮后自动进行截图。待OCT测量RNFL厚度采集工作完成后,系统自动算出视盘周围RNFL厚度,统计各部位象限及全周RNFL的平均厚度。
2 结果
2.1 2组不同时间点的RNFL厚度分析 2组治疗前、治疗后1个月视盘颞侧、上方、下方、鼻侧及平均RNFL厚度差异无统计学意义(P>0.05);病例组治疗后6个月,视盘颞侧、上方、下方、鼻侧及平均RNFL厚度均大于治疗前及治疗后1个月,差异均有统计学意义(P<0.05)。见表1。
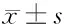
表1 对照组和病例组不同时间点的RNFL厚度分析 n=42,μm,
2.2 治疗6个月后病例组与停药2个月后RNFL厚度分析 发生视力下降及眼部体征变化者停药2个月后视盘颞侧、上方、下方、鼻侧及平均RNFL厚度均小于治疗后6个月,差异均有统计学意义(P<0.05)。见表2。
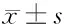
表2 病例组治疗后6个月与停药2个月时RNFL厚度分析 n=42,μm,
2.3 典型病例
2.3.1 患者,女,25岁,耐药型肺结核,抗结核方案中加用利奈唑胺,服药前视神经纤维层厚度正常,服药6个月时检查眼底发现视盘边界欠清,视网膜前出血,视神经纤维层厚度较前增厚,停药1个月后,视网膜前出血完全吸收,视神经纤维层厚度较前下降,结核科医师为控制患者全身情况,嘱患者再次服用利奈唑胺1个月后,视神经纤维层厚度再次增厚。该病例排除其他因素,在应用利奈唑胺后出现视力下降及眼部体征,用药时长与视神经厚度呈正相关性。见图1。
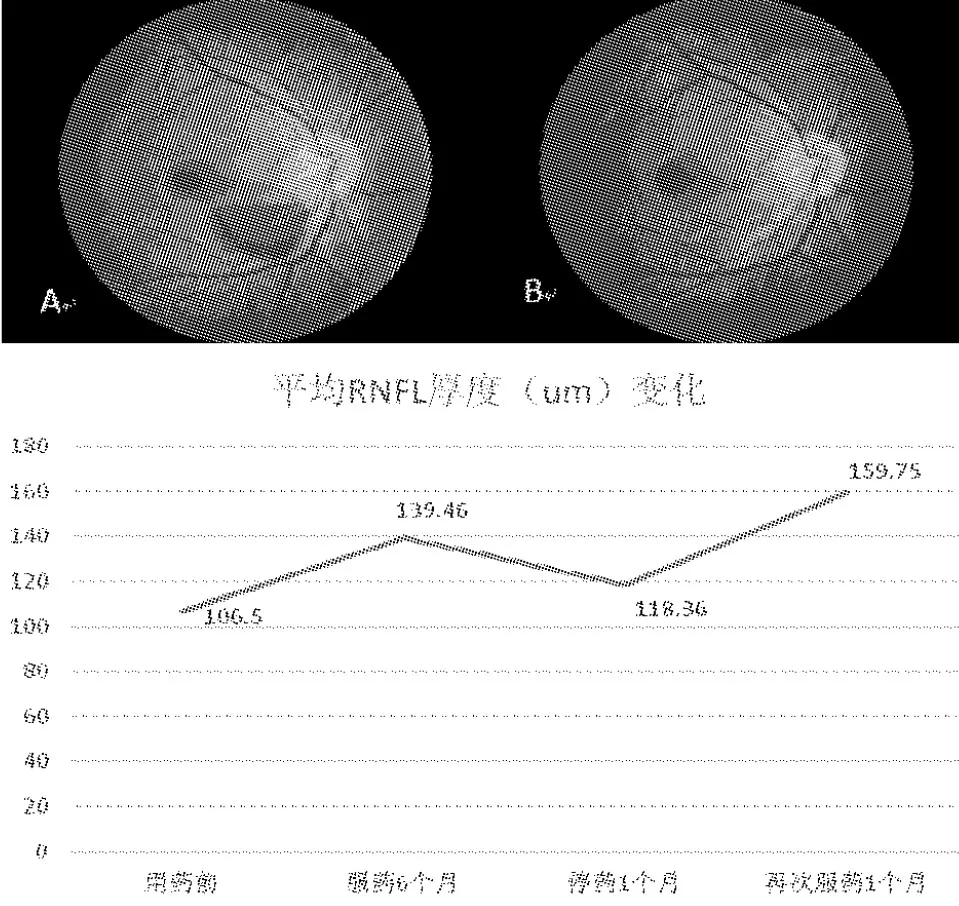
图1 图A:服用利奈唑胺6个月,患者出现右眼视盘边界欠清,视网膜前出血;图B:利奈唑胺停药后1个月,右眼视网膜前出血完全吸收;图C:服药前视神经纤维层厚度正常;服用利奈唑胺6个月,视神经纤维层厚度增厚;利奈唑胺停药后1个月,视神经纤维层厚度恢复;再次服药1个月后,视神经纤维层厚度再次增厚,视神经水肿。
2.3.2 患者,男,21岁,耐药型肺结核,抗结核方案中加用利奈唑胺,正常服药前RNFL厚度为正常范围,服药6个月时发现RNFL厚度较前增厚,未干预继续用药,服药10个月时RNFL厚度明显增厚,停用利奈唑胺1个月,RNFL厚度逐渐恢复至正常,RNFL厚度平均值随用药时间及停药后变化,从最初的103 μm增厚至最高145 μm,停药后恢复至102 μm。见图2。

图2 RNFL厚度平均值随用药时间及停药后变化
3 讨论
据世界卫生组织估计,XDR-TB是目前最为严重的一种结核病,治愈率很低,病死率极高[1]。据有关报道,2005 年全球耐多药病例中,中国、印度和俄罗斯3个国家拥有的结核病耐多药患者数约占全球的 62%[2]。中国是结核病耐药程度较高的国家之一,世界卫生组织将我国列为 “特别引起警示的国家和地区”之一[3]。我国 MDR-TB 疫情形势严峻,据全国结核病耐药基线调查报告结果表明,在 WHO 认定的 27 个MDR-TB 及 XDR-TB 高负担国家中,我国已高居榜首[4]。
2018年WHO将抗MDR-TB 的治疗指南中的药物分为3组,即A组左氧氟沙星,莫西沙星,贝达喹啉,利奈唑胺,普瑞马尼B组氯法齐明,环丝氨酸/特立齐酮 C组 乙胺丁醇,德玛替尼,吡嗪酰胺,亚胺培南—西司他定或美罗培南,乙硫异氨酸或丙硫异氨酸,对氨基水杨酸,帕斯烟肼,阿米卡星(链霉素或卷曲霉素) 。MDR-TB的治疗需要A和B组药物的连用(选取4种核心药物),C组为补充药物(即如果A组或B组中某种药物发生耐药,不能组成有效的治疗方案则选择该组药物)[6]。
本研究中的利奈唑胺为治疗耐药结核病的唑烷酮类药物的代表,是人工合成的一种新型噁唑烷酮类抗生素药,临床上主要对耐药的革兰氏阳性菌敏感[7]。通过干扰mRNA在核糖体内的翻译蛋白过程而阻断细菌的生长和繁殖。在早期的临床试验中,该药可实现MDR-TB患者培养物有效转化。但统计显示,40%~90%的患者遭受不良反应,6%~8%的患者由于神经性病变及骨髓抑制而停用该药物,因此,该药由于其毒性而在抗结核的治疗中受到限制[8];但在2019 版中国 MDR-TB 和 RR-TB 治疗专家共识中,利奈唑胺依旧为MDR-TB的核心治疗药物[9]。目前认为利奈唑胺引起视神经病变的机制是药物相关的线粒体毒性,其通过干扰线粒体氧化磷酸化而损伤视神经,大部分报道认为利奈唑胺引起的视神经病变需要数月甚至1年或更久[10-14]。视神经对线粒体依赖性较强,因而易受到线粒体损伤的影响[15],继而产生视神经炎的一系列症状。
利奈唑胺中毒性视神经病变的发病较迟缓,以视力下降、复视等症状为主要表现,双眼多同时受累,并且在早期的眼底检查多无异常改变。OCT是测量RNFL厚度的主要仪器之一,其分辨率高,无侵入性,可重复性高,能够进行清晰、直观的活体生物组织成像[16]。通过OCT检查定期监测利奈唑胺服用者早期变化,并及时停用药物对患者视觉功能恢复有一定作用。本研究对利奈唑胺服药者进行随访观察,通过临床测定服药者RNFL厚度,有效地评估了视神经损伤情况,及时对服用该药过程中出现的不良反应作出预警评判。利奈唑胺的用药时限为28 d实际临床应用中利奈唑胺属超说明书用药,使用疗程往往在6个月至1年,为了更安全用药,利用OCT无侵入精准监测RNFL厚度是一种必要的方法。
考虑利奈唑胺致中毒性视神经病变诊断时,我们需要排除结核感染及相关性视神经病变。结核感染性视神经病变是由于结核杆菌直接侵犯视神经所致,很少单独发生,在眼部常合并葡萄膜炎、视网膜血管炎等。结核感染相关性视神经病变是眼部对结核菌蛋白的变态反应所致,对糖皮质激素治疗有效[17]。 本研究中的42例病例组患者停用利奈唑胺后,视力很快得到明显的改善,且未用糖皮质激素治疗。因此,可以排除结核感染性或感染相关性视神经病变,利奈唑胺中毒性视神经病变诊断明确。
有研究发现,神经系统病变不良反应出现在使用利奈唑胺治疗的10 d~36个月,平均7.9个月[10]。视神经不良反应可完全或部分恢复,在停药后几个月中视力和色觉会明显恢复,但周围神经病变的恢复较为有限[18]。本研究通过42例病例组患者发现利奈唑胺中毒性视神经病变和利奈唑胺治疗时间有直接关系,服用药物时间较长者视力下降风险显著增加。在治疗1个月时平均RNFL厚度与对照组无显著差异,平均在治疗6个月时患者的视盘颞侧、上方、下方、鼻侧及平均RNFL厚度较治疗前明显增加,表明利奈唑胺中毒性视神经病变发生和患者用药疗程有关。且因个体差异不同,患者颞侧RNFL厚度较对照组比较变化最大,表明视盘颞侧RNFL最先受累,且损伤最为严重。可能因为视盘颞侧的乳斑束神经纤维容易发生代偿性肿胀,从而使颞侧RNFL厚度增加更为明显。因此临床对于服用利奈唑胺患者应定期监测RNFL厚度情况。
综上所述,RNFL厚度变化早于患者视功能异常,使用利奈唑胺治疗的患者应定期随访,以早期发现其视神经毒性表现,利奈唑胺中毒性视神经病变能够引起视盘周围RNFL厚度增加,用OCT作为利奈唑胺长期服药者的随访能够直观反映RNFL厚度变化情况。

