果胶钡凝胶胃内滞留释药系统制备与体外评价
王家玉,李 琳,陈 琳
(重庆医科大学附属妇女儿童医院(重庆市妇幼保健院) 药学部,重庆 401147)
双嘧达莫(dipyridamole,Dim)临床用于防治心绞痛和抗血小板凝集、防治血栓形成,通常需长期服用。但Dim具有pH溶解依赖性,在胃中酸性条件(37 ℃,pH 1.0)下溶解度较高,而在肠道碱性条件(37 ℃,pH 7.0)下溶解度极低,这种特性造成口服Dim在胃肠道中吸收、溶出不规则,个体吸收差异性大。这种pH溶解依赖性是造成Dim生物利用度较低的主要原因[1-2]。
胃漂浮型制剂是一类能延长制剂在胃内滞留时间,增加药物胃吸收程度的新型制剂[3]。果胶(pectin,Pct)是一种以多聚D-半乳糖醛酸为主链的水溶性多糖,具有良好的生物相容性和安全性。Pct分子中的羧基可与一些二价、三价金属离子反应形成网络结构的凝胶。Pct金属离子凝胶结构在胃中酸性条件下较稳定[4-5]。
本文以Pct为载体材料,钡离子为交联剂,碳酸氢钠为制泡剂,制备了果胶钡凝胶胃漂浮微丸(Dim-Ba)。为改善Dim在酸性条件中的突释,我们选取不同类型的聚丙烯酸树脂材料用于制备Dim固体分散体,再将载药固体分散体包入果胶钡凝胶微丸中。通过实现Dim在胃内持续释药,有望解决药物的pH溶解依赖性问题,实现药物在胃部的靶向缓释,长时间维持有效血药浓度,提高生物利用度。
1 仪器与材料
1.1 仪器
UV-3150型紫外分光光度仪(日本岛津公司);AR2140精密电子天平(美国OHAUS公司);85-2数显恒温磁力搅拌仪(上海司乐仪器有限公司);SHZ-88台式水浴恒温振荡仪(江苏太仓市实验设备厂);实验用水为超纯水,其他试剂均为分析纯。
1.2 试药
Dim(芮城县虹桥药用中间体有限公司);Pct(衢州果胶有限公司,酯化度15 %~25 %,黏度为0.015 Pa/s);Eudragit L100(L100,德国ENOVIK公司);Eudragit RLPO(RLPO,德国ENOVIK公司)。
2 方法与结果
2.1 载药胃漂浮微丸的制备
2.1.1 Dim果胶钡凝胶胃漂浮微丸(Dim-BaPct)的制备 精密称取适量Dim和碳酸氢钠(1.75 %,w/v),溶解于适当浓度的Pct溶液中,搅拌使其充分分散,然后将混悬液经9号针头滴入快速搅拌中的氯化钡醋酸溶液中,针头距液面8 cm,固化交联15 min,漏斗过滤,超纯水洗涤多次,40 ℃烘箱干燥1 h,即制得Dim-BaPct[6]。
2.1.2 载Dim固体分散体胃漂浮微丸(DimSD-BaPct)的制备 称取Dim,L100和RLPO适量,溶于甲醇和二氯甲烷(1:1,v/v)混合溶液,55 ℃水浴蒸干,40 ℃真空干燥12 h,充分碾磨后过100目筛,制得双嘧达莫固体分散体(DimSD)[7-8]。精密称取适量DimSD和碳酸氢钠(1.75 %,w/v),按2.1.1项下方法操作,制得载DimSD胃漂浮微丸(DimSD-BaPct)。
2.2 微丸粒径的测定
取适量DimSD-BaPct,使用标尺测量微丸直径,计算平均粒径和相对标准偏差。见图1。其外观圆整,大小均匀。将多颗微丸平行排列后测得其平均粒径(1.6±0.11)mm。

图1 微丸外观
2.3 溶胀率的测定
分别称取适量Dim-BaPct、DimSD-BaPct,投入盛有100 ml人工模拟胃液(HCl溶液,pH 1.2)的锥形瓶中。将锥形瓶置于恒温振荡仪中,转速75 r/min,温度37 ℃,测定两种微丸的溶胀情况。分别于15 min、30 min、1 h、2 h、3 h、4 h、5 h取出微丸,用滤纸吸干微丸表面水分,记录微丸此时质量Wt。按下式计算微丸溶胀率。结果见图2。
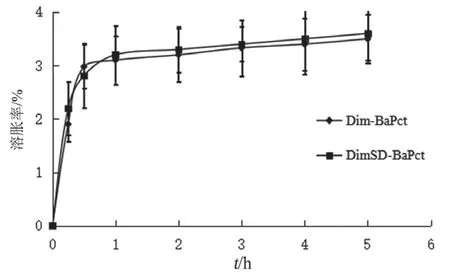
图2 Dim-BaPct和DimSD-BaPct在人工模拟胃液中的溶胀曲线(n=3)
其中,S为溶胀率,W0为微丸初始质量,Wt为溶胀过程中微丸不同时间点的质量。
由图2可见,在人工模拟胃液中,DimSDBaPct和Dim-BaPct均在1 h左右达到溶胀平衡。同时,固体分散体对于微丸的溶胀行为没有显著影响。
2.4 微丸漂浮性的测定
随机选取100颗Dim-BaPct和100颗DimSDBaPct,分别放入有100 ml人工模拟胃液的锥形瓶中,并将锥形瓶置于恒温水浴振荡仪,设置转速为75 r/min,温度为37 ℃,分别在1,2,3,4,5,6,7,8,9 h观察漂浮于液面的微丸数量,按公式计算漂浮率。
漂浮率(%)=漂浮的微丸数/100×100
Dim-BaPct和DimSD-BaPct在人工模拟胃液中持续9 h的漂浮率为96.33 %±1.15 %(n=3),Dim-BaPct和DimSD-BaPct均具有良好的漂浮性。固体分散体对微丸的漂浮性能没有显著影响。
2.5 标准曲线的制备
以人工模拟胃液配制Dim溶液,经紫外扫描确定Dim最大吸光度波长为283 nm,辅料在此波长处基本无吸收,因此以283 nm作为Dim的测定波长。精密称取Dim 10.0 mg,置于50 ml量瓶中,加人工模拟胃液至刻度,制得储备液。精密移取100,200,300,400,500,600,700 μl储备液至5 ml量瓶中,用人工模拟胃液稀释至刻度,摇匀,在283 nm波长处测定紫外吸收度(A)值,以A对相应的浓度(C,μg/ml)做线性回归,得标准曲线回归方程:A=19.67C+0.0078(r=0.9991)。
2.6 体外释放度的测定
取适量微丸,置于有100 ml人工模拟胃液的锥形瓶中,置于水浴恒温振荡仪,转速75 r/min,温度37 ℃,分别在0.5,1,2,3,4,5,6,9 h取出3 ml释放介质,同时补入同温介质3 ml。样品在4000 r/min下离心10 min,取上清0.5 ml,用人工模拟胃液定容至5 ml,于283 nm处测定样品的吸光度(A)值。按2.5项下标准曲线回归方程计算样品中Dim浓度及微丸在不同时间点的累积释放率。
2.6.1 Pct浓度对Dim-BaPct中药物释放行为的影响分别取4 %,7 %,10%Pct溶液10 ml,按2.1.1项下方法制备胃漂浮微丸(4%Dim-BaPct,7%Dim-BaPct,10%Dim-BaPct),测定Dim在人工模拟胃液中的累积释放度。结果见图3。3种微丸中的药物在1 h之内均基本释放完全,不同浓密Pct交联制备的载药微丸在人工模拟胃液中释药无明显差异,表明增加Pct浓度对Dim释放曲线无显著影响。产生这种现象最可能的原因是凝胶骨架结构空隙较大,难以阻滞Dim从微丸中快速释放。Dim-BaPct中的药物释放为扩散型,酸易溶性小分子药物在人工模拟胃液中表现为速释。
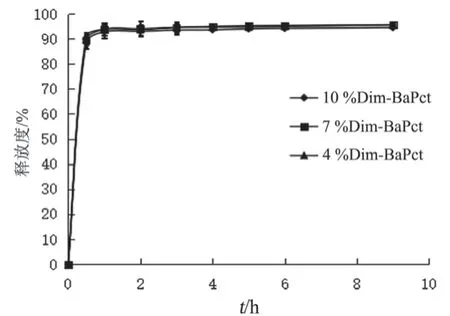
图3 Dim-BaPct在人工模拟胃液中释放曲线(n=3)
2.6.2 L100用量对DimSD-BaPct释药行为的影响 为改善Dim-BaPct在人工模拟胃液中的药物突释,酸性条件下不溶的L100被选为载体材料用于制备Dim固体分散体。按1:1,2:1,3:1的载体材料与药物摩尔比,分别精密称取L100和Dim,按2.1.2项下方法制备DimSD-BaPct,测定药物在人工模拟胃液中的累积释放度。结果见图4。
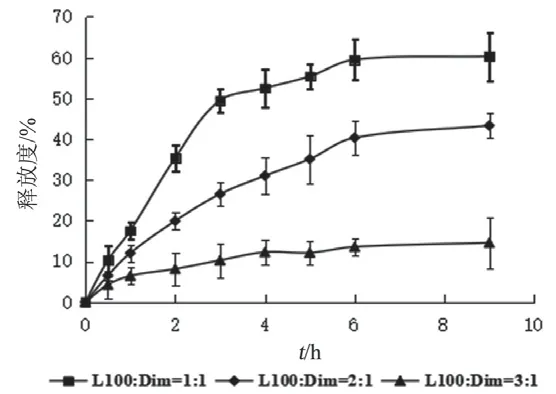
图4 按不同L100:Dim制备的DimSD-BaPct在人工模拟胃液中的释放曲线(n=3)
由图4可见,随着L100:Dim的质量比增加,Dim释放速率和累积释放度均随之下降,持续释放时间超过6 h,表明L100固体分散体可有效延缓Dim在人工模拟溶液中的释放,延长药物释放时间。造成该现象的可能原因是L100为肠溶性材料,能阻滞酸性溶液的渗入,减慢Dim在人工模拟胃液中的溶解。当L100:Dim=1:1时,Dim 9 h的累积释放率为55 %左右, L100:Dim=3:1时,9 h的累积释放度下降至15 %左右,分析原因是Dim被L100固体分散体包埋较深,导致Dim难以从微丸中扩散并释放出来。L100的比例越高,累积最大释放率越低。
2.6.3 L100、RLPO用量对DimSD-BaPct释药行为的影响 为提高DimSD-BaPct在人工模拟胃液中的最大药物累积释放率,亲水性材料RLPO和酸性条件下不溶的L100共同作为载体材料用于制备Dim固体分散体。按1:1:1,1:1:2,1:1:3的比例,分别精密称取L100、Dim和RLPO,按2.1.2项下方法制备DimSD-BaPct,考察Dim-SD-BaPct在人工模拟胃液中的释放行为。结果见图5。
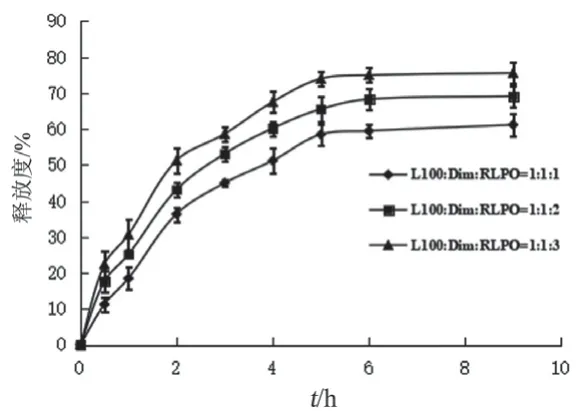
图5 不同用量L100、RLPO制备的DimSD-BaPct在人工模拟胃液中的释放曲线(n=3)
由图5可见,随着RLPO用量的增加,Dim最大累积释放率显著提高。当L100:Dim:RLPO=1:1:3,6 h的药物累积释放率可升高至70 %左右。RLPO是一种亲水性材料,通过在固体分散体中添加RLPO,使人工模拟胃液更易渗入微丸内部,药物更容易从微丸中扩散并释放出来。
基于L00和RLPO的特性,通过调整固体分散体中两种材料的比例,可按照治疗需要和药物性质获得理想的药物释放速率、药物持续释放时间和最大累积释放率。
2.7 DimSD-BaPct释放率-时间曲线模型拟合
取DimSD-BaPct(L100:Dim=1:1)、DimSDBaPct(L100:RLPO:Dim=1:1:1)和Dim-BaPct的药物释放数据,分别用零级、一级、Higuchi、Korsmeyer-Peppas释放模型拟合,结果见表1。D i m-B a P c t 释放曲线较符合一级释放模型,拟合r值为0.99901。而以L100作为载体材料和联用L100和RLPO作为载体材料所获微丸的释放曲线较符合Higuchi模型,DimSD-BaPct(L100:Dim=1:1)的拟合r值为0.99914,DimSDBaPct(L100:RLPO:Dim=1:1:1)的拟合r值为0.99855。

表1 DimSD-BaPct体外释放数据的模型拟合
3 讨论与结论
前期试验中,研究者分别用1 %,1.5 %,1.75 %,2 %,2.5 %碳酸氢钠制备微丸并考察其漂浮性能。预实验结果表明,5种微丸在外观品质和漂浮性能方面存在显著差异。在漂浮性能方面,随着碳酸氢钠浓度从1 %升高至1.75 %,微丸9 h漂浮率从84 %提升至93 %,微丸具备了良好的漂浮性能。当碳酸氢钠浓度超过1.75 %后,微丸持续9 h的漂浮率均未超过94 %。在外观品质方面,当碳酸氢钠浓度小于1.75 %时,微丸成形性和一致性较好。碳酸氢钠浓度超过1.75 %后,一部分微丸发生破裂,造成该现象原因可能是过多气泡的产生使微丸不易成形,外观一致性不佳。综合考虑,选择最优碳酸氢钠浓度为1.75 %。
本研究中采用的载体材料是低酯果胶,酯化度小于50 %。前期实验中分别用5 %,6 %,7 %,8 %,9 %果胶溶液制备微丸。结果显示,果胶浓度大于8 %时,或小于6 %时,微丸的成形性均不理想。因此,选择果胶溶液浓度为7 %。
载药果胶钡凝胶胃漂浮微丸,可实现药物主要在胃部释放,解决Dim溶解pH依赖性的问题,但果胶钡凝胶微丸难以延迟酸易溶性药物在酸性条件下的快速释放。因此,在本次研究中,具备不同溶解特性的载体材料被用于制备载药固体分散体,并用于制备载药的胃漂浮微丸。这种多单元胃漂浮给药系统具有较高的安全性、生物相容性及释放可调节性,具有良好的应用前景。

