度普利尤单克隆抗体治疗儿童中重度特应性皮炎的疗效与安全性研究
许丽,胡建,石梦醒,孙鑫雨,王雪艳,2,刘长山,2
(1.天津医科大学第二医院儿科,天津 300211;2.天津医科大学儿童呼吸及哮喘研究中心,天津 300211)
特应性皮炎(AD)是常见的过敏性疾病,我国儿童患病率约为13%[1]。AD 常起病于婴儿期,具有慢性、复发、难治的特点,常合并食物过敏、过敏性鼻炎(AR)和过敏性哮喘等过敏性共病[2]。度普利尤单克隆抗体(单抗)是一种拮抗白细胞介素(IL)-4 受体α 亚基(IL-4Rα,是IL-4 和IL-13 的共同受体)的重组人单克隆IgG4 抗体[3],其通过阻断IL-4 Rα抑制2 型炎症的核心和关键驱动因素IL-4 与IL-13 信号的转导[4]。本文回顾性分析了接受度普利尤单抗注射治疗满16 周的17 例中重度AD 儿童患者的临床疗效及安全性。
1 对象与方法
1.1 研究对象 选取2021 年4 月—2022 年9 月就诊于天津医科大学第二医院儿科哮喘和过敏专病门诊并接受度普利尤单抗治疗的中重度AD 患儿17 例。纳入标准:(1)年龄≥3 岁且≤16 岁,均符合中重度AD 诊断标准[5],伴或不伴以下疾病:哮喘[6]、AR[7]、食物过敏[8]。(2)按照指南[9]给予规范的基础治疗、外用糖皮质激素治疗后症状未控制(①外用糖皮质激素配合润肤剂治疗1~2 周后临床症状无明显改善,皮疹有反复;②外用糖皮质激素配合润肤剂治疗后临床症状有改善,但停药后皮疹出现反复或加重)。(3)接受度普利尤单抗治疗,治疗期间可局部外用润肤霜、糖皮质激素。排除标准:对度普利尤单抗所含任何成分过敏者。共纳入17 例患儿,男11 例,女6 例,年龄3~16 岁,中位年龄为9.00(7.00,12.50)岁。AD 病程为(7.29±3.69)年,5 例为中度AD,12 例为重度AD。17 例患儿中11 例同时合并哮喘和AR,其中2 例同时合并哮喘、AR 和食物过敏;2 例仅合并AR;4 例仅诊断为AD。
本研究通过天津医科大学第二医院医学伦理委员会批准(批准文号:KY2021K084),由于度普利尤单抗2021 年9 月于国内获批治疗12 岁及以上青少年中重度AD,2022 年2 月国内获批治疗6岁及以上儿童中重度AD。本研究纳入儿童中共7例为年龄超说明书用药(6 例在2022 年2 月前纳入小于12 岁,1 例在2022 年2 月后纳入小于6 岁),因此治疗前均由患儿家长或法定监护人签署知情同意书。
1.2 研究方法 资料收集:本研究为回顾性研究,一般资料包括年龄、性别、身高、体重等人口学特征和过敏性疾病家族史、AD 病程。临床资料包括AD积分指数(SCORAD)、湿疹面积及严重程度指数(EASI)、源自患者的湿疹评价(POEM)、瘙痒数字评价量表(NRS)、儿童皮肤病生活质量指数(CDLQI)、特应性皮炎控制工具(ADCT)、研究者整体评估(IGA)等临床症状评估量表以及哮喘、AR、食物过敏等过敏性共病临床指标和外周血嗜酸性粒细胞计数(EOS)水平及血清总IgE(T-IgE)水平。记录患儿用药过程中发生的不良反应及不良事件。
临床疗效评估:度普利尤单抗治疗前后AD 临床症状评估量表、过敏性共病改善情况以及外周血EOS、T-IgE 治疗前后的变化。计算治疗16 周期间达到EASI 从基线到16 周降低≥50%(EASI50)和EASI 从基线到16 周降低≥90%(EASI90)的患儿比例以及IGA 评分达到0 或1(皮疹清除或几乎清除)的比例。
度普利尤单抗给药方案:17 例患儿均在医院由护士进行度普利尤单抗皮下注射治疗,注射部位为双上臂。根据患儿体重及年龄段确定首次给药剂量及以后每次给药剂量。由于初始治疗时度普利尤单抗国内尚无200 mg 剂型,所有患儿首次给药剂量为300 mg(1 例初始治疗时体重为93 kg,首次给药剂量为600 mg),之后每2~3 周300 mg 皮下注射维持治疗(8 岁以下或30 kg 以下,每3 周1 次,其余每2 周1 次),所有患儿均完成16 周治疗。
1.3 统计学处理 计量资料符合正态分布以x±s表示,若不符合则以M(Q1,Q3)表示,计数资料以频数(%)表示。治疗前后各评分的比较采用配对样本t检验。余定量指标符合正态分布的采用配对t 检验比较,统计量为t,非正态分布的则采用秩和检验比较,统计量为Z。所有数据利用SPSS23.0 软件进行统计学分析,GraphPad Prism Version 8 作图。P<0.05 为差异有统计学意义。
2 结果
2.1 度普利尤单抗治疗前后各项量表评分的变化情况 度普利尤单抗治疗16 周期间各项量表评分变化情况如表1 所示。与基线相比,注射度普利尤单 抗 后2 周,SCORAD、EASI、POEM、NRS、cDLQI、ADCT 及IGA 即出现显著下降且差异具有统计学意义(均P<0.01)。所有AD 相关量表评分均在16 周治疗期间呈连续下降趋势,但部分相邻随访时间点之间差异无统计学意义。治疗随访期间,达到EASI50 和EASI90 的患者比例以及IGA 评分达到0或1 的患者比例如图1 所示;与治疗2 周后相比,治疗8 周后,达到EASI50、EASI90 及IGA 评分达到0 或1 的患者比例即明显增加,治疗16 周后,达到EASI50 和EASI90 的患者比例分别为100.00%(17 例)及47.06%(8 例),IGA 评分达到0 或1 的患者比例为76.47%(13 例)。

表1 17 例特应性皮炎患儿度普利尤单抗治疗前后7 项指标评分变化[M(Q1,Q3)]Tab 1 Changes in 7 index scores before and after dupilumab treatment in 17 patients with atopic dermatitis[M(Q1,Q3)]
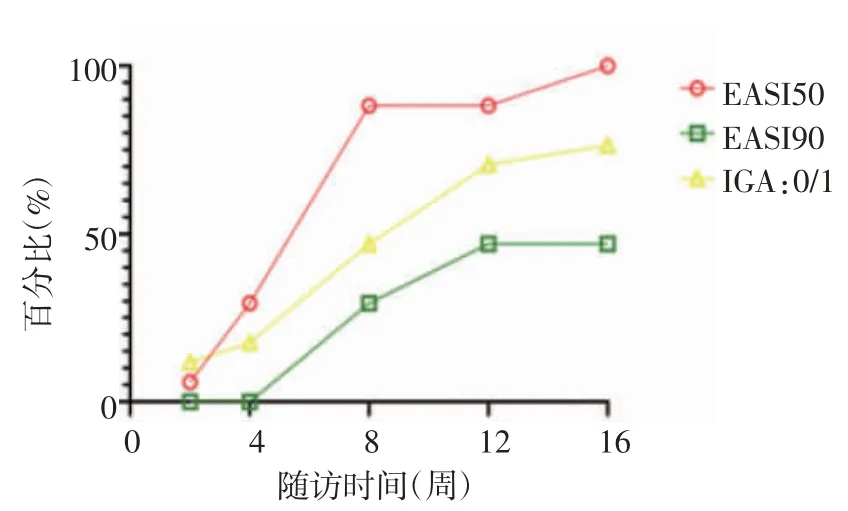
图1 度普利尤单抗治疗期间达到EASI50/90 以及IGA 达到0 或1的患儿比例Fig 1 The proportion of patients achieving EASI50/90 and with an IGA score of 0 or 1 during dupilumab treatment
2.2 外周血EOS 及血清T-IgE 治疗前后变化 度普利尤单抗治疗16 周后,17 例外周血EOS 水平由基线时的0.56(0.36,1.59)×109/L 升至0.81(0.41,1.33)×109/L,但差异无统计学意义。5 例患儿治疗前后均完成血清T-IgE 检测,1 例基线T-IgE 水平>5 000 kU/L,治疗16 周后降至2 759 kU/L,余4 例血清T-IgE 水平由基线的2 273.00(823.00,3 805.50)kU/L 降至846.00(236.88,1 333.25)kU/L,但差异无统计学意义。
2.3 过敏性共病的缓解情况 度普利尤单抗治疗16 周后合并哮喘、AR 患儿的临床症状、肺功能、FeNO 及ICS 剂量改善情况如表2 所示。2 例患儿合并食物过敏,1 例既往食用海鲜、羊肉后AD 皮疹加重,度普利尤单抗治疗8 周后,可进食上述食物,不引起皮疹加重;另1 例既往进食鸡蛋、鳕鱼等食物后AD 瘙痒症状加重,度普利尤单抗治疗12 周后,进食上述食物后瘙痒症状无加重及反复。

表2 度普利尤单抗治疗前后AD 患儿哮喘、AR 的临床指标变化[M(Q1,Q3)]Tab 2 Changes in clinical indicators of asthma and allergic rhinitis in children before and after dupilumab treatment[M(Q1,Q3)]
2.4 安全性评价 治疗期间,3 例患儿出现轻度结膜炎,余未出现明显不良反应,所有患儿均未出现不良事件或因不良事件而停药。
3 讨论
AD 是一种慢性炎症性皮肤病,表现为湿疹性病变和强烈瘙痒症状,与2 型炎症介导的皮肤屏障功能障碍和免疫失调相关[10]。包括儿童在内的中重度AD 患者症状明显,瘙痒和睡眠障碍等症状可导致生活质量下降,引起注意力缺陷障碍、日常生活活动受限以及抑郁和焦虑[11]。2017 年,度普利尤单抗首次在美国被批准用于治疗外用药控制不佳或不建议使用外用药治疗的12 岁及以上青少年、成人中重度AD 患者,并于2020 年在中国获批用于治疗成人中重度AD,2021 年9 月,度普利尤单抗在中国获批用于治疗12 岁及以上青少年中重度AD 患者,2022 年2 月获批用于6~12 岁儿童人群,关于度普利尤单抗在中重度AD 中的应用目前国内已形成专家共识[12]。
Wollenberg 等[13]对两项度普利尤单抗治疗中重度AD 儿童16 周的随机对照试验及其中一项随机对照试验后续持续52 周的开放标签队列研究进行了汇总分析,结果表明,在两项随机对照试验治疗16 周期间,患儿SCORAD 评分呈持续且显著的下降,并在随后的开放标签队列研究中持续改善至52周。另一项纳入成人中重度AD 的随机对照研究通过观察治疗期间IGA 评分达到0/1 的患者比例来评估度普利尤单抗的疗效,结果显示治疗16 周后,度普利尤单抗治疗组IGA 评分达到0 或1 的患者比例显著高于安慰剂组[14]。本研究结果也显示,与基线相比,SCORAD、EASI、NRS 及IGA 等AD 体征相关量表评分在度普利尤单抗首次注射后2 周即出现显著下降,并持续至16 周;与成人中的研究结果一致,本研究结果显示治疗16 周后,实现EASI50、EASI90 及IGA 评分达到0 或1 的患儿比例显著增加。AD 所致的瘙痒和睡眠障碍是导致儿童生活质量下降的主要原因。研究表明,度普利尤单抗治疗期间,患者瘙痒及睡眠障碍程度显著改善,AD相关生活质量明显提升[15-16]。本研究结果也表明,度普利尤单抗治疗16 周期间,患儿生活质量改善显著,POEM、cDLQI 及ADCT 等AD 相关生活质量评分呈持续下降。
与先前的研究一致[17],本研究中5 例患儿数据结果提示度普利尤治疗可能使血清T-IgE 水平下降,主要是由于度普利尤单抗阻断2 型炎症细胞因子IL-4 和IL-13,而这两种细胞因子通常诱导IgE的产生。哮喘、AR 及食物过敏等AD 过敏性共病也主要由2 型炎症介导。2018 年10 月度普利尤单抗获得美国FDA 的批准,用于治疗12 岁以上青少年和成人的中重度哮喘,目前已有研究报道了度普利尤单抗在哮喘中的应用。Bacharier 等[18]研究显示,度普利尤单抗治疗可降低中重度哮喘儿童的哮喘急性发作率,提高哮喘控制水平,并改善患儿肺功能以及气道炎症水平。本研究获得了类似结果,度普利尤单抗治疗16 周后,AD 合并哮喘及AR 患者的C-ACT/ACT、ACQ 及鼻炎VAS 等症状评分均得到显著改善,气道炎症也有明显提升,FeNO 水平及ICS 剂量均较基线显著下降;患儿肺功能也有提升,FEV1 及FEV1/FVC 均较基线提升,但后者差异无统计学意义,可能与患儿哮喘症状不重相关。在另1项病例报道中,1 例患有严重AD 共病食物过敏的患者在接受度普利尤单抗治疗3 个月后,能够耐受2 种先前诱发过敏反应的食物,并且通过口服激发实验得到证实[19]。在本研究中,2 例患者合并食物过敏,既往进食过敏食物可引起AD 症状加重,度普利尤单抗分别治疗8 周、12 周后进食曾过敏的食物未再引起皮疹反复及瘙痒症状加重,其作用机制可能与度普利尤单抗导致的2 型炎症广泛抑制相关,从而使IgE 介导的食物过敏产生耐受。
结膜炎是度普利尤单抗治疗过程中最常见的不良反应之一。在本研究中,3 例患儿分别出现不同严重程度的结膜炎,予对症治疗或未经治疗后自行缓解。其发生机制尚不清楚,可能与度普利尤单抗治疗后抑制眼结膜杯状细胞增殖和黏蛋白分泌相关[20]。同时,研究表明,这一不良反应可能与患者血清EOS 计数增高存在关联,在EOS 增高的患者中,结膜炎的发病率更高,并且嗜酸性粒细胞增高程度与结膜炎严重程度呈正相关,可能与大量嗜酸性粒细胞的结膜浸润导致杯状细胞明显减少有关[21-22];结膜杯状细胞是一种特殊的黏液分泌细胞[23],对维持眼表功能至关重要,度普利尤单抗治疗后患者眼表黏液生成减少,导致泪膜不稳定、眼表黏膜上皮屏障功能障碍,从而易于诱发结膜炎症[20]。本研究中,度普利尤单抗治疗16 周后,患儿外周血EOS 总体呈增高趋势,但无统计学意义,且与结膜炎的发生无明显相关性。未来,还需要更多研究阐述AD 儿童接受度普利尤单抗治疗后嗜酸性粒细胞增高与结膜炎之间是否存在关联及其具体机制。
综上所述,度普利尤单抗治疗中重度儿童AD的临床疗效明确,且不良反应少,并可改善哮喘、AR、食物过敏等过敏性共病。但本研究样本量小,随访时间不长,还需要更多研究进一步明确。

