鼻腔鼻窦球周皮细胞瘤12例临床病理分析
高宇慧,吴建锋
鼻腔鼻窦球周皮细胞瘤(sinonasal glomangiopericytoma, SNGP)是一种发生于鼻腔鼻窦的肿瘤,表现为血管周围肌样分化,同义词为鼻腔鼻窦血管外皮瘤样肿瘤(sinonasal hemangiopericytoma-like tumor)。SNGP于1976年由Compagno和Hyams[1]首次报道,临床较罕见,国内外报道不足200例,发病率不足鼻腔鼻窦肿瘤的0.5%,以女性略多见,发病年龄约70岁。95%的肿瘤发生于鼻腔单侧(5%发生于双侧),常累及副鼻窦,仅副鼻窦受累也有报道。临床以鼻塞和流涕为主要表现;肿瘤呈息肉状,鲜红或粉红色,质软易碎,平均最大径约3 cm[2]。虽然其分子发病机制尚未完全阐明,但近期已在SNGP中发现CTNNB1基因突变和β-catenin核阳性[3-5]。目前,SNGP的临床病理学特征研究有限,国内外也仅有小宗病例报道[6-9]。本文着重探讨SNGP的临床病理学特征、诊断及鉴别诊断,以免误、漏诊。
1 材料与方法
1.1 材料收集2006年5月~2022年2月空军军医大学第一附属医院病理科12例SNGP标本,其中男性7例,女性5例,年龄36~79岁,平均56岁。另收集12例患者的临床、影像学及随访资料。
1.2 方法标本均经10%中性福尔马林固定,常规脱水,石蜡包埋,切片,HE染色。免疫组化采用EnVision法染色,DAB显色,苏木精复染。抗体包括SMA、desmin、CD34、CD99、TLE-1、CK(AE1/AE3)、S-100、SOX10、SS18-SSX、β-catenin、Cyclin D1、STAT6、Ki-67,均购自福州迈新公司。所有病例HE及免疫组化切片,均由两位高年资头颈部专科病理医师复阅确认。
2 结果
2.1 临床特点12例SNGP肿瘤发生于左侧鼻腔5例,其中1例累及蝶窦;右侧鼻腔5例;另2例虽发生于鼻腔,但具体部位不详。10例患者临床表现为鼻腔鼻窦占位,头痛、鼻腔肿胀、鼻出血,伴打喷嚏、流清涕等;另2例具体临床症状不详。患者均行肿物切除术,术后均未行放、化疗。随访时间4~168个月,平均37个月,其中7例未发现复发和转移,1例切除后8个月复发,1例切除后14个月复发,1例切除后27个月复发,2例失访。
2.2 病理检查
2.2.1眼观 肿瘤呈灰红、灰褐色碎组织,质软或肉感,肿瘤最大径1.4~6.0 cm,平均3.0 cm。
2.2.2镜检 肿瘤表面被覆呼吸道纤毛柱状上皮或化生的鳞状上皮,肿瘤边界清晰,但无完整包膜,肿瘤细胞呈席纹状、实性或栅栏状排列(图1),细胞短梭形、上皮样或圆形,胞质嗜双色性,细胞核卵圆形,核仁不明显,核分裂象少见(<1个/10 HPF)(图2)。间质具有分支状的薄壁小血管,通常呈“鹿角样”,血管周可见特征性的玻璃样变,可见红细胞外渗,背景中可混有一些炎症细胞,如淋巴细胞、嗜酸性粒细胞(图3)。
2.3 免疫表型12例SNGP中SMA均呈阳性(12/12)(图4),染色强度从弱阳性至强阳性;β-catenin呈核阳性(12/12)(图5);5例CD34呈局灶弱阳性(5/12);12例Cyclin D1均呈阳性(12/12)(图6);1例desmin(1/12)呈弱阳性;12例CD99均呈阳性(12/12)。7例行TLE-1免疫组化检测均阴性;10例行SS18-SSX免疫组化检测均阴性。12例中CK(AE1/AE3)、S-100、SOX10、STAT6均阴性;Ki-67增殖指数1%~3%。
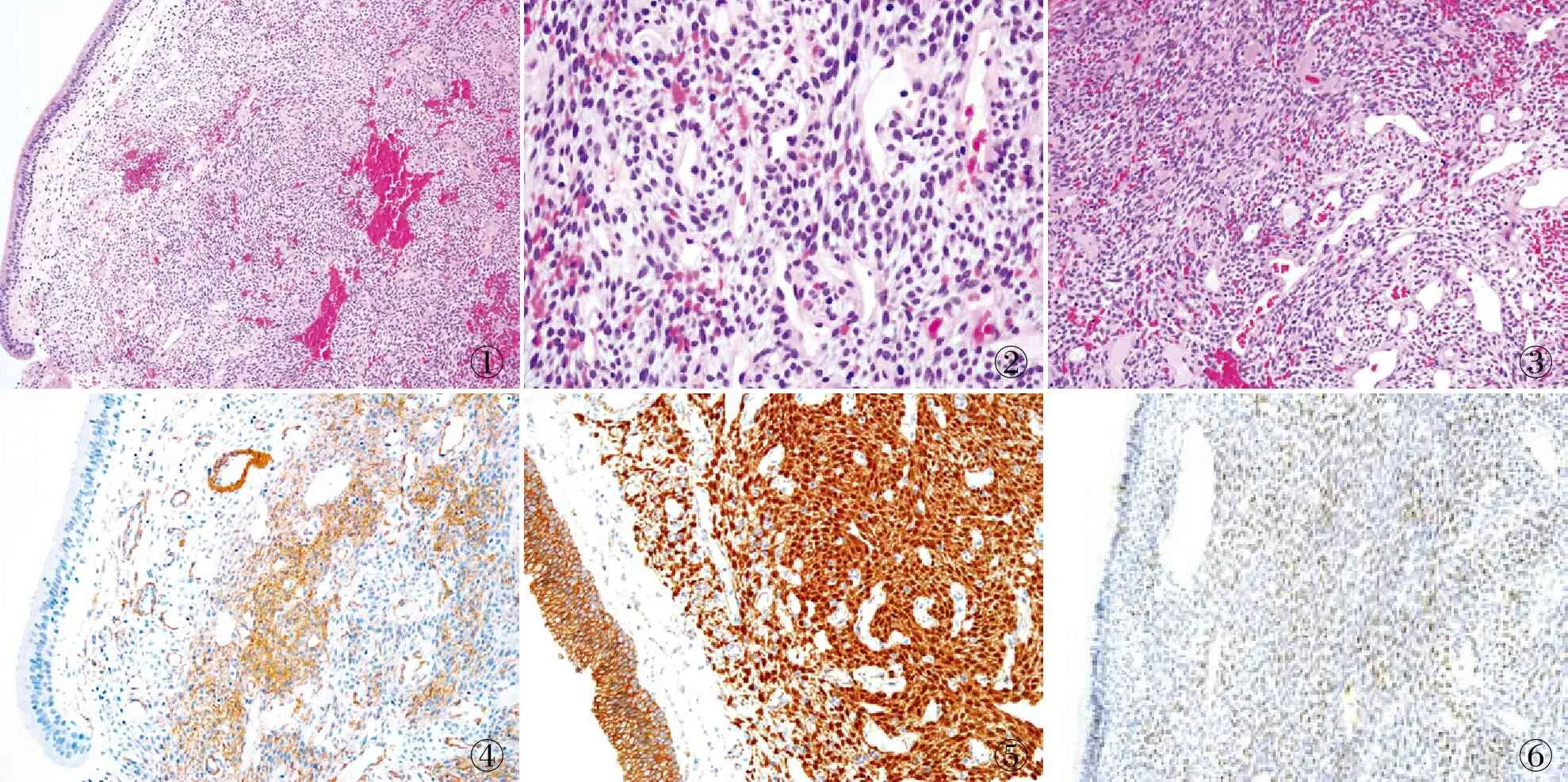
①②③④⑤⑥
3 讨论
球周皮细胞瘤是血管外皮细胞来源的一种软组织肿瘤,被认为起源于血管内皮细胞与基膜之间的周细胞。该肿瘤主要好发于腹膜及下肢,发生于鼻腔的SNGP极少见[10]。大部分SNGP患者的临床症状主要是进行性鼻塞、鼻炎、流涕、反复鼻出血、头痛等,当肿瘤进一步生长可出现眼球移位、复视、面颊部膨出等压迫症状。SNGP最初被认为是孤立性纤维性肿瘤谱系中的一部分[11],后来研究发现虽然两者组织学特征相似,但免疫表型有所不同。
SNGP患者以女性略多见,发病年龄范围广,好发于60~70岁老人。肿瘤多发生于鼻腔单侧(仅5%发生于双侧),并经常累及副鼻窦。本组收集的12例SNGP为国内最大宗报道,其中男性7例,女性5例,平均年龄56岁,肿瘤平均最大径3.0 cm,临床表现均为鼻腔鼻窦占位,头痛、鼻腔肿胀、鼻出血,伴打喷嚏、流清涕等。文献报道,SNGP免疫组化标记SMA、Cyclin D1、CD99均阳性,β-catenin为核阳性,部分病例CD34呈局灶弱阳性[12],CK(AE1/AE3)、S-100、SOX10、STAT6均阴性。由于SNGP与其他肿瘤存在组织学和免疫表型重叠,诊断具有挑战性。
SNGP组织形态学为均匀的梭形和卵圆形细胞群呈交织的短条束状,也可呈席纹状、漩涡状或栅栏状排列,间质可见毛细血管型小血管、分支状或鹿角状血管,管壁玻璃样变明显,免疫组化出现特征性的β-catenin核表达和血管周围肌样表型相结合。一项研究表明,β-catenin的突变激活和Cyclin D1过表达可能是SNGP发病机制核心[13]。β-catenin是Wnt信号通路的关键调控分子,Suzuki等[14]发现在3例SNGP中β-catenin下游的LEF1蛋白均阳性。进一步证实CTNNB1的3号外显子突变引起Wnt信号通路的激活,导致β-catenin在细胞核内积聚,并激活下游靶基因(MYC、CCND1和LEF1)的转录。
由于SNGP组织学易误诊,应与以下肿瘤进行鉴别:(1)鼻窦孤立性纤维性肿瘤:肿瘤间质内可见大量的条索状瘢痕及透明胶原纤维束,缺乏炎症细胞浸润,免疫组化标记CD34、BCL-2、STAT6均阳性,90%以上孤立性纤维性肿瘤存在NAB2-STAT6基因融合。(2)双表型鼻腔鼻窦肉瘤:好发于女性,是具有神经和肌源性特征的低级别鼻腔鼻窦肉瘤,肿瘤边界不清,可伴破坏性生长及骨组织的浸润,少数可显示横纹肌分化,免疫组化标记S-100、SMA均阳性,常见PAX3-MAML3基因融合[15]。(3)肌周细胞瘤:肿瘤细胞常围绕小至中等的血管,呈同心圆状或漩涡状生长,细胞团可突向血管内生长,免疫组化标记β-catenin核阴性,有PDGFRB突变。(4)单相型梭形细胞滑膜肉瘤:滑膜肉瘤多发于15~20岁青壮年人,以男性多见,多发生于四肢大关节附近,免疫组化标记vimentin阳性,特征性TLE1阳性,SS18-SSX、CK(AE1/AE3)、EMA、CK7、CK19、CD99、BCL-2均阳性,H3K27me3阴性,INI-1出现马赛克样阴性,分子遗传学可见t(X;18)(p11;q11)染色体易位、SYT-SSX1/2/4融合。(5)低度恶性肌纤维母细胞性肉瘤:梭形瘤细胞束状排列,核呈波浪状,部分区域可见小核仁,胞质淡染,至少局部具有轻~中度异型性,免疫组化标记vimentin阳性,部分病例actin、desmin、α-SMA、Calponin、Fibronectin和CD34中的一种或多种阳性,h-caldesmon、S-100和上皮性标记均阴性,β-catenin是否核阳性有助于两者鉴别。(6)血管球瘤:好发于肢体远端动静脉吻合支,尤其甲下,瘤细胞可呈规则的圆形,细胞核圆形、位于中央,细胞边界清晰,胞质嗜酸性或透亮。最近在良性和恶性血管球瘤中发现一种新的MIR143和NOTCH-1、NOTCH-2或NOTCH-3基因融合[16],而在SNGP中不存在;相反,在血管球瘤无CTNNB1错义突变,免疫组化标记β-catenin核阴性。(7)分叶状毛细血管瘤:属于毛细血管瘤的特殊亚型,是发生于皮肤真皮内的良性血管性肿瘤。该病多生长于头面部、颈部、上肢尤其是手指,通常表现为孤立性生长的无痛性肿块,根据其发生的部位不同,发生于表皮的通常质地脆弱,易破损及出血。患者多为20岁以上成人,发生于妊娠期女性也称妊娠期肉芽肿。由增生的毛细血管组成,毛细血管呈分叶状或结节状排列,间质水肿,伴大量炎细胞浸润,小叶间为纤维结缔组织,小叶内和小叶间可见较大的营养性血管。(8)鼻咽部血管纤维瘤:组织学表现为良性,但发生于鼻腔后壁时可局部侵犯血管。镜下表现为错综复杂的星型、鹿角状血管,管壁厚薄不一,血管壁可仅有单层内皮衬覆或数层平滑肌均可。间质细胞为梭形细胞有星芒状或短梭形细胞核,胞质呈淡空泡状,核仁不明显,无核分裂象,间质内可见成簇的多核间质细胞及肥大细胞浸润。免疫表型间质细胞AR、vimentin均阳性,β-catenin为核阳性,血管内皮标记CD34、CD31均阳性,75%病例可见CTNNB1基因3号外显子突变。
综上所述,SNGP是一种惰性肿瘤,预后较好,罕见转移,手术切除后患者的5年生存率大于90%,但手术切除不完整可复发,术后需对患者进行随访[3-9]。当肿瘤最大径>5 cm、有骨侵犯、明显的核异型、核分裂象增多(>4个/10 HPF)、坏死和增殖指数>10%时,提示肿瘤具有侵袭性,患者预后不良[2]。

