硬线产品吐丝温度及冷却工艺对氧化铁皮结构的影响
王皓,黄标彩,曹光明,魏勇,严海峰,刘振宇
(1.东北大学 轧制技术及连轧自动化国家重点实验室,辽宁 沈阳,110819;2.福建三钢闽光股份有限公司,福建 三明,365000)
线材是钢铁产业中的一个重要分支,由于其具有较高的附加值,在铁路、桥梁、海上平台和核电等重点建筑工程项目中得到了广泛应用,为国民经济的发展提供了巨大支撑作用[1-2]。在线材的热轧环节特别是碳质量分数较高的硬线产品中,表面会有一层氧化皮生成,在后续加工前需要通过如机械法、化学法、电解酸洗等除鳞措施去除,避免其对成品的表面质量造成影响。提升除鳞能力以及线材的表面质量,对高品质线材产品生产具有重要意义。
在轧制的吐丝和冷却环节,线材表面会生成氧化皮,同时相结构发生转变,冷却后表层最终的氧化皮结构会直接影响产品的除鳞效果。对此,国内外学者对线材的除鳞过程以及氧化皮的结构变化进行了研究。彭玉等[3]对72A高碳盘条在吐丝后生成的氧化铁皮机械剥离性能进行了研究,认为随着氧化铁皮的厚度增加以及FeO占比的提升,线材表层氧化皮的机械剥离性能会有所提高。BHATTACHARYA等[4]通过提高冷却速度的方式来减少线材氧化铁皮的生成,使氧化铁皮更易被去除。PAÏDASSI等[5-6]将空气中氧化后的纯铁从氧化温度快速淬火至室温,通过对比氧化铁皮厚度发现,在700~1 250 ℃长时间等温条件下形成的氧化铁皮样品中,Fe2O3和Fe3O4以及FeO层的厚度比均为1∶4∶95。氧化物相比例反映了铁在FeO中的扩散系数远远大于其在Fe3O4中的扩散系数,并且氧和铁通过Fe2O3的扩散均十分缓慢。而对于冷却过程,氧化铁皮会发生先共析转变或共析转变行为,且在不同的冷却工艺下将得到不同的氧化铁皮结构[7-8]。HAYASHI 等[9-10]研究了纯铁表面氧化铁皮的相变机理,发现高温下外层Fe3O4的生长最初占主导地位,但在共析反应前的较低温度下,Fe3O4的析出控制了初始FeO 的共析转变。OTSUKA等[11]运用原位同步辐射证实了富铁FeO 向Fe3O4和Fe的转变是氧化铁皮中层状共析组织和Fe3O4接缝层形成的根本原因。ZHOU等[12]研究了外压应力和冷却速率对钢表面氧化铁皮相变的影响,发现80 ℃/min 的快速冷却速度促进了先共析反应及Fe3O4/Fe共析组织的形成;由压应力增加导致的吉布斯能变化促进了中间产物的形成,甚至可以促进Fe3O4/Fe 共析组织在快速冷却速度下的最终形成。LI 等[13-14]通过对碳钢在不同氧化气氛下连续冷却过程中氧化铁皮的相变行为进行研究,发现当钢基体/氧化皮界面处有合金元素富集层存在时,界面可以作为离子扩散的阻挡层,降低氧化铁皮的厚度,降低氧化铁皮与基体界面的扩散速率。
对于线材的热轧生产,由于其冷却速率极快,得到的氧化铁皮主要以先共析组织和FeO 为主,其组织结构与在低冷却速率下得到的共析相的组织结构存在较大差异。本文研究不同吐丝温度及冷却工艺条件下氧化铁皮厚度与结构的演变规律,以期为线材热轧生产中吐丝及冷却工艺的优化与调整提供理论指导。
1 实验方案
以高碳钢82B的成分体系为基础,在实验室条件下熔炼得到实验材料A,并在此基础上通过降低Cr的质量分数得到材料B。熔炼后材料A与B的化学组成如表1所示。使用线切割机将试样切割成长×宽×高为5 mm×5 mm×8 mm 的长方体,并用粒径为8.4 μm和6.5 μm的砂纸将长方体的6个表面进行打磨。打磨后使用超声波和工业酒精进行清洗。使用MMS-200 热模拟试验机进行实验,实验工艺如图1所示。将试样放置于热模拟机的夹具上,在关紧实验舱后向其中通入氩气并保持5 min,防止试样在加热过程中被氧化。在升温至模拟吐丝温度后开始通入空气并保温5 min,得到原始氧化铁皮。之后采用两阶段冷却来模拟现实生产的冷却过程,其中,第一阶段统一使用10 ℃/s 的速度来降温至600 ℃,避免基体中碳化物的形成与析出,保证产品的组织和力学性能;而第二阶段则基于现场的实际冷却能力设计3种不同的冷却速度来研究相关参数对氧化皮中组织的影响。冷却结束后,将试样以0.5 ℃/s 的速度冷却至室温。实验结束后,将试样进行热镶嵌,之后经过砂纸打磨、机械抛光,并用盐酸酒精进行腐蚀后,使用电子探针(EPMA,Electron Probe Micro-Analyzer)对试样的断面形貌进行观察分析。
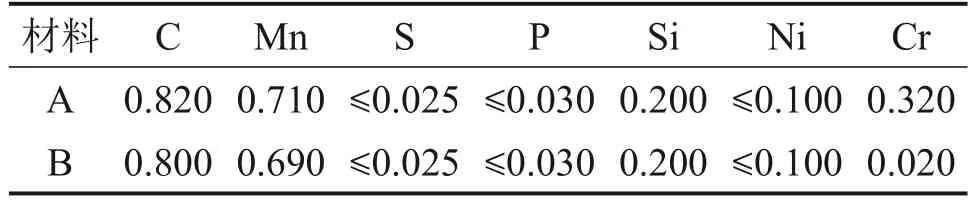
表1 实验材料的化学组成(质量分数)Table 1 Chemical composition of experimental materials(mass fraction)%
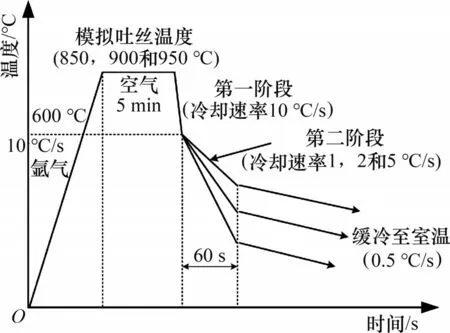
图1 实验工艺示意图Fig.1 Schematic diagram of experimental process
2 实验结果
分别对比材料A(Cr 质量分数为0.32%)与B(Cr质量分数为0.02%)在相同吐丝温度下冷却速度对氧化铁皮结构的影响。以900 ℃为例,图2所示为材料A 的断面检测结果,在此条件下氧化铁皮主要由外层的Fe3O4、内层的FeO、冷却过程中FeO析出的先共析Fe3O4构成,结合对氧化铁皮中各个位置的EDS 能谱分析结果(见表2)可知,在基体界面位置有Cr 元素的富集。由于不同试样均在相同的温度下进行高温氧化,且以较大的冷却速度降低至室温,因此,图2中不同冷却速度下得到的氧化铁皮厚度相近,均在50~55 μm 之间。但是在先共析Fe3O4的生长形式上,三者具有较大的差异,在较低的冷却速率1 ℃/s 下,形成的先共析Fe3O4的体积要明显比5 ℃/s条件下的更大;而在先共析Fe3O4的形核率方面则刚好相反,在单位面积上,5 ℃/s 条件下的氧化铁皮中先共析Fe3O4的数量要明显比1 ℃/s条件下的多。

图2 材料A在吐丝温度为900 ℃、不同冷却速率下的氧化铁皮断面形貌Fig.2 Cross section morphology of oxide scale of material A at different cooling rates when laying temperature is 900 ℃

表2 不同冷却速率下各取样点EDS扫描结果(原子分数)Table 2 EDS scanning results of different sampling points at different cooling rates(atomic fraction)%
当冷却速率为1 ℃/s 时,材料A(Fe-0.32Cr)在不同吐丝温度下氧化铁皮结构的断面形貌如图3所示,不同吐丝温度下各取样点EDS 扫描结果见表3。由图3 和表3 可知:氧化铁皮主要是由外层的Fe3O4、内层的FeO、冷却过程中FeO 析出的先共析Fe3O4以及基体界面位置处的Cr元素富集层构成。由于吐丝温度不同,氧化铁皮的厚度有较大差异:当吐丝温度为850 ℃时,氧化铁皮的厚度为27.7~28.2 μm;当吐丝温度达到900 ℃时,氧化铁皮厚度为53~55 μm;当吐丝温度为950℃时,氧化铁皮厚度为85~87 μm;同时,原始高温下Fe3O4占据氧化铁皮整体的体积分数随着吐丝温度的升高而逐渐降低:850 ℃时为21.4%,900 ℃时为16.9%,950 ℃时为14.7%;由于冷却速率没有变化,因此,在850,900 和950 ℃时最终形成的先共析Fe3O4占氧化铁皮整体的体积分数大致相同,分别为10.7%,11.3%和10.9%。

表3 不同吐丝温度下各取样点EDS扫描结果(原子分数)Table 3 EDS scanning results of different sampling points at different laying temperatures(atomic fraction)%

图3 材料A在1 ℃/s的冷却条件下不同吐丝温度的氧化铁皮断面形貌Fig.3 Cross section morphologies of oxide scale of material A at different laying temperatures under cooling conditions of 1 ℃/s
当吐丝温度为900 ℃时,对比材料B在不同冷却速度下的氧化铁皮断面形貌,结果如图4所示。由图4 可见:材料B 的氧化铁皮主要由外层的Fe3O4、内层的FeO、冷却过程中FeO 析出的先共析Fe3O4构成,与材料A不同的是,由于合金中的Cr 质量分数较低,在氧化铁皮与基体界面处并没有Cr元素富集,取而代之的是界面形成的Fe3O4接缝层。相较于材料A,材料B在900 ℃下形成的氧化铁皮厚度有所增加,整体的厚度为52~57 μm;同样地,先共析Fe3O4的形核率随着冷却速率的增加而增加,但其单位体积却随着冷却速率的增加而降低。

图4 材料B在吐丝温度900 ℃下不同冷却速率的氧化铁皮断面形貌Fig.4 Cross section morphologies of oxide scale of Material B at different cooling rates and laying temperature 900 ℃
当冷却速率为1 ℃/s时,对比材料B(Fe-0.02Cr)在不同吐丝温度下氧化铁皮结构的断面形貌,如图5所示。由图5可见,氧化铁皮主要包括外层的Fe3O4、内层的FeO 以及冷却过程中FeO 析出的先共析Fe3O4以及基体界面处的Fe3O4接缝层。由于吐丝温度不同,氧化铁皮的厚度有较大差异:当吐丝温度为850℃时,氧化铁皮的厚度为28.3~29.2 μm;当吐丝温度达到900 ℃时,氧化铁皮厚度为52~57 μm;当吐丝温度为950 ℃时,氧化铁皮厚度为87~89 μm。Fe3O4占据氧化铁皮整体的体积分数随着温度升高而降低,当吐丝温度分别为850,900 和950 ℃时,Fe3O4占据氧化铁皮整体的体积分数分别为22.4%,17.5%和15.3%,但由于冷却速率没有变化,最终形成的先共析Fe3O4在FeO 中的体积分数大致相同,分别为9.2%,9.0%和8.8%。

图5 材料B在1 ℃/s的冷却条件下不同吐丝温度的氧化铁皮断面形貌Fig.5 Cross section morphologies of oxide scale of material B at different laying temperatures under cooling conditions of 1 ℃/s
综上可知,在同一钢种且相同的吐丝温度下,氧化铁皮的厚度相当,并不会随着冷却速度的改变而发生较大变化;而且由于Cr 元素在保温过程中会形成一定厚度的Cr 富集层,起到阻碍离子扩散的作用,因此,材料A相对于材料B的氧化铁皮厚度有所减小,且原始Fe3O4层的体积分数也随着吐丝温度升高而降低。不同冷却进程对最终的氧化铁皮结构特别是先共析Fe3O4的生成形式会造成较大影响。
3 分析与讨论
3.1 先共析Fe3O4的形成与长大
在Fe-O体系下,FeO能够形成在较宽化学计量范围内可变的固溶体,当Fe离子过饱和的FeO被冷却时,将在FeO中发生先共析反应,析出Fe3O4:
式中:0<x,y<1 且x>y,即Fe1-xO 为富O 的FeO相,Fe1-yO为富Fe的FeO相。先共析Fe3O4的析出量取决于FeO中O离子浓度及冷却速度,O离子浓度越高,冷却速度越快,析出温度越低,形成的先共析Fe3O4就越少。先共析Fe3O4的析出与Fe 在FeO中的扩散有直接关系。由于FeO晶界附近有较高的结构起伏及能量起伏,先共析Fe3O4会优先在此位置发生形核。在晶核附近的FeO 中,Fe 离子的浓度高于FeO中Fe的平均浓度,会导致Fe的上坡扩散。若冷区温度足够低且冷却时间长,则随着Fe 离子的浓度增加,未发生先共析反应的FeO成分会逐步接近共析成分,之后再形成Fe+Fe3O4的片层状共析组织。当FeO的Fe3O4发生相变形核时,假设形成的晶坯为球形,则当FeO 随着温度降低出现过冷时,总体的自由能变化量为
其中:ΔG为单位体积自由能的变化量,该参数与过冷度有关;σ为比表面能;r为形核半径。而为了形成稳定的晶核,所需的临界形核半径r*可以表示为
式中:Tm为理论结晶温度,ΔH为融化潜热[15]。根据式(3)可知,临界晶核半径由r*决定,冷却速度越快,过冷度越大,r*越小,形核概率越大,晶核的数量越多。按照扩散长大的规律,在Fe-O 合金中可以推导出与先共析Fe3O4的长大有关的参数。先共析Fe3O4的长大模型如图6所示,在FeO/先共析Fe3O4界面处,FeO 析出先共析Fe3O4(浓度为cFe3O4)后,FeO 成分中Fe 离子的浓度由cFeO升高为cFeO-Fe3O4。Fe3O4相在FeO 相界面处析出,然后向晶内长大,如FeO/先共析Fe3O4界面为非共格,Fe3O4相长大受Fe离子在FeO中的扩散所控制。

图6 先共析Fe3O4的长大模型示意图Fig.6 Schematic diagram of growth model of proeutectoid Fe3O4
假设FeO/先共析Fe3O4界面在dτ时间内,由于Fe离子扩散进入FeO中,在单位面积上向前沿x轴推进dL,则新相Fe3O4新增体积为dL,扩散离去的Fe离子的物质的量dm1为
根据菲克第一定律,当界面处FeO 中Fe 离子的浓度梯度为dc/dx,Fe 离子在FeO 相中的扩散系数为D,那么dτ时间内扩散到单位面积界面Fe 离子的物质的量dm2为
在平衡时,dm1=dm2,
根据式(6),可以得到界面移动速度v:
采用l和L分别表征FeO 和Fe3O4内部Fe 离子发生浓度变化的距离,则有
由式(7)和(8)可得
图6 中,面积S1相当于先共析Fe3O4中减少的Fe 离子的物质的量,面积S2相当于FeO 中增加的Fe离子的物质的量。S1=S2,则有:
根据式(9)和(11)可得
由于cFeO-Fe3O4≫cFe3O4,cFeO≫cFe3O4,cFeO-Fe3O4≈cFe3O4,则有(cFeO-Fe3O4-cFe3O4)≈(cFeO-cFe3O4),所以,式(12)可以简化为
或
对式(14)两边积分可得:
将式(16)代入式(13)可得
由式(17)可知先共析Fe3O4的生长速度v并非恒定速度,v与离子的扩散系数D及时间τ有关,扩散系数越大,长大速度越大,呈现非线性关系;时间越长,长大速度越小,且随着时间的延长而变慢。而扩散系数D可以由Arrhenius 方程[16]计算得到:
这同样意味着先共析Fe3O4的形核与长大受到了温度的限制。温度越低,v越小,进而造成最终共析组织的生长也受到影响。同时,Fe3O4的形核受到了过冷度的影响。在较低的温度下,由于过冷度较大,先共析Fe3O4会产生大量的形核核心。在本实验中,较低冷却速率会使FeO 在高温区的停留时间相对延长,形成的先共析Fe3O4更倾向于以少量形核但单个核心体积较大的方式生长;而在较高冷却速率时先共析Fe3O4倾向于以大量形核的方式生长,如图7所示。

图7 先共析Fe3O4在不同冷却速率下的生长过程Fig.7 Growth processes of proeutectoid Fe3O4 at different cooling rates
3.2 Cr元素对先共析反应的影响
合金中的Cr 元素在高温条件下,能够形成富Cr 氧化层,提高材料的抗氧化性[17-19]。这是由于Cr 与O 的亲和力要比Fe 基材的高,在高温氧化性气氛下,Cr 元素会优先发生选择性氧化,在基体表面形成一层致密的氧化层,图8所示为氧化铁皮-基体界面处元素扫描分析结果。从图8 可以看出Fe-0.32Cr在界面上有Cr元素富集层出现。Fe-Cr-O三元氧化物的平衡相图如图9所示。当Cr 的质量分数为0.02%时,在整个区间内并没有含有Cr 元素的氧化物生成;而当Cr 的质量分数达到0.32%时,经过高温氧化后会有FeCr2O4形成。图9 中,AB段(红色箭头所示)是FeO→α-Fe+Fe3O4反应中FeO 的稳定性曲线。随着Cr 质量分数升高,AB段所对应的温度由呈现上升趋势,说明Cr 元素的添加对离子的高温扩散起到抑制作用。FeCr2O4的生成过程如下:

图8 氧化铁皮-基体界面处元素扫描分析Fig.8 Element analysis of surface at the interface between oxide scale and substrate

图9 Fe-Cr-O三元平衡相图Fig.9 Fe-Cr-O ternary equilibrium phase diagram
Cr 富集层的出现也会对FeO 中的先共析反应产生一定的影响。富铁FeO向Fe3O4和Fe的转变是氧化铁皮中层状共析组织和Fe3O4接缝层形成的根本原因。Fe3O4接缝层充当Fe的扩散屏障,能防止Fe 穿过FeO/Fe 基体界面向内扩散以及促进FeO 基体中的Fe过饱和[20]。同样地,基体界面的富Cr层也能够实现相近的作用。但是,Fe-0.32Cr 中氧化铁皮界面的富Cr 层是在高温下形成的,而Fe-0.02Cr 中的Fe3O4接缝层需要在冷却的过程中逐渐生成。由于Fe-0.32Cr中富Cr层的优先形成能更早地抑制Fe离子的双向扩散,使得靠近Fe3O4一侧位置的FeO共析反应孕育期缩短,造成Fe3O4-FeO界面处会优先完成先共析Fe3O4的长大过程;相应地,在相同的吐丝温度以及冷却速度下,Fe-0.32Cr中的先共析程度会较Fe-0.02Cr中体积增大程度更大。
4 结论
1)线材经过吐丝及冷却过程后得到的氧化铁皮组织主要以Fe3O4和FeO以及先共析Fe3O4为主,其界面位置依据合金中Cr 质量分数的不同会有Fe3O4接缝层或Cr富集层生成。
2)吐丝温度直接影响原始Fe3O4在氧化铁皮中的体积分数,而冷却速度对FeO中先共析Fe3O4的形核率及形核尺寸有直接关系,冷却速率越快,先共析Fe3O4的形核率越高,但是单个Fe3O4的体积会越小。
3)Cr 的氧化富集层会在高温氧化过程中的氧化铁皮-基体界面形成,相对于冷却过程中形成的Fe3O4接缝层,会更早地阻碍界面位置的离子扩散,使先共析反应进程提前。

