血清TGF-β、IL-6与溃疡性结肠炎患者肠道菌群的相关性
金洋,韦周兵,左逢胜
( 1.信阳市中心医院 消化内科,河南 信阳 464000;2.信阳职业技术学院附属医院 消化内科,河南 信阳 464000 )
目前,溃疡性结肠炎(ulcerative colitis, UC)的病因和发病机制尚未完全明确,但与环境、肠道功能屏障障碍、免疫功能异常等密切相关[1]。且越来越多的研究证实,肠道菌群的失调与UC的发生密切相关[2-3]。肠道菌群失调可导致肠道黏膜屏障的完整性及功能受到损害,且致病菌增殖及其分泌的肠毒素可导致肠道微环境改变,进一步增加肠道通透性,促使大量细菌及产物进入机体,影响肠道免疫功能,进而发病。另有研究证实,肠道内菌群失衡可能是UC发生发展的始动因素[4]。因而,UC患者的肠道菌群情况得到了临床医生的重视。另外,免疫调节异常也是UC发病的重要机制,而在UC免疫异常中,细胞因子发挥着重要作用,相关的抗炎及促炎因子的平衡失调可导致免疫功能异常[5]。生长转化因子-β(transforming growth factor-β, TGF-β)是具有多种生物活性的多肽,参与B细胞活化和体液免疫反应;白细胞介素-6(interleukin-6, IL-6)是一种重要促炎因子,可增加巨噬细胞所产生的炎性细胞因子,促使中性粒细胞浸润与肠道病变部位,引起肠道免疫功能异常。另有研究指出,肠道内菌群紊乱是造成炎症反应和免疫应答改变的重要因素[6]。但是血清TGF-β、IL-6水平与肠道内菌关系的临床报道较少。鉴于此,本研究通观察血清TGF-β、IL-6及肠道菌群在UC患者中的表达,进一步分析血清TGF-β、IL-6水平与UC患者肠道菌群的关系,以此为UC的临床诊疗提供更多的参考,现报道如下。
1 资料与方法
1.1 一般资料
纳入2020年4月至2021年4月于信阳市中心医院消化内科就诊的102例UC患者作为本次研究对象。102例UC患者中男49例,女53例,年龄28~55岁,平均(40.86±4.71)岁;病程8~31个月,平均(20.58±4.12)个月;发病部位:直肠39例,乙状结肠27例,降结肠36例。本研究经医学伦理委员会批准,且研究对象均签署知情同意书。
纳入标准:①UC符合《炎症性肠病诊断与治疗的共识意见(2018年,北京)》[7]中相关标准,即患者多伴有腹泻伴粘液脓血便、腹痛、腹胀等症状,且经结肠镜、粪便等检查确诊;②疾病处于活动期(改良Mayo评分[8]>2分);③病程>4周;④神志清晰,均可配合本次研究。排除标准:①近期接受激素、益生菌、免疫抑制剂等药物治疗;②伴有细菌型痢疾、肠结核等感染性结肠炎;③肠道出血、肠穿孔;④伴有其他自身免疫性疾病;⑤处于妊娠期或哺乳期。
1.2 方法
1.2.1 病情程度评估方法 患者就诊时均接受体格、血常规及相关实验室指标检查,参照改良Truelove和Witts疾病严重程度分型标准[9]评估患者病情评估患者的病情严重程度。划分标准:①轻度:大便次数<4次/d;便血轻或无;脉搏≤90次/min;体温<37.5℃;血红蛋白正常(正常值:男性120~160 g/L,女性110~150 g/L);红细胞沉降率<20 mm/h。②重度:排便≥6次/d;便血较重;脉搏>90次/min;体温>37.8℃;血红蛋白<75%正常值;红细胞沉降率>30 mm/h。③中度介于轻、重度之间。其中红细胞沉降率、血红蛋白检测方法:取患者就诊时空腹静脉血6 mL,均分成2份(每份3 mL),其中1份样本注入含有EDTA-2K的抗凝管中,充分混匀,以3 500 r/min速度离心10 min,取血浆,采用全自动血细胞分析仪(深圳市普康,PE-7200型)及配套试剂盒检测血红蛋白水平;采用红细胞沉降率测定仪(北京普朗,PUC-2068B型)检测红细胞沉降率。
1.2.2 血清TGF-β、IL-6水平检测方法 取另一份血液样本,不进行抗凝处理,以3 000 r/min速率离心15 min,离心半径为11 cm,取血清,放置于-70℃冰箱中保存待检验;采用酶联免疫吸附法检测血清TGF-β水平,试剂盒选自上海酶联生物;化学发光法检测血清IL-6水平,试剂盒选自湖南宜乐芯康生物。
1.2.3 肠道菌群检测方法 采集患者就诊时的新鲜粪便标本1.5 g,加入4.5 mL厌氧菌稀释液,放于涡旋振荡器上震荡至粪便均质化(3 000 r/min速率下震荡1 min),取无菌试管7个,并进行编号,分别加入9 mL稀释液,然后从匀浆小瓶取出1 mL,放于第2管内,充分混匀,依次类推进行倍比稀释,至10稀释度,将培养基平板放于37℃培养箱内烘干过夜,选取合适的稀释度进行滴种,从高稀释度开始,每次吸取20 μL混匀的稀释菌液,滴种于各平皿相应的稀释度,每个稀释度重复3次;滴种结束后,待液滴吸收,平板反转,分别进行需氧和厌氧培养,计算细菌数。细菌数=菌落数均值×50×稀释度。
1.3 统计学方法
采用SPSS 25.0统计学软件进行数据分析。Shapiro-Wilk检验计量资料正态性,符合正态分布计量资料以均数±标准差(±s)表示,多组间比较采用单因素方差检验,组间两两采用LSD-t检验;计数资料用百分率(%)表示;采用双变量Kendall的tau-b(K)直线相关性检验血清TGF-β、IL-6水平、肠道菌群与UC患者病情程度的相关性;经双变量Pearson直线相关性检验血清TGF-β、IL-6水平与UC患者肠道菌群的相关性;P<0.05为差异有统计学意义。
2 结果
2.1 UC患者病情程度评估情况
102例UC患者中,38例病情为轻度,占37.25%(38/102);30例为中度,占 29.41%(30/102);34例为重度,占33.33%(34/102)。
2.2 不同病情程度UC患者血清TGF-β、IL-6水平
中度组、重度组血清TGF-β、IL-6水平高于轻度组,且重度组血清TGF-β、IL-6水平高于中度组,差异有统计学意义(P<0.05)。见表1。
表1 不同病情程度UC患者血清TGF-β、IL-6水平比较 (±s, pg/mL)
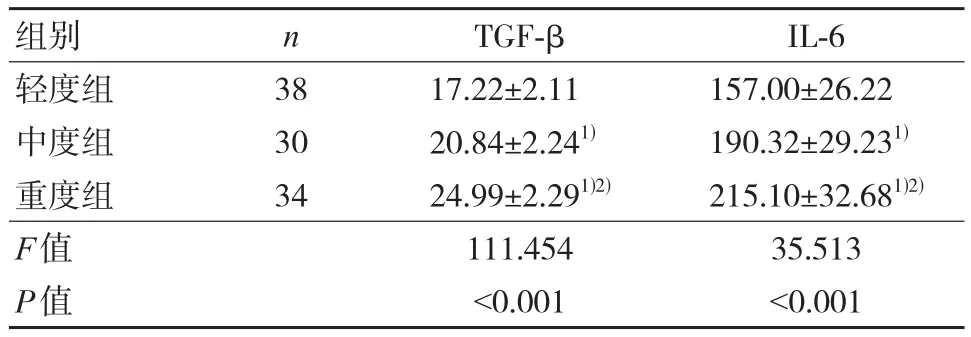
表1 不同病情程度UC患者血清TGF-β、IL-6水平比较 (±s, pg/mL)
注:1)与轻度组比较,P<0.05;2)与中度组比较,P<0.05。
组别轻度组中度组重度组F值P值n 38 30 34 TGF-β 17.22±2.11 20.84±2.241)24.99±2.291)2)111.454<0.001 IL-6 157.00±26.22 190.32±29.231)215.10±32.681)2)35.513<0.001
2.3 不同病情程度UC患者肠道菌群情况
中度组、重度组肠杆菌、肠球菌数量高于轻度组,双歧杆菌、乳杆菌数量低于轻度组;且重度组肠杆菌、肠球菌数量高于中度组,双歧杆菌、乳杆菌数量低于中度组,差异有统计学意义(P<0.05)。见表 2。
表2 不同病情程度UC患者肠道菌群情况 (±s, cfu)
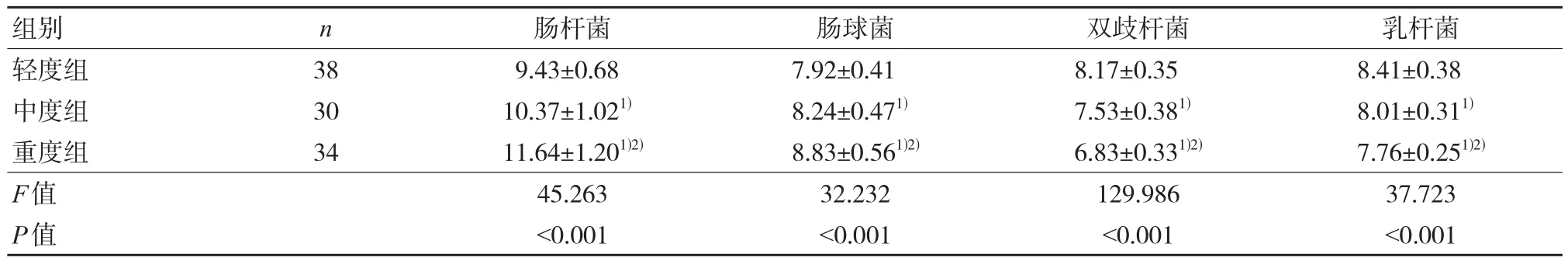
表2 不同病情程度UC患者肠道菌群情况 (±s, cfu)
注:1)与轻度组比较,P<0.05;2)与中度组比较,P<0.05。
组别轻度组中度组重度组F值P值n 38 30 34肠杆菌9.43±0.68 10.37±1.021)11.64±1.201)2)45.263<0.001肠球菌7.92±0.41 8.24±0.471)8.83±0.561)2)32.232<0.001双歧杆菌8.17±0.35 7.53±0.381)6.83±0.331)2)129.986<0.001乳杆菌8.41±0.38 8.01±0.311)7.76±0.251)2)37.723<0.001
2.4 血清TGF-β、IL-6水平、肠道菌群与UC患者病情程度的相关性
经双变量Kendall的tau-b(K)直线相关性检验结果显示,血清TGF-β、IL-6水平、肠杆菌及肠球菌数量与UC患者病情程度呈正相关(r=0.706、0.530、0.555、0.511,P均<0.05),双歧杆菌、乳杆菌数量与UC患者病情程度呈负相关(r=-0.720、-0.545,P均<0.05)。
2.5 血清TGF-β、IL-6水平与UC患者肠道菌群的相关性
经双变量Pearson直线相关性检验,血清TGF-β、IL-6水平与UC患者肠杆菌及肠球菌数量呈正相关(r>0,P<0.05),与双歧杆菌、乳杆菌数量呈负相关(r<0,P<0.05)。见表3。
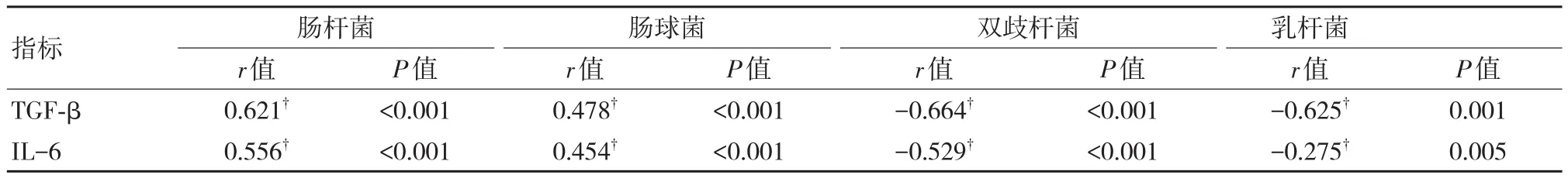
表3 血清TGF-β、IL-6水平与UC患者肠道菌群的相关性
3 讨论
人体肠道内存在种类繁多、数量巨大的细菌群体,构成了一个复杂活跃并具有广泛生物活性的生态系,参与肠内的分解、代谢,对维持宿主正常生理功能机及稳定正常免疫系统具有重要的意义,与肠道疾病的发生、发展过程密切相关。有研究显示,肠道菌失衡,肠杆菌、肠球菌等致病菌大量繁殖并被Toll样受体识别,可激活肠黏膜的炎症反应,导致UC患者病情进展[10]。本研究观察不同病情程度的活动期UC患者的肠道菌群情况,结果发现,随着病情的加重,肠杆菌、肠球菌数量不断升高,而双歧杆菌、乳杆菌数量不断降低,也证实了上述研究。其原因可能是,肠道菌群是一个复杂多样的生物群落,其中双歧杆菌、乳杆菌为肠道优势菌群,参与维护肠道上皮细胞完整性,对失调的肠道微生态群具有调节作用,其数量的降低可促使肠道菌群失衡,为致病菌增殖提供良好的环境;肠杆菌为革兰氏阴性菌,是较为常见的致病菌,可协助致病菌通过调节免疫球蛋白破坏肠道上皮屏障,同时肠杆菌产生的毒素因子也可导致肠道上皮屏障损害,进而引起肠道菌紊乱,进而导致肠道疾病发生、发展;肠球菌为革兰氏阳性菌,也是一种条件致病菌,可损伤肠道上皮屏障,促进肠道疾病发生、发展[11-12]。因而,肠道菌群与UC患者的病情进展可存在一定的联系,且本研究通过相关性分析也证实了这一推测。因此,临床医师可将调节肠道菌群作为临床治疗UC患者的一个靶点。
在UC发病的免疫学机制中,关于细胞因子的研究已较为广泛与深入,肠黏膜中的细胞因子可由肠上皮细胞、巨噬细胞等分泌,可作为细胞间的信号传递分子在免疫系统与其他系统中充当信使的作用,形成较为完整的网络系统、调节及介导免疫应答等[13]。IL-6被诸多研究证实在UC发生、发展中发挥重要的促炎作用,参与细胞免疫应答,促使炎症不断发生、发展[14-15]。且有研究证实,IL-6也可用作反映肠道炎症疾病的严重程度的重要指标[16]。本研究也证实可血清IL-6可随着UC患者病情进展而呈升高趋势,且与病情程度密切相关。提示了,IL-6参与UC病理过程,同时可检测病情的严重程度。TGF-β是一种抑炎因子,可下调相关炎症介质(如肿瘤坏死因子),促进体液免疫反应,对修复肠道黏膜具有积极的作用。但本研究中,随着病情的进展,血清TGF-β却呈升高趋势,可能是由于UC发生时,机体的免疫反应被激活,血清TGF-β升高参与抗炎反应,但抗炎因子的过量表达,可促使机体处于免疫抑制状态或无反应状态,促使病情不断进展。且有研究指出,UC患者血清TGF-β呈高表达时,提示UC患者的TGF-β的信号传导可能存在异常,导致其抗炎作用无法发挥作用[17]。但抗炎因子与UC发生、发展的具体关系还需进行分析。
由此可知,肠道菌群、血清TGF-β及IL-6与UC患者疾病发生、发展有关。而肠道菌群在免疫反应中发挥重要的作用,故推测,血清TGF-β、IL-6可能与UC患者肠道菌群存在一定的联系。为了验证此推测,本研究通过相关性分析证实了这一推测。分析其机制可能是肠道致病菌的产物可与各自Toll样受体结合,进而诱导抗原递呈细胞分泌IL-6,可诱导TGF-β表达,促使免疫反应,当血清TGF-β、IL-6过量表达,可促使机体处于免疫抑制状态,促发炎症级联反应,导致黏膜微循环障碍,削弱肠道黏膜的屏障功能,从而介导肠道黏膜的损伤,可导致肠道内微环境进一步失衡,引起致病菌增殖、有益菌减少等[18]。由此可见,肠道菌群与血清TGF-β、IL-6可相互作用,促使UC发生、发展。但是肠道菌群失调是导致UC的原因还是结果,还需进行深入探讨。
综上所述,UC患者存在肠道菌群失衡,血清TGF-β、IL-6与UC患者肠道菌群数量存在相关性。但本研究仅证实了血清TGF-β、IL-6水平与UC患者肠道菌群的关系,但二者的具体因果关系尚未清楚,仍需进行大样本量、前瞻性研究,为临床诊疗UC提供更多参考依据。

