胃癌肝转移化疗疗效评估模型的构建及预测价值
麻百家 陈清锋 吴懿俊 李成章 陈旦东 张志平
我国是胃癌高发病率国家,以进展期胃癌为主,约10.0%~18.7%胃癌患者诊断时已发生肝转移,胃癌肝转移治疗效果差,5年存活率5%~19%[1-2]。《胃癌肝转移诊断与综合治疗中国专家共识(2019版)》[3]在日本《胃癌治疗指南》基础上拟定新的胃癌肝转移临床分型体系及治疗决策,然而可切除或潜在可切除胃癌肝转移患者治疗选择上是先行化疗还是先行手术存在一定争议。因此预测胃癌肝转移患者系统化疗疗效可筛选出化疗受益人群,指导胃癌肝转移治疗决策。列线图是基于多因素统计模型预测个体临床事件发生概率的可视化图形工具,本研究回顾53例胃癌肝转移患者的临床资料、胃镜病理检查结果和腹部增强CT影像学信息,探讨影响胃癌肝转移化疗疗效因素,并初步构建胃癌肝转移化疗疗效评估模型,优化胃癌肝转移评估体系,为制定更加合理、准确的个体化诊疗方案提供参考。
1 对象和方法
1.1 对象 回顾2015年1月至2019年6月宁海县中医医院普外科11例和宁波市第一医院胃肠外科42例收治的胃癌肝转移患者共53例。纳入标准:(1)经胃镜及病理检查诊断为胃腺癌;(2)包括B超、增强CT、增强MR检查中有2个或以上影像学检查临床诊断胃癌肝转移,或肝穿刺病理检查提示转移性腺癌;(3)无幽门狭窄、梗阻、出血等并发症,能够口服药物;(4)东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)体力评分≤2分;(5)心肺功能良好,能够耐受化疗;(6)完成3个周期的化疗,且临床病理资料及随访资料完整。排除标准:(1)胃镜活检病理免疫组化人表皮生长因子受体-2(epidermal growth factor receptor 2,Her-2)+++,或Her-2++且荧光原位杂交阳性;(2)胃癌原发病灶T分期为T4b;(3)腹部增强CT检查评估D2清扫区域外淋巴结转移;(4)弥漫性肝转移,肝转移负荷≥50%;(5)肝外转移;(6)异时性肝转移。本研究经宁海县中医医院和宁波市第一医院医学伦理委员会批准。
1.2 方法 所有肿瘤基线评估及疗效评价依据腹部增强CT检查结果,肿瘤分期方法采用第7版美国癌症联合委员会(American Joint Committee on Cancer,AJCC)TNM分期,所有患者化疗3~4个周期后进行增强CT检查。疗效评估采用实体瘤疗效反应评价标准(Response Evaluation Criteria In Solid Tumors,RECIST)1.1版[4],分为完全缓解(completely remission,CR):肿瘤完全消失;部分缓解(partial remission,PR):肿瘤缩小>30%;病灶稳定(stable diease,SD):肿瘤缩小<30%或增大<20%;病灶进展(progressive diease,PD):肿瘤增大>20%。疗效评判为CR、PR和SD的患者为疾病控制患者。
1.3 化疗方案 (1)mFOLFOX6方案:奥沙利铂针(江苏恒瑞医药股份有限公司,国药准字:H20000337,规格:50 mg/支)85 mg/m2,静脉滴注,第1天;亚叶酸钙针(广东岭南制药有限公司,国药准字:H20180321,规格:100 mg/支)400 mg/m2,静脉滴注,第 1天;氟尿嘧啶针(山西普德药业有限公司,国药准字:H02200605,规格:0.25 g/支)400 mg/m2,静脉推注,第1天,2 400 mg/m2,46 h持续静脉滴注,第1天;2周为1个周期;(2)SOX方案:替吉奥胶囊(齐鲁制药有限公司,国药准字:H20100150,规格:20 mg/粒)80 mg/m2,口服,2次/d,第1~14天;奥沙利铂针(江苏恒瑞医药股份有限公司,国药准字:H20000337,规格:50 mg/支)130 mg/m2,静脉滴注,第1天,每3周为1个周期;(3)XELOX方案:卡培他滨片(上海罗氏制药有限公司,国药准字:H20073024,规格:0.5 g/片)2 000 mg/m2,口服,2次/d,第1~14天;奥沙利铂针(江苏恒瑞医药股份有限公司,国药准字:H20000337,规格:50 mg/支)130 mg/m2,静脉滴注,第1天,每 3周为 1个周期;(4)其他化疗方案:①FLOT方案:多西他赛(江苏恒瑞医药股份有限公司,国药准字:H20020177,规格:30 mg/支)50 mg/m2,静脉注射,第1天;奥沙利铂针(江苏恒瑞医药股份有限公司,国药准字:H20000337,规格:50 mg/支)85 mg/m2,静脉注射,第1天;亚叶酸钙针(广东岭南制药有限公司,国药准字:H20180321,规格:100 mg/支)200 mg/m2,静脉注射,第1天;氟尿嘧啶针(山西普德药业有限公司,国药准字:H02200605,规格:0.25 g/支),2 600 mg,静脉注射,维持46 h,2 周为1个周期;②DOX方案:多西他赛针(江苏恒瑞医药股份有限公司,国药准字:H20020177,规格:30 mg/支)75 mg/m2,静脉滴注,第1天;奥沙利铂针(江苏恒瑞医药股份有限公司,国药准字:H20000337,规格:50 mg/支)130 mg/m2,静脉滴注,第2天;卡培他滨片(上海罗氏制药有限公司,国药准字:H20073024,规格:0.5 g/片)2 000 mg/m2,口服,2次/d,第1~14天;每3周为1个周期。根据患者化疗反应调整药物剂量。
1.4 腹部增强CT检查评估 所有患者治疗前,化疗3~4周期后行腹部增强CT评估,所有患者均采用飞利浦64排256层CT。选用连续容积扫描模式,扫描范围从膈顶至盆底,使用高压注射器注入碘海醇(350 mg/ml)80 ml,注射速率为 2.5~3.0 ml/s,采用团注追踪法,当腹主动脉腔内感兴趣区CT值达到150 Hu时行动脉期扫描,之后分别延迟30、120 s扫描获得静脉期和延迟期图像。评估内容包括肝转移灶的数量及分布、最大转移灶的大小(轴位扫描,测量最长径)、原发病灶大小及侵犯深度、周围淋巴结转移、影像学鉴别有无远处转移,并计算胃原发病灶及肝最大转移灶三期(动脉期、静脉期和延迟期)峰值强化数值。
1.5 统计学处理 采用SPSS 18.0统计软件。计数资料比较采用χ2检验或Fisher确切概率法;将单因素分析差异有统计学意义的指标纳入多因素logistic回归,相对风险用HR和95%CI表示。通过R语言“pROC”包绘制ROC曲线,计算AUC,通过R软件的“rms”包构建胃癌肝转移转化治疗疗效列线图预测模型,将所有危险因素的评分相加,得到总分对应的概率即为化疗后进展风险,得分越高表明患者化疗后疾病进展风险越高。采用Bootstrap法重复抽样1 000次对列线图模型进行内部验证,并计算一致性指数(concordance index,c-index)确定模型区分度。绘制校准曲线评估预测结果与实际结果的一致性。P<0.05为差异有统计学意义。
2 结果
2.1 胃癌肝转移化疗疗效的因素分析 疾病控制31例,疾病进展22例。单因素分析显示,疾病控制和疾病进展患者血清癌胚抗原(carcinoembryonic antigen,CEA)水平>5 ng/ml、肝转移数目>3个、最大肝转移病灶直径≥3 cm、胃癌病灶静脉期或延迟期增强、肝转移病灶静脉期或延迟期增强的差异均有统计学意义(均P<0.05),见表1。将上述差异有统计意义的指标纳入多因素logistic回归,结果显示,肝转移数目和胃癌病灶增强模式是影响胃癌肝转移化疗疗效的独立危险因素(均P<0.05),见表2。
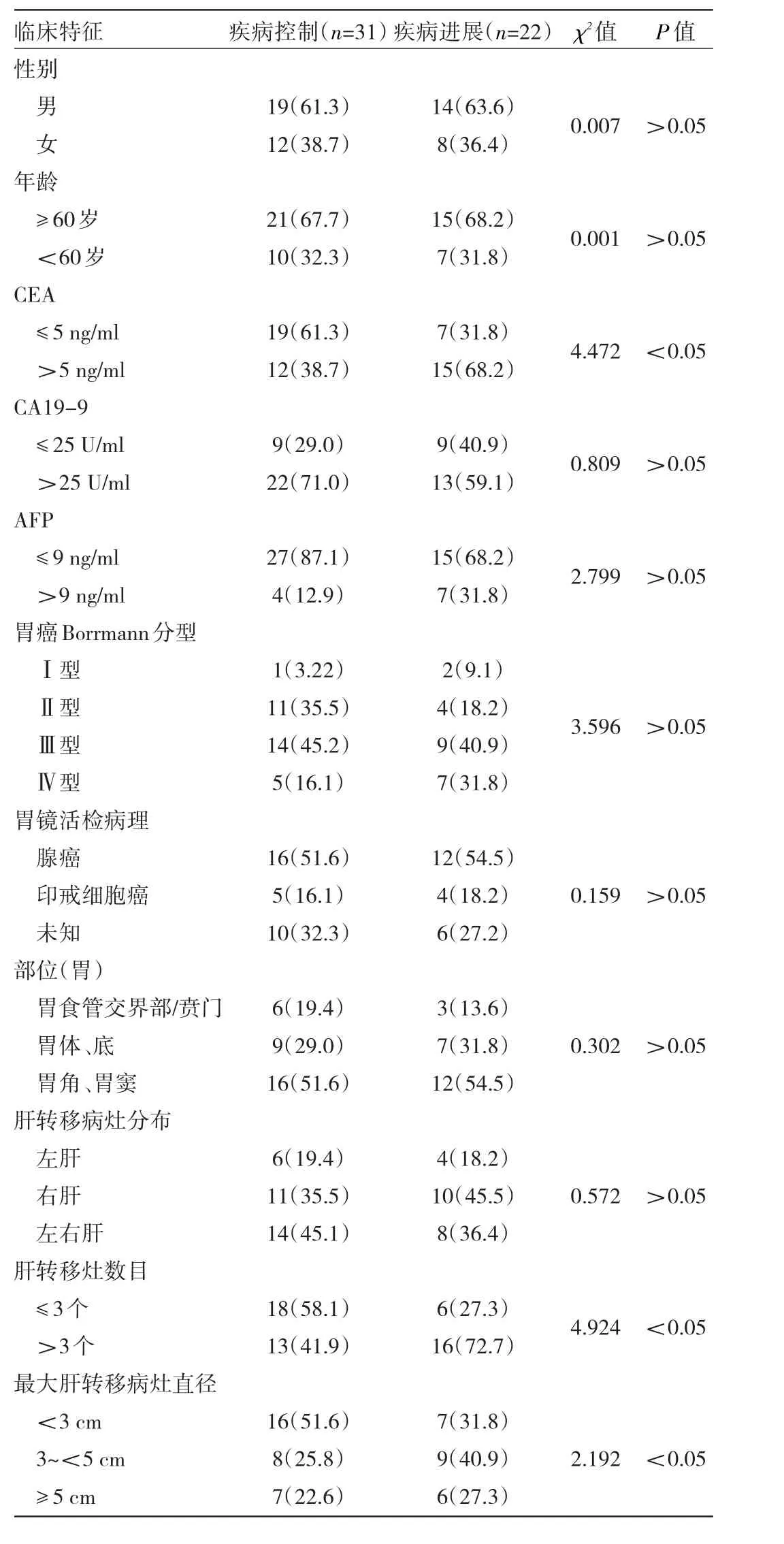
表1 影响53例胃癌肝转移化疗疗效单因素分析[例(%)]
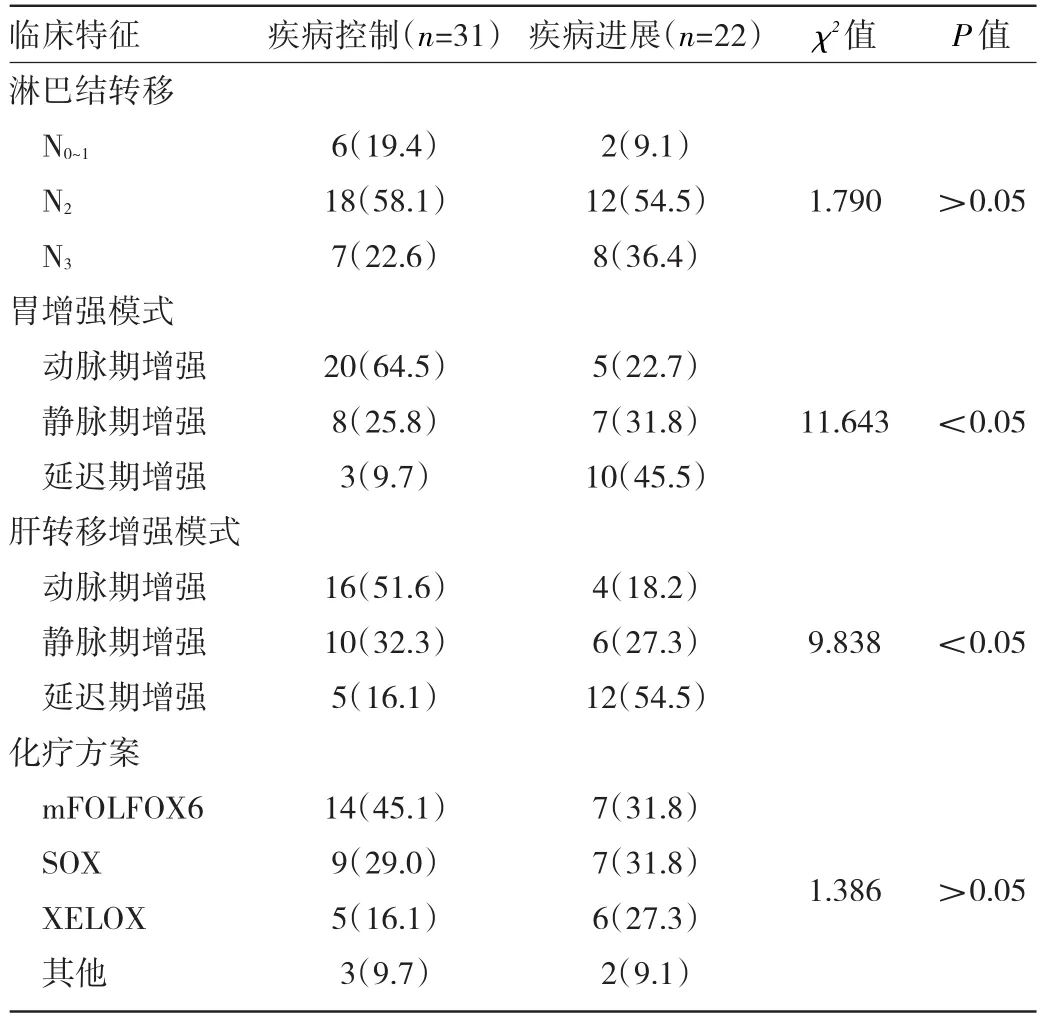
续表1

表2 胃癌肝转移化疗疗效多因素logistic分析
2.2 不同因素联合模式预测胃癌肝转移患者化疗疗效分析 绘制独立危险因素肝转移数目联合胃癌病灶增强模式两因素和血清CEA水平、肝转移数目、最大肝转移直径、胃癌病灶增强模式和肝转移病灶增强模式五因素的ROC曲线,结果显示,肝转移数目联合胃癌病灶增强模式两因素AUC为0.806,血清CEA水平、肝转移数目、最大肝转移直径、胃癌病灶增强模式和肝转移病灶增强模式五因素AUC为0.873,血清CEA水平、肝转移数目、最大肝转移直径,胃癌病灶增强模式和肝转移病灶增强模式五因素具有更好地预测胃癌肝转移患者化疗疗效价值,见图1。
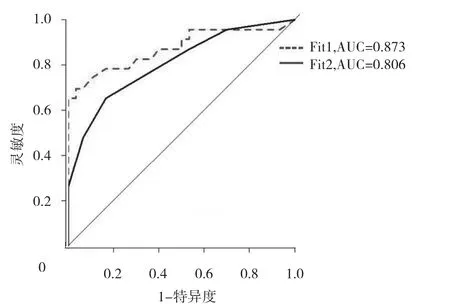
图1 不同因素联合模式预测胃癌肝转移患者化疗疗效的ROC曲线
2.3 列线图预测模型的建立及内部验证 将上述多因素logistic回归筛选出的变量代入列线图模型,结局指标选取胃癌肝转移化疗3周期后疾病进展风险,建立胃癌肝转移化疗有效预测模型,见图2。根据每个危险因素对应列线图上方的标尺得到该因素分数,通过对各因素评分相加得到总分,总分对应的值即为列线图模型预测胃癌肝转移化疗后疾病进展风险。使用Bootstrap法重抽样对模型进行内部验证,内部重复抽样1 000次,同时绘制校准曲线,见图3。3条曲线走向一致且靠拢,显示本模型的预测概率和实际概率具有较好的一致性。该模型内部验证显示:Emax=0.122,Evag=0.060,U=0.038,c-index=0.914。由此可见,本模型与理想模型最大偏移及最小偏倚小,与理想模型接近。
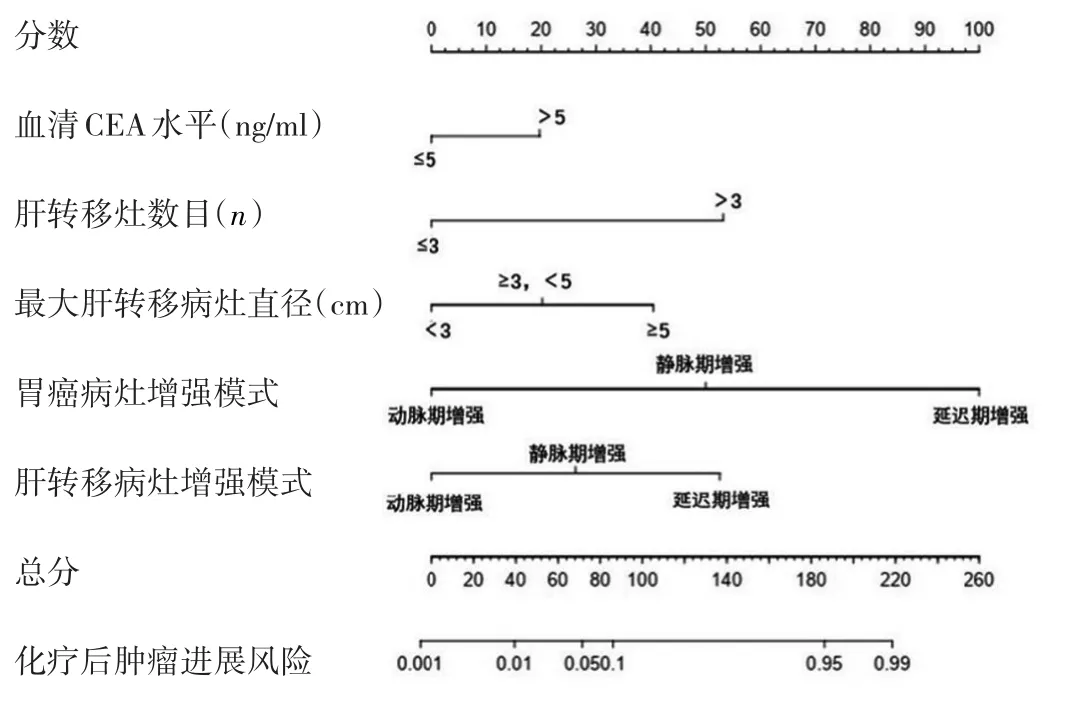
图2 胃癌肝转移化疗疗效的列线图

图3 胃癌肝转移化疗疗效列线图模型内部验证图
3 讨论
胃癌肝转移因侵袭性的肿瘤行为且往往伴有其他部位远处转移,一直被认为是胃癌晚期无法行根治性切除,美国国立综合癌症网络指南推荐根据患者体力情况行全身化疗或最佳支持治疗[5]。近年来,虽然化疗和分子靶向生物治疗取得了重大进展,但到目前为止,治疗后患者中位生存时间不超过12个月[6-7],有学者探究了外科手术切除等针对肝转移灶局部治疗的措施,部分患者获得了生存时间的受益,显示出多学科综合治疗对于改善胃癌肝转移患者预后的潜在前景。虽然REGATTA试验未能提高接受胃切除加术后化疗晚期胃癌患者的生存期(14.3个月比16.6个月)[8],但是AIO-FLOT3结果显示与单独接受化疗的患者相比,接受术前化疗然后行手术切除患者的生存期更长(22.9个月比10.7个月)[9]。两项研究设计的设计及结果差异提示,患者选择、手术策略和治疗模式是影响胃癌肝转移患者预后的关键因素之一。从常规临床应用的角度出发,客观评估胃癌肝转移患者的临床资料是研究胃癌肝转移治疗策略的必要条件,而胃癌肝转移组织学类型、浸润模式和肿瘤的病理、分子生物学信息无法通过术前胃镜等检查来实现,因此针对胃癌肝转移患者建立化疗疗效预评估系统,有着重要的临床决策指导意义。
肿瘤标志物在许多研究中报道可以初步评估胃癌的疾病分期,肝转移数目、最大肝转移直径、胃原发病灶和淋巴结转移评估是胃癌肝转移分型的重要标准[10],本研究发现,血清CEA水平、肝转移灶数目、最大肝灶转移直径与胃癌肝转移患者化疗后疗效评估有关,多因素logistic分析显示肝转移数目是影响胃癌肝转移化疗疗效的独立预后因素之一。影像学评估是胃癌肝转移临床评估分期的重要手段,目前已有多位学者报道,胃癌的CT增强方式因组织学类型而异,未分化型胃癌在延迟期表现为峰值强化,CT衰减值明显高于其他类型胃癌[11]。由标记纤维组织间质构成丰富的胃癌在三相螺旋CT上表现为逐渐强化。印戒细胞组织学的胃癌在门脉期比其他组织学的胃癌表现出更高程度的对比增强。大多数印戒细胞癌表现为恶性细胞群的弥漫性浸润性生长,并与未成熟和成熟的纤维化混杂在一起,因此往往表现为逐渐强化,成熟的瘢痕(纤维化)主要由致密的胶原纤维组成,细胞和血管较少,而早期或未成熟的纤维化则含有丰富的成纤维细胞和新生血管。有研究探讨了CT增强与胃癌根治性切除术后复发的关系,发现胃癌病变动脉期明显增强与肿瘤血管生成和淋巴管侵犯有关,与血行性或淋巴性复发的高发生率有关[12]。本研究结果显示,胃癌肝转移患者原发病灶及最大肝转移病灶的动脉期峰值强化预示较好的化疗临床获益,动脉期强化往往提示分化型胃癌病例分型,且肿瘤间质未成熟纤维化,或许和良好的化疗反应相关,联合胃癌肝转移原发病灶及最大肝转移病灶的强化模式评估患者化疗疗效具有重要临床价值。
本研究将胃癌肝转移相关临床病理学因素纳入并构建胃癌肝转移化疗疗效风险评估模型,列线图的分数可以更简便、更准确地预测胃癌肝转移治疗疗效,可以为临床工作提供一定的帮助。但本研究为单中心的回顾性研究,还有待外部队列的验证和多中心的前瞻性研究来进一步验证其临床应用价值。
综上所述,胃癌肝转移治疗存在一定争议,本文系统性回顾胃癌肝转移患者的临床资料,结合肿瘤增强CT检查的影像表现,分析并预测胃癌肝转移患者化疗后进展风险,初步构建列线图模型,对于指导临床医师胃癌肝转移治疗的临床决策具有一定参考价值。

