吡咯替尼联合卡培他滨在老年HER-2阳性晚期乳腺癌患者中的应用效果
莫淑芬 钟海鸣 许靖靖 郁德杰
广东省农垦中心医院肿瘤内科,广东湛江 524000
乳腺癌发病率较高,是威胁女性生命的常见疾病,家族史、肥胖、饮食不调、饮酒等均会增加发病风险。人类表皮生长因子受体-2(human epidermal growth factor receptor-2,HER-2)是确诊乳腺癌分子类型的重要检查指标,HER-2阳性的乳腺癌恶性程度较高,其侵袭性更高,肿瘤进展更快,复发转移的风险较高,临床预后差,需给予积极抗HER-2治疗[1-2]。卡培他滨(Capecitabine,Cap)是治疗晚期乳腺癌的重要药物,对肿瘤细胞进行靶向性杀伤,可控制肿瘤进展,但应用有限[3]。吡咯替尼可抗HER-1、HER-2、HER-3及HER-4活性,抑制肿瘤细胞生长,在晚期乳腺癌治疗中有一定优势。既往研究表明[4],其与Cap联用在晚期乳腺癌上疗效显著,副反应小。在HER-2阳性乳腺癌的二线治疗中,吡咯替尼和拉帕替尼是常用的药物,最新的研究表明,吡咯替尼对于HER-2阳性乳腺癌的疗效比拉帕替尼更好,更能延长患者无进展生存期[5]。基于此,本研究旨在观察吡咯替尼联合Cap在老年HER-2阳性晚期乳腺癌患者中的应用效果。现报道如下。
1 资料与方法
1.1 一般资料
本研究经医院医学伦理委员会审批通过(NKLL20009),选取2019年6月至2021年6月广东省农垦中心医院收治的40例老年HER-2阳性晚期乳腺癌患者,通过随机数表法分为两组,每组各20例,对照组年龄60~80岁,平均(67.58±4.73)岁;东部肿瘤协作组评分[5]:2例0分,18例1~2分;激素受体状态:阳性11例、阴性9例;家族史2例;转移部位数量:13例<3处,7例≥3处。观察组年龄60~82岁,平均(67.13±4.81)岁;东部肿瘤协作组评分:3例0分,17例1~2分;激素受体状态:阳性10例、阴性10例;家族史4例;转移部位数量:14例<3处,6例≥3处。两组患者一般资料比较,差异无统计学意义(P> 0.05),具有可比性。患者均自愿签署知情同意书。纳入标准:①晚期乳腺癌符合2018年诊疗专家共识[6]中相关标准,且经影像学、组织病理学检查确诊;②经免疫组化检查,HER-2阳性(HER-2 3+或HER-2 2+,荧光原位杂交检测提示HER-2基因扩增阳性);③患者年龄≥60岁;④依从性好,可配合研究;⑤对本研究药物无过敏史;⑥为二线治疗患者。排除标准:①合并其他恶性肿瘤者;②伴精神系统疾病者;③存在感染性疾病者;④HER-2状态不明盲用靶向治疗者。
1.2 方法
对照组口服Cap片(江苏恒瑞医药,国药准字H20133366,规格:0.15 g/片)1000 mg/m2,2次/d,早晚各1次,连用2周,休息1周,21 d为1个周期,持续治疗2个周期后评价治疗效果;观察组接受Cap联合吡咯替尼治疗,Cap片用药方法及剂量同对照组,并口服吡咯替尼片(江苏恒瑞医药,国药准字H20180013,规格:80 mg/片)治疗,400 mg/d,1次/d,于餐后30 min内口服,每日同一时间用药,连续用药21 d为1个周期,持续治疗2个周期后评价治疗效果。
1.3 观察指标及评价标准
①临床疗效:治疗2个周期后参照实体瘤相关标准[7]评价疗效,其中完全缓解(complete remission,CR):病灶完全消失,持续时间>1个月;部分缓解(partial remission,PR):肿瘤最长径乘积缩小≥50%,至少维持1个月;稳定(stable disease,SD):两直径乘积缩小<50%,且增加≤25%,持续时间>1个月;进展(progressive disease,PD):两直径乘积增加>25%,或出现新病灶。临床控制率(disease control rate,DCR)=(CR+PR+SD)例 数/总例数×100%。②血清肿瘤标志物:于治疗前后采集患者空腹外周静脉血3 ml,以3000 r/min速率离心10 min,取血清,利用美国R&D公司提供的试剂盒,并采用电化学发光法测定血清癌胚抗原(carcino-embryonic antigen,CEA)、糖 类 抗 原125(carbohydrate antigen 125,CA125)水平。③无进展生存期(progression free survival,PFS):随访时间截至2022年6月,记录患者从治疗至疾病进展或病死时间。④毒副反应:比较两组腹泻、恶心呕吐、手足综合征、肝功能受损、粒细胞减少、血小板减少、贫血毒副反应发生情况。
1.4 统计学方法
采用SPSS 25.0统计学软件分析数据,符合正态分布的计量资料以均数±标准差(±s)表示,组间比采用独立样本t检验,组内行配对样本t检验,计数资料以[n(%)]表示,采用χ2检验,采用Kaplan-Meier法绘制生存曲线,组间比较行Log-rank检验,P< 0.05为差异有统计学意义。
2 结果
2.1 两组临床疗效比较
观察组DCR为95.00%,高于对照组的65.00%(P< 0.05)。见表1。
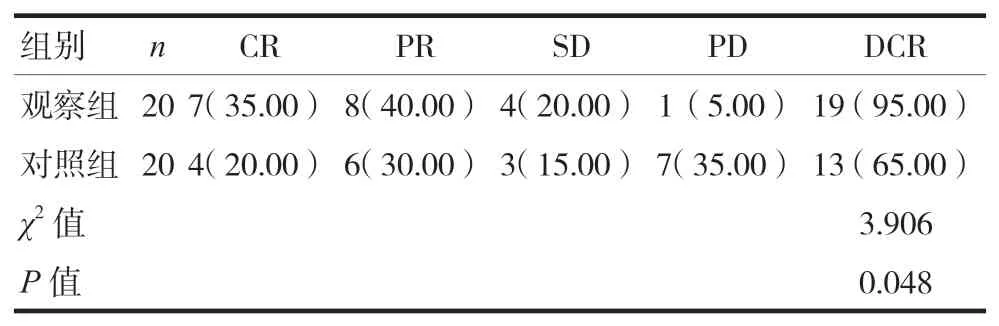
表1 两组临床疗效比较[n(%)]
2.2 两组血清肿瘤标志物比较
治疗前,两组血清肿瘤标志物比较,差异无统计学意义(P> 0.05);治疗后,两组血清CEA、CA199水平显著下降,且观察组低于对照组(P< 0.05)。见表2。

表2 两组血清肿瘤标志物比较(x ± s)
2.3 两组PFS比较
随访时间截至2022年6月,对照组PFS平均为9.286个 月(95%CI:8.213~10.359);观 察 组PFS平均为11.314个月(95%CI:10.889~11.739),观察组PFS明显长于对照组,差异有统计学意义(χ2=4.930,P=0.026)。见图1。
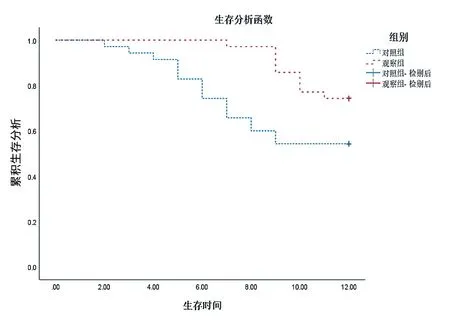
图1 两组晚期乳腺癌患者PFS曲线图
2.4 两组毒副反应比较
两组毒副反应比较,差异无统计学意义(P> 0.05)。见表3。
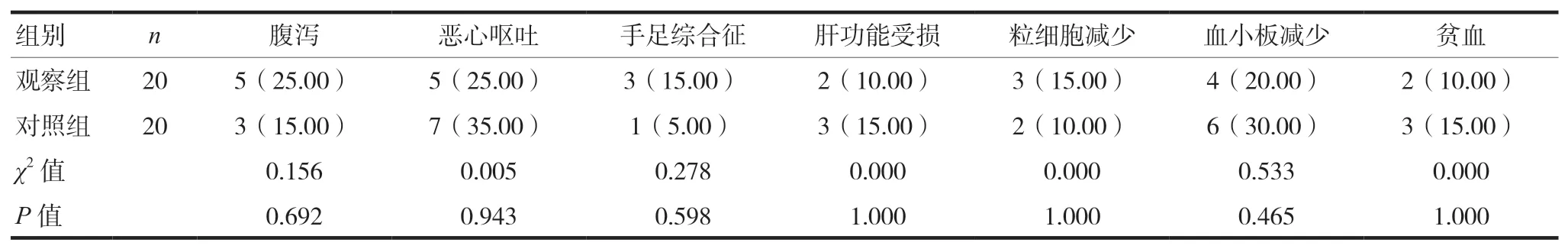
表3 两组毒副反应比较[n(%)]
3 讨论
乳腺癌是女性发病率最高的癌症,且趋于年轻化,病死率较高,仅次于肺癌,严重威胁女性生命安全,15%~20%乳腺癌患者HER受体呈过表达,位于17号染色体上,对化疗药物不敏感,HER-2阳性侵袭性更强,预后差[8-9]。因此,HER-2阳性乳腺癌以抗HER-2蛋白靶向药物治疗为主。曲妥珠单抗是以往治疗乳腺癌经典靶向药物,能明显改善HER-2阳性乳腺癌患者预后,延缓疾病进展,但部分患者对该药物耐药,应用受限[10]。因此,需采取其他有效治疗方案以延长HER-2阳性晚期乳腺癌患者的生存时间。
吡咯替尼是不可逆酪氨酸激酶抑制剂,可通过阻断细胞内HER-2发挥作用,分子质量较小,能够口服用药,与细胞内表皮生长因子受体、HER-2中ATP共价结合,阻止HER-2同质,抑制其磷酸化,进而阻断下游信号通路,达到控制肿瘤生长的目的[11-12]。与曲妥珠单抗比较,吡咯替尼具有一定优势,如作用稳定,口服后耐受性好,能够透过血脑屏障,在治疗乳腺癌中有一定价值[13]。郑向欣等[14]研究报道,吡咯替尼联合Cap治疗HER-2阳性乳腺癌患者,能够延缓疾病进展,提高生存质量,给患者带来希望。
血清CEA、CA125均是乳腺癌常见肿瘤标志物,其中CEA对定性诊断乳腺癌、评估病情及预后等均有较高价值;CA125最初被认为是卵巢癌标志物,但既往研究发现,乳腺癌发生转移时,CA125水平显著升高,对评估乳腺癌病情也有积极意义[15]。本研究结果显示,观察组治疗后DCR高于对照组,血清CEA、CA125水平低于对照组,且PFS明显长于对照组,结果表明,吡咯替尼联合Cap治疗老年HER-2阳性晚期乳腺癌患者效果确切,可控制肿瘤进展,改善肿瘤标志物,延长PFS。这也与郑向欣等[14]研究报道结果一致。吡咯替尼属于小分子酪氨酸激酶抑制剂,与其他常规靶向药物比较,其更容易透过血脑屏障,穿透细胞膜,并直接作用于细胞内靶点,进而阻止肿瘤细胞生长的信号通路,有效抵抗肿瘤,进而降低肿瘤标志物水平,延长患者PFS。吡咯替尼与Cap联合应用,可发挥协同作用,更有效达到抗肿瘤作用[16]。本研究两组毒副反应比较差异无统计学意义(P> 0.05),说明两种药物联用不会增加毒副反应,安全性高。但本研究也有一定局限性,如研究周期有限,随访时间较短,仅观察吡咯替尼联合Cap对老年HER-2阳性晚期乳腺癌患者近期生存情况的影响,关于远期效果还需今后延长随访时间进一步证实。
综上所述,吡咯替尼联合Cap治疗老年HER-2阳性晚期乳腺癌患者,可提高DCR,降低肿瘤标志物水平,延长PFS。

