保安湖水体细菌群落结构时空变化特征及驱动因子
薛 璐 向冬芳 鲜 博 鲍少攀 唐 巍 罗 帅 熊 杰 方 涛
(1. 中国科学院水生生物研究所, 武汉 430072; 2. 中国科学院大学, 北京 100049; 3. 大连海洋大学, 大连 116023)
保安湖(30°12′—30°18′ N, 114°39′—114°46′E)位于长江中下游南岸, 隶属梁子湖水系, 是一个典型的浅水草型湖泊, 由扁担塘、肖四海、桥墩湖和主湖区共四个湖区组成。扁担塘、肖四海、桥墩湖与主湖区之间虽有围栏阻隔, 但湖水仍可通过水道与主湖区保持相通[1,2]。保安湖生物资源丰富,有大型水草20余种, 各类鱼类50余种, 底栖动物70余种, 浮游动物110余种。作为一个拥有优良水资源及丰富生物资源的草型湖泊, 保安湖有条件建设成为我国发展优质高效渔业的重要基地[3]。目前, 关于保安湖生物多样性的研究主要集中在水生植物、底栖动物、浮游动物和鱼类群落等方面[2,4—9],关于细菌群落结构及分布格局仍不清楚。
事实上, 细菌在水环境中发挥着至关重要的作用。细菌作为浮游动物等的被捕食对象是水生态系统食物网中重要组成部分, 在淡水水生环境特别是富营养湖泊中的物质分解及营养循环过程中发挥着重要作用[10,11]。细菌还可以指示、影响和调节湖泊水质, 如蓝藻是水体富营养化的标志, 放线菌可以促进水生态修复及水质净化[12]。此外, 水体细菌群落组成变化也可影响水生动物体表和肠道微生物群落组成, 从而影响水生动物健康[13]。
近几十年来, 随着科技的飞速发展, 微生物检测技术也在不断更新发展并运用于相关领域中。在微生物研究初期, 主要采用纯培养方法对环境微生物进行研究, 但环境中只有0.001%—10%的微生物可供培养, 因此传统的微生物研究方法具有极大的局限性[14]。为了克服传统方法的缺陷, 越来越多的分子生物学方法被应用到微生物研究中, 如荧位原光杂交(FISH)[15]、限制性片段长度多态性分析技术(RFLP)[16]、末端限制性片段长度多态性分析技术(T-RFLP)[17]、变性梯度凝胶电泳(DGGE)[18]、实时定量PCR技术(Real-Time PCR)[19]、宏基因组学技术[20]和高通量测序技术[21]等, 这些方法具有灵敏度高、通量高和无需体外培养等优点, 并且可以快速分析微生物群落结构及多样性[22]。其中宏基因组测序技术通过对环境样品中微生物的总DNA进行测序分析, 规避了传统方法中的缺陷, 全面真实地揭示微生物群落多样性, 提供更加精确的物种分类, 因此近年来被广泛应用于研究环境细菌群落结构和多样性以及关键影响因子[23—26]。
本研究通过对保安湖细菌群落和水质因子周年的季度调查监测, 应用宏基因组测序技术获取保安湖水体细菌群落信息, 分析保安湖细菌群落组成结构、多样性及时空分布特征; 通过建立零模型和网络分析, 解析细菌群落构建过程及种间相互作用;通过典范对应分析探讨细菌群落与环境因子的相关性, 揭示保安湖水域细菌多样性变化的关键影响因子, 为维持和保护渔业湖泊生物多样性提供理论依据。
1 材料与方法
1.1 采样区概况
本研究采样点覆盖范围为114°39′43″E—114°44′27″E, 30°12′36″N—30°17′47″N, 其中在扁担塘设置3个采样点, 肖四海设置3个采样点, 桥墩湖设置4个采样点, 主湖区设置10个采样点。全湖共设置20个采样点, 样点位置见图 1。
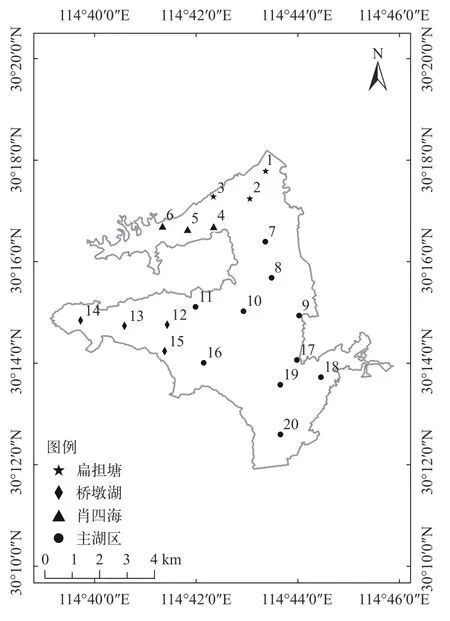
图1 保安湖采样点分布Fig. 1 Sampling stations in Bao’an Lake
1.2 样品采集及测定
于2019年4月(春季)、7月(夏季)、10月(秋季)及2020年1月(冬季)进行采样,其中10月份样品设置了3次平行采样。采取表层0.5 m水样2 L。其中500 mL水样用于水质指标测定, 温度(T)、溶解氧(DO)和pH等水质参数用YSI多参数水质监测仪现场测定, 总氮(TN)、总磷(TP)、氨氮(NH3-N)、硝氮、亚硝氮、高锰酸盐指数(CODMn)和叶绿素a(Chl.a)指标按照《水和废水监测分析方法》[27]检测。每个样点均取350 mL水样经200 μm滤网过滤掉大颗粒, 摇晃均匀后加入1000个嗜热四膜虫(SB210细胞株), 抽滤至0.22 μm PC膜上, 并保存于-80℃冰箱, 用于后续微生物多样性检测。
采用CTAB法提取DNA, 即用CTAB分离缓冲液溶解DNA后, 使用氯仿-异戊醇去除蛋白质, 再使用1%琼脂糖凝胶分析DNA降解程度及潜在污染。使用纳米光度计(IMPLEN, CA, USA)测定DNA纯度, 使用Qubit 2.0 荧光仪(Life Technologies, CA,USA)测定DNA浓度。选取浓度大于1 μg的质量合格的DNA, 打断为350 bp左右长度的片段, 补齐末端后向3′端加上“A”尾构成测序文库。质检合格的文库基于Illumina HiSeq 4000平台进行测序。
1.3 数据处理与统计分析
使用fastQC(v0.11.9)和Fastx trimmer(v0.0.14)对测序所得原始数列进行质量评估及过滤得到有效序列, 通过BLASTN比对至SILVA数据库, 筛选出rDNA相关读段(reads)(e<10-5)。使用MEGAHIT(v1.1.3)对rDNA reads进行组装, 得到所有样本的rDNA叠连群(contigs)。基于16S的hmm profile,使用nhmmer比对确定rDNA contings中16S区域并截取。将相似度97%以上的16S rDNA序列聚合得到rDNA参考序列。使用bwa(0.7.17-r1188)将所有样品rDNA reads一一对比至参考序列, 使用feature-Counts(v.1.6.0)统计结果, 使用RPKM(Reads Per Kilobase per Million mapped reads)标准化得到OTU(Operational Taxonomic Units)丰度表, 并以SB210细胞为内参细胞对OTU丰度进行均一化, 得到最终的OTU丰度表。为提高物种注释精度, 将OTU的代表序列与SILVA、PR2、nt多个数据库进行比对。
根据所得OTU丰度表, 计算保安湖水体细菌不同季节、不同湖区的Alpha多样性指数并进行显著性差异检验, 基于Bray-Curtis距离算法进行非度量多维尺度分析(NMDS)来可视化不同季节和湖区之间细菌群落的Beta多样性差异, 以期研究保安湖水体细菌群落多样性的时空动态差异。通过典范对应分析(CCA)确定保安湖水质因子对细菌群落组成的解释力, 并结合Mantel检验进行保安湖水体细菌群落组成和环境因子的相关性分析。通过零模型衡量确定性过程和随机性过程在保安湖水体细菌群落构建过程中的主导地位, 计算出的标准化随机率(Normalized stochasticity ratio, NST)若低于0.5,则群落构建过程由确定性过程主导, 若高于0.5, 则由随机性过程主导[27]。对于符合正态分布的变量使用方差分析检验显著性差异, 不符合正态分布的变量使用非参数检验分析显著性差异。使用R包“Vegan”进行alpha多样性指数计算、Mantel检验及典范对应分析(CCA), 使用R包“spaa”计算生态位宽度, 使用R包“NST”计算标准化随机率(NST), 使用R语言计算所有OTU两两之间的 Spearman相关性,设置相关性阈值为r≥0.6或r≤-0.6, 显著性值P<0.01, 使用“Gephi”软件绘制无向网络图。所有图表均用R语言、Origin Pro 2021及Gephi进行绘制。
2 结果
2.1 保安湖细菌多样性分析
对保安湖全湖进行宏基因组测序分析, 共获得4192个OTUs, 其中2568个OTUs为细菌, 占据了全部OTUs的61.26%。从细菌OTU数目上来看, 保安湖水体细菌种类呈现秋、夏、春、冬逐渐减少的季节趋势, 且主湖区可观测到最多的细菌种类, 其次为桥墩湖(图 2)。

图2 不同湖区细菌OTU数目的季节变化Fig. 2 Seasonal changes of the numbers of bacteria OTUs in different lake areas
双因素Scheirer-Ray-Hare非参数检验表明, 保安湖水体细菌丰富度指数、均匀度指数、香农指数及辛普森指数均存在显著的季节性差异(HRichness=68.18,HPielou=40.47,HShannon=54.53,HSimpson=39.55,P<0.05), 但在湖区间无明显差异(HRichness=1.72,HPielou=3.20,HShannon=2.23,HSimpson=2.30,P>0.05),且季节和湖区间无交互作用(HRichness=1.66,HPielou=13.52,HShannon=8.74,HSimpson=13.13,P>0.05)。保安湖水体细菌丰富度指数呈现主湖>扁担塘>桥墩湖>肖四海的空间变化趋势, 但湖区之间均无显著差异(P>0.05), 季节性变化表现为秋季>夏季>春季>冬季, Kruskal-Wallis检验(K-W检验)成对比较结果表明, 秋季丰富度显著高于春、夏季, 春、夏季显著高于冬季(P<0.05)。均匀度指数空间变化趋势表现为主湖>桥墩湖>肖四海>扁担塘(P>0.05), 季节变化趋势为夏季>秋季>冬季>春季, K-W检验表明夏季均匀度显著高于春、冬季, 秋季显著高于春季(P<0.05)。香农指数及辛普森指数空间变化趋势为主湖>桥墩湖>扁担塘>肖四海(P>0.05), 香农指数季节变化趋势表现为秋季>夏季>春季>冬季, 辛普森指数季节变化趋势为夏季>秋季>春季>冬季, KW检验表明保安湖水体细菌夏、秋季香农指数和辛普森指数显著高于春、冬季(P<0.05; 表 1和表 2)。总体来说, 在OTU水平上, 保安湖水体细菌Alpha多样性空间差异性不显著, 但季节性差异显著, 表现为秋季最高, 夏季次之, 其次是春季, 冬季最低。

表1 各季节保安湖细菌多样性指数Tab. 1 Seasonal diversity index of bacteria in Bao’an Lake

表2 不同湖区保安湖细菌多样性指数Tab. 2 Diversity index of bacteria in different lake area of Bao’an Lake
保安湖水体细菌群落Beta多样性分析如图 3所示, Stress<0.01表明分析结果具有较好的代表性,说明2019年保安湖水体细菌群落不同季节结构差异明显, 且春、冬季细菌群落结构较为相似, 夏、秋季细菌群落结构较为相似, 而不同湖区之间细菌群落结构无明显差异。

图3 保安湖细菌Beta多样性分析Fig. 3 Beta diversity of bacteria in Bao’an Lake
在保安湖水体共检测到34个菌门, 主要菌门有7个(占比1%以上), 如图 4A所示, 结果表明保安湖水体主要菌群来自于变形菌门(Proteobacteria)、放线菌门(Actinobactetiota)、蓝藻门(Cyanobacteria)、拟杆菌门(Bacteroidota)、疣微菌门(Verrucomicrobiota)、浮霉菌门(Planctomycetota)和绿弯菌门(Chloroflexi)。其中, 保安湖春、冬季优势菌群为变形菌门、放线菌门, 夏、秋季优势菌群为变形菌门、蓝藻门及放线菌门。图 4B显示了主要菌门不同季节之间的显著性差异, 在夏、秋季, 放线菌门及变形菌门相对丰度显著降低, 蓝藻门及浮霉菌门相对丰度则显著增加, 拟杆菌门和绿弯菌门相对丰度在春季最高, 夏季最低, 且存在显著差异(P<0.05)。

图4 保安湖不同季节主要细菌群落相对丰度与差异性显著分析Fig. 4 Relative abundance and significant difference analysis of main bacterial phylum in Bao’an Lake in different seasons
2.2 保安湖细菌群落与环境因子的关系
对保安湖细菌群落与环境因子之间的相关性进行Mantel tests统计检验及CCA分析。CCA结果表明: 环境因子对保安湖细菌群落组成的总解释量为68.2%, 轴一解释度为57.01%, 轴二解释度为11.19%(图 5)。在不同季节下, 保安湖细菌群落结构受环境因子影响不同。夏季样点主要分布在第一象限, 说明保安湖夏季细菌群落组成主要和T、CODMn、TP及pH呈正相关关系; 秋季样点主要分布在第四象限, 说明保安湖秋季细菌群落组成主要和Chl.a、DO呈正相关关系; 春、冬季样点主要分布在第二象限, 说明春冬季细菌群落组成主要和SD呈正相关关系。另外, 通过Mantel检验可知,SD、T、pH、DO、CODMn、Chl.a和TP是对保安湖细菌群落组成具有显著影响的因子(表 3)。

表3 保安湖细菌多样性与环境因子相关性分析Tab. 3 Correlation analysis between bacterial diversity and environmental factors in Bao’an Lake

图5 保安湖细菌多样性与环境因子的相关性分析Fig. 5 Correlation analysis between bacteria and environmental factors in Bao’an Lake
2.3 保安湖细菌群落构建过程
为了明确确定性和随机性过程在保安湖细菌群落组装过程的主导地位, 通过计算零模型NST进行分析。结果显示, 春、夏、秋季NST>0.5, 表明随机过程主导了春、夏、秋季保安湖水体细菌群落构建过程, 而冬季NST<0.5, 表明确定性过程在冬季保安湖细菌群落构建中占支配地位(图 6A)。不同季节细菌生态位宽度不一, 保安湖水体秋季细菌生态位宽度最大, 其次为夏季、春季, 冬季最低(图 6B)。
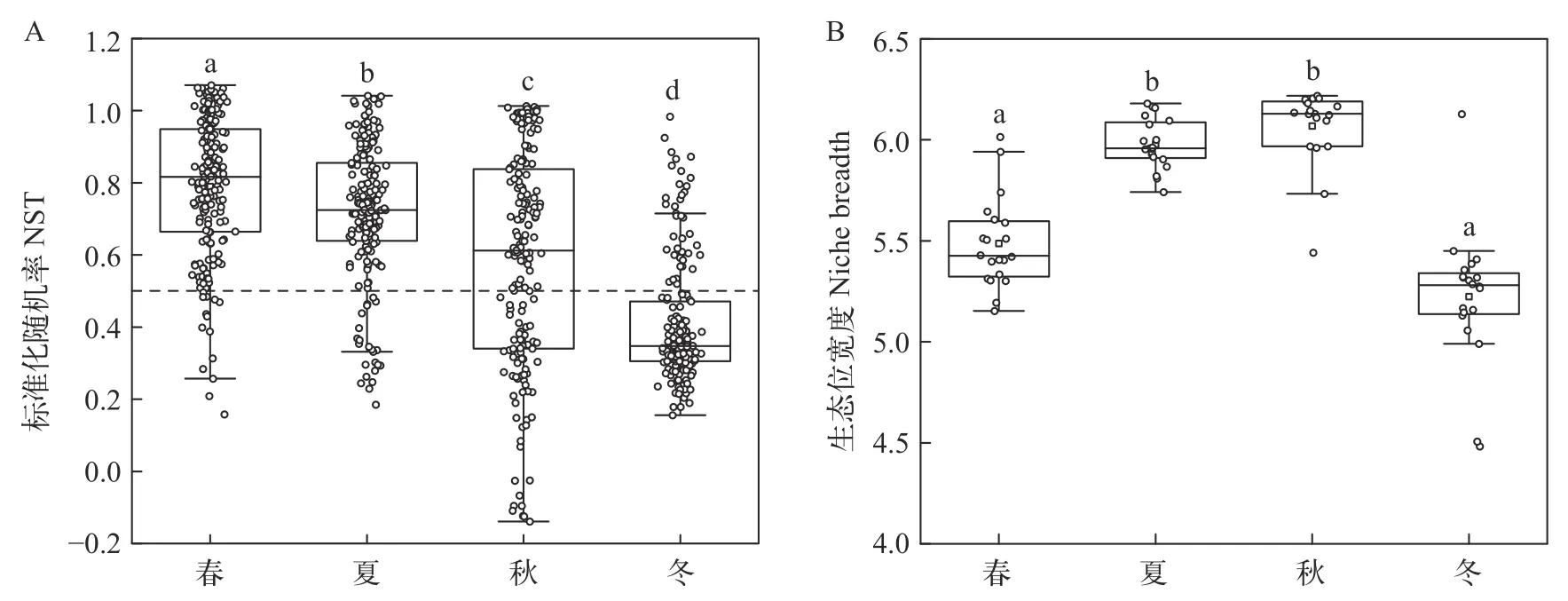
图6 不同季节保安湖细菌NST值分布和生态位宽度Fig. 6 Seasonal NST value and niche breadth of bacteria in Bao’an Lake
2.4 不同季节保安湖细菌互作网络
计算不同季节两两OTU之间的Spearman相关系数, 基于显著相关性(P<0.01, Spearman相关系数r≥0.6和r≤-0.6)构建了2019年不同季节保安湖细菌的互作网络(图 7), 模块化分析发现春、夏、秋、冬季保安湖水体细菌互作网络分别可以划分为9、5、6和5个主要模块(OTU占比大于1%的模块), 在网络图中相同颜色的节点表示同一模块的细菌, 它们更倾向于占据相同生态位。从细菌互作网络拓扑参数(表 4)可以看出, 保安湖水体细菌相互作用以正相互作用为主, 从春季到冬季, 正相互作用比例逐渐增高。保安湖冬季细菌互作网络节点数、平均路径长度均低于其余季节(除秋季平均路径长度外), 而边数、平均度和网络密度均明显高于其余季节, 这表明保安湖冬季细菌之间的互作网络格局最复杂紧密。从春季到冬季, 保安湖细菌互作网络存在着由简单松散到复杂紧密的变化趋势, 表明保安湖水体细菌之间相互作用从春季到冬季变得更加复杂。

表4 不同季节保安湖细菌互作网络拓扑性质Tab. 4 Topological properties of bacterial interactions network in Bao’an Lake from different seasons
3 讨论
3.1 保安湖细菌群落时空分布特征
2019年保安湖水体细菌菌群主要由变形菌门、放线菌门、蓝藻门、拟杆菌门、疣微菌门、浮游菌门及绿弯菌门构成(图 4), 这和淡水湖泊中细菌群落研究结果基本相似[28—30]。
保安湖水体细菌多样性季节性差异显著, Beta多样性分析结果表明春、冬季细菌群落结构相似,优势菌群为变形菌门、放线菌门, 夏、秋季细菌群落结构相似, 优势菌群为变形菌门、蓝藻门及放线菌门。一般来说, 变形菌门和放线菌门通常是水质较好的淡水中的主导菌群[31,32], 这和本研究结果一致, 对保安湖水体富营养化状况评价发现保安湖水体春、冬季富营养化程度表现为接近中营养化水平, 夏、秋季表现为接近轻度富营养化水平。保安湖水体细菌群落Alpha多样性在夏、秋季多样性显著高于春、冬季, 且保安湖水体细菌群落丰富度及多样性与重度富营养化的汤逊湖、青菱湖和黄家湖相比更高[33], 在Wang等[34]对不同富营养化水平淡水湖泊中微生物群落多样性的研究中也发现了相同规律, 轻度富营养化湖泊中微生物多样性高于中度富营养化和重度富营养化湖泊, 说明轻度富营养化湖泊环境可能更适合细菌生存, 随着水质恶化,水体细菌多样性会有所降低。夏秋季细菌多样性高于春冬季, 这可能是由于夏秋季水温高, 氮、磷营养盐较丰富, 有利于微生物繁殖生长, 从而导致不同季节间出现较大的细菌群落差异[35]。蓝藻门相对丰度从春季到夏秋季显著升高, 到了冬季又显著降低, 这是因为高温和高磷是有利于蓝藻生长的因素[36], 保安湖夏、秋季较高的水温和总磷浓度更适合蓝藻门生长, 张雅洁等[28]也发现T和TP的变化导致了蓝藻丰度的变化。而放线菌门相对丰度变化与蓝藻门相对丰度变化呈现完全相反的趋势, 先前也有研究表明放线菌门和蓝藻门之间存在负相关关系, 前者在营养物质丰富和适宜蓝藻生长的温度条件下, 占比无法超越后者[37], 这可能是因为蓝藻大量繁殖会导致放线菌新陈代谢活动减弱, 细菌数量减少[38]。浮霉菌门在夏秋季相对丰度显著高于春冬季, 可能是因为保安湖水体夏、秋季溶解氧较高, 而浮霉菌门中的浮霉菌属和小梨形菌属等都是好氧菌, 在夏秋季水体环境中更适合生长。
在空间上, 保安湖水体细菌多样性空间差异性不显著, 不同湖区间细菌群落结构较相似。在主湖区、桥墩湖可以观测到更多的细菌种类, 这可能是由于主湖区和桥墩湖富营养化水平高于扁担塘及肖四海, 营养盐较多, 可以为细菌提供更多的营养物质促进生长[39]。
3.2 保安湖细菌群落对环境因子的响应
水体中细菌群落结构和环境因子的相关性受到广泛关注。Qu等[40]通过高通量测序技术研究了南水北调工程中线末端水库(密云水库)细菌群落动态及与环境参数的关系, 结果表明密云水库细菌群落结构与温度、溶解性固体、总磷、溶解氧及总氮浓度显著相关。黄小兰等[41]对赣江下游河湖交错带微生物群落的研究表明影响冬季和夏季微生物分布特征的主要理化因子为总氮、总磷、pH。由此可见, 水环境因子能显著影响水体细菌群落结构组成, 不同水体细菌群落结构的驱动因子不同,但也存在共性。在本研究中, pH、T、SD、DO、TP 、CODMn及Chl.a是保安湖水体细菌群落组成的重要驱动因子。由Mantel检验结果可知, T对保安湖水体细菌群落结构影响最大(R=0.6013,P<0.01),Zhang等[42]和Song等[43]对巢湖、西湖的研究也发现T是影响水体细菌群落结构的主要因素, 因为在一般情况下, 不同细菌适宜生长和繁殖的最佳温度有所差异, 比如蓝藻门中Microcystis最佳生长温度为25—32℃,Aphanizomenon最佳生长温度范围为23—29℃[44], 这就导致T对水体细菌群落结构可直接产生影响。保安湖水体夏季细菌群落结构与T和TP呈正相关性, 因为夏季水温高, 比较适合细菌特别是蓝藻门的生长[35], Jiang等[45]也发现蓝藻门在高温夏季相对丰度有所增加。一般来说, TP含量越高, 蓝藻门的相对丰度也越高, 在本研究中也发现了类似结果, 保安湖夏、秋季水体总磷含量较高,蓝藻门相对丰度在夏、秋季也显著高于春、冬季。Shang等[46]研究发现pH和溶解氧是导致淡水湖泊微生物群落季节性变化的潜在主要因素, 这和本研究所得结果一致, pH不仅可以直接影响细菌生长状态, 也能通过改变水的理化特性影响细菌群落结构和多样性。DO浓度可能也会影响水体细菌群落结构, 因为需氧菌由于缺乏抗氧化酶需要氧气才能生长发育, 而厌氧菌则需生活在缺氧环境中[47], 保安湖夏、秋季DO浓度较高, 有利于浮霉菌属、小梨形菌属等好氧菌生长, 这可能是浮霉菌门在夏、秋季相对丰度显著增加的原因。Chl.a是浮游植物现存量的重要指标[48], 异养细菌的代谢与浮游植物密切相关, 浮游生物的代谢产物、分泌物及浮游动物的滤食作用均会影响细菌群落组成[49], 从而导致Chl.a对水体细菌群落结构产生影响, 本研究中保安湖水体细菌多样性与Chl.a含量变化趋势一致, 且在秋季存在显著正相关, 一些研究也表明细菌丰度和Chl.a之间存在正相关关系[50,51]。保安湖春、冬季水体细菌群落组成与SD呈正相关性, 保安湖春、冬季SD高于夏、秋季, 这是因为夏、秋季蓝藻的大量繁殖降低了水体的透明度。
3.3 保安湖细菌群落构建过程
生态位宽度是影响物种多样性及群落结构的关键因素, 常用来表示一个种群在群落中所利用资源的总和[52]。保安湖细菌生态位宽度从大到小排序依次为秋、夏、春、冬(图 6B), 这是因为保安湖细菌丰富度及多样性也呈现秋、夏、春、冬依次递减的趋势。在这种情况下, 秋季种间竞争更加激烈, 此时较宽的生态位可以使种群得到足够的资源;而冬季细菌种类少, 种间竞争力减小, 并且秋末冬初保安湖水生植物的凋零分解为细菌生长提供了营养物质, 在食物丰富的环境中, 可能导致细菌选择性利用资源和狭窄的生态位宽度[53]。
群落的确定性或随机性组装过程决定了微生物群落的组成和多样性, 并决定了其功能[54]。确定性过程基于生态位理论, 强调确定性的非生物因素(如温度、光照等环境条件)和生物因素(如共生、竞争等相互作用)主导微生物群落构建过程[55], 而随机性过程基于中性理论, 强调随机过程如出生、死亡、扩散等主导微生物群落构建过程[56]。本研究通过计算不同季节保安湖水体细菌群落标准化随机率发现, 春、夏、秋季NST>0.5, 表明细菌群落构建过程中由随机性过程主导, 在冬季NST<0.5,表明细菌群落构建过程由确定性过程主导(图 6A)。这可能是由于春、夏、秋季保安湖水体细菌具有更广泛的生态位[57], 且降水较多, 与枯水期相比湖泊生境均匀性和河流连通性更高, 导致细菌迁移率更高, 扩散能力增强[58], 而冬季保安湖细菌生态位宽度相对较窄, 受扩散限制影响更大[57]。生境过滤作用是指某类型生境通过水文、气候等环境条件及生态位的分化将适宜物种筛入相同生态位的过程[59,60], 本研究通过对保安湖水体细菌互作网络模块化发现, 春、夏、秋、冬季保安湖水体细菌互作网络可分为101、97、66和10个模块, 其中各季节主要模块(OTU占比大于1%的模块)数分别为9、5、6和5, 而模块代表可以位于同一生态位的物种集合, 相比较于其他季节, 保安湖水体细菌在冬季占据更多的相同生态位, 因此我们推测生境过滤作用可能是冬季保安湖水体细菌群落构建过程的驱动因子。
3.4 保安湖细菌群落的互作关系
自然生态系统中的微生物并不是个体种群的简单累积, 而是通过竞争、互利共生、偏害共生、掠食和寄生等相互作用形成复杂的生态网络, 利用网络分析可以研究不同生境下微生物间的相互作用[61—63]。网络分析结果显示各季节参与互作的主要菌群基本相同, 为变形菌门、拟杆菌门、蓝藻门、Patescibacteria、放线菌门、疣微菌门、浮霉菌门和绿弯菌门等, 但不同季节细菌参与互作的比例有所不同, 如变形菌门在冬季互作网络占比为31.03%, 明显低于春、夏、秋季(春、夏、秋季占比分别为35.60%、36.06%和35.90%), 拟杆菌门在春、夏、秋季互作网络中占比分别为11.64%、11.60%和11.34%, 在冬季占比增加到了13.60%, 这一变化趋势在放线菌门中也有所体现。正相互作用主导了保安湖水体细菌相互作用, 表明保安湖水体细菌之间更多的是合作而不是竞争[64], 此时共生网络中相同颜色的节点在环境中更倾向于占据相似的生态位。负相互作用可能会促进网络稳定性,从春季到冬季, 保安湖细菌相互作用负/正比逐渐降低, 说明保安湖冬季细菌网络更易受到外部环境的扰动, 群落相互作用的稳定性较差, 但细菌仍可以通过减少竞争和加强合作来应对环境压力[65]。在本研究中, Spearman相关性分析表明保安湖水体菌门之间显著正相关作用在冬季明显增多, 如疣微菌门和拟杆菌门在春、夏、秋季呈负相关性, 在冬季则呈显著正相关(P<0.05), 蓝藻门和绿弯菌门正相关性从春季到冬季逐渐增强, 在冬季达到显著(P<0.05)。保安湖冬季水体细菌群落构建过程由确定性过程主导, 说明冬季细菌群落具有更强的生境过滤作用和种间交互作用, 而保安湖细菌冬季互作网络格局最复杂, 也表明了细菌之间的相互作用更复杂或者生态位重叠程度更高(图 7)。由于春、夏、秋季细菌多样性高于冬季, 种间为了食物、生存空间等资源而导致的竞争也更激烈, 为了避免竞争, 在进化过程中占据相似生态位的物种向栖息地分化、食物特化等不同方向进行生态位分化, 生态位的显著分化使得细菌在群落中可以长期共存, 同时这种生态位分化可能会抑制不同物种之间的相互作用。相比之下, 冬季保安湖细菌生态位的弱分化可能导致细菌之间的相互作用更强[66]。

图7 保安湖细菌互作网络Fig. 7 Interaction network of bacteria in Bao’an Lake
4 结论
(1)保安湖水体细菌群落结构具有明显的季节特征, 夏、秋季细菌群落多样性显著高于春、冬季,春、冬季优势菌群为变形菌门、拟杆菌门, 夏、秋季优势菌群为变形菌门、拟杆菌门及蓝藻门。(2)SD和保安湖春、冬季水体细菌群落结构呈显著正相关关系, pH、TP、CODMn、T和保安湖夏季水体细菌群落组成呈显著正相关, DO、Chl.a和保安湖秋季水体细菌群落结构呈显著正相关, SD、T、CODMn、TP、pH、Chl.a和DO是决定保安湖水体细菌群落组成的主导因子。(3)春、夏、秋季保安湖水体细菌群落组装过程由随机性过程主导, 冬季由确定性过程主导。保安湖冬季水体细菌间相互作用更复杂, 生态位重叠程度更高。
本研究主要在门水平上分析了保安湖细菌群落结构时空特征, 后续可在其他分类水平上进一步分析, 以便更全面地了解保安湖水体细菌群落结构特征; 并结合梁子湖流域其他湖泊微生物多样性及生境因子分析, 揭示渔业湖泊水域生境退化与微生物多样性演变的关键驱动因子。

