低切迹同步适稳颈椎融合系统在颈椎退行性疾病中的应用
柯晓斌 杨声坪 刘联群
颈椎前路椎间盘切除减压植骨融合术(anterior cervical discectomy and fusion,ACDF)是治疗脊髓型颈椎病、神经根型颈椎病、颈椎间盘突出症等颈椎退行性疾病的经典手术方式[1],ACDF的主要优势在于充分减压、重建颈椎稳定性并恢复颈椎生理曲度。传统的ACDF多采用颈前路钢板椎间融合系统(plate cage benezech implant,PCB),其临床疗效经研究证实可靠,但术后存在吞咽困难、临近节段退变等并发症[2-3]。近年来,一种由一块三角板及一个椎间融合器一体化组成的低切迹同步适稳颈椎融合系统已广泛应用于临床。该融合系统可以减少软组织刺激,简化手术步骤,在减少术后吞咽困难及临近节段退变方面具有一定的优势[4]。研究通过回顾性分析,对比低切迹同步适稳颈椎融合系统与PCB融合系统治疗颈椎退行性疾病的效果,以期为临床上ACDF术中椎间融合器的选择提供参考依据。
1 资料与方法
1.1 一般资料
本研究为回顾性队列研究,回顾性分析本院2014年1月—2019年12月收治的28例颈椎前路椎间盘切除减压植骨融合术治疗单节段颈椎退行性疾病患者。
纳入标准:(1)影像学资料提示单节段颈椎病(脊髓型、神经根型)或颈椎间盘突出。(2)临床表现为颈肩部酸痛、上肢放射痛或四肢麻木、乏力。(3)影像资料与临床症状的受累节段相符。(4)系统保守治疗6周以上效果欠佳。(5)初次手术,采用ACDF术式治疗。(6)随访超过12个月,临床症状相符。
排除标准:(1)合并颈椎骨折、颈椎不稳、后纵韧带骨化或神经系统疾病者。(2)既往颈椎手术史。(3)术前已有吞咽困难或邻近节段骨化。(4)严重基础疾病不能耐受手术者。
共纳入28例患者,根据已使用的不同融合系统分为两组:观察组共11例,其中男性5例,女性6例,年龄32~80岁,平均(47.73±13.15)岁,其中C3~4节段5例,C4~5节段2例,C5~6节段4例。对照组共17例,其中男性10例,女性7例,年龄40~74岁,平均(54.47±9.72)岁,其中C3~4节段3例,C4~5节段2例,C5~6节段11例,C6~7节段1例。两组患者的性别、年龄、手术节段差异无统计学意义(Z=0.480,P=0.488;t=-1.561,P=0.806;Z=3.648,P=0.302),有可比性。研究对资料统计者进行施盲。研究经泉州市正骨医院医学伦理委员会审查同意后开展;本研究为回顾性研究,研究结果不包含参与对象的个人信息数据,不需要获得受试者知情同意。
1.2 方法
手术方法:所有患者均采用全麻(气管插管及静脉复合麻醉),仰卧位,颈肩部垫布垫使颈椎呈中立位。采用右侧颈前路横切口入路操作。逐层切开皮肤、皮下组织、颈阔肌及深筋膜浅层,沿血管鞘与内脏鞘间隙钝性分离至椎前,定位针定位,C 型臂X 线机透视确认节段。撑开器适当撑开固定椎间隙,切除椎体前缘骨赘,尖刀切开前纵韧带及椎间盘前纤维环,利用髓核钳、刮匙及超薄枪状钳切除椎间盘髓核、上下终板、椎体后缘骨赘及后纵韧带行椎管减压,探查确认减压充分。融合器试模,选择合适型号。取自体骨或同种异体松质骨置于相应融合器中,然后将融合器置入椎间隙、钢板置于椎前。透视融合器及钢板型号与位置满意,拧入螺钉锁固钢板。其中置入的内固定物分别为,(1)观察组:采用低切迹同步适稳颈椎融合系统(上海三友,Carmen)。(2)对照组:采用PCB融合系统(美国美敦力,枢法模)。再次透视了解内固定物型号及位置满意后,冲洗切口,彻底止血,放置引流管引流,逐层缝合切口并包扎伤口。所有患者手术由同一组手术医生完成。
术后处理:所有患者术后均常规应用注射用甲泼尼龙琥珀酸钠(比利时辉瑞制药公司,规格:500 mg,批准文号:H20130303、H20170198)、甲钴胺注射液(卫材(中国)药业有限公司,规格:1 mL∶0.5 mg,批准文号:H20130206、H20174048)。术后3 d颈托保护下下床活动,颈托制动1个月,1个月后行颈部功能锻炼。
1.3 观察指标
1.3.1 随访时间定义
因患者随访病情变化及随访依从性差异,将随访时间定义如下:术后1周:术后3~7 d;术后1个月:术后3~5周;术后6个月:术后5.5~6.5个月(22~26周);术后1年:术后11~13个月(48~56周)。
1.3.2 神经功能评估
分别于术前、术后1周、术后1个月、术后6个月、术后1年采用日本骨科学会(Japanese Orthopaedic Association,JOA)评分[5]及颈椎功能障碍指数(neck disability index,NDI)[6]进行神经功能评估。其中JOA为对上肢运动功能、下肢运动功能、感觉和膀胱功能日本进行颈脊髓功能评分法,总分17分;分数越低,表明脊髓功能障碍越严重。NDI包括颈痛及相关的症状(疼痛的强度、头痛、集中注意力和睡眠)和日常生活活动能力(个人护理、提起重物、阅读、工作、驾驶和娱乐),两部分10个项目,每个项目最低得分为0分,最高得分为5分,分数越高表示功能障碍程度越重。NDI(%)=[受试者评估总分/(受试者完成项目数×5)]×100%。
1.3.3 术后吞咽困难程度
根据Bazaz评分[7]将术后吞咽困难程度分为无(未发生)、轻度(很少发生)、中度(偶尔发生)、重度(经常发生);于术后1周、术后1个月、术后6个月、术后1年进行评价,统计不同程度吞咽困难的例数。其中,吞咽困难的定义为:进食时出现咽下困难、无力、呛咳等吞咽功能障碍或吞咽时出现异物感、哽咽感、烧灼感等不适。
1.3.4 影像学评估
(1)手术节段Cobb角:手术节段上位椎体上终板与下位椎体下终板间的夹角。于术前、术后1个月、术后6个月、术后1年随访行颈椎正侧位X线片后测量所得。(2)椎间融合情况:根据Pitzen等[8]的描述进行椎间融合情况评估,即X线片上融合节段有骨小梁通过椎间融合器且周围无透亮带。于术后1年随访行颈椎正侧位X线片后评估所得,统计椎间融合率。(3)临近节段退变情况:根据Park等[9]的描述进行临近节段退变评估的评估:0级,邻近节段无骨化形成;1级,有骨化形成,但骨数未超过椎间隙的1/2;2级,骨化超过椎间隙的1/2,但未跨越椎间隙;3级,骨化跨越椎间隙,形成连骨桥。于术后1年随访行颈椎正侧位X线片后评估所得,统计不同级别临近节段退变的例数。
1.4 统计学分析
采用 Excel 2010进行数据录入,使用 SPSS 16.0统计学软件进行统计分析。计数资料以n(%)表示,行χ2检验,计量资料以(±s)表示,行t检验;等级资料以例数表示,采用Mann-Whitney秩和检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者JOA评分比较
两组患者术前、术后1周、术后1个月、术后6个月、术后1年JOA评分差异无统计学意义(P>0.05);两组术后各时间点JOA评分均高于术前,差异有统计学意义(P<0.001),见表1。
表1 两组患者JOA评分得分情况(分,±s)

表1 两组患者JOA评分得分情况(分,±s)
注:相比 术 前,*P<0.001;at=-8.004,bt=18.287,ct=13.166,dt=16.583,et=-10.547,ft=15.864,gt=15.148,ht=-13.727。
组别 术前 术后1周 术后1个月 术后6个月 术后1年观察组(n=11) 11.18±1.17 14.00±1.18*a 16.00±0.63*b 15.91±0.54*c 16.18±0.75*d对照组(n=17) 11.35±1.22 14.47±0.08*e 16.24±0.75*f 16.29±0.69*g 16.41±0.80*h t 值 0.368 1.260 0.858 1.570 0.763 P值 0.855 0.271 0.124 0.089 0.628
2.2 两组患者NDI评分比较
两组患者术前、术后1周、术后1个月、术后6个月、术后1年NDI评分差异无统计学意义(P>0.05);两组术后各时间点NDI评分均低于术前,差异有统计学意义(P<0.001),见表2。
表2 两组患者NDI评分比较(%,±s)

表2 两组患者NDI评分比较(%,±s)
注:相比术前,*P <0.001;at=8.146,bt=16.092,ct=28.722,dt=31.652,et=10.579,ft=31.817,gt=44.332,ht=41.164。
组别 术前 术后1周 术后1个月 术后6个月 术后1年观察组(n=11) 35.10±1.95 30.60±2.12*a 22.00±2.56*b 17.27±1.29*c 15.16±1.51*d对照组(n=17) 34.49±1.63 30.04±1.61*e 20.31±2.02*f 16.88±1.26*g 14.86±1.62*h t 值 0.885 0.795 1.946 0.791 0.489 P值 0.801 0.115 0.727 0.445 0.819
2.3 两组患者Bazaz评分比较
两组患者术后1周、术后1个月、术后6个月、术后1年Bazaz评分差异有统计学意义(P<0.05),见表3。

表3 (续)
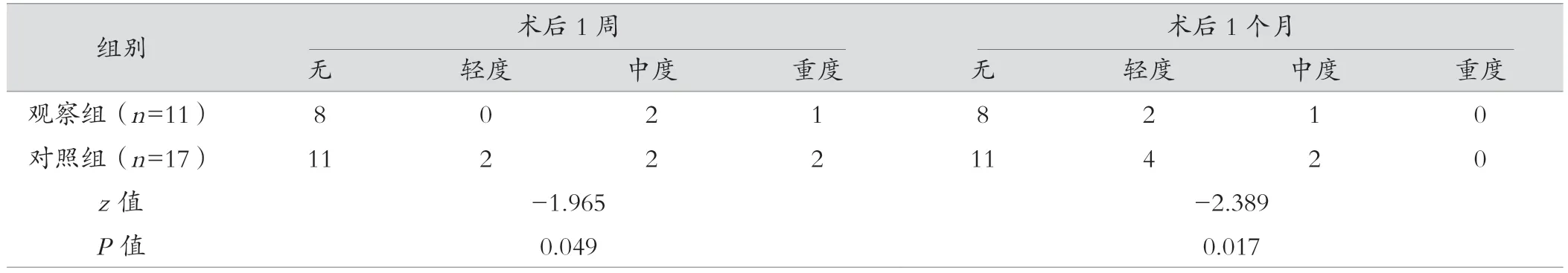
表3 两组患者Bazaz评分结果 (例)
2.4 两组患者手术节段Cobb角比较
两组患者术前、术后1周、术后1个月、术后6个月、术后1年手术节段Cobb角比较,差异无统计学差异(P>0.05);两组术后各时间点手术节段Cobb角均高于术前,差异有统计学意义(P<0.001),见表4。
表4 两组患者手术节段Cobb角比较(°,±s)

表4 两组患者手术节段Cobb角比较(°,±s)
注:相比术前,*P < 0.001;at=-13.166,bt =-11.840,ct=-15.588,dt=-17.331,et=-8.444,ft=-8.789,gt=-9.169,ht=-10.404。
组别 术前 术后1周 术后1个月 术后6个月 术后1年观察组(n=11) 7.73±1.68 12.45±1.92*a 12.64±1.80*b 12.64±1.75*c 13.00±1.61*d对照组(n=17) 8.29±1.49 12.76±1.52*e 12.82±1.47*f 12.88±1.41*g 13.12±1.32*h t值 0.936 0.476 0.301 0.411 0.211 P值 0.716 0.276 0.411 0.227 0.532
2.5 两组患者椎间植骨融合情况
术后1年进行椎间植骨融合情况评估,观察组融合率高于对照组,差异有统计学意义[100%(11/11)vs. 94.12%(16/17),Z=-4.470,P<0.001)。
2.6 两组患者临近节段退变情况
术后1年进行临近节段退变情况评估,观察组临近节段退变例数少于对照组,差异有统计学意义(P<0.05),见表5。

表5 两组患者临近节段退变情况比较(例)
3 讨论
本研究结果显示两组之间JOA、NDI等神经功能评估指标差异无统计学差异(P>0.05),两组临床疗效相当,但观察组的影像学结果优于对照组。在并发症方面,观察组的术后吞咽困难发生率低于对照组,术后临近节段退变低于对照组。
ACDF术式自20世纪50年代开始应用于颈椎退行性疾病,其主要的手术意义在于解除了脊髓及神经根的压迫,恢复并维持颈椎椎间隙高度及生理曲度。本研究中两种颈椎融合系统应用于ACDF均取得了神经功能的改善及椎间植骨的有效融合,临床疗效满意。两组患者术后Cobb角均高于术前,也同样证实了ACDF术式对恢复并维持颈椎椎间隙高度及生理曲度的意义。一方面,低切迹同步适稳颈椎融合系统的融合器上下表面采取生理曲度解剖形状设计,在恢复与维持颈椎生理曲度具有优势;另一方面,低切迹同步适稳颈椎融合系统,独创三角稳定设计,其特点在于三个顶角贴合椎体前缘、植入物低切迹,可以有效控制生理曲度。
吞咽困难是ACDF术后的常见并发症之一,国外对1 015例颈椎退行性改变首次行ACDF的研究结果显示,其发生率约9.5%,其可能原因包括软组织水肿、食管损伤、术后手术部位血肿及钛板周围粘连等[10]。Lee等[11]研究认为,吞咽困难与钢板厚度相关,使用较薄的钢板可以降低吞咽可能的发生率;该研究同样指出,女性的吞咽困难发生率约为男性的两倍,本研究结果支持该观点。低切迹同步适稳颈椎融合系统的钢板厚度为16~18 mm,薄于传统PCB系统的钢板厚度21~23 mm。此外,低切迹同步适稳颈椎融合系统手术时间较短,对椎体前缘组织分离较少,减轻了软组织损伤,减少了术中的过度牵拉,可能是降低术后吞咽困难的原因之一。
临近节段退变的发生机制尚不明确。有研究对41例ACDF患者进行长期随访(5~8.3年),结果显示约50%患者存在临近节段退变,而其中仅5%存在相关症状,且仅2%需要二次手术处理[12]。Kim等[13]研究认为临近节段的退变与内固定物相关,当钛板上下缘与相邻椎间盘距离<5 mm时,临近节段退变风险增高。Lee等[14]研究使用较长的螺钉以缩短钛板的长度,可以有效降低临近节段的发生率和严重程度。低切迹同步适稳颈椎融合系统使用新型低切迹接骨板,缩短钛板的长度,减少术中椎前显露范围,有效地降低临近节段退变的发生率。除此之外,国内有研究显示临近节段退变的危险因素还包括高龄、女性、术中出血多、骨质疏松等[15],本研究结果支持该观点。
据文献报道,颈椎前路零切迹椎间融合器(Zero-Plant,Zero-P)同样广泛应用于ACDF,在术后吞咽困难和术后临近节段退变方面都具有一定的优势[16]。由于低切迹同步适稳颈椎融合系统为国产系统,且上市时间较晚,目前未见相关两种融合系统的对比研究。另一方面,Zero-P需要较大的进钉角度,在处理C3/4节段置钉时可能存在在下颌骨阻挡。而低切迹采用一体式装置,且螺钉向尾侧倾斜角度明显小于Zero-P,可明显避免下颌骨对螺钉置入的影响。
本研究遵守观察性研究报告规范(strengthening the reporting of observational studies in epidemiology,STROBE)进行报告。不可避免,本研究存在一定的局限性。首先,本研究为单中心回顾性队列研究,可能存在一定的选择偏倚。其次,本研究样本量较小,结果可信度降低。此外,本研究随访时间为1年,缺乏中长期的随访结果。
综上所述,低切迹同步适稳颈椎融合系统应用于ACDF,可以改善患者神经症状,有效恢复并维持颈椎生理曲度,临床治疗效果满意。其能有效降低术后吞咽困难、临近节段退变等并发症的发生率。

