二陈汤对非酒精性脂肪性肝病FXR信号通路及胆汁酸水平的影响*
崔佳斌 郑栋栋 陈 奇 江岸林
海盐县中医院 浙江 海盐 314300
非酒精性脂肪性肝病(NAFLD)是指除酒精和其他明确的肝损害因素所致的,因大量脂质在肝脏沉积,以弥漫性肝细胞大泡性脂肪变为主要特征的临床病理综合征,NAFLD可进一步演变为非酒精性脂肪性肝炎、肝纤维化、肝硬化甚至肝癌[1],已逐渐成为最主要的肝脏疾病之一。二陈汤出自《太平惠民和剂局方》,由半夏、橘红、白茯苓、甘草、乌梅和生姜组成,具有燥湿化痰、理气和中之功效,广泛用于NAFLD的治疗[2]。近年来发现,法尼酯衍生物X受体(FXR)在物质代谢及肠道稳态中发挥重要的作用,通过调节胆汁酸(BA)、脂类及糖等代谢,可调控NAFLD的发展和转归[3]。本课题就二陈汤是否通过调控FXR信号通路干预NAFLD进行研究。
1 材料与方法
1.1 实验动物:SPF级雄性SD大鼠51只,4周龄,体重(100±10)g,由上海斯莱克实验动物有限公司提供,动物许可证号:SCXK(沪)2012-0002,饲养于浙江中医药大学实验动物中心。适应性喂养1周后随机分成2组:对照组8只,造模组43只,对照组予常规饲养,造模组予高脂饲料喂养,高脂饲料配方:基础饲料72.6%,猪油10%,胆固醇2%,胆盐0.4%,蛋黄粉5%,蔗糖10%。造模组于造模第8、10和12周各处死1只大鼠,取肝脏组织做HE染色,判定造模情况。
1.2 药物及试剂:奥贝胆酸(美国Sigma),二陈汤(法半夏、茯苓各9g,陈皮、乌梅、生姜各6g,炙甘草3g,由海盐县中医院中药房提供);RNA纯化试剂盒(北京天根生化),PCR试剂盒(上海士锋生物),蛋白提取试剂盒(杭州联科),FXR、小异二聚体伴侣(SHP)、胆固醇7α羟化酶(CYP7A1)和胆盐输出泵(BSEP)一抗(英国Abcom),二抗(北京中杉金桥),BA检测试剂盒(上海武昊),引物(生工生物工程)。引物序列:FXR(5’-CCATTTACAAGCCACGGACG-3’、5’-CCCAGGTTGGAATAATAGGACG-3’),SHP(5’-CTCCCCCGATGAAGGTCGAT-3’、5’-CTCTAAGACGCTCACAGTCTCT-3’),CYP7A1(5’-TGAAGAGTACCACACCAGG-3’、5’-CATCAGACTATGGCGCAGGT-3’),BSEP(5’-GGGCATCTCAAGCAAACACC-3’、5’-AATGGCATTCCCTCCAGAGC-3’)。
1.3 实验仪器:精密电子秤(Sartorius,BT-224S),高速低温离心机(Eooendorf,15R),全自动生化分析仪(北京朗普,SMT-120VP),紫外/可见分光光度计(上海谱元,α-1860),恒温水浴箱(上海精密实验,DK-S24),电子显微镜(Thermo Fihser,L120C TEM),荧光定量 PCR仪(ABI,7300),超净工作台(苏净,sW-CJ-2FD),电泳仪(Hexagon,DE214),全自动蛋白印迹处理系统(广州博鹭腾生物,WB-600Auto)。
1.4 实验分组及方案:造模12周后将造模组随机分成模型组,奥贝胆酸组,中药高、中、低剂量组,各组8只,进行药物干预。奥贝胆酸组:奥贝胆酸以成人25mg/d剂量,按体表面积换算成大鼠剂量为2.25mg/kg·d,以0.5%羧甲基纤维素钠为溶剂;二陈汤高、中、低剂量组:分别为4.86g/kg·d,2.43g/kg·d和1.22g/kg·d;模型组及对照组予同等剂量的生理盐水,灌胃体积为10mL/kg,2次/d,持续4周,干预期间,喂养方式不变。
1.5 样本采集:干预结束后,禁食8小时后大鼠按30mg/kg腹腔注射1%戊巴比妥麻醉,腹主动脉采血、离心后,取上层血清。处死大鼠后,取肝脏左叶固定位置,修剪其大小为5mm×5mm×3mm左右,放置10%中性福尔马林溶液中固定,待HE染色。取大鼠肝右叶固定位置,2块大小约5mm×5mm×5mm左右组织,以DEPC处理过的PBS冲洗干净,分装与冻存管中,先置于液氮中,后转于-80℃保存待用。
1.6 检测指标及方法:分述如下。
1.6.1 肝脏组织石蜡切片HE染色:取大鼠肝组织常规石蜡包埋、切片(5μm)、脱蜡、脱水,苏木素-伊红(HE)染色后,在光镜下观察。
1.6.2 肝脏和血清BA检测:取50mg肝组织,以酶联免疫吸附法测定肝脏组织BA;生化仪检测大鼠血清BA。
1.6.3 Realtime-PCR检测:按Trizol Reagent试剂盒提取总RNA,检测浓度及纯度。反应条件:94℃、2min变性,95℃、40s,50℃~65℃、40s循环40次。定量分析采用公式:△△Ct=(Ct1-Ct2)-(Ct3-Ct4),Ct1、Ct2为处理样品待测基因和管家基因循环次数,Ct3、Ct4分别对照样品待测基因和管家基因循环次数。
1.6.4 Western blot检测:组织充分匀浆后提取蛋白,按提取试剂盒说明进行操作。Bradford法检测蛋白浓度后,上样进行SDS-PAGE电泳,浓缩胶80V、20min,分离胶100V、1h;转膜至PVDF膜上并以考马斯亮蓝染色,封闭2h,一抗杂交,4℃孵育过夜,洗膜后二抗杂交反应1h,最后ECL发光照相测定蛋白表达量。
1.7 统计学方法:采用SPSS 21.0统计分析软件进行计算。本试验研究均采用双侧检验,以P<0.05作为显著性差异的标准。计量资料以均数±标准差表示,采用单因素方差分析,两两比较用LSD法;不符合正态分布数据以中位数表示,用非参数检验,如Wilcoxon秩和检验、Kruskal-wallis的H检验等。
2 结果
2.1 对NAFLD大鼠肝脏组织学的影响:如图1所示,正常组肝组织形态大致正常;模型组大鼠肝细胞呈中-重度脂肪变,肝细胞肿胀,细胞核被挤向一边,大量脂肪空泡充斥于包浆内,可见大小不等的脂滴,符合NAFLD病理表现;经奥贝胆酸及中药治疗后,肝细胞脂肪变有不同程度改善,脂肪空泡不同程度减少,以奥贝胆酸及中药高剂量组最为显著。

图1 肝脏病理学检测
2.2 对NAFLD大鼠肝脏及血清BA的影响:如表1和图2所示,经高脂饲料喂养后,NAFLD模型大鼠肝脏和血清BA明显升高,经药物干预后有不同程度的降低,以奥贝胆酸和高剂量组最为显著,且二陈汤各组呈剂量依赖性。说明在降低NAFLD肝脏BA方面,奥贝胆酸与二陈汤高剂量疗效相当,而在降低血清BA方面二陈汤高剂量优于奥贝胆酸。
表1 各组大鼠肝脏及血清BA对比(±s)
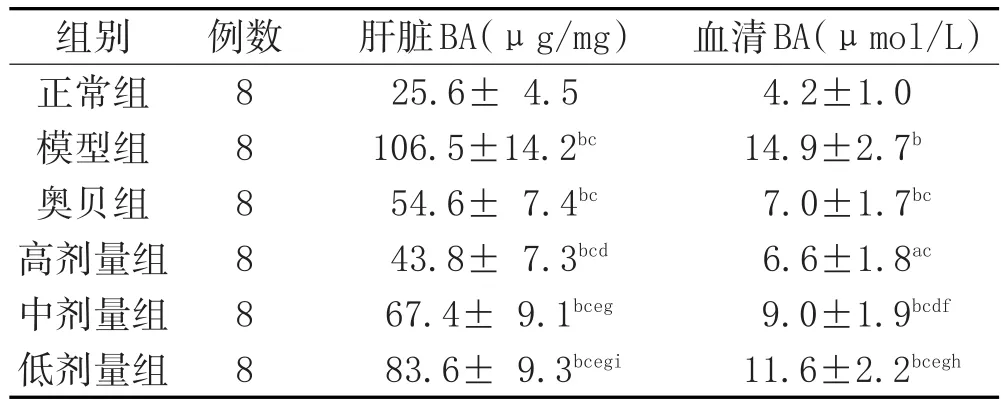
表1 各组大鼠肝脏及血清BA对比(±s)
注:与正常组对比,aP<0.05,bP<0.01;与模型组对比,cP<0.01;与奥贝组对比,dP<0.05,eP<0.01;与高剂量组对比,fP<0.05,gP<0.01;与中剂量组对比,hP<0.05,iP<0.01。
组别正常组模型组奥贝组高剂量组中剂量组低剂量组例数8 8 8 8 8 8肝脏BA(μg/mg)25.6±4.5 106.5±14.2bc 54.6±7.4bc 43.8±7.3bcd 67.4±9.1bceg 83.6±9.3bcegi血清BA(μmol/L)4.2±1.0 14.9±2.7b 7.0±1.7bc 6.6±1.8ac 9.0±1.9bcdf 11.6±2.2bcegh

图2 肝脏及血清BA水平对比
2.3 对NAFLD肝脏FXR信号通路的影响:如图3所示,NAFLD模型组大鼠FXR、SHP及BSEP mRNA表达较正常组显著下降,CYP7A1 mRNA表达显著上调;经奥贝胆酸及二陈汤治疗后,FXR、SHP及BSEP mRNA表达具有不同程度上调,CYP7A1 mRNA表达不同程度下调,其中以奥贝胆酸及二陈汤高剂量最为显著。

图3 FXR、SHP、CYP7A1和BSEP mRNA表达的对比
对各组大鼠肝脏FXR、SHP、CYP7A1和BSEP蛋白表达的影响如图4所示,NAFLD模型组大鼠FXR、SHP及BSEP蛋白表达较正常组显著下降,CYP7A1蛋白表达显著上调;经奥贝胆酸及二陈汤治疗后,FXR、SHP及BSEP蛋白表达不同程度上调,CYP7A1蛋白表达不同程度下调,其中以奥贝胆酸及二陈汤高剂量最为显著。

图4 FXR、SHP、CYP7A1和BSEP蛋白表达的对比
3 讨论
本病可归属于中医学“肝癖”“痰浊”“肥气”等范畴,脾虚运化失权、痰湿内生是重要病机,痰、湿、浊、瘀、热为主要病理因素[4]。由于现代饮食结构及生活方式的改变,饮食因素在本病的发生发展中占有主导地位[5]。《儒门事亲》:“膏粱之人,奉养过度,起居闲逸,酒食所伤,以致中脘留饮胀闷。”[6]痰湿停滞于脏腑、经络,妨碍气血运行,致气血瘀滞、痰瘀互结,产生新的致病因素。学者统计发现,湿浊内停证在NAFLD中占34.5%,是最常见的证型[7]。二陈汤是治疗痰湿的代表方,亦是基础方,广泛用于NAFLD等代谢综合征。
就本病发病机制而言,我们对本病的认识,从最早的“二重打击”学说逐渐发展到目前的“多重打击”学说[8]。临床研究发现NAFLD患者血清胆汁酸水平明显升高[9],Thompson等[10]亦发现NAFLD小鼠胆汁酸池增大,胆汁酸组成改变,提示胆汁酸过多引起的细胞毒性亦参与了本病的发生发展。胆汁酸是胆汁的主要成分,在肝脏依赖CYP7A1生成后,由BSEP泵入胆小管,储存于胆囊,最后排放入小肠发挥生理作用[11]。
FXR可通过调节胆汁酸代谢,干预NAFLD的进展。无论是人还是动物研究均发现,FXR表达下调与NAFLD进展间存在正相关[12]。FXR激活后诱导SHP的表达,可促使肝脏核受体-4与肝受体同源物-1结合的共活化物解离并失活,从而降低对CYP7A1的转录活化作用,抑制胆汁酸的生成;此外,FXR还通过上调BSEP的表达促进肝脏分泌胆汁酸,并使胆汁酸转变为胆汁,从而增加胆汁酸的排泄[13]。
本研究首次发现,二陈汤可激活NAFLD大鼠肝脏FXR,进而上调SHP及BSEP,抑制CYP7A1的表达,从而降低肝脏及血清BA水平,改善肝脏脂肪病变情况,且二陈汤激活FXR信号通路的程度呈剂量依赖性。综上所述,本研究为临床二陈汤治疗NAFLD提供了一定的理论支撑。

