大导管型及小导管型肝内胆管癌的临床病理特征及预后分析
姚 平,阮 萍,刘 莹,郑 玲,林国彪
(1.广西中医药大学附属瑞康医院病理科,广西 南宁 530011;2.广西中医药大学药学院药理学教研室,广西 南宁 530200)
胆管癌(cholangiocarcinoma,CCA)是一种起源于胆管上皮的恶性肿瘤,根据其解剖位置,CCA可分为肝内胆管癌(intrahepatic cholangiocarcinoma,ICCA)、肝门周胆管癌(perihilar cholangiocarcinoma,PCCA)和远端CCA(distal cholangiocarcinoma,DCCA)。其中ICCA发病率占胃肠道系统所有恶性肿瘤的3%,已成为仅次于肝细胞性肝癌的第二大肝脏恶性肿瘤,占原发性肝癌发病率的10%~20%[1]。 2019年第5版《WHO消化系统肿瘤分类》将ICCA分为大导管型及小导管型[2]。目前国内尚无开展关于两种亚型ICCA的大样本临床研究,故本研究就此进行相关分析。报告如下。
1 资料与方法
1.1一般资料 收集2012年1月-2020年12月在广西中医药大学附属瑞康医院接受手术治疗后并随访的ICCA患者91例。纳入标准:①手术方式为根治性手术及区域淋巴结清扫;②术后石蜡病理证实为ICCA;③有完整随访资料;④术前影像检查证实无远处器官转移。排除标准:①存在射频消融、放疗、化疗史者;②混合型肝癌;③合并其他恶性肿瘤;④围手术期死亡病例;⑤随访中发生非肿瘤相关死亡。收集患者的性别、年龄、肝病史、肿瘤大小、肿瘤发病部位、病理学分级、AJCC第八版临床分级、有无淋巴结转移、有无血管及神经侵犯、周边肝组织病变等数据。通过电话和门诊复诊方式随访,所有病例每3个月定期随访1次。无瘤生存时间定义为手术日期至第1次临床确诊肿瘤的复发日期或末次随访日期。总生存时间定义为手术日期至死亡日期。随访截止日期为2021年1月,随访期限内随访结束日期为患者死亡日期。
本研究经广西中医药大学附属瑞康医院伦理审查委员会批准通过。所有患者或其法定监护人均知情同意并签署知情同意书。
1.2诊断标准 病理诊断和形态学分类采用苏木精-伊红染色、辅以免疫组织化学及AB-PAS染色综合分析。病理切片由2位病理医师复阅,参照2019年第5版《WHO消化系统肿瘤分类》[2],并结合Hayashi等[3]的标准将肿瘤进行评估分型(表1),大导管型指标数量>小导管型指标数量诊断为大导管型,反之为小导管型,其余诊断为不确定型。结论不一致者由第3名医师进行评估,最后讨论达成共识。
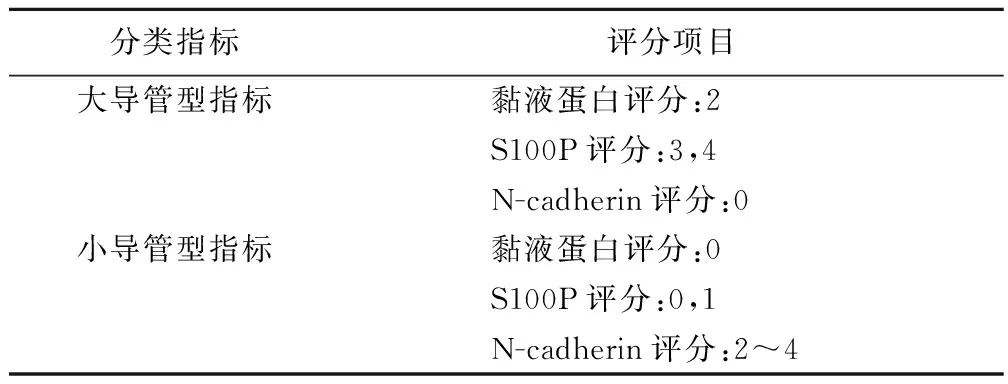
表1 结合黏液蛋白和免疫表型的ICCA分类评分表 Table 1 ICCA classification score table combining mucin and immunophenotype
1.3特殊染色及免疫组织化学染色 所有标本均充分取材,经10%中性福尔马林固定,常规脱水,石蜡包埋,组织切片3~4 μm厚,HE染色。特殊染色采用AB-PAS法对黏液蛋白进行评估。染色后,光镜下观察黏液蛋白呈蓝色。采用半定量评价:评分0分,腺腔内黏液蛋白积聚<10%;评分1分,腺腔黏液蛋白积聚10%~50%;评分2分,腺腔内黏液蛋白积聚>50%或胞浆内黏液蛋白丰富。
免疫组织化学染色用LUMATAS自动免疫组织化学染色机(美国,Lumatas BioSystems Inc)进行。切片用下列抗体染色:福州迈新公司鼠抗人S100P单克隆抗体( 编号MAB-06997, 工作浓度1∶200),鼠抗人N-cadherin单克隆抗体( 编号MAB-0571, 工作浓度1∶300)。二抗、显色系统、脱蜡液、缓冲液、抗原修复液和抗体稀释开放试剂瓶均由全自动染色仪配套提供。S100P主要染色部位为细胞核/细胞质,N-cadherin主要染色部位为细胞膜/细胞质。对这些抗体的免疫反应性半定量评估如下:得分0,<1%阳性细胞;1分,1%~25%阳性细胞;2分,26%~50%阳性细胞;3分,51%~75%阳性细胞;4分,76%~100%阳性细胞[3]。
1.4统计学方法 应用SPSS 17.0统计软件分析数据。计数资料比较采用χ2检验,等级资料比较采用秩和检验。采用Kaplan-Meier生存分析法做无复发生存曲线及总生存曲线分析,Log-rank法比较组间生存率。采用Cox比例回归风险模型分析大导管型肝内胆管癌患者预后的影响因素。P<0.05为差异有统计学意义。
2 结 果
2.1病理形态学改变 91例ICCA患者随访时间为0.70~76.50个月。根据黏蛋白状态、S100-P及N-cadherin对ICCA进行组织学分类,其中大导管型52例(57.14%),小导管型32例(35.16%),未确定型7例(7.69%)。各种类型的ICCA均可见管状、腺泡状、筛状、实体状等组织结构。大导管型ICCA的肿瘤细胞多呈高柱状,形成大的腺管样结构(图1A),细胞胞浆及腺腔内多可见黏液(图1B)。免疫组织化学S-100P染色常为阳性(图1C)。间质纤维化明显,常可见神经侵犯,癌周胆管上皮内瘤变易见。小导管型ICCA的肿瘤细胞体积较小,多呈矮柱状或立方状,形成腺泡或小管状结构(图1D),细胞胞浆及腺腔内黏液稀少(图1E),免疫组织化学N-cadherin染色多为阳性(图1F)。

图1 大、小导管型ICCA的病理组织学特点A.大导管型ICCA大腺管结构明显,细胞呈高柱状,可见细胞内黏液(箭头示)(HE ×200);B.大导管型ICCA可见胞浆内及腺腔内黏液(*示)(AB-PAS ×200);C.大导管型ICCA S-100P阳性表达(IHC ×200);D.小导管型ICCA呈小管状结构,细胞呈立方状(箭头示)(HE ×200);E.小导管型ICCA黏液蛋白缺失(AB-PAS ×200)F.小导管型ICCA N -cadherin阳性表达(IHC ×200)Figure 1 Pathohistopathological characteristics of large-duct subtype and small-duct subtype ICCA
2.2临床病理特征比较 大导管型及小导管型ICCA患者淋巴结转移、血管侵犯、CA199水平、TNM分期及肝内胆管结石病史等临床病理特征差异有统计学意义(P<0.05)。2组性别、年龄、肿瘤大小、肿瘤分化、肝内寄生虫感染史、乙型肝炎感染等临床病理特征差异无统计学意义(P>0.05)。见表2。

表2 2种类型ICCA患者临床病理特征比较 Table 2 Comparison of clinicopathological features between two types of ICCA (例数,%)
2.3生存分析 截至随访日期,大导管ICCA组存活5例(5/52,9.62%),死亡47例(47/52,90.38%),中位总生存时间11.20个月(0.70~61.00个月),中位无复发生存时间20.30个月(0.70~49.60个月);小导管ICCA组存活6例(6/32,18.75%),死亡26例(26/52,81.25%),中位总生存时间30.80个月(5.33~76.50个月),中位无复发生存时间41.37个月(18.43~66.00个月)。大导管ICCA组术后1、3、5年总生存率(分别是48.08%、13.46%、1.92%)明显低于小导管ICCA组(分别是78.13%、32.33%、6.25%;P<0.05),大导管ICCA组术后1、3、5年的无复发生存率(分别是9.61%、5.77%、0.00%)与小导管ICCA组(分别是28.13%、18.75%、3.13%)差异无统计学意义(P>0.05)。见图2。

图2 大、小导管型ICCA患者的总生存期和无复发生存期的Kaplan-Meier曲线图A.总生存期;B.无复发生存期Figure 2 Kaplan-Meier curve of o-verall survival and recurrence-free survival of patients with large duct type and small duct type ICCA
2.4预后分析 以预后为因变量,以肿瘤大小、血管侵犯、淋巴结转移、TNM分期、肿瘤分化及肝内胆石病史为自变量,变量赋值见表3,进行多因素Cox模型分析。结果显示,淋巴结转移、TNM分期是大导管型ICCA患者总生存期的预后不良因素,血管侵犯、TNM分期是无复发生存期的预后不良因素,见表4,5。

表3 预后情况多因素Cox分析变量赋值表Table 3 Variable assignment table of multivariate Cox analysis of prognostic factors

表4 大导管型ICCA患者生存的多因素分析Table 4 Multivariate analysis of survival in patients with large duct type ICCA

表5 大导管型ICCA患者复发的多因素分析Table 5 Multivariate analysis of recurrence in patients with large duct type ICCA
3 讨 论
在过去10年间,ICCA的发病率增加近20%[4]。ICCA发病隐匿,恶性程度高,晚期5 年生存率为 5%~15%[5]。手术治疗是首选方案,但术后复发率高达60%~70%[6],且ICCA高度促结缔组织增生的能力、多样的肿瘤微环境及高度的异质性决定了其易对化疗药物产生耐药性[7]。在最新的第5版WHO分类中,根据组织形态特点,ICCA可分为大导管型及小导管型[8]。小导管型ICCA可能来源于小叶间胆管和间隔胆管,肿瘤细胞起源为小的肝内胆管、前体细胞及成熟的肝细胞,表现为小的管状或腺泡状腺癌,没有或很少产生黏蛋白。大导管型ICCA多起源于段、叶等较大胆管或伴发的胆周腺,是由产生黏液的柱状细胞排列成大腺管或乳头状结构构成[9-11]。基于这两种类型之间的生物学差异,对ICCA进行亚型分类已成为ICCA病理组织学诊断的重要组成部分,并与临床的治疗及预后评估密切相关。
本研究通过单中心样本对大导管型、小导管型ICCA的临床特征及生存期进行比较,并对大导管型ICCA进行生存分析,比较不同临床特征与预后之间的关系。结合HE组织形态、免疫组织化学标记及黏蛋白等综合分析,91例ICCA中,大导管型ICCA 52例,小导管型ICCA 32例,未确定型7例。小导管型ICCA患者的5年总生存率均高于大导管型患者,与Hayashi等[3],Chung等[12]及Liau等[13]的研究结果一致。而Sigel等[14]研究提示,大导管型及小导管型ICCA患者的疾病特异性生存率及无复发生存率差异无统计学意义,这可能与该研究中大导管型ICCA患者例数过少(14例,8%)有关。
大导管型、小导管型ICCA表现出不同的临床病理特征。在肿瘤的肝脏背景病变中,大导管型ICCA往往与肝内胆管结石和胆管上皮内瘤变相关[12],本研究中大导管型ICCA的肝内导管结石发生率明显高于小导管型。这可能是由于肝内胆管结石机械性刺激和胆汁淤积损伤胆管上皮细胞,改变了胆管组织周围的微环境,从而导致胆管上皮再生、不典型增生、上皮内瘤变,最终导致胆管上皮癌变[15]。本研究对临床特征进行单因素分析发现,肝内导管结石是大导管型ICCA的预后不良因素,这与叶冠雄等[16]研究结果一致。ICCA的转移方式不同于肝细胞癌的经门静脉血运转移为主,而是以淋巴回流的形式向腹腔淋巴结转移及肝外脏器的直接浸润的方式进行[17]。第8版AJCC分期系统建议至少清扫6个淋巴结,以获得准确的N分期[18]。淋巴结转移对更准确地评估ICCA预后方面起着重要作用。许多研究都集中在淋巴结转移数目和位置与预后的关系。然而,淋巴结清扫术是否能提高ICCA患者的存活率仍存在争议。本研究结果显示,与小导管型ICCA比较,大导管型ICCA的淋巴结转移及血管侵犯发生率、血清CA199水平、TNM分期等明显升高,这意味着大导管型ICCA比小导管型有更高的淋巴结转移风险。淋巴结转移是大导管型ICCA患者总生存期的预后不良因素,提示大导管型ICCA有必要进行系统性淋巴结清扫。而肿瘤标志物CA199的增高及TNM分期都说明,与小导管型ICCA比较,大导管型ICCA的预后较差。TNM分期是大导管型ICCA患者总生存期及无复发生存期的预后不良因素,这与以往的一些ICCA患者的预后研究相似[19-21]。
综上所述,大导管型、小导管型ICCA患者的临床病理特征有一定差异,大导管型ICCA的预后更差,淋巴结转移、血管侵犯及TNM分期是其总生存期及无复发生存期的影响因素。由于病因和临床转归不同,不同类型的ICCA对治疗的反应也可能不同,对ICCA进行组织学亚型分类有一定的临床意义。本研究的不足是小导管型ICCA病例数较少,后期仍需要扩大样本数量并开展多中心研究以进一步验证。

