碱改性g-C3N4管及其光催化降解四环素性能
李乔颖 ,李冰雪 ,陈建军,梅美玉,王雨佳,黄慧萌,林文慧
(郑州师范学院 化学化工学院,环境与催化工程研究所,河南 郑州 450044)
四环素是常用的一类抗生素,然而人体肠胃不能完全将其吸收,其很容易通过排泄进入到自然环境中,对人类的生存和生活环境造成了很大的危害。因此,如何有效地去除废水中的四环素是当前急需解决的问题。半导体光催化技术可以通过活性超强的氧化基团对各种有机污染物进行降解,是解决环境污染问题的有效途径。
作为一种新型的n型半导体非金属光催化材料,石墨相氮化碳(g-C3N4)具有较好的化学稳定性、能吸收可见光、易得等特点,但同时也存在一定的局限性,如电子空穴极易复合、可见光响应范围较窄[1]。因此,需要对g-C3N4进行改性,常见的改性方法为元素掺杂、构造异质结和形貌调控(制备纳米纤维、纳米片、纳米管和分级孔)[2-12]。形貌调控中,g-C3N4管(tg-C3N4)因具有较大的比表面积、更多的活性中心和独特的结构,引起了研究者的关注。然而对tg-C3N4进行进一步剥离以形成更多活性位点,并用于降解四环素的研究还未见报道。基于以上分析,本文利用热聚合法合成tg-C3N4,采用不同浓度的NaOH溶液对tg-C3N4进行了处理。并以四环素作为目标降解物,对样品的可见光催化性能进行了探究。
1 实验部分
1.1 tg-C3N4的制备
将5 g三聚氰胺加入到50 mL去离子水中,超声振荡30 min后将溶液转移到100 mL反应釜中,在200 ℃下加热12 h。自然冷却至室温后将溶液抽滤,再用去离子水和无水乙醇进行洗涤,烘干后置于坩埚中,然后在550 ℃下保温4 h,冷至室温后即获得g-C3N4管,记为tg-C3N4[12]。
1.2 碱改性tg-C3N4的制备
将0.5 g的tg-C3N4,分别加入到40 mL不同浓度(0.05、0.1、0.2、0.3 mol/L)的NaOH溶液中,搅拌均匀后转移至50 mL反应釜里,在80 ℃下保温6 h。冷至室温后进行减压抽滤,然后用去离子水和无水乙醇洗涤3次,烘干后即可得到碱改性的tg-C3N4,分别记为tg-C3N4-0.05、tg-C3N4-0.1、tg-C3N4-0.2和tg-C3N4-0.3。
1.3 样品的表征
采用UItimaIV型X射线衍射仪对样品的物相结构进行表征,工作电压为40 kV,工作电流为40 mA。采用FTIR-2000型红外光谱仪对样品的官能团结构进行表征。采用Cary-5000型UV-Vis漫反射光谱仪对样品的光吸收性能进行表征。采用为OmniFuo960型荧光分光光度仪对样品进行荧光发射光谱分析,激发波长为380 nm。使用CHI-660E型的电化学工作站对样品的电化学性能进行表征。
1.4 光催化性能测试
将20 mg催化剂和20 mg/L四环素溶液100 mL加入到反应器中,暗反应30 min之后,取10 mL于离心管中。然后依次打开冷凝水和氙灯(采用420 nm的滤光片获得所需的可见光),每隔10 min取一次样,开灯后取样4次,离心分离10 min后,取上层清液在波长为360 nm处测定其吸光度,根据朗伯-比尔定律计算催化剂对四环素的降解率。
2 结果与讨论
2.1 物相分析
图1为tg-C3N4和碱改性tg-C3N4样品的X射线衍射图。
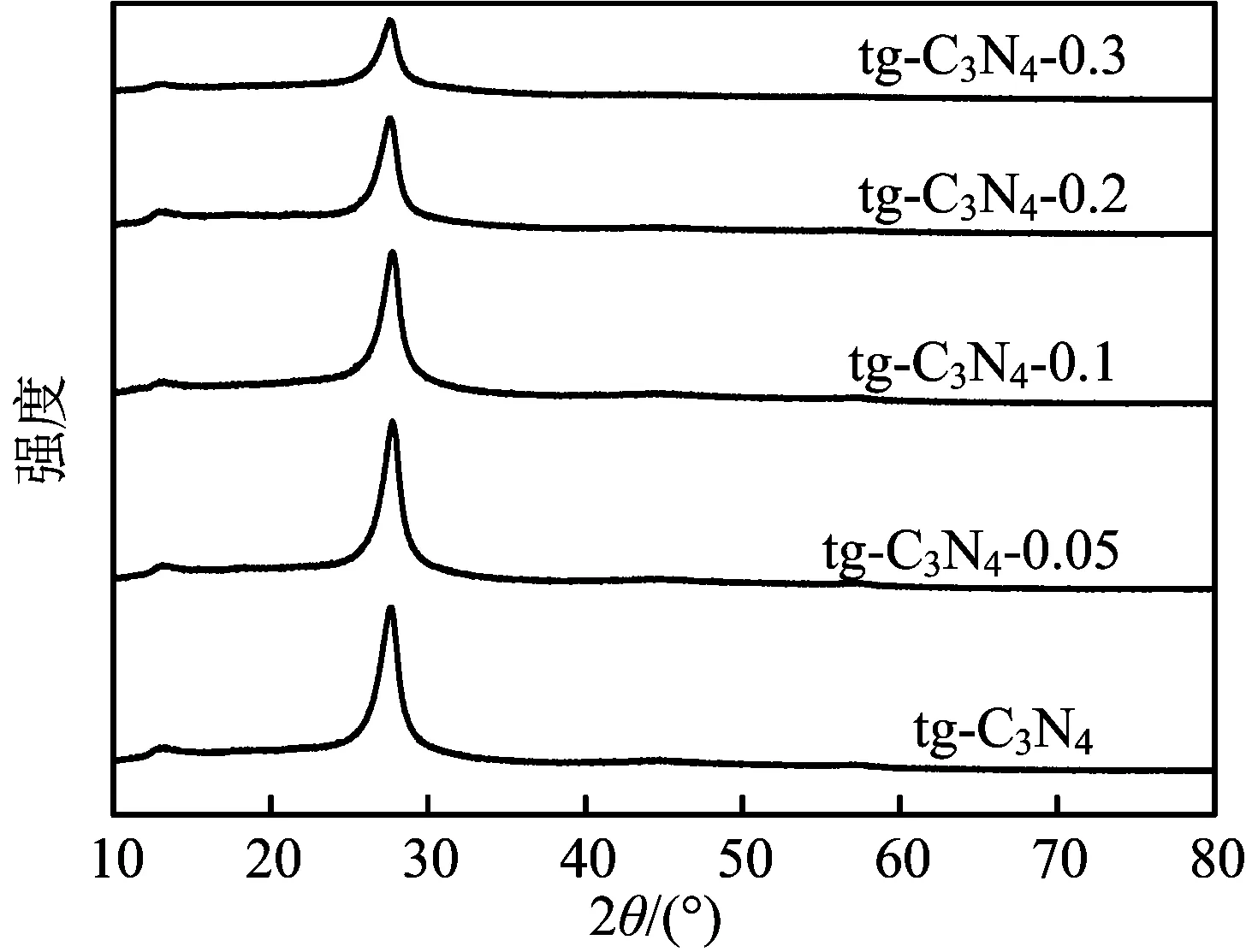
图1 制备样品的XRD图
由图1可知,所有样品在2θ=27.3°处存在明显的衍射峰,为共轭芳香体系层与层间周期性叠加形成的。13.2°处形成的衍射峰为3-S-三嗪环结构,这两个峰分别对应于石墨相氮化碳的(002)和(100)晶面。随着NaOH浓度的增加,2θ=27.3°处衍射峰的强度逐渐降低,这是因为OH-会破坏其层间结构,导致衍射峰的强度降低。
2.2 FT-IR分析
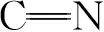
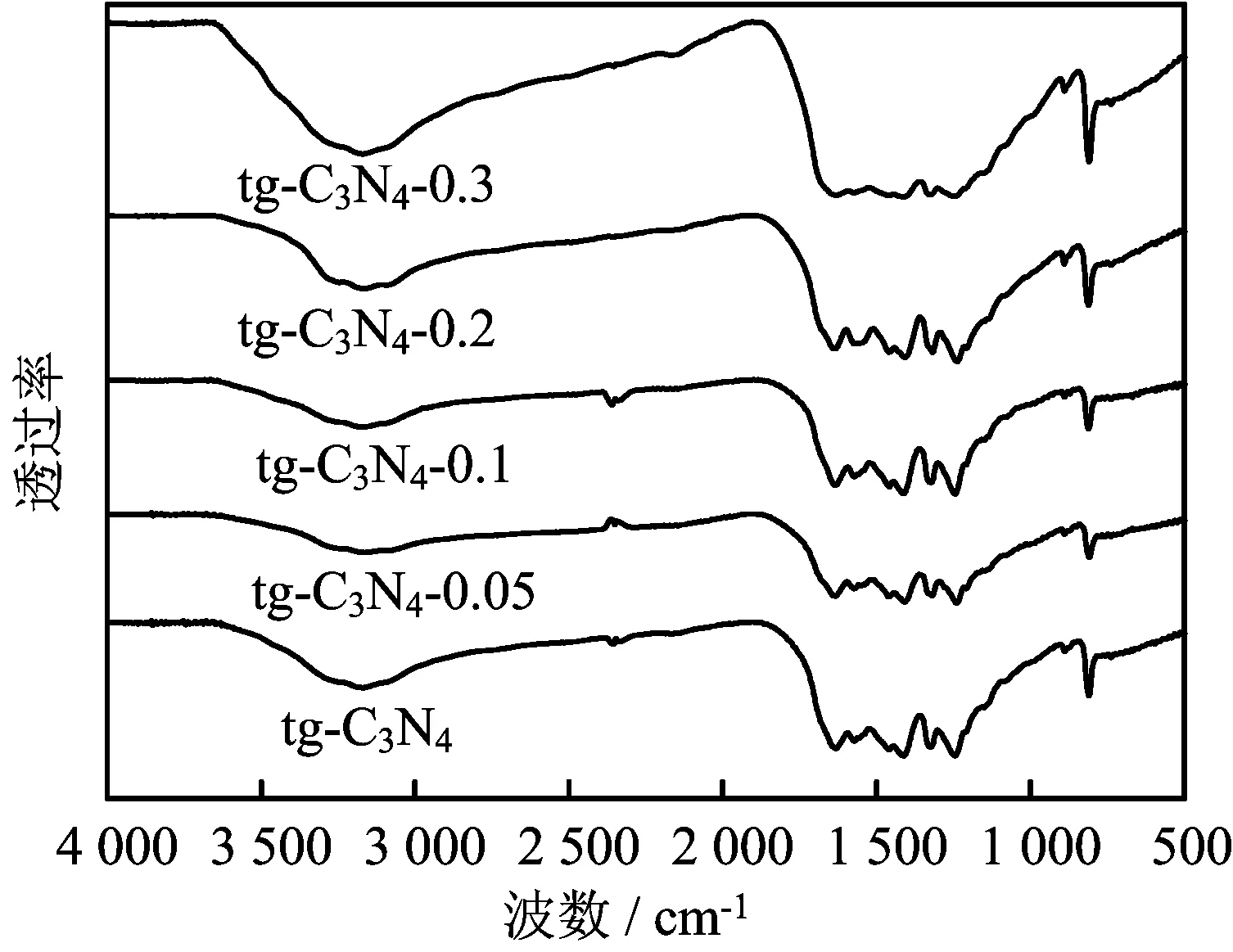
图2 制备样品的FTIR图
由图2可知,随着NaOH的浓度增加,样品在3 317~3 000 cm-1处的伸缩振动峰呈现变强变宽趋势,这是因为随着NaOH浓度的增加,tg-C3N4表面上的—OH基团数量增多,导致峰强度增加[14]。
2.3 光吸收性能分析
通过紫外可见漫反射光谱对样品的光吸收性能进行分析,结果见图3。从图3(a)可以看出,所有样品在可见光区都有吸收,当对tg-C3N4进行碱处理后,样品的光吸收强度都有不同程度的增强,这是由于OH-的加入改变了g-C3N4的电子结构,最终导致其光学性质发生了变化。图3(b)为样品的带隙图,与tg-C3N4(2.47 eV)相比,碱处理后的tg-C3N4的禁带宽度变窄(2.24 eV),能扩展光吸收的范围,进而有利于光催化性能的提高。
2.4 电化学性能分析
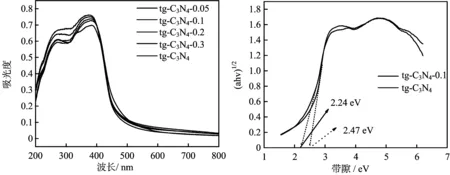
图3 样品的UV-Vis漫反射光谱(a)及带间隙图(b)
为了探究催化剂的空穴与电子的分离效果,对样品进行了阻抗的测定。样品的阻抗图见图4。
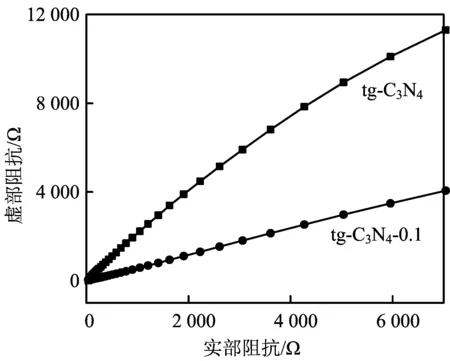
图4 可见光照射下tg-C3N4和tg-C3N4-0.1的阻抗谱图
由图4可知,tg-C3N4-0.1的弧度半径比tg-C3N4的弧度半径小,圆弧半径越小表明电子和空穴越不易复合,能够产生更多的光催化活性基团。
2.5 荧光图谱分析
图5为tg-C3N4和tg-C3N4-0.1的荧光光谱图,从图5可以看出,tg-C3N4-0.1的荧光强度弱于tg-C3N4。理论上样品的荧光强度越弱,光生电子和空穴复合的程度也就越小,参与反应的活性基团就越多,与电化学性能测试结果一致。
2.6 光催化性能分析
通过可见光下样品对四环素的降解效果,对材料的光催化性能进行探究。图6(a)为降解图,在可见光下照射40 min后,tg-C3N4对四环素的降解率只有17.4%,NaOH处理tg-C3N4后样品的光催化降解效果都有了一定的提高。其中tg-C3N4-0.1表现出最佳的光催化降解效果,其对四环素降解率达到了42.2%。样品降解四环素动力学曲线如图6(b)所示,tg-C3N4、tg-C3N4-0.05、tg-C3N4-0.1、tg-C3N4-0.2、tg-C3N4-0.3的表观速率常数分别为:0.005 03、0.007 1、0.013 4、0.009 5、0.008 7 min-1,其中tg-C3N4-0.1的反应速率常数最大,为tg-C3N4的2.68倍。综上所述,tg-C3N4-0.1具有最佳的降解率和反应速率。这是因为与tg-C3N4相比,碱处理后的tg-C3N4不仅具有更强的光吸收性能,而且其电子和空穴复合率更低,能为催化反应提供更多的活性基团,从而能高效地降解四环素。
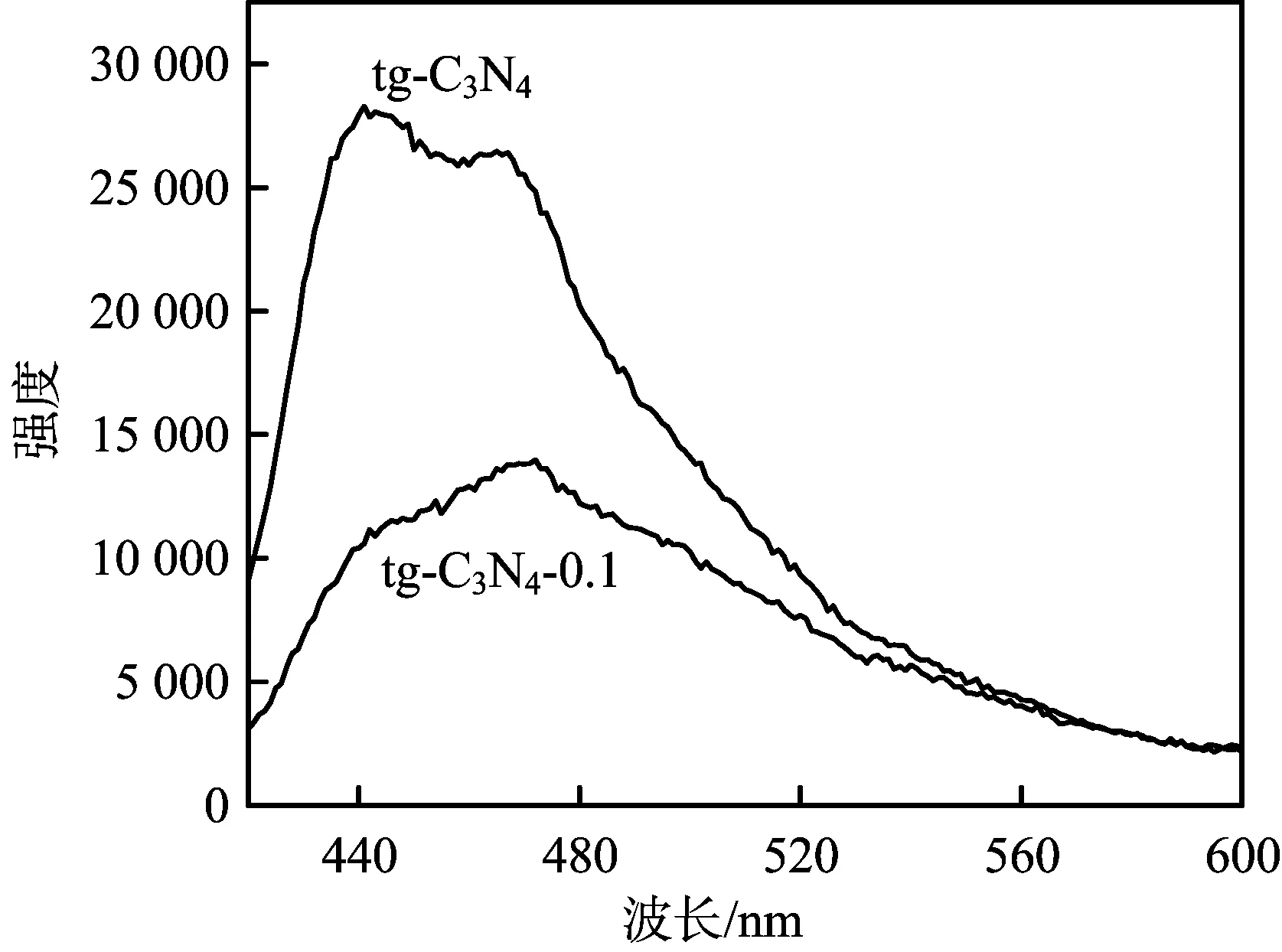
图5 tg-C3N4和tg-C3N4-0.1的荧光光谱图
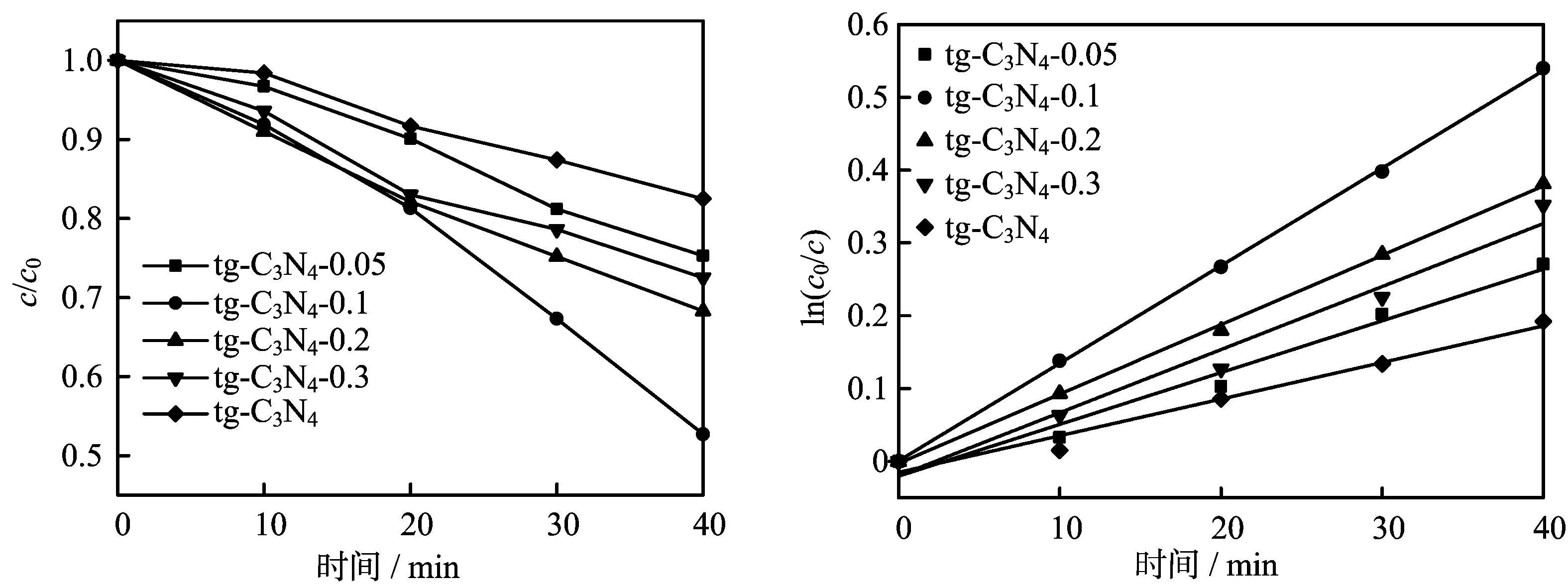
图6 样品的光催化性能分析
3 结论
通过热聚合工艺制备了tg-C3N4,用不同浓度的NaOH处理tg-C3N4。光催化实验结果表明:NaOH处理过的tg-C3N4可见光催化降解四环素的性能均得到了提高。其中0.1 mol/L NaOH碱处理后的tg-C3N4具有最佳的光催化性能,其对四环素的降解速率(0.013 4 min-1)是tg-C3N4(0.005 0 min-1)的2.68倍。这是因为NaOH处理tg-C3N4后的样品不仅光吸收能力增强,而且更有利于电子和空穴的分离,在催化反应中能产生大量的活性基团,进而增强光催化性能。

