锰基钠离子电池正极材料Jahn-Teller效应抑制方法进展
王绍聪,李 伟,黄瑞琴,郭艺飞,刘 峥
(桂林理工大学化学与生物工程学院,电磁化学功能物质广西区重点实验室,广西 桂林 541004)
在各种储能系统中,电化学储能系统(EES)因其使用寿命长、成本低、投资少、易于安装等优点,被认为是平衡可再生能源循环特性的有效方法,而电化学储能中二次电池储能具有巨大潜力。由于锂(Li)资源储量有限且分布不均以及锂的多方面消耗,人们对锂离子电池大规模应用产生担忧[1]。为了缓解该问题,相关领域已经提出用丰度大的元素,如钠(Na)替代锂,以制备新一代低成本、环保的二次离子电池[1]。在过去的几十年里,人们见证了二次离子电池发展,主要是基于多种具有里程碑意义的正极材料,其中锰由于其经济因素和特性已被广泛考虑其应用价值[2]。但Mn3+引起的Jahn-Teller 效应,极大地扭曲了局部晶格结构,降低电化学稳定性。本文概述了抑制Jahn-Teller效应的方法,归纳总结有希望消除Jahn-Teller效应的研究方法,以使这一重要的正极材料家族走向实际应用。
1 钠离子电池正极材料
现在典型的正极材料有层状过渡金属氧化物、聚阴离子化合物、普鲁士蓝类化合物,硫化物、氟化物以及其他有机正极材料。相比较而言聚阴离子化合物具有结构稳定性更高、有可调节氧化还原电位和其他性能,可将其转化为一种潜在低成本、环保型正极材料[3]。其一般结构通式为AMx[(XO)y]z,A是碱金属元素或碱土金属元素(如Li、Na、K、Mg、Ca等),M是过渡金属元素(如Fe、V、Ti、Mn等),X是非金属元素(如P、S等)。针对聚阴离子基团类型及研究现状,聚阴离子正极材料可以粗略地分为磷酸盐系列、硫酸盐系列,聚阴离子单一系列、混合聚阴离子系列4 个主要类型[4]。钠离子电池因其价格低廉,资源丰富,工作电压可控等优点而成为替代锂离子电池的有力竞争者之一。聚阴离子化合物因其特殊的框架结构所带来的高离子导电性,“诱导效应”所带来的可控电压平台以及其在电化学过程中所表现出的优异的结构和热稳定性而成为开发低成本、高性能钠离子电池的理想之选[5]。尽管聚阴离子化合物在理论上具有良好的应用前景,但其因为自身较差的电子导电性以及较低的理论比容量,用作钠离子电池正极时受到一定程度的限制。因此,如何有效提高聚阴离子化合物的导电性以及电化学性能成了当前研究的重中之重[6]。
正极材料作为钠离子电池的核心组成部分之一,其性能的好坏直接决定了钠离子电池性能的优劣。通常,钠离子电池正极材料需具备如下特征:①为提高钠离子电池的输出电压,电极材料应具有较高的氧化还原电位;②为提高钠离子电池的比容量,电极材料本身的理论比容量应较高;③为提高钠离子电池的倍率性能,电极材料应具有良好的电子导电率和离子导电率;④为提高钠离子电池的循环性能,电极材料在充放电过程中应具有良好的结构稳定性;⑤为提高钠离子电池在整个电压窗口范围内的化学稳定性,电极材料应在电化学反应过程中具有良好的化学稳定性,且不与电解液等发生化学反应;⑥为提高钠离子电池的实用性,电极材料需环境友好、原材料丰富、制备工艺简单且价格低廉[7]。
1.1 锰基层状过渡金属氧化物
热力学稳定的锰基层状氧化物通常有O'3单斜晶型NaMnO2(C2/m空间群)和P'2 斜方晶型NaxMnO2(Cmcm空间群)两种。1985年首次报道了钠离子在O'3型NaMnO2中有效嵌入/脱出的电化学行为,其电化学性质于2011 年得到重新研究,并且发现O'3 型Na1-xMnO2具有更宽的可逆范围(x<0.8)[8]。尽管Na1-xMnO2的钠离子可逆脱嵌数量范围比Na1-xFeO2的范围要广,但其作为钠离子电池电极材料时的循环性能并不理想,且其工作电压低于Na1-xFeO2。P2 型NaxMnO2的电化学性能在一些早期的文献中也进行了报道,其钠离子可逆嵌入/脱出数量的范围比O'3 型Na1-xMnO2更宽,可逆比容量可超过150 mAh/g。这是因为,相对于O'3型层状结构材料而言,P'2型层状结构材料的钠离子扩散路径更开放,且具有更小的离子扩散势垒以及更高的离子导电率[9]。值得注意的是,O3-P3和P2-O2 相变可以改变钠离子在晶面的扩散机制。Lee 等[10]根据第一性原理计算得知,P2 型Nax[Ni1/3Mn2/3]O2(2/3>x>1/3)的钠离子扩散活化能在转变为O2 型Nax[Ni1/3Mn2/3]O2(1/3>x>0)后会显著增加(>100 mV)。此外,P2 和P3 相中棱柱位点处的钠离子的局部环境及其扩散路径是不同的,由此可以预判两相中钠离子的迁移率可能不同。
1.2 聚阴离子化合物——氟磷酸盐
聚阴离子型化合物是指化合物结构中有一系列由四面体型(XO4)n-阴离子级及其衍生单元(XmO3m+1)n-(X=S,P,Si,As,Mo,W)和多面体单元MOx(M代表过渡金属)组成的化合物。此类化合物由于含有大量牢固的X—O 共价键,大大增加了晶格中氧的稳定性,提高了材料的安全性。多数聚阴离子化合物,(XO4)n-阴离子单元既能使离子在一个公开的结构框架内迅速传导,并且能使过渡金属氧化还原电对保持稳定[11]。
氟磷酸盐类正极材料的化学通式为Na2MPO4F,其中M一般代表铁、锰、钒等过渡金属族元素。由于氟原子的引入,一方面需要引入一个钠离子进行电荷补偿,另一方面氟较之氧更大的电负性导致化学键更强的离子性及更高的氧化还原电位,因此这类材料具有高比容量、较高的工作电压的特点[12]。目前,被广泛关注的氟磷酸盐主要包括钒基碱金属氟磷酸盐,锰基碱金属氟磷酸和铁基碱金属氟磷酸盐。这类材料由于合成材料价格较低、应用安全、工作电压高以及有较高的理论比容量等优点,有望成为最具有前景的锂离子电池正极材料替代物[13]。
1.2.1 聚阴离子型Na2MnPO4F正极材料
Na2MnPO4F 属于单斜结构,空间群为P21/n,在Na2MnPO4F 的结构中,由MnO4F2形成隧道结构,其中Mn八面体只共享一个F顶点形成平行于b轴的Mn2F2O8单斜晶胞链[14]。这些链是沿PO4相连四面体中a和c方向组成三维交叉隧道结构,因此钠离子能在这种隧道结构中传输。Na2MnPO4F 具有较高的理论容量(124 mAh/g)和较高的电压平台(3.66 V),这二者是构建高能量密度电池的重要参数。但Na2MnPO4F 较低的电子和离子电导率限制了其电化学性能,主要就是由于Mn3+的Jahn-Teller效应导致其晶体结构发生改变[15]。
锰基氟磷酸盐Na2MnPO4F 具有高的电压平台(3.66 V),有望实现较高的能量密度。而且Mn盐价格低廉,为Na2MnPO4F的大范围应用提供了更多可能性。Na2MnPO4F最早是由Lin等[16]提出,属于单斜结构,空间群为P21/n,Na2MnPO4F的晶胞参数为a=13.683Å,b=5.3170Å,c=13.717Å,β=119.67°,晶胞体积为867.13Å。Na2MnPO4F的每个晶胞都有两种类型的独立Mn离子,两种类型的磷离子和四种钠原子。在Na2MnPO4F中,MnO4F2八面体顶点被O原子和F原子占据,每个MnO4F2八面体共用F顶点形成平行于b轴的Mn2O8F2晶胞链,Mn2O8F2晶胞链通过PO4四面体连接形成三维(3D)交叉隧道结构,钠离子能在这种隧道结构中传输,因此Na2MnPO4F具有储钠性能。Na2MnPO4F 具有较高的理论容量(124 mAh/g)和电压平台(3.66 V),这二者是构建高能量密度电池的重要参数。然而,这种通过共享顶点连接的多面体导致材料的本征电导较低,限制了其在高能量密度电池中的应用[17]。
1.2.2 Na2MnPO4F电池容量衰减机理
(1)Mn 的溶解:材料中的Mn3+在热力学角度中处于容易发生歧化反应的不稳定状态,即:2Mn3+→Mn4++Mn2+
Mn2+可溶,从正极中迁出时,会滞留在负极表面,还原成金属Mn,对负极的固体电解质相界面(SEI)膜产生毒化作用,造成电池容量衰减。Mn2+也可与电解液的分解产物反应,形成氟化物或氧化物,沉积在电极表面,阻塞Na+扩散通道,造成阻抗增加,引起容量衰减。生成的Mn4+具有强氧化性,容易与电解液发生反应[18]。
(2)电解液的分解:电解液是电池中的重要组成部分,在正负极之间起传导电流的桥梁作用。钠离子电池一般以NaClO4、NaFP6以及NaTFSI等钠盐溶于碳酸丙烯酯(PC)、碳酸乙烯酯(EC)以及碳酸二甲酯(DMC)等有机溶剂中作为电解液的组成,其中,碳酸乙烯酯(EC)是必不可少的一种溶剂。传统的电解液在工作电压高于4.5 V时,容易发生分解,一部分是由于组分中的有机碳酸酯类溶剂氧化电位较低,在高电压下不能稳定存在;另一部分是由于NaFP6会与电解液中的痕量H2O反应,生成H+,H+与F-结合,生成HF气体;生成的H+,还会促进电极溶解,生成非完全电化学活性的λ-MnO2。
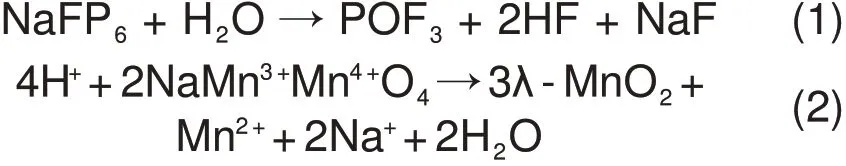
式(1)反应生成的HF 与式(2)反应生成的H2O,构成了一个相互促进的恶性循环,会加速Mn 在循环过程中的溶解,电池容量衰减更快。需要注意的是,正极片未经过干燥就进行电池组装,也可能会引进痕量的H+[19]。
1.3 含多氟钠离子电池正极材料
为了解决电子电导性问题,研究人员曾提出了许多改性策略来解决锰基正极材料的不足。表面改性可以通过防止电解质腐蚀正极材料和抑制氧气流失来提供良好的电化学性能。然而,额外的涂层工艺将导致生产成本的增加。虽然颗粒形状的工程化也能够提高速率性能和循环稳定性等,但是这种方法不适合大规模生产[20]。相反,元素部分替代是一种简单有效的方法,没有复杂的操作过程和多余的成本。一般来说,有三个位置可供替代或掺杂:过渡金属(TM)位置、Na 位置和O 位置[21]。其中,在材料合成过程中直接加入F-[22]可以减少不可逆转的氧损耗,并通过保护正极材料表面不受高频攻击来稳定晶体结构。保护正极材料表面不受高频攻击,并抑制相从层状到尖晶石状的相变。此外,它还可以减少电荷转移的阻力,加速Na+的扩散,这有利于优化电池的速率性能。另外所提出的F-引入策略的制备过程简单,只需要高温固态反应,比较容易实现大规模工业化生产。
2 抑制Jahn-Teller效应的方法
2.1 Jahn-Teller效应抑制原理
Jahn-Teller 效应描述了基态时有多个简并态的非线性分子的电子云在某些情形下发生的构型形 变[23]。Jahn-Teller 效 应 最 早 由Jahn 和Teller 于1937 年提出,并解释了Jahn-Teller 效应产生的原理[24-26]。在八面体MnO6的非线性磁场中,Mn3+通常表现出高自旋态,具有非常大的磁矩和MnO2部分沿长轴的共线J-T排序,导致强烈的Jahn-Teller扭曲[图1(a)]。对八面体配位高自旋(t2g3eg1)Mn3+以上阳离子,仅1 个电子占1 个eg(eg1)轨道,造成了eg轨道的不对称占据态。分布于dx2-y2、dz2等轨道的电子,对于不同取向的Mn 原子核将呈现出不同的屏蔽效果。在此配置下,整个d轨道已经不符合八面体Oh对称性了,使中心Mn3+阳离子不稳定。为使Mn3+以上的阳离子保持稳定,在八面体MnO6内部,两个纵向Mn—O 键伸长,而另外4 个层次的Mn—O 键则发生了缩合,如图1(a)中所表示的那样[9]。该畸变使得MnO6八面体在Oh至D4h之间对称性减弱,随着简并轨道被淘汰、系统能量下降,晶体结构失真。尤其对含高自旋Mn3+的LMLO离子(t2g3)因Jahn-Teller效应,在循环过程中常发现电化学性能存在缺陷。

图1 八面体MnO6中的Jahn-Teller(J-T)效应示意图 [11]:(a) 八面体MnO6在J-T畸变前后的示意图;(b) 八面体MnO6的分子轨道能量图和Mn2+/Mn3+/Mn4+离子的电子轨道;(c) 计算的八面体Mn3+O6和Mn4+O6的微分电荷密度。蓝色和黄色区域分别代表下降和上升的电子密度。电荷密度的等值面设定为0.015 e/Bohr;(d) 具有高/低自旋Mn3+离子的Mn3d轨道示意图Fig. 1 Schematic diagram of the Jahn-Teller (J-T) effect in octahedral MnO6: (a) Schematic diagram of octahedral MnO6 before and after J-T distortion; (b) Molecular orbital energy diagram of octahedral MnO6 and the electronic orbitals of Mn2+/Mn3+/Mn4+ ions; (c) Calculated differential charge densities of octahedral Mn3+O6 and Mn4+O6. The blue and yellow areas represent the falling and rising electron densities, respectively. The equivalence plane of the charge density is set to 0.015 e/Bohr; (d) Schematic diagram of Mn3d orbitals with high/low spin Mn3+ ions
对Mn3+以上阳离子自旋态(S)的调控,为Jahn-Teller 畸变的消除提供一种内在策略。我们还通过引入一个与电荷有关的参数来解释这种自旋态上的极化子现象。对Mn3+而言,菱面体的LiMnO2相(r-LiMnO2)可假定为两个自旋构型,由高自旋态(t2g3eg1,S=2)和低自旋态(t2g4eg0,S=1)组成。尤其适用于自旋较小的状态,在Mn3+中,电子占了全部t2g能级,自旋向下的电子[图1(d)],导致r-LiMnO2中Mn3+的Jahn-Teller 效应不活跃。将不同配体引入Mn 配位体系,低自旋Mn3+配合物可被制备[11]。最近,微结构设计为消除LiMnO2阴极的Jahn-Teller效应提供了新的见解。界面轨道排序,尖晶石和层状晶域的dz2轨道垂直的界面轨道排序可能会破坏长程轨道排序,从而显著降低Jahn-Teller效应。
除了调整晶畴成分和电子结构的策略外,还提出了许多其他策略来长期抑制稳定正极材料的J-T畸变[27]。
2.2 元素掺杂(不同元素举例)
以锰基层状氧化物LMLO 为例[11],一种常用的策略是LMLO 中的大量元素替代/掺杂。根据取代/掺杂位点,包括过渡金属离子(TM)、Li和O,可以得出三种类型的掺杂剂[图2(a)]。TM位点常用的掺杂剂包括Ni、Co、Fe、Al、Ti、Mg和Cr,从母体LiMnO2产生许多TM 取代/掺杂的化合物,例如LiMn0.5Ni0.5O2和LiMn0.9Co0.1O2这些掺杂剂可以改变Mn 离子的相邻原子结构,从而产生比原始材料更稳定的平均结构,或者直接将Mn 的化合价调整到+3.5 以上的水平避免剧烈的Jahn-Teller 区域,例如将低价元素Mg2+/Ni2+引入体相[28]。将Na、K 和Ti掺杂剂引入层状结构的Li位点也可以提高结构稳定性,因为Li 层中的大量掺杂剂可以将键长调整均匀,从而保持MnO6八面体的对称性。在MnO6的O位点掺杂阴离子物质也有类似的结果,这可归于Mn—X 相互作用(X=F-、S2-和PO43-等),从而可以抑制MnO6八面体的畸变[11]。
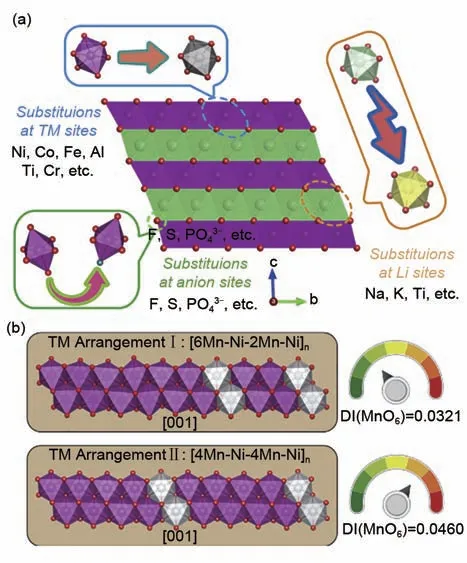
图2 防止J-T效应的策略示意图[11]:(a) LMLO中体元素替代/掺杂策略的示意图;(b) 代表LiMn0.8Ni0.2O2的TM层中的TM(Mn和Ni)排列Fig. 2 Schematic diagram of the strategy to prevent J-T effect: (a) Schematic diagram of the bulk element substitution/doping strategy in LMLO; (b) TM (Mn and Ni) arrangement in the TM layer representing LiMn0.8Ni0.2O2
以P2型Na2/3MnO2为例,这种结构的容量衰减是由于以下两个原因造成的[29]。首先,Jahn-Teller畸变与Mn3+的Na 排序相耦合,当Na+浓度增加时会引起很大的体积变化。层状Na2/3MnO2,稳定在六方P2 结构和斜方P'2 结构中,含有Jahn-Teller效应的Mn3+。Na2/3[Mn3+2/3Mn4+1/3]O2,其中缺钠会在晶体中产生Mn4+结构。变形程度可以使用较长的b轴与较短的a轴的比值来衡量[见图1(a)]。其次,Mn3+与Mn2+和Mn4+的歧化可能导致酸性电解质中的锰的溶解。最近,Fang 等[14]提出了一种Jahn-Teller 效应对MnO6八面体的新机制,该机制提供了屈曲能力以降低Na 迁移势垒,从而促进Na+扩散。此外,掺杂部分Ti4+导致Jahn-Teller 效应最小化,从而抑制了Mn 溶解并提高了电化学性能。过去的文献报道了正交P'2 型Na2/3[Mn1-xFex]O2(x=0.22)可最大限度地减少晶体结构中Jahn-Teller 畸变效应的影响,从而提高电极性能。一般来说,由X射线吸收近边结构(XANES)光谱可知,在1~2 Å范围内观察到的第一个峰与过渡金属周围的氧(Me—O 键)有关,而在2~3 Å 范围内的第二个峰与过渡金属之间的键有关,Na2/3[Fe0.2Mn0.8]O2中Mn—O和Mn—Mn 键的幅度和强度变化小于Na2/3MnO2。这些变化与MnO6和(Fe0.22Mn0.78)O6八面体在晶体结构中的运动有关,较少的运动表明抑制了由MnO6八面体引起的Jahn-Teller畸变,从而延长了在轨道上沿晶体结构的Mn—O 距离z轴。在这种情况下,深度放电的Na2/3[Fe0.22Mn0.78]O2在八面体环境中形成了O—Fe3+—O—Mn3+—O 键;然而,MnO6八面体与Fe3+O6八面体共享氧,因此Mn—O 键的异常运动可以由Fe—O 键控制。实际上,对于P2-Na2/3MnO2(Na2/3[Mn3+0.67Mn4+0.33]O2),Mn 的平均氧化态为3.33+。从X射线吸收光谱中可以看出,Mn在充电时被氧化为Mn4+,并在放电结束时返回到Mn3+,其中Jahn-Teller效应在完全钠化状态下占主导地位。更重要的是,过渡金属层中的Jahn-Teller畸变被Fe—O八面体提供的氧共享显著抑制。这种对Jahn-Teller 效应的抑制削弱了MnO6八面体中Mn3+—O距离的不必要伸长,从而阻止了在放电结束时P''2的形成[30]。
由于P2-Na0.67MnO2的晶格畸变,在初始循环中可以获得200 mAh/g的高比容量,但由于急剧的Jahn-Teller,随后容量迅速衰减。为了解决由Mn3+(t2g3eg1)引起的大的Jahn-Teller畸变,从而导致在充电或放电过程中出现严重的循环退化问题[31],人们尝试了用离子掺杂取代锰位,通过控制Mn 的平均氧化态来稳定P'2型NaxMnO2的晶体结构,例如用不同的金属元素(如Mg,Ni,Fe,Al,Zn,Co,Cu,Ti)部分取代/掺杂Mn 位点。最典型的例子是Na0.67MgxMn1-xO2和Na0.67AlxMn1-xO2,其中Mg2+和Al3+掺杂,可以平滑充放电曲线并提高结构稳定性[18]。与Mn3+不同,Mn4+(t2g3eg0)占据八面体位置从能量观点其电子结构是稳定的。尽管这种金属掺杂锰位有助于提高容量保持率,但它们的容量保持率仍然不足以使Mn 基层状氧化物满足其实际应用。此外,由于Na+的离子半径较大,在脱钠过程中,NaxMO2通常比LiMO2在脱锂过程中发生更剧烈的结构变化,这使得其脱嵌更加困难。因此,抑制Jahn-Teller 对于将其用作传统正极材料至关重要[32]。一些研究试图使用理论和实验方法来了解正极材料在钠脱出时的电子结构和热力学稳定性,因为这种稳定性与NaxMO2的容量保持直接相关。在这方面,减少Mn3+的量和抑制脱钠过程中的结构变化对于提高Mn 基层状氧化物的容量保持率可能是必不可少的。考虑到Jahn-Teller 畸变主要是由Mn3+引起的,并且Mn 基层状氧化物结构变化与其热力学不稳定性密切相关,因此Xiao 等[33]将二价Zn 掺杂到P2 型Na0.833[Li0.25Mn0.75]中取代锰位。选择P2 型NLMO 的原因是将Li 引入过渡金属层可以增加Na 含量,从而提高其容量。(Na0.833Zn0.0375)[Li0.25Mn0.7125]O2(NLMO-Zn)是通过溶胶-凝胶工艺结合随后的热处理实现了Zn 掺杂。这种掺杂不仅增加Mn 的平均氧化态来减轻Jahn-Teller 畸变,而且还降低了结构变化或不稳定性[34]。
对于NVMP正极材料来说[18],通过固态反应制备的NVMP正极表现出可逆容量提升有限,而极化显著,容量保持差。这种较差的性能可归因于其有限的电子导电性和循环过程中形成Jahn-Teller活性Mn3+。为了解决这个问题,已经开发了一种碳涂层(≈8.6%)纳米NVMP 正极,它显示出更高的倍率性能和循环寿命。但这种方法费时费力,并且所得正极在实际应用中具有较低的能量密度(因为其较高的碳含量和较低的填充密度)。另外,尽管其高压充电过程提供了增加的容量,但随后的放电并不是完全可逆。这归因于与从Na 位点脱出钠离子相关的不可逆结构转变。此外,NVMP正极在高压窗口(4.2~2.75 Vvs.Na+/Na)循环时容量迅速下降[35]。为了解决上述问题,Ghosh等[18]提出了一种化学方法,用电化学惰性阳离子(Mg2+和Al3+)部分替代NVMP正极的Mn2+。该方法旨在降低NVMP正极中锰阳离子的浓度,从而抑制Jahn-Teller畸变,并通过诱导更短的(V/Mn/Mg/Al)—O 键长来增加材料晶体结构框架的共价性,这可以提高其结构稳定性和循环寿命。此外,在NVMP 框架中异价Al3+阳离子的取代锰位会产生钠离子空位,这有望降低活化能并提高钠离子迁移率。
以NVMP正极材料为例,Ghosh等[18]为了解决Jahn-Teller畸变,提出用电化学惰性阳离子(Mg2+和Al3+)部分替代NVMP正极的Mn2+,旨在降低NVMP正极中锰阳离子的浓度,从而抑制Jahn-Teller 畸变,并通过诱导生成更短的(V/Mn/Mg/Al)—O 键来增强材料骨架的稳定性,从而增强其结构稳定性和循环寿命。因此,Mg和Al取代的NVMP正极与未取代的样品相比,显示出更高的倍率性能和循环稳定性。此外,在100 次循环后在NVMP 和Al-NVMP 正极上收集了非原位XRD 图案,以了解它们在长期循环期间的结构稳定性(图3)。NVMP 正极的XRD 峰在100 次循环后变宽且强度降低。这可能是由于在循环过程中反复形成Jahn-Teller扭曲的Mn3+,导致结构退化。另一方面,与原始电极相比,循环后的Mg-和Al-NVMP 正极呈现出让人联想到的XRD 峰,从而证实了它们在长期循环中的结构稳定性[8]。这些观察结果证实了Mg 和Al 替代物对NVMP 的好处,这抑制了Jahn-Teller 畸变效应。

图3 原始和循环 NVMP 和 Al-NVMP 阴极的非原位 XRD图谱[18]Fig. 3 Non-in situ XRD patterns of pristine and circulating NVMP and Al-NVMP cathodes
还有一项策略是基于保持锰的平均氧化态接近+4的想法[36],这样可以不采用其他一价或二价阳离子取代Mn3+的方法来抑制Jahn-Teller 效应。然而,研究人员目前没有找到完全理解和解决层状NaxMnO2中存在的协同Jahn-Teller 畸变(CJTD)缺点。在这项研究中,Kumakura 等[36]专注于P2 型Na2/3MnO2材料是否具有CJTD 的研究。通过制备P2-Na2/3MnO2多型的高纯度样品并讨论多晶型特性如何在(去)钠化过程中带来电化学和结构性质的差异,同时证明了包含CJTD 的MnIII/IV 氧化还原电对在层状结构中的高可逆性氧化物。
为了尽量减少长期循环过程中Jahn-Teller效应导致的局部结构变化,Zhang 等[37]将大的四面体P多阴离子引入层状氧化物中。如预期的一样,P掺杂的氧化物在长期循环中呈现出更好的电化学性能。因此,多阴离子掺杂提供了一种新的固定母层结构来抑制Jahn-Teller效应的新途径,可稳定富锂层状氧化物作为电池正极材料的能量密度。
为了减少循环过程中因Jahn-Teller效应导致的结构崩溃,大多数研究人员通常采用阳离子掺杂方法,但是大部分报道的工作都忽略了晶体结构中因氧阴离子被破坏的不利影响。An等[38]从稳定氧层结构的角度出发,将硫掺杂取代到正极材料的氧阴离子,以改善材料结构的稳定性和循环性能;通过模拟软件包VASP 的初步计算结果证明,少量硫掺杂有利于稳定材料的晶体结构,平衡锂离子嵌入和脱出的能量。进一步的电化学测试结果表明,掺硫的富锂材料的初始效率高达96%,比容量为293.3 mAh/g,同时拥有更好的循环稳定性和倍率性能(117 mAh/g 保持在5 C 的电流密度下)。这项工作为开发避免结构变化的层状金属氧化物正极材料提供了一种新的掺杂方式。
锰基层状氧化物正极材料在低电位时受到锰氧八面体中Mn3+的Jahn-Teller 效应的影响,在高电位时阴离子氧化引发结构退化。事实证明,在过渡金属层中引入空位可以有效地稳定高电位和低电位下的材料结构。Yang等[39]特别设计了含空位的P2-Na2/3[Zn1/9Mn7/9□1/9]O2(NZMO-VAC)和无空位的P2-Na2/3[Zn2/9Mn7/9]O2(NZMO),以阐明空位如何调整Mn3+的旋转状态并加强结构稳定性。一方面,在过渡金属离子层(TM)引入空位提高了该P2 型材料中锰离子的价位,增强了Mn/Zn/□的有序排列,促进了阴离子氧化还原能力及其可逆性。另一方面,TM空位改变了Mn3+的旋转状态,并通过缩短Mn—O 键的长度增加了放电Na2/3[Zn1/9Mn7/91/9]O2中低旋转Mn3+的比例。密度泛函理论(DFT)计算结果与磁感应强度分析和X 射线吸收光谱(XAS)测量验证上述理论。
2.3 包覆
通常,容量衰减是由于电极材料和电解质之间进行过度的界面反应,特别是在高温下。显然,表面涂层是一种在电极和电解质之间形成稳定界面的可控方法。Manthiram 等[40]报道了裸露的LiMn2O4表面被2%的5 nm厚度的非晶Al2O3层均匀覆盖。2% Al2O3包覆的LiMn2O4的初始放电比容量为118.6 mA/g,而裸LiMn2O4的初始放电比容量为119.7 mAh/g。经过25次循环后,2% Al2O3包覆的LiMn2O4的放电比容量保持在90.2 mAh/g,而裸LiMn2O4的放电比容量降至68.9 mAh/g。Li 等[30]报道了采用两步溶胶-凝胶法合成纳米Al2O3包覆的LiMn2O4正极材料。在温度升高至60 ℃、1 C 的电流密度下,原始LiMn2O4的放电比容量在循环300 次后从108.1 mAh/g衰减到46.6 mAh/g,容量保持率为43.1%。1.5%的涂层样品表现出与原始样品几乎相同的106.6 mAh/g 的初始放电比容量,300次循环后放电比容量保持在92.5 mAh/g,容量损失仅为13.2%。以上报道表明,纳米Al2O3涂层可以提高LiMn2O4正极材料的循环性能和热稳定性。由于Al2O3涂层的存在,电极材料在0.5 C的恒定速率下表现出较好的循环稳定性。同时,Al2O3涂层有助于保持结构稳定性,在3.5~4.3 V下具有较少的电解质副反应[图4(a)]。从图4(b)可以看出,Al2O3包覆LiMn2O4材料(133.5 mA/h)的初始比容量比原始LiMn2O4材料(138.6 mAh/g)的初始比容量高。LiMn2O4和Al2O3包覆LiMn2O4在循环100 次后的容量保持率分别为89.5%和98.6%。Al2O3包覆LiMn2O4较高的容量保持率可归因于均匀的涂层,这不仅抑制了锰的溶解和LiMn2O4材料的Jahn-Teller 效应[41]。Zhao 等[42]通过化学沉积法利用FeF3对溶胶-凝胶法合成的尖晶石锰酸锂正极材料进行表面改性,提高了正极材料的循环性能和热稳定性。在室温和高温下对循环性能进行了全面的研究和比较。与原始LiMn2O4相比,FeF3涂覆的LiMn2O4电极显示出更强的循环稳定性。尤其是5% FeF3包覆的LiMn2O4表现出最好的循环性能,在室温(25 ℃)下循环200 次后的容量保持率为68.2%,在高温(55 ℃)下循环100 次后的容量保持率为61.5%,远好于原始材料的容量保持率(49.8%和40.2%)。Liu等[43]通过化学方法用ZnO对尖晶石LiMn2O4表面进行修饰,以改善其高温电化学性能。在55 ℃下以1 mA/cm2在3.0~4.4 V的范围内进行材料的充/放电。ZnO 涂覆的LiMn2O4的放电容量(117 mAh/g)在循环60 次后显示初始容量(121 mAh/g)仅损失了3%。包覆ZnO 的尖晶石LiMn2O4在高温下表现出循环能力的改善。Yu 等[44]通过简单的溶胶-凝胶法用TiO2修饰尖晶石LiMn2O4表面,以改善其在高温和高工作电位下的电化学性能。与未改性LiMn2O4相比,表面改性提高了材料的循环稳定性。TiO2改性的LiMn2O4在室温下以3.0~4.8 V 的高电位循环60 次后容量保持率大于85%,在55 ℃的高温下以1 C 充放电速率循环30次后容量保持率接近90%。

图4 (a) LMO和(b) LMO@Al的EDX元素映射图像,(c) 电子探针对LMO@Al的微观分析[30]Fig. 4 (a) EDX elemental mapping images of LMO and (b) LMO@Al. (c) Microscopic analysis of LMO@Al by electron microprobe
2.4 Jahn-Teller抑制效果评价
由以上总结分析我们可以得出,对于锰基钠离子电池正极材料掺杂抑制Jahn-Teller效应,效果比较好的掺杂是Zn 元素掺杂[45]、Cr 元素掺杂[46]和Ti元素掺杂[47]。Zn2+掺杂后材料的初始比容量能够达到118.3 mAh/g,在1 C 倍率下循环100 次后仍具有95.1%的高容量保持率;而Cr3+掺杂后材料的初始比容量能够达到119.6 mAh/g,在1 C 倍率下循环300次后还具有91.8%的高容量保持率,充分说明Jahn-Teller 效应得到抑制。Ti4+掺杂可以抑制Mn—O 八面体结构的收缩或伸长,从而最大限度地减少被钛包围的Mn原子的Jahn-Teller畸变。P2-Na0.86Co0.475Mn0.475Ti0.05O2可以提供超过110 mAh/g的可逆比容量、良好的倍率性能和优异的长循环性能(在5 C的高倍率下循环200次后容量保持率达到81.1%)[35]。Fe 取代Na2Mn2-xFexP3O11结构中的Mn不仅可以提高电化学性能,而且可以提高电导率,实现快速反应动力学。虽然Fe3+掺杂后材料的初始比容量只有103 mAh/g,但是在1 C 倍率下循环1000次后竟然还具有91%的高容量保持率[32]。
控制Mn—O键的长度,是从结构上抑制Jahn-Teller 效应的重要方法[48]。Jahn-Teller 效应从结构上来看会表现出明显的结构畸变。如果不采取抑制手段,正极材料结构中所有基于Mn—O 的八面体都存在扭曲。以MnO6为例,它包含四个长的Mn—O 键(1.97 Å×2,1.98 Å×2)和两个短的Mn—O 键(1.92 Å×2)。所有的Mn—O八面体结构都存在收缩或伸长现象,这使得Mn3+的Jahn-Teller 畸变在材料中表现得异常活跃,容易导致容量迅速衰减。
包覆手段能够有效将材料和电解液隔离开,避免材料溶解在电解液中造成不可逆损失,同时保证材料的热稳定性。如TiO2包覆改性的LiMn2O4在室温下以3.0~4.8 V 的高电位循环60 次后容量保持率大于85%,在55 ℃的高温下以1 C 充放电速率循环30 次后容量保持率接近90%,是非常优异的包覆材料[44]。
3 结论与展望
在钠离子电池的研究中,正极的研究尤为重要。现有的锰基钠离子电池正极体系仍没有一个稳定可逆循环较多次数的电池正极材料,因此,锰基钠离子电池正极材料的改性和Jahn-Teller效应的抑制具有重要的理论和实际意义[8]。目前,在锰基钠离子电池正极材料整个电化学循环过程中,对锰离子价态的调节和控制是最重要的,以此来避免Jahn-Teller效应和抑制结构畸变。主要结论如下:
(1)抑制Jahn-Teller效应有效的方法之一是使用金属或过渡金属元素进行替代/掺杂,可以提高锰离子的平均价态。
(2)引入Mn 或O 离子的空位或利用阴离子掺杂也可以有效地控制Jahn-Teller效应,原理是抑制拉长的键和调整Mn离子的价态。
(3)通过外部刺激来稳定可转移结构是获得特定正极材料的独特方法。例如,在高压和(或)高温环境下,化学键的长度可以改变,从而直接增强八面体MnO6的对称性。
(4)局部结构设计也显示出明显的效果,它可以将变形单元限制在具有短程排序的局部区域,而不影响整体结构。
综上文献报道,掺杂抑制Jahn-Teller优于包覆手段。Mn3+的掺杂取代需要遵循几个规则[48]:
(1)引入的掺杂离子半径要尽量接近Mn3+半径,以确保掺杂原子与原晶格的相容性;
(2)引入的掺杂离子可以将Mn 的平均氧化态提高到+3以上,以抑制Jahn-Teller效应的产生;
(3)具有较大的M—O键能(M代表掺杂元素),以增强整体结构的稳定性;
(4)由于加入过多的掺杂元素会导致容量的大幅损失,掺杂元素的含量要适量。
综观文献[11],未来为解决结构的不可逆结构退化、锰元素的溶解、(脱)锂/钠过程中的大体积变形,以及Mn3+导致的Jahn-Teller 效应等问题,可以设计具有特定结构的功能单元,从局部结构和微观结构入手,通过调整晶域和电子状态来实现对Jahn-Teller效应进行更好地抑制。通过对锰基聚阴离子材料的体相结构进行调控和微观纳米结构重新设计等改性研究也可以作为未来抑制Jahn-Teller效应的新思路。可以预期,一旦Jahn-Teller效应得到适当解决,锰基钠离子电池正极材料必将取得重要进展。

