超声引导下微波消融治疗侵犯被膜的甲状腺乳头状癌
伍 洁,魏 莹,赵朕龙,彭丽丽,李 妍,卢乃聪,于明安
(中日友好医院介入医学科,北京 100029)
甲状腺乳头状癌(papillary thyroid carcinoma, PTC)是甲状腺癌的最常见病理类型。邻近甲状腺被膜的PTC可侵犯被膜。组织学上,甲状腺被膜由紧贴并覆盖腺体表面的固有被膜、来自颈深筋膜的外科被膜及两层被膜之间的疏松结缔组织层构成;其内层固有被膜及结缔组织层内包含的神经、血管及淋巴管等成分形成纤维囊,向内穿过并分隔甲状腺实质,使之形成若干小叶结构。甲状腺癌侵犯被膜指癌肿仅浸润甲状腺周围被膜而未侵犯其周围组织[1-2],是PTC发生淋巴结转移的独立危险因素[3-4],并可能影响手术方式及手术范围。超声引导下微波消融(microwave ablation, MWA)是治疗PTC的有效方法[5-6],但目前关于MWA治疗PTC合并被膜侵犯的研究较少。本研究观察超声引导下MWA治疗侵犯被膜的PTC的有效性及安全性。
1 资料与方法
1.1 一般资料 回顾性分析2015年8月—2021年6月72例于中日友好医院接受超声引导下MWA治疗的单发PTC患者,男20例、女52例,年龄24~74岁、平均(45.3±12.1)岁。纳入标准:①经细针穿刺诊断PTC,且患者拒绝接受开放手术;②影像学检查示病灶单发,伴甲状腺被膜侵犯(声像图示病灶邻近甲状腺被膜,且被膜的线样高回声连续性中断),未见淋巴结转移或远处转移;③术后随访>9个月。排除有MWA禁忌证者。患者术前均签署知情同意书。
1.2 仪器与方法 采用GE Logiq E9型彩色多普勒超声仪,配备9L型高频线阵探头(频率9 MHz);MWA系统和一次性消融针(南京亿高),其发热点距针尖长约3.5 mm。超声造影(contrast-enhanced ultrasound, CEUS)时,以SonoVue六氟化硫微泡(Bracco)为造影剂,经肘正中静脉团注,每次2~3 ml。
嘱患者仰卧,充分暴露颈部,以高频超声评估病灶,观察有无被膜侵犯及其程度;根据横切面声像图所示甲状腺被膜邻近解剖结构,将侵犯被膜部位分为前被膜、内侧被膜、外侧被膜和后被膜。以1%利多卡因局部麻醉穿刺部位,于超声引导下将18G PTC穿刺针经皮插入病灶与邻近重要结构之间,将针尖置于受侵犯的甲状腺被膜之外注射隔离液(0.9%生理盐水),使消融区与周围结构分离至少5 mm。而后于超声引导下将消融针穿入病灶,以30~35 W功率行多点消融,每次消融10~15 s;期间经PTC针同步持续缓慢注射隔离液,维持隔离带宽度并防止热损伤,直至消融灶范围完全覆盖病灶并至少超过其边缘2 mm(完全覆盖并超过被侵犯的被膜)时停止消融;行CEUS评估MWA效果,以增强区覆盖整个病灶、且覆盖范围至少超过病灶边缘2 mm为完全消融(图1)。如消融灶内出现结节样强化,或扩大消融范围距病灶边缘<2 mm,则以上述方法行补充消融。结束消融后局部按压30 min,患者无异常时送返病房,留院观察至少24 h。
1.3 相关指标观察及随访 消融后第1年内每3个月、之后每6个月复查颈部超声,测量病灶最大径,计算病灶体积(V)和体积缩小率(volume reduction ratio, VRR):VRR=(消融前病灶体积—随访病灶体积)/消融前病灶体积×100%。将消融区仅显示线状瘢痕判定为完全吸收(即病灶消失),统计随访期间各时间点消失病灶的数目。评估肿瘤进展情况,包括局部复发、新发病灶、颈部淋巴结转移及远处转移等。
1.4 统计学分析 采用SPSS 20.0统计分析软件。以±s表示符合正态分布的计量资料,以中位数(上下四分位数)表示不符合者,采用秩和检验比较各时间点病灶最大径、体积及VRR。P<0.05为差异有统计学意义。
2 结果
72例PTC中,57例T1a期,15例T1b期。72个病灶中,位于甲状腺左叶29个、右叶39个、峡部4个;其最大径0.3~2.0 cm,平均(0.83±0.39)cm;其中28个病灶仅侵犯单处甲状腺被膜,包括前被膜14个、后被膜6个、外侧被膜5个、内侧被膜3个;38个侵犯2处被膜,包括前、内侧被膜17个,前、外侧被膜9个,后、内侧被膜7个,后、外侧被膜3个及前、后侧被膜2个;6个侵犯3处被膜,其中4个侵犯前、外及内侧被膜,1个侵犯前、外及后被膜,1个侵犯外、后及内侧被膜。
2.1 疗效及安全性 消融后即刻CEUS显示对所有病灶均一次性完全消融,技术成功率100%。2例(2/72,2.78%)术后因喉返神经损伤出现声音嘶哑,分别于术后4个月和6个月时自行恢复。未见其他并发症。
消融前及消融后1、6、12、18个月病灶最大径、体积和VRR总体差异均有统计学意义(P均<0.01),MWA后1、6个月病灶最大径、体积均较消融前增大(P均<0.05),消融后12及18个月则均显著缩小(P均<0.05),见表1及图1。

图1 患者女,42岁,甲状腺左叶PTC侵犯被膜,接受超声引导下MWA A.术前超声声像图示甲状腺左叶低回声结节(箭)伴被膜侵犯(箭头); B.消融前CEUS图示动脉期低增强病灶(箭)侵犯被膜(箭头); C.于超声引导下经皮将18G PTC穿刺针(箭头)刺入病灶(箭)与邻近重要结构之间,使针尖位于受侵甲状腺被膜外,注射0.9%生理盐水,以建立液体隔离带; D.消融前病灶呈高回声(箭示病灶,箭头示消融针); E.消融后即刻CEUS图示消融区未见增强(箭示病灶,箭头示侵犯被膜); F.MWA后1个月复查超声声像图示低回声消融灶(箭)
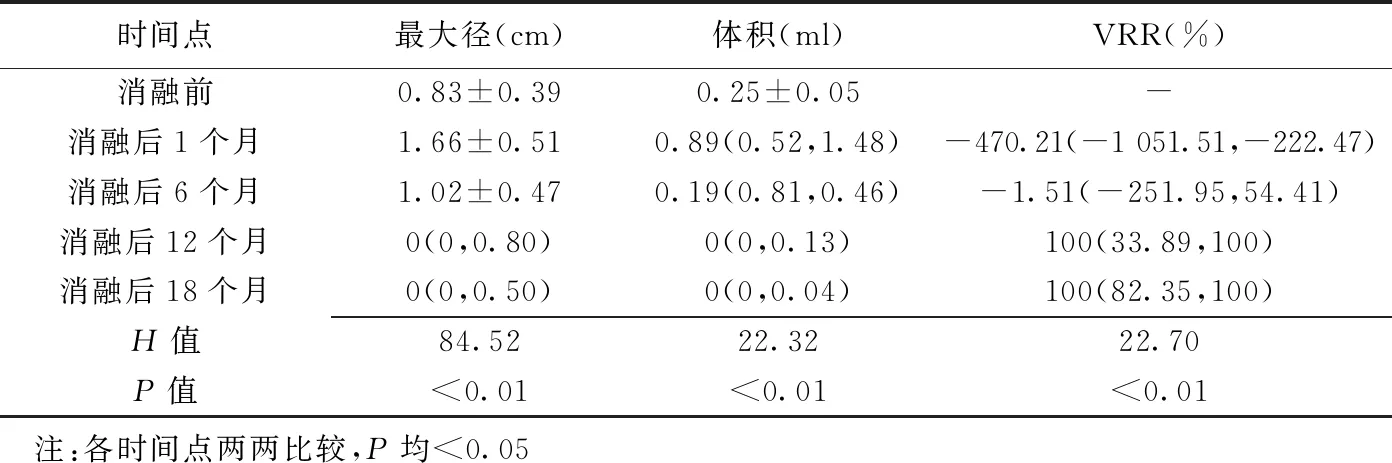
表1 MWA治疗前、后侵犯被膜的PTC最大径、体积及VRR比较
2.2 预后 随访9~36个月, 6、9、12、18、24、30及36个月分别有2、13、19、6、2、6及2个病灶消失,消融后36个月病灶消失率69.44%(50/72)。
随访期间未见局部复发及远处转移。2例(2/72,2.78%)分别于随访23、36个月时于原病灶对侧出现新发PTC病灶;2例(2/72,2.78%%)分别于随访6、24个月出现颈部淋巴结转移,分别位于原病灶同侧、对侧。对上述4例均以相同方法予以再次消融治疗,后续随访未见新发病灶及淋巴结转移。
3 讨论
超声引导下热消融治疗PTC具有微创、安全、有效、保留甲状腺功能等诸多优势[7],现已用于治疗甲状腺微小癌[8-9]及T1N0M0期PTC[10],在峡部[11]、邻近被膜[12]及T2期[13]PTC中亦显示出较好的效果。既往研究[14]提示,外科手术治疗后,相比无被膜侵犯PTC患者,合并被膜侵犯等微小甲状腺外侵犯(minimal extrathyroid extension, mETE)PTC患者死亡率、复发率均未增加。
本研究对72例侵犯被膜PTC予超声引导下MWA治疗,结果显示全部病灶均一次性完全消融,且随访期内未见局部复发,提示MWA可用于合并被膜侵犯的PTC。为完全消融病灶及受侵犯被膜,可采用扩大消融技术,但可能增加周围重要结构的损伤风险,尤其PTC侵犯甲状腺内侧被膜时;此时可应用液体隔离技术(在拟消融区与周围重要结构间进行液体分离)作为保护策略,通过持续注射生理盐水有效分离拟消融区与其周围重要结构,避免扩大消融造成周围重要结构热损伤。本组消融后仅2例因喉返神经受损致声音嘶哑,均于6个月内自行恢复;未见其他并发症。本研究随访结果显示,消融后36个月病灶消失率69.44%(50/72),期间未见局部复发及远处转移;2例(2/72,2.78%)出现新发病灶,2例(2/72,2.78%)出现颈部淋巴结转移,均予再次消融治疗,此后未见复发或转移;与既往研究[15-16]结果相符合。
综上所述,超声引导下MWA治疗侵犯被膜的PTC有效且安全。但本组样本量有限,其均来自单中心,有待后续进一步深入观察。

