经腹腔和经腹膜后入路机器人辅助腹腔镜治疗巨大体积肾上腺肿瘤45例分析
韩毅力,赵佳晖,罗 勇,李明川,魏德超,姜永光
(首都医科大学附属北京安贞医院泌尿外科,北京 100029)
临床上通常界定直径超过6 cm的肾上腺肿瘤为巨大肾上腺肿瘤。巨大肾上腺肿瘤多与周围组织粘连,并可能浸润邻近器官及大血管,常有变异血管,同时这类肿瘤位置深在,空间占位效应明显,因此增加了手术难度。在对其进行的手术治疗中关于入路的选择自腹腔镜时代就存在较大争议[1-2]。首都医科大学附属北京安贞医院泌尿外科自2016年开始应用机器人技术治疗肾上腺疾病。针对巨大肾上腺肿瘤,采用不同入路进行手术治疗。从2017年1月-2021年12月,共治疗巨大肾上腺肿瘤45例,现进行回顾性分析。
1 资料与方法
1.1 一般资料本组病例45例。患者年龄34~68岁,中位年龄为42岁。男性19例,女性26例。左侧23例,右侧22例。41例表现为高血压,规律服用降压药物,血压控制良好。4例表现无症状,因其他系统问题检查或体检发现。术前行内分泌检查以及肾上腺计算机断层扫描(computed tomography,CT)和增强扫描明确诊断。肿瘤均为单发,最大径6.6~10.8 cm,平均为(8.18±1.21)cm。所有患者均行机器人手术,手术为同一主刀医师带领团队完成,术前进行系统评估,排除严重心血管、出凝血异常等手术禁忌的患者。根据手术入路不同分为腹膜后入路组(robot-assisted retroperitoneal adrenalectomy,RARA)和腹腔入路组(robot-assisted transperitoneal adrenalectomy,RATA),其中腹膜后入路为17例,腹腔入路为28例。
1.2 手术方法
1.2.1术前准备 围手术期准备同开放手术和腹腔镜手术。考虑为嗜铬细胞瘤时,术前应用α受体阻滞剂药物和液体扩容。对合并心动过速者应用β受体阻滞剂。醛固酮增多症患者术前使用螺内酯纠正低钾血症,控制血压平稳;术前常规备红细胞悬液。
1.2.2手术入路及步骤 应用第三代达芬奇手术操作系统进行手术。
RARA组: 患者全身麻醉,健侧卧位,垫起腰桥,机器人手术车位于患者头端,气腹压为15 mmHg(1 mmHg=0.133 kPa)。Trocar布局同传统后腹腔镜手术入路。髂嵴腋中线为机器人镜头孔,肋缘下腋前、后线为两个机器人操作孔。并在髂前上嵴内上方放置12 mm Trocar作为助手操作通道。手术步骤同传统后腹腔镜手术。清理腹膜后脂肪后,依次打开肾周筋膜、脂肪囊,于肾脏内上方寻找肾上腺,按照传统的3个解剖层面(肾上腺的腹面、背面以及肾面)游离肾上腺肿瘤。手术的关键点是血管的处理,因为嗜铬细胞瘤的血供非常丰富,异位血管主要位于靠近大血管侧,如下腔静脉、腹主动脉或者肾血管,同时由于肿瘤体积大、占位效应明显、空间狭小,分离过程中容易损伤出血。因此在分离过程中,对于异位血管的处理主要以hem-o-lock钳夹离断为主。同时可靠地处理中央静脉,将肿瘤完整切除(图1)。
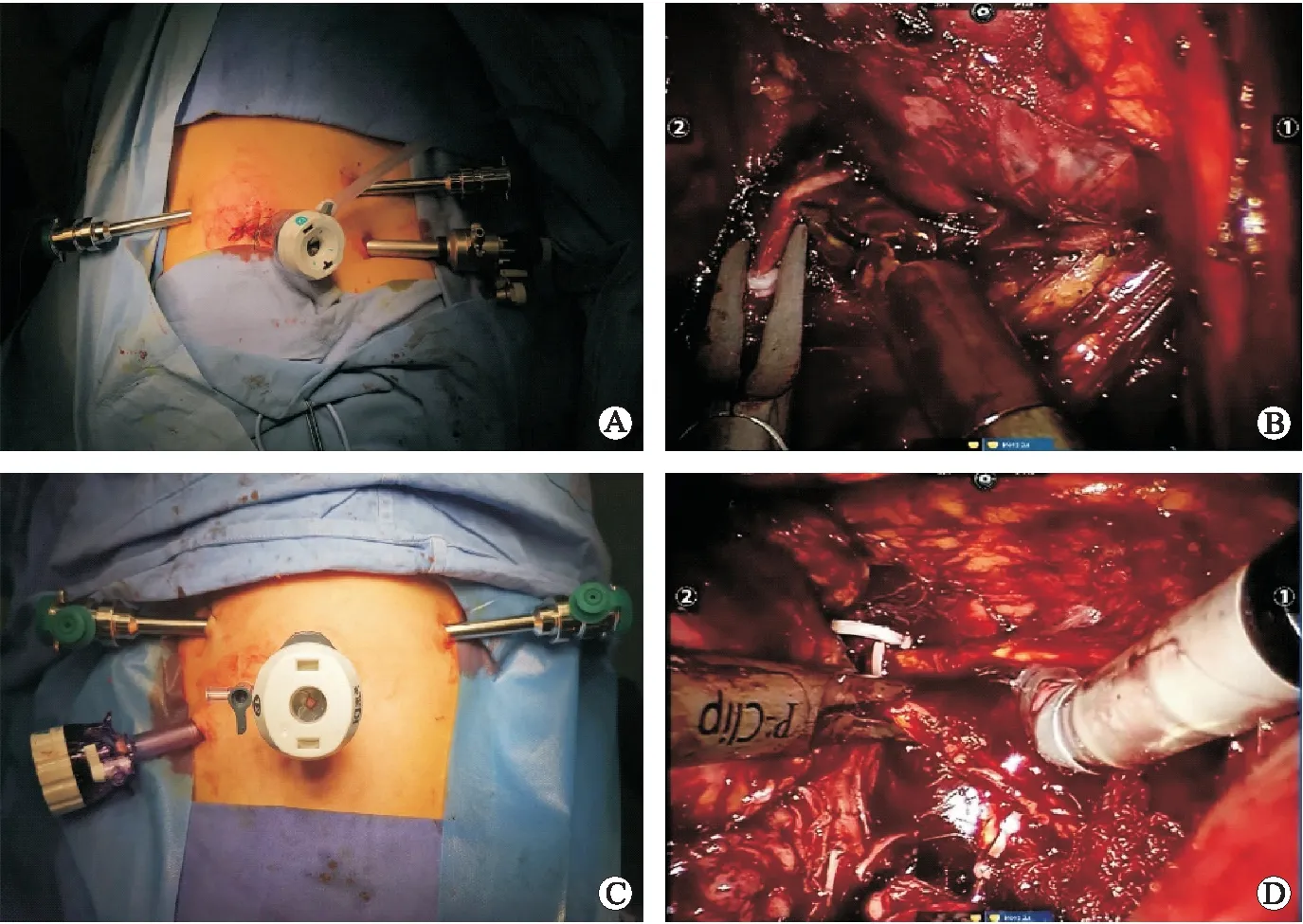
A:右侧腹膜后入路Trocar布局;B:右侧肾上腺肿瘤切除;C:左侧腹膜后入路Trocar布局;D:左侧肾上腺肿瘤切除。
RATA组:患者全身麻醉,侧卧60°,稍升起腰桥,机器人手术车位于患者背部头端,气腹压为15 mmHg(1 mmHg=0.133 kPa)。根据患者体型,将机器人观察孔置入脐部或者脐部患侧方。在锁骨中线肋缘下和麦氏点/反麦氏点建立机器人操作通路。在观察孔和两个操作孔之间建立两个助手操作通路。如果为右侧手术,需要在剑下腋中线建立操作通路挡肝。手术步骤:首先沿结肠旁沟切开侧腹膜。锐性分离Gerota筋膜前层和结肠融合筋膜之间的间隙,将结肠推向内侧。左侧者向上切断脾结肠韧带,脾膈韧带和脾肾韧带,结肠脾曲翻向内下;右侧者切断肝三角韧带和肝镰状韧带,将结肠肝曲翻向内下,并用举肝器托举肝脏以利更好地显露术区。左侧注意保护脾脏和胰尾,右侧注意保护肝脏和十二指肠。依次切开腹膜后脂肪、肾周筋膜以及脂肪囊,寻找肾上腺,余处理同腹膜后入路手术(图2)。
1.3 两种入路的对比分析收集资料并比较两组患者的一般参数和围手术期临床参数,包括手术时间、术中出血量、引流时间、术后住院时间、首次进食时间。
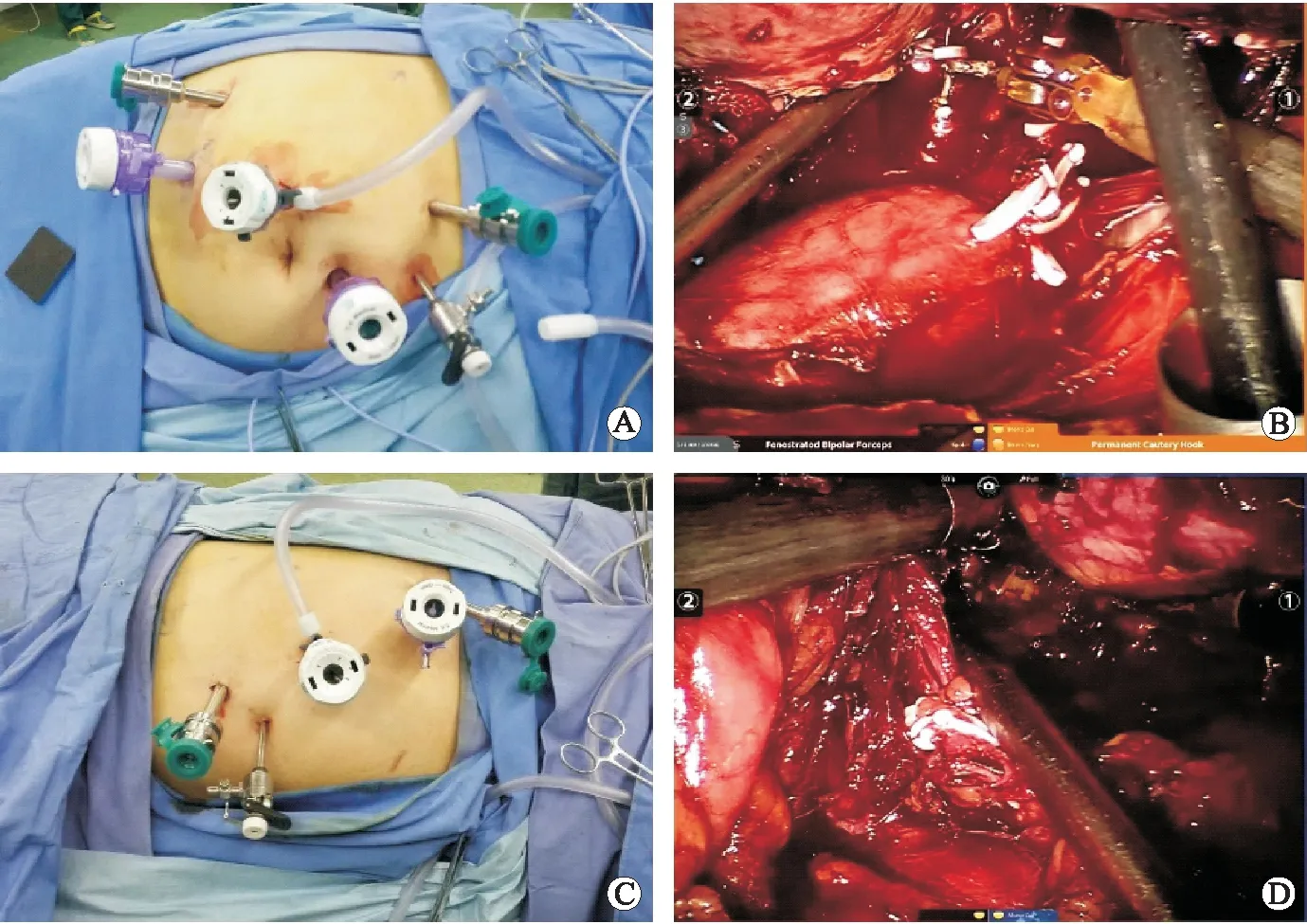
A:右侧腹腔入路Trocar布局;B:右侧肾上腺肿瘤切除;C:左侧腹腔入路Trocar布局;D:左侧肾上腺肿瘤切除。
2 结 果
2.1 两组术前一般资料比较两组间基线值比较差异无统计学意义(P>0.05),具有可比性(表1)。
2.2 两组围手术期指标比较两组平均手术时间、失血量、引流时间、术后住院时间比较,差异无统计学意义(P>0.05),而首次进食时间比较差异有统计学意义(P<0.01,表2)。
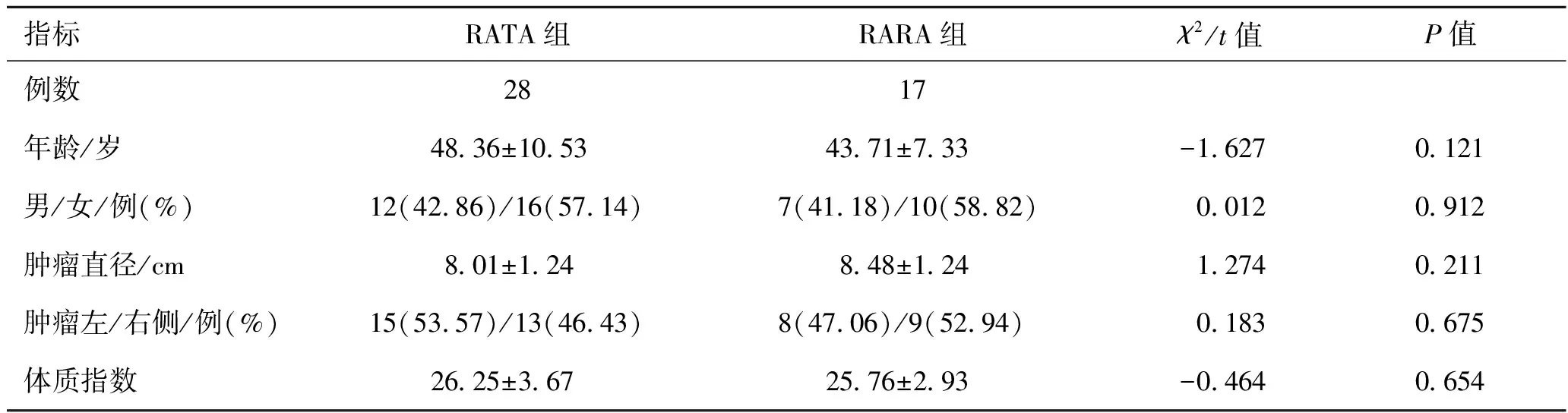
表1 机器人手术治疗巨大肾上腺肿瘤患者不同入路组术前临床参数基线值比较

表2 机器人手术治疗巨大肾上腺肿瘤患者不同入路组围手术期指标比较
45例患者均顺利完成手术,无中转开放,无输血,术后无严重并发症。术后病理提示39例为嗜铬细胞瘤,1例为肾上腺髓样脂肪瘤,3例为肾上腺皮质腺瘤,1例为肾上腺大结节病,1例为肾上腺转移癌,考虑原发病灶为肺脏肿瘤,患者转胸外科就诊。其中,RARA组包括1例肾上腺髓样脂肪瘤,1例为肾上腺转移癌和15例嗜铬细胞瘤。RATA组包括24例嗜铬细胞瘤,3例肾上腺皮脂腺瘤以及1例肾上腺大结节病。
首次随访时间为术后3月,以后改为每年1次随访。除肾上腺转移癌未在我科随访,其余患者均常规进行CT检查。随访时间6~36个月,未见肿瘤复发,全部患者血压控制良好。
3 讨 论
腹腔镜手术是目前肾上腺肿瘤治疗的金标准[3]。过往GAGNER等[4]1992年首次报道了腹腔镜肾上腺肿瘤切除术。2001年HORGAN等[5]首次应用达芬奇机器人治疗肾上腺肿瘤。
机器人技术治疗肾上腺肿瘤的安全性和有效性是明确的,研究显示与传统腹腔镜手术相比较,采用机器人技术治疗肾上腺肿瘤具有出血少、并发症少的优点[6]。这得益于机器人手术的三维放大成像系统对组织结构的清晰显示、灵活的机械手保证操作的精细化、术者不易疲劳和解除了生理振动对手术的影响等优势。超过6 cm的肿瘤被认为是巨大肾上腺肿瘤[7]。巨大肾上腺肿瘤往往血供比较丰富,与周围组织界限不清以及巨大体积所带来的占位效应,因此对于传统的腹腔镜,手术难度明显加大[8]。我们尝试应用机器人手术来处理巨大体积的肾上腺肿瘤45例,无明显并发症发生。
机器人技术治疗肾上腺肿瘤目前有经腹腔和腹膜后两种途径,各有优缺点。经腹腔途径操作空间大,但是容易受到腹腔脏器的干扰,甚至造成腹腔脏器的损伤。而由于腹腔镜技术的延续,中国医师更熟悉腹膜后入路。腹膜后入路的解剖环境相对简单,但手术空间小,加之肿瘤的位置和占位问题,使操作困难化。在本研究当中,两种入路均无中转开放,无严重术后并发症,证实了两入路在巨大肾上腺肿瘤治疗的可行性。
我们的经验首先在于病例的选择。对于肥胖且无腹部手术史的患者可选择经腹入路,减少脂肪层对手术的干扰,因这类患者如果行腹膜后入路,术中可能需要清除腹膜后和肾周脂肪。其次是肿瘤的位置,对于位置较高,如位于肾脏上方、肾脏或下腔静脉背侧的肿瘤可以考虑腹膜后入路;而对于位置较低,如肾脏内侧靠近肾门或下腔静脉腹侧的肿瘤选择经腹入路更佳。同时要考虑到肾周脂肪粘连对于腹膜后入路手术的影响,通常可以根据术前影像学检查结合梅奥粘连概率评分(Mayo adhesive probability score,MAP评分)进行选择[9-11],如评分高,则考虑腹腔入路。
术中的关键问题在于对出血的控制。往往巨大体积的肾上腺肿瘤血供丰富,表面血管迂曲扩张,尤其是靠近大血管侧。以右侧为著,通常是由于肿瘤深入肝脏下方造成的,而且距离下腔静脉近,有较多的肿瘤血管直接汇入下腔静脉。加之肿瘤体积巨大,周围解剖结构不清,因此容易出血。而机器人手术的优势恰恰在于视野放大清晰,稳定防抖动,操作更精准。对巨大肾上腺肿瘤可以做到更加精准的解剖、游离,控制血管,从而达到控制出血的目的。在本组病例中,所有患者手术顺利,术中术后无输血。
术中另外一个关键点是对患者血压的调控。由于术中器械操作的刺激导致嗜铬细胞瘤激素释放增多,影响机体血流动力的稳定性。传统腹腔镜由于较大的操作幅度,相对刺激较大,容易引起激素释放。而机器人手术可以依靠灵活的腕部操作,减少这种刺激。同样地,相比较而言,腹膜后入路相对操作空间较小,也存在容易造成瘤体刺激,因此在减少瘤体刺激方面经腹腔入路可能更有优势。同时,在术中尽可能早地寻找和处理中央静脉也能够有效减少激素释放。
肿瘤体积对手术的影响是存在的,因此,美国胃肠道和内镜外科协会对于超过6 cm的肾上腺肿瘤,建议选择经腹腔入路[12]。时京等[13]也认为对于巨大肾上腺肿瘤选择经腹腔入路,操作空间更大。贾卓敏等[14]认为超过10 cm的肾上腺肿瘤选择经腹腔入路更有优势。而在腹膜后途径处理大体积肾上腺肿瘤中,我们的经验就是尽可能地扩大操作空间。具体包括:建立操作通道时,利用气囊扩大空间;清除腹膜后和肾周脂肪;助手通过辅助通道牵拉推移肾脏或者肿瘤,同时结合灵活的机械手腕,为术者提供足够的空间。
国内外诸多研究明确了机器人手术治疗巨大体积肾上腺肿瘤的安全性和有效性[15],而手术入路无论是腹腔入路还是腹膜后入路都可以根据实际情况采用。本研究也证实除首次进食时间外,围手术期的多数临床参数如手术时间、平均失血量、引流时间、术后住院时间上两者并没有统计学差异。具体入路的选择可以根据术者习惯、肿瘤大小和部位、患者情况等因素来进行选择。同时,考虑到本研究样本量小,因此研究结果可能存在有偏倚,下一步应当继续扩大样本量进行总结。

