前列腺癌局灶治疗的新进展
张梦洁,张 青,郭宏骞
(1.东南大学医学院临床医学专业,江苏南京 210009;2.南京大学医学院附属鼓楼医院泌尿外科, 江苏南京 210008)
前列腺癌是男性常见的恶性肿瘤之一。根据最新的全球肿瘤数据,前列腺癌在2020年男性最常见的恶性肿瘤中排第2位,仅次于肺癌,其致死率排名全球第5[1]。在中国,前列腺癌的发病率也日益增高。根据WHO发布的数据,2020年全国前列腺癌新发病例约11万例,排名第10位;当年死亡例数约5万例,5年患病总人数约为40万。
低风险的局限性前列腺癌患者通常选择监测或全腺治疗。监测的弊端主要表现为重复多次的活检,可能会增加患者的经济负担;其次规律、长期、严格的监测,对患者的依从性和心理承受能力都有较高的要求[2-3]。全腺治疗指针对整个前列腺进行的治疗,主要包括根治性前列腺切除术(radical prostatectomy,RP)和根治性放疗(radical radiotherapy,RT)。全腺治疗导致的相关并发症目前还无法完全避免,例如根治术后的勃起功能障碍、尿失禁、淋巴瘘等[4-5],放疗后的尿路梗阻、出血、直肠尿道瘘、盆腔骨并发症等[6-7]。所以,全腺治疗在降低患者生活质量的同时,又带来了额外的治疗及经济负担。
由于上述监测与全腺治疗的缺点,前列腺癌的局灶治疗逐渐获得泌尿外科医生的重视。局灶治疗是消除局部已明确的病灶,同时监控其他剩余的腺体(图1)。2009年的一项研究表明,前列腺癌的转移灶均来源于同一克隆体,称为主要病灶。如果能准确识别并锁定主要病灶,局灶治疗可以获得更好的治疗效果[8-9]。本文就局灶治疗的现状作一综述。
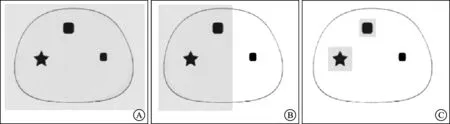
A:全腺治疗;B:半侧腺体治疗;C:局灶治疗。★:主要病灶;■:小病灶。
1 病灶的定位
局灶治疗的总体疗效和安全性取决于治疗前和治疗期间肿瘤的精确定位,而这主要依赖于术前的多参数磁共振成像(multiparameter magnetic resonance imaging,MP-MRI)。研究显示,MP-MRI增加的弥散加权成像(diffusion weighted imaging,DWI)、动态对比增强(dynamic-contrast enhanced,DCE)、表观弥散系数(apparent diffusion coefficient,ADC)图像可显著改善前列腺MRI的成像;此外,随着前列腺成像报告和数据系统(prostate imaging-reporting and data system,PI-RADS)的发布及更新,为每个序列的病灶评分提供了明确的标准,将各个序列的结果进行综合得到总体评分后,可以更准确地判断病灶是否具有临床意义[10-12]。
MP-MRI不但可以对病灶进行更准确的定位,还可以检测肿瘤内部的形态学变化,以评估治疗反应[13-14]。FELKER等[15]证实,病灶激光消融后预测肿瘤残留时,使用MP-MRI显著优于连续前列腺特异性抗原(prostate specific antigen,PSA)测量。
然而,MP-MRI也有局限性。首先,在Gleason评分较低的前列腺癌病例中,它经常会低估病灶的大小[16];第二,MP-MRI仍可能排除具有临床意义的前列腺癌,这可能会导致活检或局灶治疗时遗漏病灶[17]。因此局灶治疗时病灶定位还需MP-MRI与术中超声进行准确地融合。
2 局灶治疗方法
2.1 高强度聚集超声高强度聚集超声(high-intensity focused ultrasound,HIFU)是现在较为常用的局灶治疗方式之一。手术开始后将超声探头置于直肠内,先测量前列腺体积,并创建图像。医生将治疗区域标注在图像上,通过HIFU,精确、聚集的超声波被输送到目标组织,在2~3 s内组织的温度可以提高到近100 ℃,并导致凝固性坏死[18]。
GUILLAUMIER等[19]的研究是目前为止HIFU治疗前列腺癌最大的临床试验,研究纳入625例非转移性前列腺癌患者。整个患者队列的5年无失败生存率和总生存率分别为88%和99%。NAHAR等[20]的研究共纳入52例患者,术后12个月17%(5/30)的患者活检结果为阳性。GHAI等[21]在5个月后,发现有7%(3/44)的患者在治疗部位检测到残留的前列腺癌。另外,ALBISINNI等[22]的研究表明HIFU与RP后因疾病进展需要进一步治疗的概率无统计学差异。这些研究均证实:HIFU在进行前列腺癌的局灶治疗时能取得较好的肿瘤控制结果。
与此同时,HIFU在安全性方面也具有明显的优势:GUILLAUMIER等[19]的研究中,98%(241/247)的患者实现了完全无垫尿控;NAHAR等[20]的研究中患者泌尿系统功能3~6个月恢复至基线水平,性功能在12个月恢复。GHAI等[21]提出,术后5个月患者的中位国际勃起功能指数(international index of erectile function,IIEF)和国际前列腺症状评分(international prostate symptom score,IPSS)与基线数据无明显统计学差异;HIFU拥有较好的治疗成功率,且安全性有保证,同时手术可以在脊柱麻醉或静脉麻醉下进行,不需要在皮肤上进行切口[18],患者术后恢复较快。但GUILLAUMIER等[19]的研究中对患者随访不够充分,仅有222例患者在治疗后接受了穿刺活检,作者得到的结果可信度不够。因此仍需要大样本、长期随访的临床研究观察HIFU的治疗效果。
2.2 局灶激光消融局灶激光消融(focal laser ablation,FLA)的治疗方法是经会阴或经直肠将小的激光光纤插入肿瘤,采用其放电的热量迅速升温,造成可控区域的凝固性坏死,从而降低相邻结构损伤的风险[23]。有关FLA的临床研究数量较少,且大多数都是小样本的。
WALSER等[24]的研究纳入了120例中低危前列腺癌患者,17%(20/120)的患者在直肠FLA治疗1年后,因复发接受了进一步治疗[24]。ALHAKEEM等[25]的临床研究也得到了类似的结论,治疗后有20.4%(10/49)的患者在治疗区域仍存在肿瘤。但是根据美国权威的癌症统计数据库——Surveillance,Epidemiology,and End Results (SEER)数据库得到的数据表明,FLA和RP的癌症特异性死亡率(cancer specific mortality,CSM)差异无统计学意义[26],而RT在生存获益方面具有明显优势[27]。
FLA的优势主要体现在有效性和安全性:大多患者IPSS和男性性健康调查表(sexual health inventory in men,SHIM)评分无明显差异,部分患者即使受到影响,随着时间的推移也会恢复至基线[24];此外FLA可以在局部麻醉下进行,手术风险较小。其缺点主要体现在技术方面对临床医生的要求更高[28],同时仍缺乏长期的随访数据。
2.3 冷冻疗法冷冻疗法(cryotherapy)主要包括快速冷冻、缓慢解冻和冻融循环的重复。冷冻手术对组织的破坏主要有2个机制:一个是冷却和加热循环对细胞的损害;另一个是组织微循环的进行性衰竭和血管淤滞。对于肿瘤治疗来说,冷冻组织的温度应达到-50 ℃,但冷冻的最佳持续时间尚未有统一的意见[29]。
CHUANG等[30]对61例患者进行了半侧冷冻治疗:治疗后6个月82%(50/61)的患者活检阴性,18个月时82%(22/27)的患者活检阴性。TAN等[31]使用部分冷冻消融,其1~5年无失败生存率分别为98%、89%、84%、75%和75%。MERCADER等[32]通过危险分层发现,低、中、高风险组的生化无进展生存率分别为70.2%、70.3%和50.0%,但他们的研究对前列腺体积较大的患者使用了3个月的新辅助治疗。OISHI等[33]回顾了160例接受半侧冷冻消融的患者,其中131例为中危或高危;第5年的无治疗失败生存率为85%,无生化失败生存率为62%。另外,从SEER得到的数据发现,冷冻和手术的10年肿瘤特异性生存率分别为98.1%、 99.2%。冷冻也能达到较好的结局[34]。
另外,上述研究也对安全性进行了分析,术后95%~100%的患者可以保持无垫控尿[31-33]。SHAH等[35]发现术后12月IPSS、IIEF评分恢复至基线的概率分别为78%和85%。
通过以上分析可以发现,冷冻治疗拥有较好的肿瘤学结局,但治疗的规范流程仍需进一步探索,有研究提示,在前列腺癌冷冻治疗前进行三维标测活检可以更好地对患者进行危险分层,降低治疗的失败率[36]。同时冷冻消融对功能有一定影响,在后续的使用中需要进行更多的探索。
2.4 不可逆电穿孔应用脉冲电场后导致细胞膜通透性的增加,被称为电穿孔现象。根据不同的电流参数和细胞特征,电穿孔可以是可逆或不可逆的。不可逆电穿孔(irreversible electroporation,IRE)的原理正源于此[37]。IRE通过在细胞膜内形成纳米孔导致细胞死亡,同时不会引起热效应。其显著优势在于,不会因热能损失导致能量耗散而影响治疗效果[38]。一项犬类的临床前研究表明,IRE治疗后血管、神经等胶原结构没有受到损伤[39]。如果这一发现在人类研究中得到证实,更能促进IRE的推广使用。
BLAZEVSKI等[40]的临床试验纳入了123例患者,术后3年无失败生存率为96.75%、无转移生存率为99%。COLLETTINI等[41]的小样本研究认为6个月后复发率为17.9%(5/28)。此外,IRE用于前列腺顶点消融也取得了令人惊喜的结局,随访超过3年后,无失败生存率为90%(36/40)[42]。
IRE术后1年内患者总体尿控功能基本恢复到基线水平,甚至76%~94%患者术后仍能保持勃起功能[40-42]。
IRE具有很好的肿瘤学结局,同时治疗后并发症发生率较低;因其可能具有选择性,可保留血管、神经等组织,具有广阔的应用前景。IRE的缺陷主要表现在治疗时需要全身麻醉和评估[38],治疗过程中可导致患者发生心律失常。但治疗中脉冲频率与心脏节律同步可降低心律失常的发生率[43]。
2.5 光动力疗法光动力疗法(photodynamic therapy,PDT)主要取决于3个组分:光敏化合物、可见光和氧气。光敏化合物选择性地在过度增生的靶细胞中蓄积,随后在可见光和活性氧的作用下,靶细胞发生坏死和凋亡[44]。体外实验证实,光动力疗法的作用机制是通过改变线粒体膜的通透性最终导致靶细胞死亡,提示线粒体膜通透性相关蛋白的调节可能成为光动力治疗疗效的关键[45]。本文主要讨论血管靶向光动力疗法(vascular-targeted photodynamic therapy,VTP)。
FLEGAR等[46]对VTP和RP进行对比,得出的结论并不乐观,但本研究随访薄弱、没有对VTP和RP患者进行匹配,且仅有79%的患者在VTP之前接受MP-MRI和靶向穿刺活检,导致结果有偏倚。而VTP与主动监测相比仍有较大优势,4年后VTP组和主动监测组活检的阴性率分别为50%(104/206)和14%(30/207)。同时VTP后进一步治疗的概率更低[47]。
VTP有一定的副作用,FLEGAR等[46]的研究中,有12%的患者发生了膀胱出口梗阻。TRACEY等[47]研究纳入的患者有12%(6/50)发生了3级治疗相关不良反应。此外,VTP术后患者排尿、勃起功能评分均有下降,恢复至基线水平的时间较长[48-49]。
VTP也是局限性前列腺癌有前景的治疗方式之一,但目前相关研究较少,且都是小样本研究,肿瘤学结局相对较差,也需要更多更长时间的随访来确定其疗效和副作用。
3 总结与展望
各类局灶治疗的机制及关键临床研究总结见表1、表2。通过全文可以看出,HIFU和FLA具有更好的无失败生存率和术后功能控制,同时治疗的流程也更完善和标准,结合近年来的专家共识、鼓楼医院经验,前列腺癌局灶治疗的理想人群为:①PSA<15 ng/mL;②临床分期≤T2a;③Gleason评分≤ 3+4 (ISUP2);④预期寿命 > 10年;⑤PI-RADS 评分4~5分(没有包膜和精囊浸润);⑥患者充分知情[50-51]。结合上文的讨论,以下几种患者也可以考虑进行局灶治疗:①早期前列腺癌不愿接受主动监测;②希望最大限度保护原有功能;③高龄或无法耐受全麻手术。
尽管缺乏长期的随访数据,局灶治疗仍是局限性前列腺癌非常有前景的治疗方式。但在广泛应用之前,其适应证和更加标准的治疗方案仍需国内外专家达成共识,并分析其长期肿瘤学结局和对患者生活质量的影响。

表1 针对前列腺癌各类局灶治疗的机制
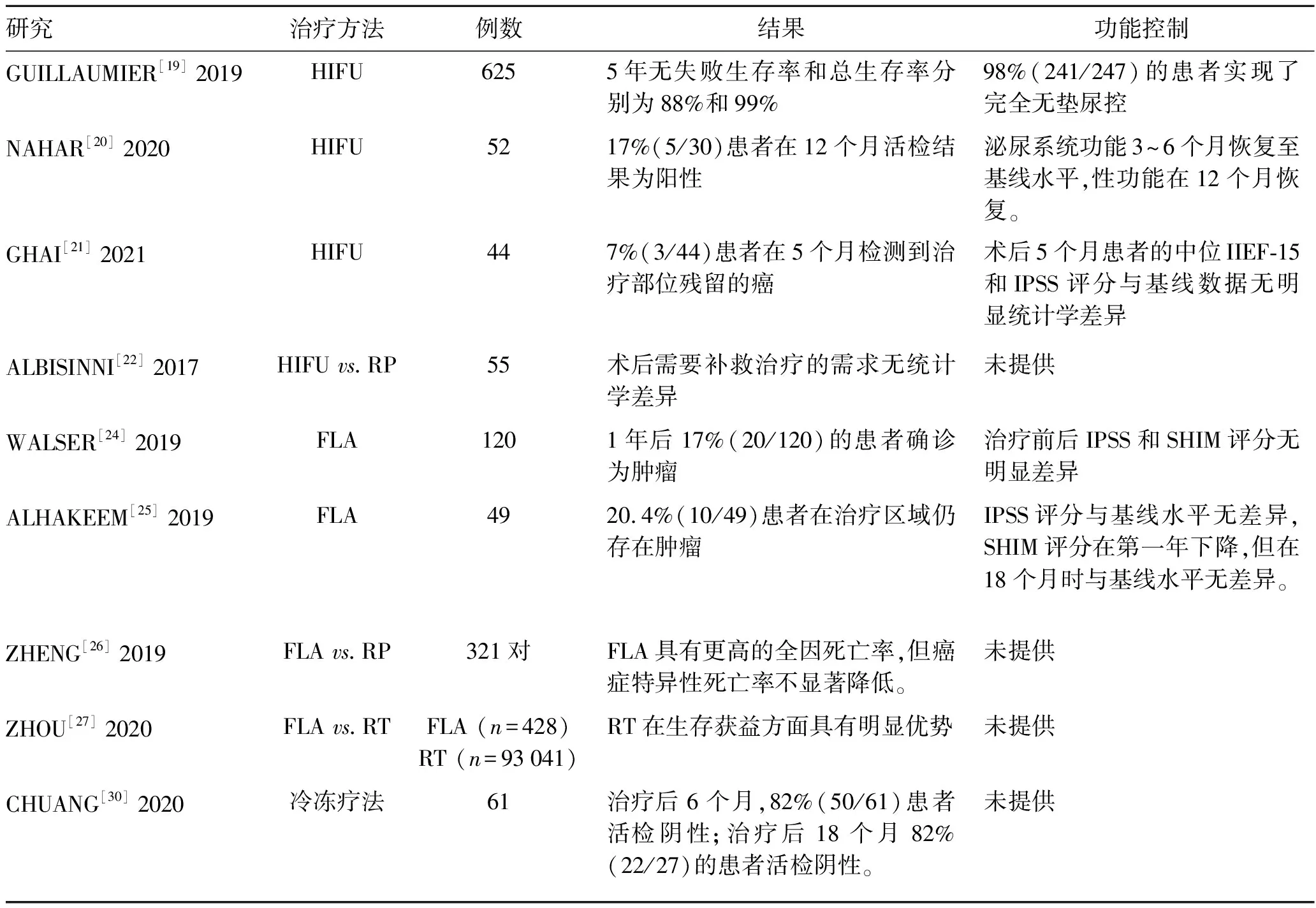
表2 不同类型局灶治疗前列腺癌的关键临床研究
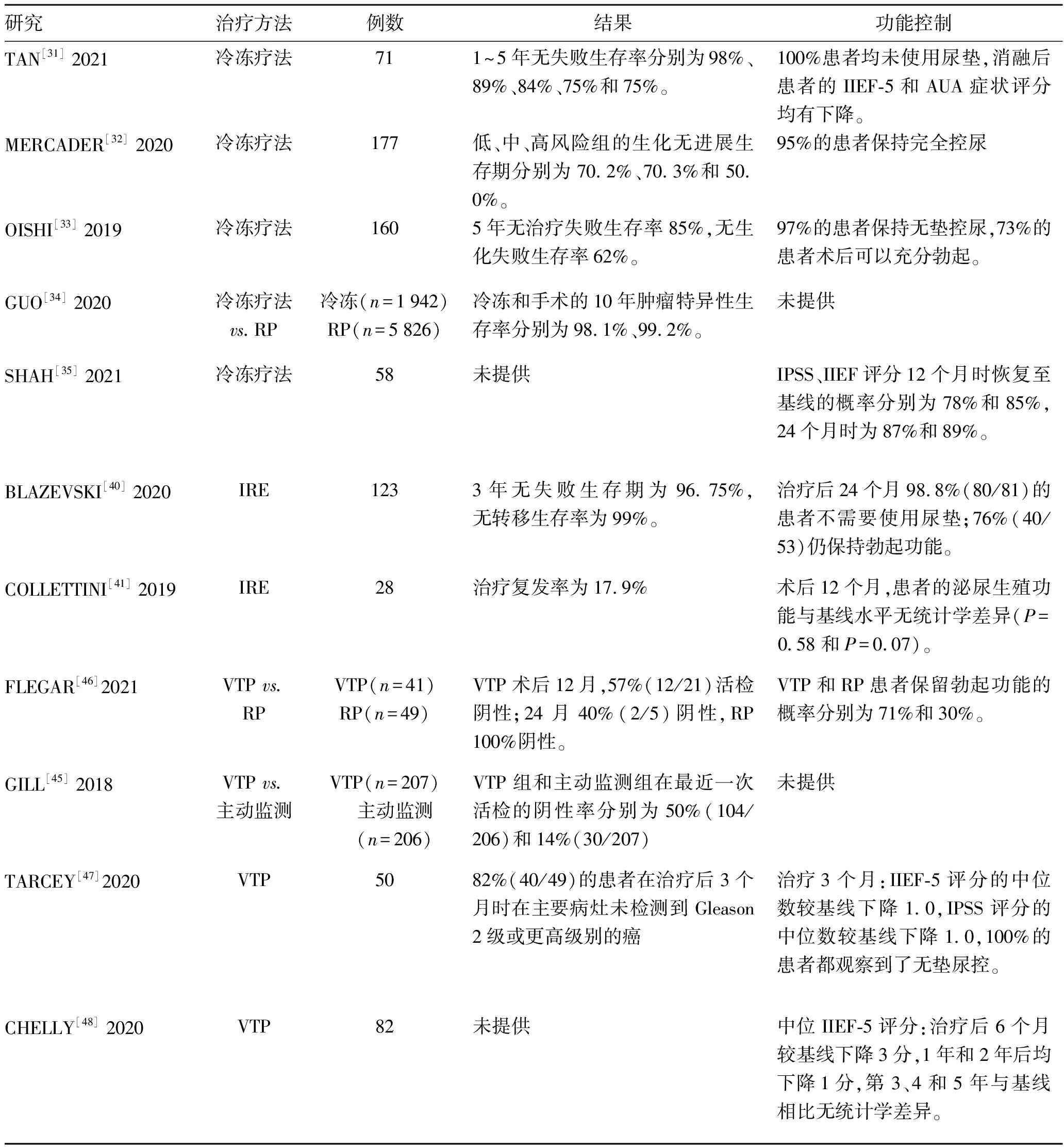
续表2

