DN-HCC及DN患者超声造影及CEUS LI-RADS标准分类结果观察
师旭 乔向彬 刘佳 肖保军
作者单位:102600 北京市大兴区人民医院超声科
我国肝细胞瘤(HCC)年发病数占全球发病总数的50%以上,恶性程度较高,早期诊断难度较大,手术根治率偏低,并且术后易复发,整体预后差[1-3]。文献报道,约90%的HCC经历了自大再生结节发展为LGDN/HGDN,再到DN-HCC、高/中/低分化HCC,其中DN为HCC癌前病变[4]。自DN进展而来的HCC癌变组织仍有门脉供血,可见与门脉、胆管不伴行的不成对动脉,且数量不等,典型HCC影像学表现往往缺乏[5]。自LI-RADS发布以来,CEUS等影像学检查应用更为广泛,极大地满足了临床对结构化影像报告系统的需求。本研究对比分析了DN-HCC及DN的CEUS表现特征及CEUS LI-RADS v2017标准分类结果,旨在为提高对DN-HCC和DN的认识与诊断正确性积累经验。
资料与方法
一、一般资料
2019年10月至2021年10月,北京市大兴区人民医院收治的肝脏局灶性病变患者78例,共有80个病灶,其中DN 12个,DN-HCC 68个。患者均于入院时确诊[6],慢性HBV感染69例,慢性HCV感染2例,药物性肝病1例,血吸虫肝病1例,无慢性肝病病史1例,慢性HBV合并HEV感染4例。排除标准:不稳定性心绞痛、严重肺动脉高压;先天性肝纤维化和肝血管疾病(如淤血性心脏病、布加综合征等)所致肝硬化;其他类型恶性肿瘤;CEUS图像不完整或图像质量不佳;既往有精神病史或语言障碍史。
二、方法
使用Philips Epiq7、 Philips Epiq5、 Philips iU Elite、 Siemens ACUSONS3000彩色多普勒超声诊断仪,患者先行常规二维超声及彩色多普勒超声检查, 取合适体位,于患者平静呼吸下选择病灶显示最佳切面固定探头,实时双幅CEUS模式启动后肘前静脉团注造影剂(意大利博莱特公司)1.5~2.4 mL。造影剂注入当即计时,动脉期采集后予门脉期、延迟期间隔采集,存储动态图像,不同部位或显像不充分时,间隔 10 min 再次行造影检查。CEUS时相划分参考相关标准[7]。动脉期增强类型分为不均匀低增强、同步等增强、局部高增强和高增强。CEUS LI-RADS v2017分类标准参照美国放射学会发布的CEUS LI-RADS v2017分类标准[8]。
三、统计学方法
应用SPSS 22.0统计软件。计数资料以例数(%)表示,比较行χ2检验,P<0.05为差异有统计学意义。
结 果
一、两组CEUS动脉期、门脉期及延迟期表现比较
DN组动脉期同步等增强占比高于DN-HCC组,动脉期高增强占比低于DN-HCC组,门脉期-延迟期回声改变中高-高回声改变占比高于DN-HCC组(P<0.05)。见表1。1例59岁男性DN-HCC患者影像学表现见图1。
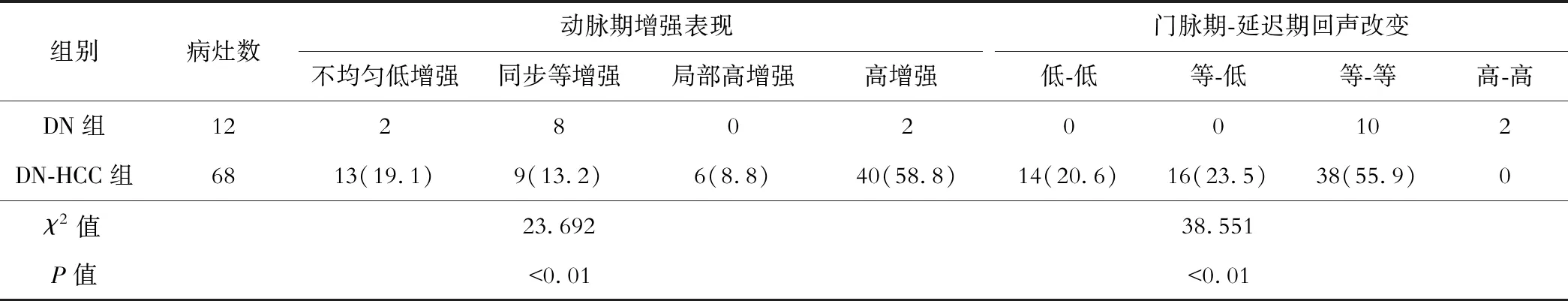
表1 两组CEUS动脉期、门脉期及延迟期表现比较[例(%)]
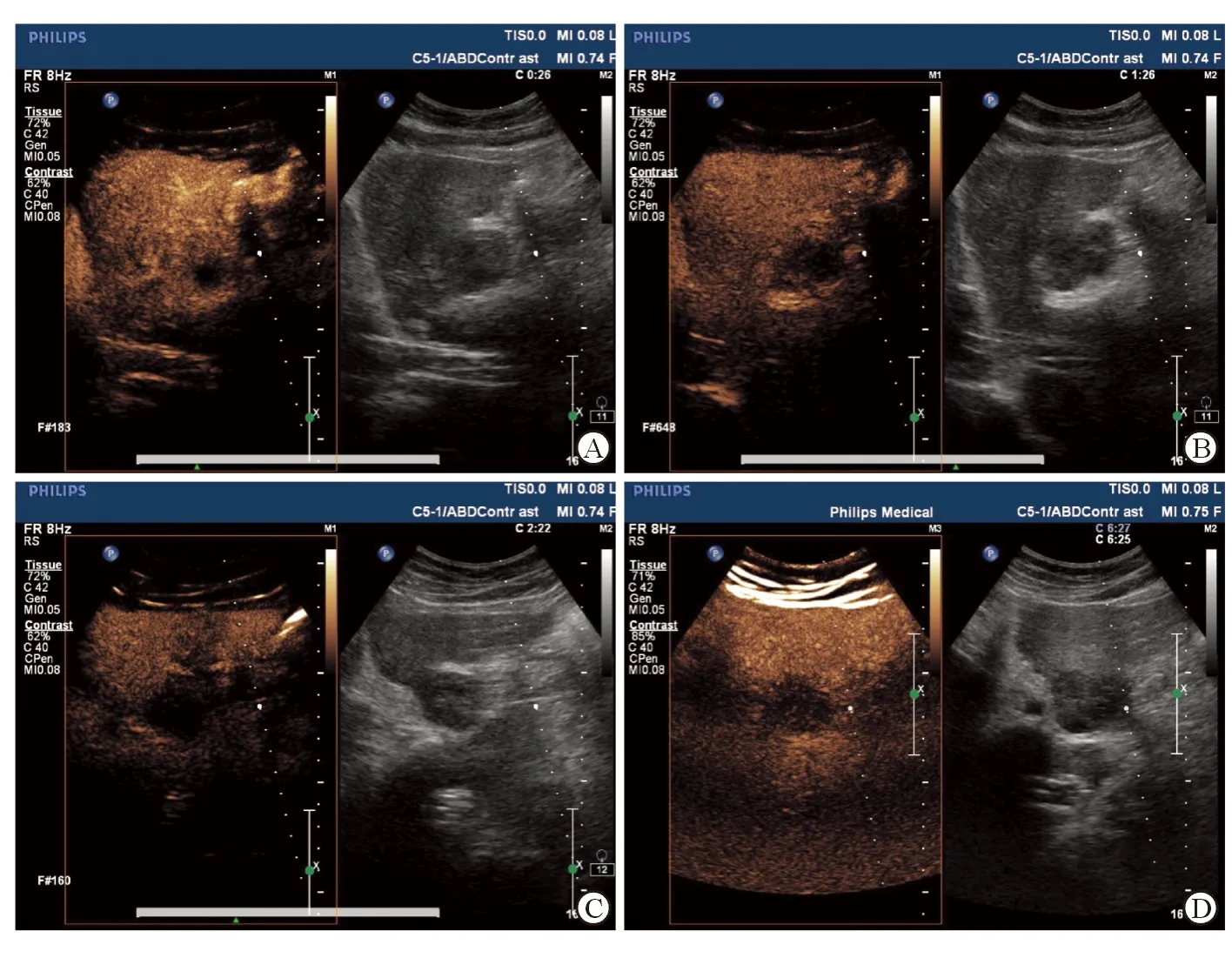
A:CEUS动脉期结节不均匀等增强,同步于肝实质;B:门脉期结节低增强,早于肝实质廓清;C、D:延迟期结节低增强
二、两组CEUS增强模式比较
DN组病灶动脉期和延迟期CEUS增强模式包括三种,低/等占3/12,等/等占8/12,高/高占1/12。DN-HCC组CEUS增强模式包括六种,其中等/等占4.4%(3/68),低/低占5.9%(4/68),等/低占8.8%(6/68),低/等占13.2%(9/68),高(含局部高增强)/低占29.4%(20/68),高(含局部高增强)/等占38.2%(26/68)。
三、两组CEUS LI-RADS标准分类结果比较
DN组CEUS LI-RADS标准分类中LR-3类占比高于DN-HCC组,LR-4类占比低于DN-HCC组(χ2=8.661,P<0.05),见表2。
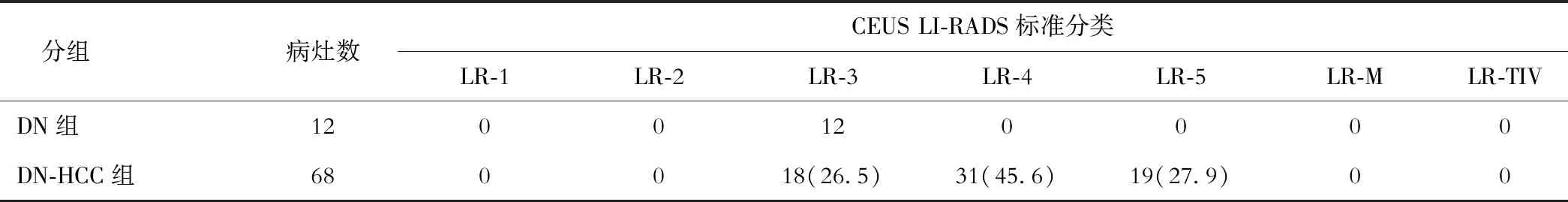
表2 两组CEUS LI-RADS标准分类比较
讨 论
2015版原发性肝癌规范化病理诊断指南认为肝细胞异型增生、异型增生灶、LGDN、HGDN及肝细胞腺瘤为HCC癌前病变,其中HGDN癌变风险极高[9-10]。Joo等[11]报道DN 50个月累计恶变率为40%,100个月累计恶变率高达75%。而在肝硬化肝移植标本和肝癌切除标本中通常仔细检查能发现DN,但当前影像学发现率偏低,其原因与此类病变体积偏小、缺乏典型影像学特征有关。尤其是针对DN与早期HCC,因两者存在诸多共同病理特征(如细胞密度增大、细胞中度异型、无包膜、脂肪变性、可有汇管区、存在数量不等的不成对动脉等),导致鉴别难度较大。
有研究显示,常规超声对HCC的敏感度高达84%,但对早期HCC的敏感度仅为47%[12]。欧洲肝病学会、亚太肝病学会和美国肝病学会也建议将超声纳为HCC高危人群的随访监测手段[13]。研究表明,CEUS诊断HCC敏感度并不逊于增强MRI或增强CT,其可实时连续观察整个动脉期,弥补增强MRI或增强CT因扫描时间间隔所致部分动脉相信息丢失缺陷,实时探查肝组织内微血管结构,系统揭示肝肿瘤血流动力学[14]。
本研究结果显示,DN组动脉期同步等增强占比较DN-HCC组高,动脉期高增强占比较DN-HCC组低,提示DN-HCC动脉期以高增强为主要表现,DN以同步等增强为主要表现,而部分DN-HCC仍以门脉供血为主导,与以往研究吻合[15]。本研究中,3例DN-HCC动脉期不均匀低增强,动脉早期病灶周围见环状高增强区。Renzulli等[16]报道DN-HCC演变过程中病变内不成对动脉数量递增,以周围为主增多至内部、周边俱增,表明肝癌演变过程中周围纤维包膜血管是其动脉血供的主要来源。Fan等[17]也发现约100.0%的HGDN和97.6%的早期HCC动脉期表现为向心性填充增强,即周围血管型增强,而本研究中未发现DN此表现。
DN-HCC镜下常见灶性瘤细胞及浸润间质,结中结表现较少,一旦有此表现,则高度提示为癌变。而CEUS LI-RADS将结中结表现作为诊断HCC的重要辅助特征,因为子结节基本属高、中分化HCC,母结节则属DN或高分化HCC。本研究中,6例DN-HCC动脉期局部高增强,有结中结表现。Wu等[18]通过对27个DN-HCC的CEUS不同增强表现区域进行穿刺活检,发现DN区为动脉期同步或缓慢增强区,癌变区为动脉期高增强区,而延迟期癌变区域呈局部减退表现。但本研究中,有少量DN-HCC门脉期、延迟期造影剂廓清,有低回声改变情况,而DN未出现此情况。
CEUS LI-RADS是美国放射学会仿照CT/MRI LI-RADS在临床中成功应用,于2016年9月正式推出的仅适用于HCC高危人群,随后为与CT/MRI LI-RADS v2017相协调,经过临床应用与医师反馈于2017年推出了最新版,主要按照HCC高危患者肝内结节大小和CEUS表现对其进行分类,其中自LR-3类至LR-5类HCC可能性逐渐增加。本研究结果显示,根据CEUS LI-RADS v2017分类标准,仅27.9%的DN-HCC确诊为LR-5类,明确为HCC;26.5%的DN-HCC与100.0%的DN均确诊为LR-3类,提示为可疑HCC,HCC和良性结节的概率均等,表明两者动脉期均见不均匀低增强或同步增强。Park等[19]报道DN的CEUS增强模式主要以低/等、等/等为主,与本研究结论相似。
综上所述,在DN与DN-HCC的鉴别诊断中,CEUS动脉期高增强或延迟期减退有助于提高诊断敏感性。但本研究中受超声透声窗等影响,CEUS检查不能充分评估全肝及多发性病灶具体情况,未来仍有待进一步研究。
利益冲突声明:所有作者均声明不存在利益冲突。

