儿童遗传性胰腺炎及其家系分析一例报道并文献复习
何小莉,梁淑恒,李妙遐,孔晋亮,单庆文*
遗传性胰腺炎(hereditary pancreatitis,HP)是一种外显率达80%的罕见常染色体遗传病,好发于儿童、青少年,性别分布均等,排除已知的诱发因素(如胆结石、酒精、感染、药物等),以急性胰腺炎(acute pancreatitis,AP)和复发性急性胰腺炎(recurrent acute pancreatitis,RAP)为特点,年轻时即可进展为慢性胰腺炎(chronic pancreatitis,CP),甚至并发3c型糖尿病(type 3c diabetes mellitus,T3cDM)和胰腺癌[1-3]。国外研究结果显示,HP发病率为0.30/10万~0.57/10万[4-5]。在国内,关于HP的研究十分少见,大部分为个案报道及综述[6-7],这可能是由于HP的发病率因地区而异或临床对该病认识不足。在线人类孟德尔遗传(OMIM)数据库数据表明,编码阳离子胰蛋白酶原的丝氨酸蛋白酶1(serine protease 1,PRSS1)基因杂合突变可发生HP(OMIM:167800)[8],该基因是HP最常见的发病基因,p.Val39Ala(V39A)是其罕见的突变位点[9]。在PubMed、万方数据知识服务平台进行文献检索,发现截至2022年3月,V39A突变在我国尚未见相关病例报道。现报告国内1例V39A突变相关HP家系,并分析其临床特点、并发症等,为临床医师及早诊治该病提供参考。
1 病例简介
患儿,男,6岁9个月,因“腹痛半天”于2021-01-14于广西医科大学第一附属医院进行治疗。患儿入院前半天在无明显诱因下出现腹部阵发性隐痛,以左上腹为主,伴食欲减退,无恶心、呕吐、腹泻,无发热,腹痛渐加重,在当地医院急查上腹部CT平扫+三维重建示:胰腺体积增大,形态不规则,边缘毛躁,体尾部显示欠清,胰管扩张,胰周见片状低密度影,周围脂肪间隙模糊,考虑胰腺炎,未予处置。为进一步诊疗而至广西医科大学第一附属医院就诊。患儿近1年半有3次AP发作,均予禁食、静脉补液、奥曲肽等治疗后缓解。入院查体:生命体征正常,体质量23 kg,身高125 cm,发育正常,营养良好。意识清晰,皮肤无黄染、皮疹。心肺查体无异常。腹软,左上腹压痛,无反跳痛,无包块,肝脾肋下未触及,Murphy征阴性,肠鸣音正常。四肢及神经系统查体无特殊。实验室检查结果,白细胞计数:11.39×109/L,中性粒细胞百分比:0.838;白介素6:688.7 ng/L;血淀粉酶:14 U/L;血脂肪酶:17.8 U/L;尿淀粉酶:2 939 U/L;空腹血糖:3.17 mmol/L;C反应蛋白、降钙素原、电解质、糖化血红蛋白、凝血四项等无异常。腹部MRI+胰胆管造影提示:主胰管扩张,边缘尚光整,胰尾部稍肿胀,边缘模糊;考虑CP急性发作(图1~2)。因患儿胰腺炎反复发作,病因未明,经家长知情同意,行全外显子组高通量测序,结果示,患儿7号染色体PRSS1基因的2号外显子存在杂合变异:c.116T>C(胸腺嘧啶>胞嘧啶)/p.Val39Ala(缬氨酸>丙氨酸,即V39A)。根据美国医学遗传学与基因组学学会(American College of Medical Genetics and Genomics,ACMG)遗传变异分类标准,c.116T>C/p.Val39Ala变异可归类为“可能致病性变异”。经Sanger测序家系验证,患儿及其母亲均携带c.116T>C/p.Val39Ala杂合变异,患儿父亲未检测到该变异(图3)。患儿家族谱系分析显示患儿c.116T>C/p.Val39Ala突变来源于母亲,符合常染色体显性遗传(图4)。结合患儿母亲也有CP病史,患儿最终被确诊为HP。予暂禁食、肠内营养、醋酸奥曲肽抑制胰腺分泌、西咪替丁抑酸等治疗8 d后,尿淀粉酶恢复正常,腹痛缓解出院。出院后随访8个月,患儿时有腹痛复发,予抑制胰酶分泌等内科治疗可好转。
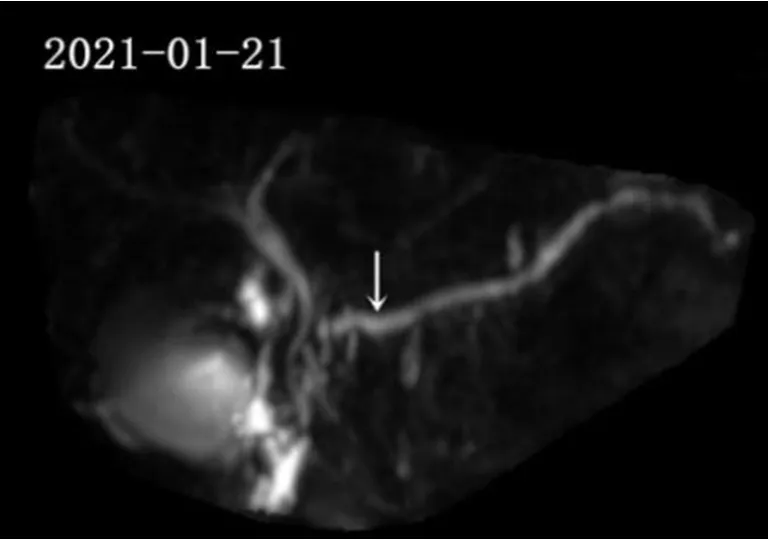
图1 2021年1月患儿胰胆管造影结果Figure 1 Cholangiopancreatography results of the child performed on January 21,2021
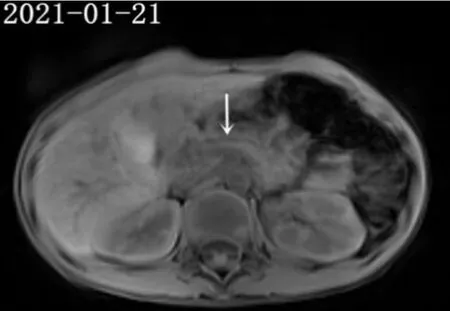
图2 2021年1月患儿腹部MRI结果Figure 2 Abdominal MRI results of the child performed on January 21,2021
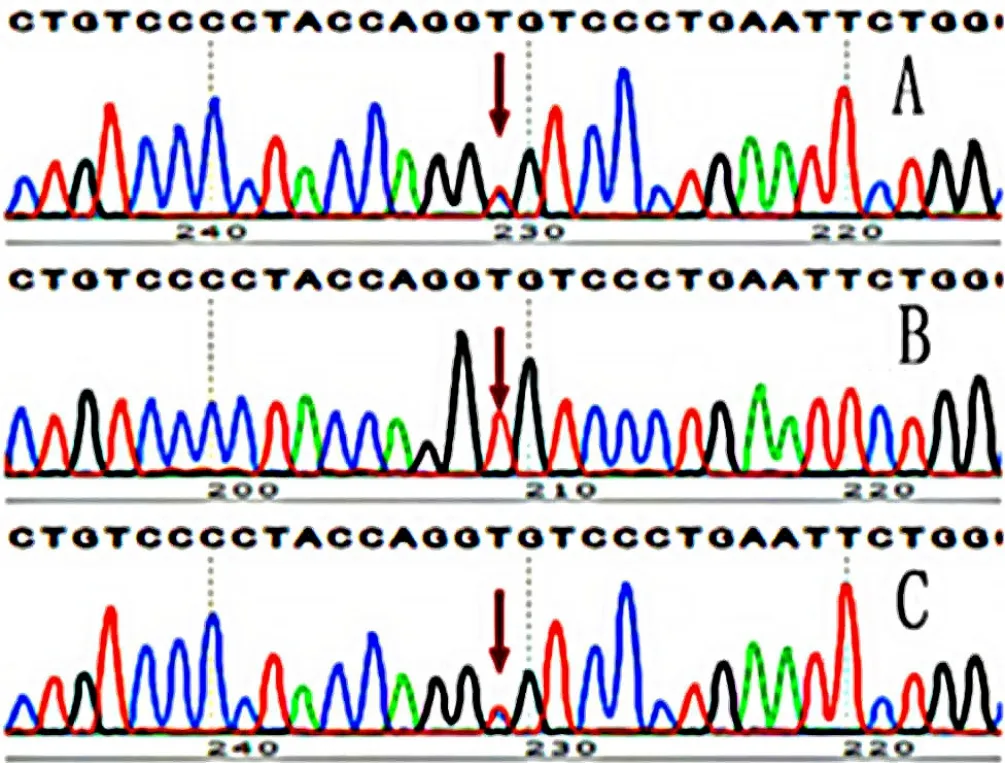
图3 HP患儿及其父母基因测序结果Figure 3 Gene sequencing results of the child with hereditary pancreatitis and his parents
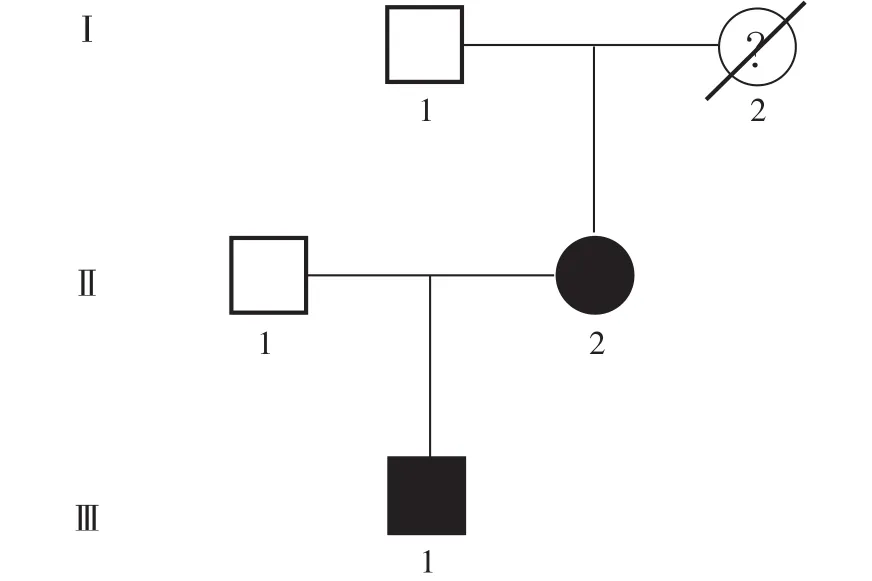
图4 HP患儿家族谱系图Figure 4 Pedigree chart of the child with hereditary pancreatitis
2 家系调查
患儿父母非近亲婚配,患儿母亲自幼反复腹痛,多次至外院及广西医科大学第一附属医院住院治疗,20岁前被诊断为CP;21岁其在外院行胰腺假性囊肿引流术,术后至广西医科大学第一附属医院复查腹部CT示:胰腺增大,头部及体部见多个大小不等的囊状低密度区,最大为7.0 cm×6.5 cm×3.0 cm,边界基本清楚,增强无强化,包膜轻度强化,胰管不规则扩张,可见钙化,胰实质不规则强化(图5);22岁其因“反复胸闷、气喘2个月”至外院就诊,查空腹血糖未见异常,但2次查餐后2 h血糖均>11.1 mmol/L,诊断为:(1)胸腔积液,(2)CP。因胸腔积液性质不明至广西医科大学第一附属医院进一步诊疗,查2次空腹血糖均正常,行腹部超声提示:肝左叶下方、胰腺区域不规则无回声区(6.6 cm×3.3 cm,囊肿?)、右侧胸腔积液、肝胆回声未见异常;胸部CT提示:右侧胸腔大量积液并右肺膨胀不全(图6),排除结核性胸膜炎等疾病,诊断为:(1)胰源性胸腔积液,(2)CP,经胸腔穿刺引流、护胃等治疗后好转。出院前查腹部CT提示:胰腺体尾部萎缩变小,头部相对稍增大,胰管明显扩张,其内可见钙化影(图7);22~32岁有间断腹痛发作,尚可忍受,内科治疗好转,期间监测血糖无明显异常;33岁(在随访患儿期间)出现了血糖升高,外院诊断为糖尿病,控制饮食后血糖较前下降,但近期血糖出现明显波动,饮食控制效果欠佳。患儿父亲体健。患儿外婆有血糖升高病史,外院曾诊断为糖尿病,无腹痛病史,在患儿母亲年幼时即去世,死因不详。患儿外公否认腹痛及血糖升高病史,否认家族中其他成员遗传性疾病病史。
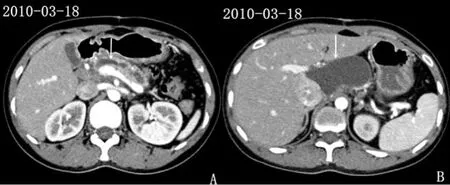
图5 2010年3月患儿母亲腹部CT结果Figure 5 Abdominal CT results of the child's mother performed in March,2010
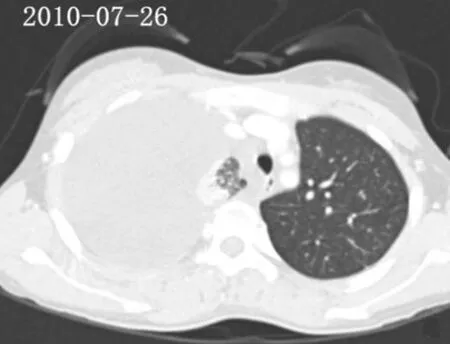
图6 2010年7月患儿母亲胸部CT结果Figure 6 Chest CT results of the child's mother performed in July,2010
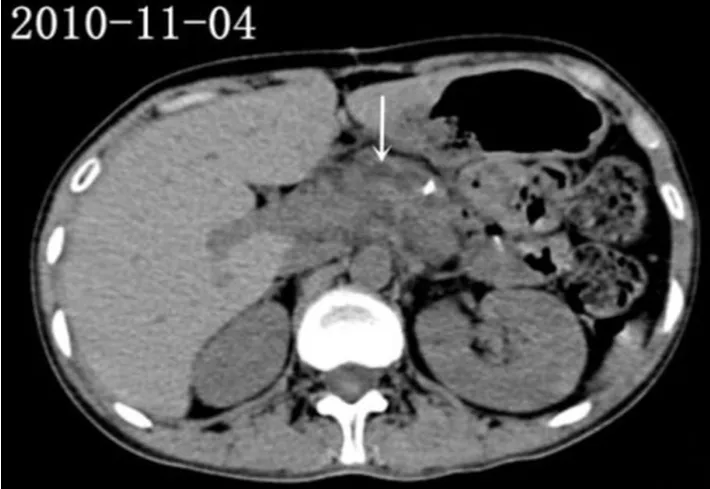
图7 2010年11月患儿母亲腹部CT结果Figure 7 Abdominal CT results of the child's mother performed in November,2010
3 讨论
HP临床表现多种多样、无特异性,包括腹痛(主要为左、中上腹部疼痛)、恶心呕吐、食欲减退、餐后上腹饱胀、脂肪泻或腹泻、营养吸收障碍、体质量下降、脂溶性维生素(维生素A、D、E、K)缺乏、内外分泌功能受损、腹腔积液、脾大、胆管和十二指肠梗阻、阻塞性黄疸、假性囊肿、胰腺癌等,发作时血尿淀粉酶、脂肪酶等升高,这与其他原因引起的胰腺炎相似,但HP发病年龄常较小,患者多有家族史,而且HP常有胰腺萎缩、胰管内钙化和主胰管扩张等3种影像学表现,但并非所有患者有这3种表现,部分患者胰腺影像学检查结果是正常的,且这些影像学表现在不同突变基因导致的HP患者中的发生频率和严重程度也不同。此外,慢性酒精性胰腺炎亦可出现上述3种影像学表现,临床上需注意结合病史加以鉴别[10]。本例胰腺炎患儿影像学提示主胰管扩张,其母亲除主胰管明显扩张外,尚存在胰管钙化及胰腺萎缩,患儿属学龄期儿童且无饮酒史,故应注意存在HP的可能。在临床中,当患者满足以下1个或多个标准时需考虑HP,并行基因检测[11]:(1)有特发性CP、RAP家族史或儿童时期不明原因胰腺炎;(2)有与HP相关的已知突变的亲属;(3)25岁以下且患特发性CP;(4)原因不明的RAP。而本文患儿根据病史、家族史、基因测序结果及HP的定义,即CP患者家族内,在两代或两代以上的亲属中,存在至少2个一级亲属或至少3个二级亲属罹患CP或RAP[12],最终确诊为HP。
目前发现HP相关基因主要有PRSS1、囊性纤维化跨膜传导调节因子(cystic fibrosis transmembrane regulator,CFTR)、丝氨酸蛋白酶抑制因子Kazal 1型(serine protease inhibitor Kazal 1type,SPINK1)、糜蛋白酶C(chymotrypsin C,CTRC),其中以 PRSS1基因最常见,该基因以R122H(占65%)、N29I(占25%)突变位点多见,其他突变位点如V39A、L104P、D22G、N29T、K23R、D19A、C139S 等 罕 见[9,12-16]。欧洲人群由PRSS1基因突变导致的HP最普遍,携带R122H和N29I突变者分别占52%、21%[12]。而中国人群PRSS1突变频率较低,台湾地区特发性CP PRSS1基因突变频率仅为4.6%(6/129)[17]。本文患儿的PRSS1基因突变位点为V39A,国内至今(2022年3月)尚未见报道,国外仅有一篇文献报道显示在1个意大利家系三代人中共有7名无诱发因素的成年CP患者携带V39A(c.116T>C)突变,符合HP诊断标准,先证者是1名57岁CP并发胰腺癌的男性患者[9,12]。
目前认为胰蛋白酶原突变体(即PRSS1基因突变体,如V39A)在胰腺内自激活(即胰蛋白酶激活胰蛋白酶原的过程)增加是HP的主要原因。CTRC可通过将胰蛋白酶原激活肽加工成更易被胰蛋白酶切割的形式,刺激阳离子胰蛋白酶原的自激活,而突变体V39A(突变型阳离子胰蛋白酶原)可减少或减慢阳离子胰蛋白酶原降解,造成胰蛋白酶原自激活增加,引起胰腺自身消化、腺泡细胞损伤相关的炎性反应而导致胰腺炎发生。研究证实,在CTRC存在的情况下,与野生型阳离子胰蛋白酶原相比,V39A对胰蛋白酶原的自激活明显增加,且胰蛋白酶活性水平升高,而无CTRC时,V39A对胰蛋白酶原的自激活无显著影响,提示V39A发挥功能需要依赖CTRC的调节[18-20]。
目前针对HP治疗尚无特定的药物,治疗上与其他原因引起的胰腺炎相似,通过避免诱因、控制疼痛、药物治疗内外分泌功能不足、内镜或外科手术治疗并发症(如胆管和十二指肠梗阻、假性囊肿、胰源性腹腔积液等)、监测胰腺癌等方式来进行,但应注重个体化、多学科治疗。同时,避免导致胰腺炎恶化的环境因素,如吸烟、饮酒、使用与药物性胰腺炎相关的药物(如血管紧张素转化酶抑制剂、羟甲基戊二酸辅酶A还原酶抑制剂和选择性5-羟色胺再摄取抑制剂等)[2,21-22]。有学者通过统计1998—2012年的相关数据,提出大多数儿童和青少年HP患儿可通过内镜获得初步治疗,但发现手术治疗后疼痛持续缓解时间(9.1年)较前者(3.4年)可能更长[23]。本例患儿目前通过药物即可控制病情,尚不需内镜、手术等干预,但应避免加重诱因,定期监测,以防病情加重出现严重并发症。
HP可出现胰腺外分泌功能异常,高达80%患者可继发T3cDM[24]。T3cDM是一种继发于胰腺疾病或胰腺外分泌功能障碍的糖尿病,也叫胰源性糖尿病或胰腺外分泌型糖尿病[24-25]。该并发症发病年龄较早,血糖水平波动较大,常需胰岛素治疗[26]。然而由于临床上对T3cDM的认识不够充分,常被误诊为2型糖尿病(type 2 diabetes melitus,T2DM)。有研究显示,559例继发于胰腺疾病的新发糖尿病成年患者中,仅2.7%被诊断为T3cDM,而高达87.8%被误诊为T2DM[27]。T3cDM患者重度低血糖和低血糖昏迷的发生率明显高于T2DM[28],前者中有79%出现过一过性低血糖,41%出现过重度低血糖,且低血糖较难纠正,生活质量显著下降,平均生存时间明显缩短,死亡率较高[27]。一项对2 000多例CP患者的随访发现,在确诊为CP 10年后,有28%的患者出现T3cDM,且随病程的延长,T3cDM发生率明显升高(50年后高达90%)[29]。已有研究表明,PRSS1基因外显子异常可显著增加T3cDM的发生风险[30]。本文患儿母亲20岁前即诊断为CP,22岁时曾出现2次餐后2 h血糖>11.1 mmol/L,当时未被诊断为糖尿病,后近10年血糖无明显异常,但33岁出现血糖异常后被确诊为“糖尿病”,结合其病史、基因检测结果,可诊断为T3cDM。此外,患儿外婆有糖尿病病史,但无腹痛表现,既往研究提示我国CP患者中约10%的患者无腹痛症状,部分表现为亚临床过程[31]。既往研究表明,胰腺外分泌功能损伤在普通人群中的发生率较高,提示普通人群中CP(亚临床)发病率被低估,同样T3cDM的诊断可能也被低估了[32]。患儿外婆罹患糖尿病,不除外其为HP合并T3cDM患者,但因其逝世较早,未能进行基因测序确诊。但综合上述分析,患儿母亲的V39A突变来自患儿外婆可能性大(患儿外公并无胰腺炎及糖尿病病史),且患儿及其母亲均明确携带该突变,符合常染色体显性遗传规律。
HP可并发胰腺癌,一项关于胰腺癌的大数据研究结果显示,CP和糖尿病均是胰腺癌高危因素,而二者并存可致胰腺癌风险增加33.52倍[33]。CP引起的T3cDM可能是癌前状态,27%~88%的患者确诊胰腺癌前2~3年会出现新发糖尿病[32,34-35]。研究表明,PRSS1过度表达和基因突变对胰腺癌发生有重要影响[36]。本例患儿母亲系PRSS1基因突变,20岁前确诊CP,33岁时出现了新发糖尿病,其患胰腺癌的危险性增加,应定期体检行胰腺癌筛查。
综上,HP属罕见常染色体遗传病,国内尚未见相关文献报道V39A突变引起的HP家系。T3cDM是HP的并发症,但临床上对T3cDM认识不足,常被误诊为T2DM,且T3cDM容易发生难以纠正的低血糖甚至低血糖昏迷,死亡率较高,希望引起临床医师对HP并发T3cDM的重视。此外,HP可造成营养吸收不良导致儿童生长发育障碍,且可因反复腹痛而增加儿童就诊及住院次数,久之将影响儿童身心健康,故临床上对AP反复发作或CP患儿,应警惕HP的可能,若有条件应及早进行基因测序,以期早确诊、干预,减少并发症发生和提高患儿生活质量。
作者贡献:何小莉收集资料、撰写文章;梁淑恒、李妙遐提供部分资料;孔晋亮负责提供技术支持;单庆文进行写作指导,对文章内容进行审阅与修订。
本文无利益冲突。

